DERAJAT KEASAMAN p H p H Derajat Keasaman
























- Slides: 27

DERAJAT KEASAMAN (p. H)

p. H ( Derajat Keasaman) 1. 2. 3. Asam Basa Campuran A. Buffer / Penyangga B. Hidrolisis

1. p. H Asam a. Asam Kuat Contoh: Tentukan derajat keasaman (p. H) HCl 0, 01 M

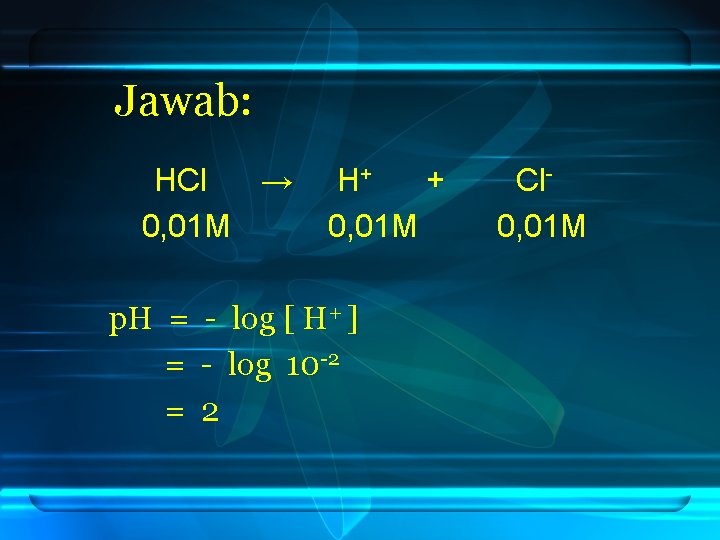
Jawab: HCl → 0, 01 M H+ + 0, 01 M p. H = - log [ H+ ] = - log 10 -2 = 2 Cl 0, 01 M

b. Asam Lemah Contoh: Tentukan derajat keasaman(p. H) CH 3 COOH 0, 1 M dengan Ka CH 3 COOH = 10 -5

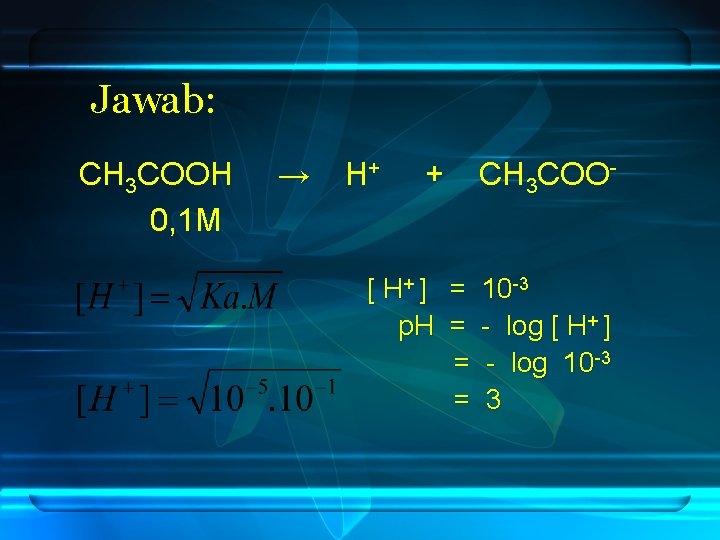
Jawab: CH 3 COOH 0, 1 M → H+ + CH 3 COO- [ H+ ] = 10 -3 p. H = - log [ H+ ] = - log 10 -3 = 3

2. p. H Basa a. Basa Kuat Contoh: Tentukan derajat keasama(p. H) Ca(OH)2 0, 01 M

Jawab: Ca(OH)2 → Ca 2+ + 2 OH 0, 01 M 0, 02 M p. OH = - log [ OH- ] = - log 2 x 10 -2 = 2 – log 2 p. H = 14 – (2 – log 2 ) = 12 + log 2

b. Basa Lemah Contoh: Tentukan derajat keasaman (p. H) NH 4 OH 0, 1 M dengan Kb NH 4 OH = 10 -5

Jawab: NH 4 OH → 0, 1 M Kb = 10 -5 NH 4+ p. OH = - log [ OH- ] = - log 10 -3 = 3 p. H = ( 14 – 3 ) = 11 + OH-

3. p. H Campuran A. Buffer / Penyangga 1. Asam 2. Basa

Contoh: 1. Sebanyak 10 m. L CH 3 COOH 2 M direaksikan dengan 10 m. L Na. OH 1 M, Ka = 10 -5 , tentukan p. H campuran!

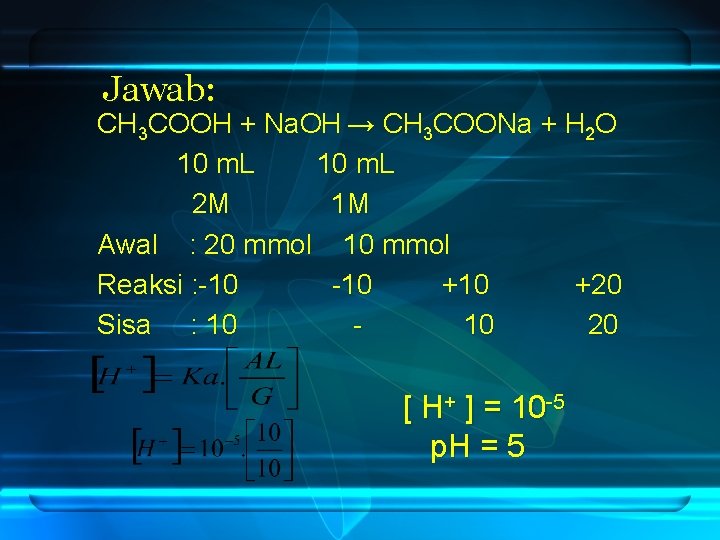
Jawab: CH 3 COOH + Na. OH → CH 3 COONa + H 2 O 10 m. L 2 M 1 M Awal : 20 mmol 10 mmol Reaksi : -10 +10 +20 Sisa : 10 10 20 [ H+ ] = 10 -5 p. H = 5

Contoh: 2. Sebanyak 10 m. L HCl 1 M direaksikan dengan 10 m. L NH 4 OH 2 M, Kb = 10 -5 , tentukan p. H campuran!

Jawab: HCl + 10 m. L 1 M Awal : 10 mmol Reaksi : -10 Sisa : - NH 4 OH → NH 4 Cl + H 2 O 10 m. L 2 M 20 mmol -10 +10 10 [ OH- ] = 10 -5 p. OH = 5 p. H = 9

Kegunaan larutan buffer dalam makhluk hidup diantaranya: 1. Mempertahankan p. H darah, untuk menjaga agar p. H darah tidak berubah. Maka dalam darah terdapat sistem penyangga antara H 2 CO 3 dan HCO 3–. 2. Dalam cairan sel tubuh terdapat sistem penyangga H 2 PO 4– dan HPO 42– yang juga berperan dalam ekskresi ion H+ di ginjal.

B. Hidrolisis 1. Asam Kuat dengan Basa Lemah 2. Asam Lemah dengan Basa Kuat 3. Asam Lemah dengan Basa Lemah

1. Hidrolisis Asam Kuat Dengan Basa Lemah Contoh: 1. Sebanyak 10 m. L HCl 1 M direaksikan dengan 10 m. L NH 4 OH 1 M, Kb = 10 -5 , tentukan p. H campuran!

Jawab: HCl + NH 4 OH → NH 4 Cl + H 2 O 10 m. L 1 M 1 M Awal : 10 mmol Reaksi : -10 +10 Sisa : 10 10 [ H+ ] = 2, 24 x 10 -5 p. H = 5 – log 2, 24

2. Hidrolisis Asam Lemah Dengan Basa Kuat Contoh: 1. Sebanyak 10 m. L CH 3 COOH 1 M direaksikan dengan 10 m. L KOH 1 M, Ka = 10 -5 , tentukan p. H campuran!

CH 3 COOH + 10 m. L 1 M Awal : 10 mmol Reaksi : -10 Sisa : - KOH → CH 3 COOK + H 2 O 10 m. L 1 M 10 mol -10 +10 10 10 [OH- ] = 2, 24 x 10 -5 p. OH = 5 – log 2, 24 p. H = 9 + log 2, 24

Contoh: 2. Sebanyak 20 m. L HCl 1 M direaksikan dengan 10 m. L NH 4 OH 1 M, Kb = 10 -5 , tentukan p. H campuran!

Jawab: HCl + NH 4 OH → CH 3 COOK + H 2 O 20 m. L 1 M 1 M Awal : 20 mmol 10 mmol Reaksi : -10 +10 Sisa : 10 10 10 [H+ ] = 0, 33 [H+] = 3, 3 x 10 -1 p. H = 1 – log 3, 3

Pertanyaan: 1. Suatu larutan yang mempunyai p. H di bawah 7 akan bersifat … Asam

2. Larutan garam CH 3 COONa merupakan garam terhidrolisis yang bersifat … Basa

