Keasaman Tanah Konsep Asam Basa Dalam larutan encer

Keasaman Tanah

Konsep Asam Basa • Dalam larutan encer, senyawa asam menyumbangkan H+ ke beberapa senyawa lainnya dan sebaliknya, senyawa basa menerima H+ • Contoh: CH 3 COOH ↔ CH 3 COO- + H+ HCl ↔ Cl- + H+ Na. OH ↔ Na+ + OH-

Konsep Asam Basa • Disosiasi H+ dari asam kuat seperti HCl mencapai 100% sedangkan asam lemah seperti CH 3 COOH hanya sekitar 1% • Dengan demikian, keasaman aktif, ion H+, meningkat dengan meningkatnya kekuatan asam • Senyawa asam yang tidak terdisosiasi merupakan keasaman potensial

Konsep Asam Basa • Keasaman total adalah jumlah konsentrasi keasaman aktif dan keasaman potensial • Contoh; • keasaman aktif 0, 099 M dan keasaman potensial 0, 001 M maka keasaman total 0, 100 M dan karena keasaman aktif hampir sama dengan keasaman total maka larutannya disebut asam kuat

Konsep Asam Basa • Air murni mengalami sedikit ionisasi H 2 O ↔ H+ + OH- • Karena H+ dan OH- dihasilkan, H 2 O disebut senyawa asam lemah dan basa lemah • Konsentrasi masing-masing H+ (atau H 3 O+) dan OH- dalam air murni adalah 10 -7 • Konstanta disosiasi air (Kw) adalah hasil kali konsentrasi H+ dan OH-
![Konsep Asam Basa • [H+]·[OH-] = [10 -7]·[10 -7] = 10 -14 • Dalam Konsep Asam Basa • [H+]·[OH-] = [10 -7]·[10 -7] = 10 -14 • Dalam](http://slidetodoc.com/presentation_image_h2/479497991d6100a773be1d2297bcfa1f/image-6.jpg)
Konsep Asam Basa • [H+]·[OH-] = [10 -7]·[10 -7] = 10 -14 • Dalam kesetimbangan dengan CO 2 di atmosfer, p. H air biasanya berkisar 5, 7 karena • H 2 O + CO 2 ↔ H 2 CO 3 ↔ H+ + HCO 3 • Penambahan asam ke H 2 O akan meningkatkan [H+] tapi menurunkan [OH-] karena Kw konstan di 10 -14
![Konsep Asam Basa • Contoh: • Dalam larutan 0, 1 M HCl, [H+] adalah Konsep Asam Basa • Contoh: • Dalam larutan 0, 1 M HCl, [H+] adalah](http://slidetodoc.com/presentation_image_h2/479497991d6100a773be1d2297bcfa1f/image-7.jpg)
Konsep Asam Basa • Contoh: • Dalam larutan 0, 1 M HCl, [H+] adalah 10 -1 M sehingga [OH-] adalah • Kw = [H+]·[OH-] = 10 -14 • [OH-] = 10 -13 M • [H+] dalam larutan biasanya dinyatakan dengan p. H dan didefinisikan sbb: p. H = - log [H+]

Konsep Asam Basa • Dengan demikian, peningkatan 1 satuan p. H sama dengan penurunan 10 kali [H+] • Larutan dengan p. H < 7 disebut asam, p. H = 7 netral, dan p. H > 7 disebut basa • p. H hanya mewakili konsentrasi [H+] dalam larutan dan tidak mengukur keasaman potensial (tak terdisosiasi)

Konsep Asam Basa • Contoh: • p. H 0, 1 M HCl yang terdisosiasi sempurna adalah 1, sedangkan p. H 0, 1 M CH 3 COOH adalah 3 • p. H 0, 1 M Na. OH (basa kuat) adalah 13 sedangkan p. H 0, 1 M NH 4 OH (basa lemah) adalah 11 • Bila asam dan basa bereaksi, ke 2 nya akan ternetralisir dan menghasilkan garam + air

Sistem Penyanggah • Sistem penyanggah (buffer = ketahanan terhadap perubahan p. H) dapat mempertahankan p. H larutan dalam kisaran yang sempit apabila ditambahkan asam atau basa • Larutan penyanggah biasanya merupakan larutan yang mengandung asam lemah dan garam asam lemah-basah kuat atau basa lemah dan garam asam kuat-basah lemah (contohnya larutan 1 M CH 3 COOH dan 1 M CH 3 COONa dengan p. H 4, 6 )

Sistem Penyanggah • CH 3 COOH ↔ H+ + CH 3 COO • CH 3 COONa ↔ Na+ + CH 3 COO • Jadi penambahan CH 3 COONa ke larutan CH 3 COOH meningkatkan konsentrasi CH 3 COOsehingga mendorong kesetimbangan ke bentuk CH 3 COOH tak terdisosiasi • Hal ini menyebabkan p. H larutan tetap 4, 6 walaupun diencerkan 10 kali dengan H 2 O

Sistem Penyanggah • Jika 10 ml dari 1 M HCl ditambahkan ke larutan penyanggah CH 3 COOH/CH 3 COONa, p. H hanya turun menjadi 4, 5 karena tambahan H+ akan mendorong reaksi CH 3 COOH ↔ H+ + CH 3 COO- ke arah kiri dan penurunan CH 3 COO- akan digantikan oleh CH 3 COOdari disosiasi CH 3 COONa • Sebaliknya jika 10 ml 1 M Na. OH ditambahkan, OHmenetralkan H+ membentuk air tapi keberadaan CH 3 COOH tak terdisosiasi mendorong reaksi ke kanan sehingga H+ yang ternetralisir tergantikan sehingga p. H hanya menjadi 4, 7

Sistem Penyanggah • Tanah-tanah biasanya berperilaku seperti larutan penyanggah asam lemah dimana KTK humus dan mineral liat sebagai penyanggah untuk p. H larutan tanah

Keasaman Tanah • Sumber keasaman tanah adalah bahan organik, mineral-mineral liat, oksida-oksida Fe dan Al, Al 3+dd (dapat dipertukarkan), garam-garam terlarut dan CO 2 • Bahan organik tanah atau humus mengandung grup fenolik dan karboksilik reaktif yang berperilaku sebagai asam lemah dengan melepaskan H+ • Pada tanah organik dan tanah mineral berbahan organik tinggi, asam organik berperan sangat nyata terhadap keasaman tanah

Keasaman Tanah • Mineral-mineral liat seperti kaolinit dan montmorilonit dapat menyanggah p. H tanah melalui disosiasi H+ pada pinggiran patahan • Tanah-tanah berkadar liat tinggi memiliki kapasitas penyanggah yang lebih besar dari tanah -tanah bertekstur kasar/pasir • Gambar berikut menunjukkan muatan tergantung p. H dan kapasitas penyanggah mineral-mineral liat, oksida Al dan Fe, serta bahan organik
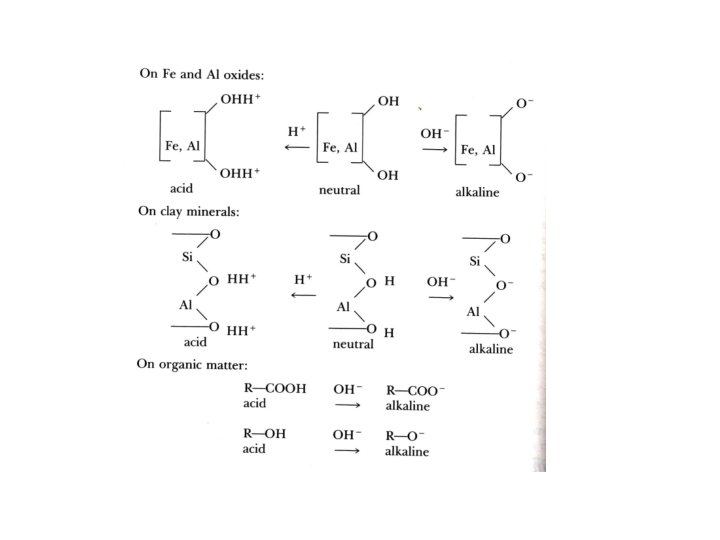

Keasaman Tanah • Ion-ion Al 3+ yang digantikan dari KTK terhidrolisis menjadi senyawa kompleks Alhidroksi • Hidrolisis Al 3+ melepaskan H+ dan dapat menurunkan p. H jika tak ada sumber OH- untuk menetralisir • Reaksi-reaksi berikut menggambarkan kesetimbangan antar jenis-jenis Al
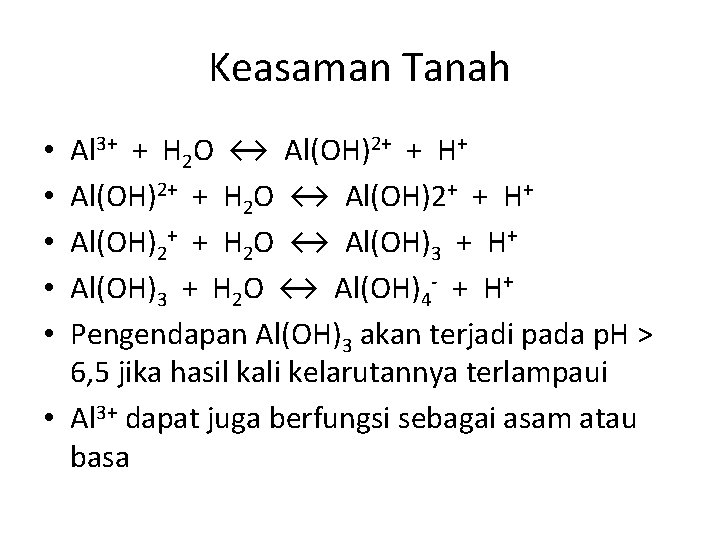
Keasaman Tanah Al 3+ + H 2 O ↔ Al(OH)2+ + H+ Al(OH)2+ + H 2 O ↔ Al(OH)3 + H+ Al(OH)3 + H 2 O ↔ Al(OH)4 - + H+ Pengendapan Al(OH)3 akan terjadi pada p. H > 6, 5 jika hasil kali kelarutannya terlampaui • Al 3+ dapat juga berfungsi sebagai asam atau basa • • •

Keasaman Tanah • Al sebagai basa Al(OH)3 + H+ ↔ Al(OH)2+ + H 2 O Al(OH)2+ + H+ ↔ Al 3+ + H 2 O Al(OH)3 + 3 H+ ↔ Al 3+ + 3 H 2 O • Al sebagai asam Al 3+ + OH- ↔ Al(OH)2+ + OH- ↔ Al(OH)3 • Al sebagai anion Al(OH)3 + OH- ↔ Al(OH)4 -
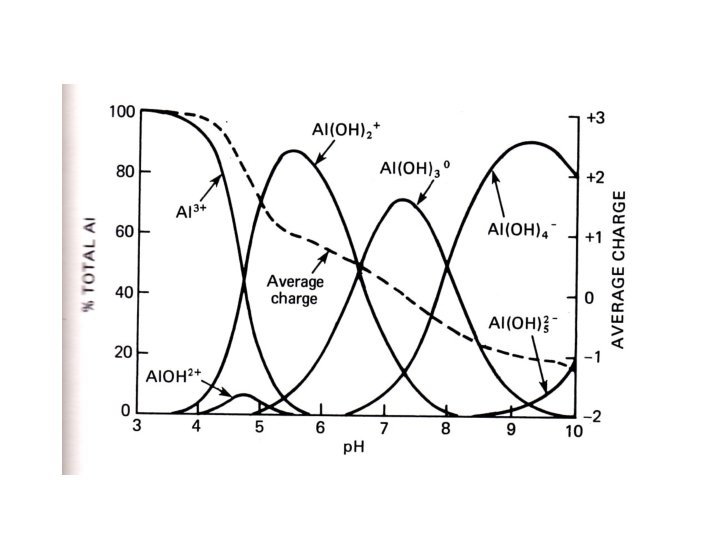

Keasaman Tanah • KTK tanah dapat dipengaruhi oleh Polymer Al karena polymer Al memiliki muatan positif yang tinggi dan tak dapat dipertukarkan • Pada p. H tinggi, KTK meningkat akibat pengendapan Al(OH)3 dan pembentukan polymer Al bermuatan positif menurun, sebaliknya pada p. H rendah, pembentukan polymer Al bermuatan positif meningkat dan terjerap pada permukaan liat sehingga KTK turun

Keasaman Tanah • Hidrolisis Fe sama seperti hidrolisis Al • Walaupun reaksi hidrolisis Fe lebih asam dari hidrolisis Al, keasamannya disanggah oleh reaksi hidrolisis Al • Fe 3+ + H 2 O ↔ Fe(OH)2+ + H+ • Dengan demikian, hidrolisis Fe hanya berpengaruh sedikit terhadap p. H tanah kecuali kebanyakan Al tanah telah bereaksi

Keasaman Tanah • Polymer Al dan Fe dapat berbentuk koloid berkristal atau amorf yang menyelimuti liat dan permukaan mineral-mineral lain

Keasaman Tanah • Garam basa, garam asam, garam netral dalam larutan tanah berasal dari pelapukan mineral, dekomposisi bahan organik, atau ditambahkan dalam bentuk pupuk anorganik dan pupuk organik • Kation-kation dari garam-garam tersebut menggantikan Al 3+ terjerap pada tanah asam sehingga p. H larutan tanah menurun (kation divalen lebih besar pengaruhnya dalam menurunkan p. H dibandingkan kation monovalen)

Keasaman Tanah • p. H pada tanah-tanah berbahan induk kapur dipengaruhi oleh tekanan parsial CO 2 dalam udara tanah • p. H tanah mengandung Ca. CO 3 bebas dalam kesetimbangan dengan CO 2 atmosfer adalah 8, 5; tapi peningkatan CO 2 dalam udara tanah menyebabkan p. H turun menjadi 7, 3 – 7, 5

Keasaman Tanah • Dekomposisi bahan organik dan respirasi akar meningkatkan CO 2 dalam udara tanah, dan CO 2 ini berkombinasi dengan air menghasilkan H+ sehingga menurunkan p. H • H 2 O + CO 2 ↔ H 2 CO 3 • H 2 CO 3 ↔ H+ + HCO 3 -

Faktor-Faktor Yang Mempengaruhi Keasaman Tanah • Peningkatan keasaman tanah disebabkan oleh: • 1. Penggunaan pupuk komersil, khususnya NH 4 -N yang menghasilkan H+ dalam proses nitrifikasi • 2. Serapan kation oleh akar tanaman • 3. Pencucian kation-kation yang digantikan oleh H+ dan kemudian oleh Al 3+ • 4. Dekomposisi bahan organik • Pengasaman alami tanah meningkat dengan meningkatnya curah hujan karena p. H hujan sekitar 5, 7 (tergantung kandungan SO 2, NO 2, dan lain-lain)
- Slides: 27