KINETIKA KIMIA 1 TEORI TUMBUKAN DARI LAJU REAKSI


KINETIKA KIMIA 1 TEORI TUMBUKAN DARI LAJU REAKSI 2 TEORI KEADAAN TRANSISI DARI LAJU REAKSI 3 HUKUM LAJU REAKSI 4 FAKTOR-FAKTOR LAJU REAKSI 5 MEKANISME REAKSI 6 ENZIM SEBAGAI KATALIS

TEORI TUMBUKAN DARI LAJU REAKSI • LAJU REAKSI BERBANDING LURUS: - FREKUENSI TUMBUKAN (x) - FRAKSI MOLEKUL TERAKTIFKAN (f) - PELUANG UNTUK BERTUMBUKAN (p) Reaksi : A + B C+D Laju reaksi = f. p. x = f. p. [A]. [B] = k. [A]. [B]
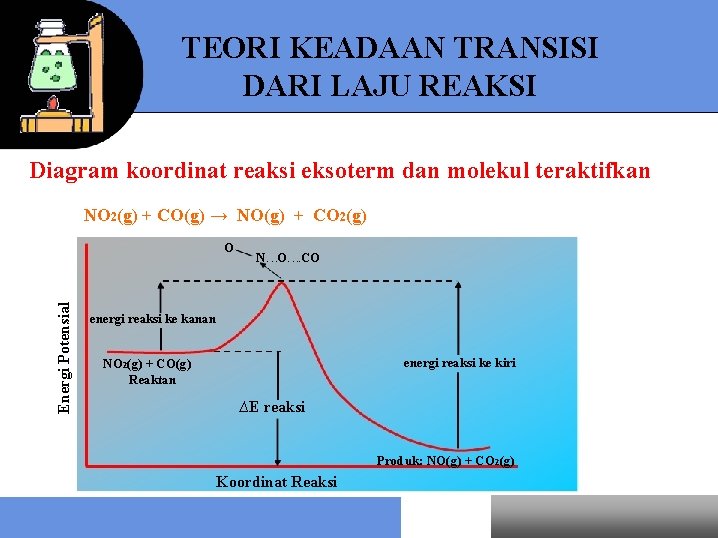
TEORI KEADAAN TRANSISI DARI LAJU REAKSI Diagram koordinat reaksi eksoterm dan molekul teraktifkan NO 2(g) + CO(g) → NO(g) + CO 2(g) Energi Potensial O N…. O…. . CO energi reaksi ke kanan energi reaksi ke kiri NO 2(g) + CO(g) Reaktan ∆E reaksi Produk: NO(g) + CO 2(g) Koordinat Reaksi

HUKUM LAJU REAKSI NO 2(g) + CO(g) NO(g) + CO 2(g) • Laju pengurangan konsentrasi reaktan terhadap waktu • Laju kenaikan konsentrasi produk terhadap waktu Laju reaksi Laju = - d[NO 2] = - d[CO] = d[NO] = d[CO 2] dt dt Reaksi umum : Laju = - a. A + b. B 1 d[A] 1 d[B] =a dt b dt c. C + d. D = 1 c d[C] dt = 1 d[D] d dt

Contoh 1 Pada suhu tinggi, HI bereaksi menurut persamaan berikut: 2 HI(g) → H 2(g) + I 2(g) Pada suhu 443°C laju reaksi meningkat seiring dengan meningkatnya konsentrasi HI sebagai berikut: [HI] (mol/L Laju (mol/L detik) 0, 0050 7, 5 x 10 -4 0, 010 3, 0 x 10 -3 0, 020 1, 2 x 10 -2 a. Tentukan orde reaksi dan tulislah hukum lajunya b. Hitunglah tetapan laju dan nyatakan satuannya c. Hitunglah laju reaksi untuk HI dengan konsentrasi 0, 0020 M
![Penyelesaian a. Hukum laju pada dua konsentrasi [HI]1 dan[HI]2 yang berbeda ialah: n laju Penyelesaian a. Hukum laju pada dua konsentrasi [HI]1 dan[HI]2 yang berbeda ialah: n laju](http://slidetodoc.com/presentation_image/2ca762bf0863bb5d5e2494903823ed20/image-7.jpg)
Penyelesaian a. Hukum laju pada dua konsentrasi [HI]1 dan[HI]2 yang berbeda ialah: n laju 2 [HI]2 laju 1 = k([HI]1)n laju 2 = k([HI]2)n laju 1 = [HI]1 3, 0 x 10 -3 = 0, 010 7, 5 x 10 -4 0, 0050 4 = (2)n n n = 2 Hukum laju = k[HI]2

b. Tetapan laju k dihitung dengan memasukan nilai pada set data yang mana saja dengan menggunakan hukum laju yang sudah ditetapkan. Misalnya, jika kita ambil set data pertama: 7, 5 x 10 -4 mol L-1 s-1 = k(0, 0050 mol L-1)2 Jadi, k = 30 L mol-1 s-1 c. Laju dapat dihitung untuk [HI] = 0, 0020 M: laju = k[HI]2 = (30 L mol-1 s-1)(0, 0020 mol L-1)2 = 1, 2 x 10 -4 mol L-1 s-1
![Orde Reaksi Orde Nol a. A → Produk Laju = k [A]n. . . Orde Reaksi Orde Nol a. A → Produk Laju = k [A]n. . .](http://slidetodoc.com/presentation_image/2ca762bf0863bb5d5e2494903823ed20/image-9.jpg)
Orde Reaksi Orde Nol a. A → Produk Laju = k [A]n. . . n = orde reaksi (tidak berkaitan langsung dengan koefisien a) -d[A] = k [A]0 dt [A] d[A] = -kdt [A] – [A]0 = -kt [A]0 Laju = k (orde nol) Waktu (t)

Laju yang berkaitan pada dua atau lebih unsur kimia yang berbeda a. A + b. B → Produk 1 d[A] 1 d[B] Laju = =a dt b dt = - k [A]m [B]n
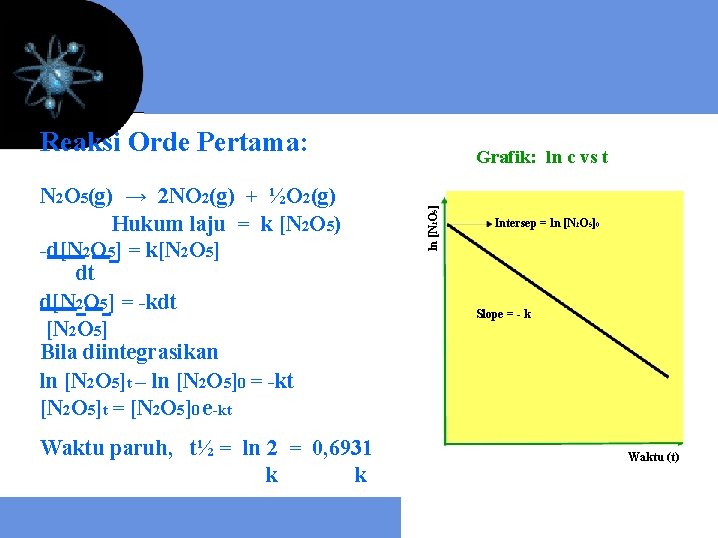
Reaksi Orde Pertama: Waktu paruh, t½ = ln 2 = 0, 6931 k k ln [N 2 O 5] N 2 O 5(g) → 2 NO 2(g) + ½O 2(g) Hukum laju = k [N 2 O 5) -d[N 2 O 5] = k[N 2 O 5] dt d[N 2 O 5] = -kdt [N 2 O 5] Bila diintegrasikan ln [N 2 O 5]t – ln [N 2 O 5]0 = -kt [N 2 O 5]t = [N 2 O 5]0 e-kt Grafik: ln c vs t Intersep = ln [N 2 O 5]0 Slope = - k Waktu (t)

Contoh 2 Penguraian termal aseton pada suhu 600 o. C merupakan reaksi orde pertama dengan waktu paruh 80 detik 1. Hitunglah nilai konstanta laju reaksi (k) 2. Berapa waktu yang diperlukan agar 25% dari contoh aseton itu terurai

Penyelesaian 1. k = 0, 693/t½ = 0, 693/80 detik = 8, 7 x 10 -3 detik-1 2. Jika yang terurai 25% maka yang tersisa = 100% - 25% = 75% kt = 2, 303 log [A]0 [A]t (8, 7 x 10 -3) t = 2, 303 (log 1, 0/0, 75) t = 23 detik
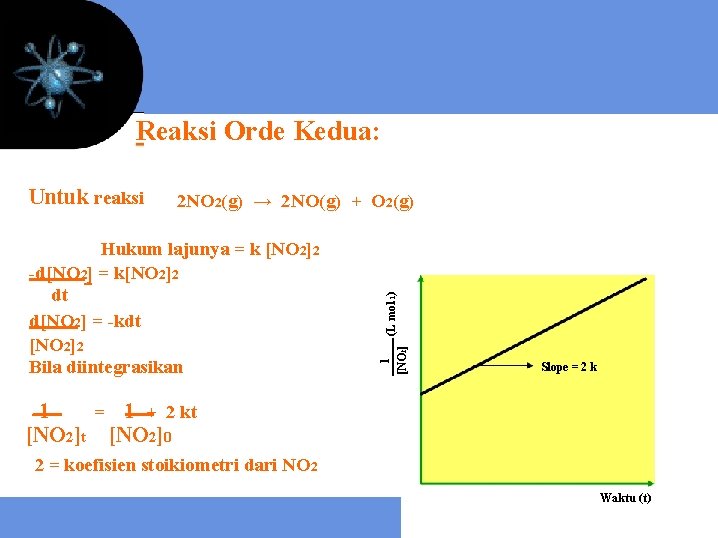
Reaksi Orde Kedua: 2 NO 2(g) → 2 NO(g) + O 2(g) Hukum lajunya = k [NO 2]2 -d[NO 2] = k[NO 2]2 dt d[NO 2] = -kdt [NO 2]2 Bila diintegrasikan 1 (L mol-1) [NO 2] Untuk reaksi Slope = 2 k 1 = 1 + 2 kt [NO 2]0 2 = koefisien stoikiometri dari NO 2 Waktu (t)

Reaksi Orde Pertama Semu Merupakan reaksi orde kedua atau orde yang lebih tinggi tapi mengikuti reaksi orde pertama Contoh: C + D hasil reaksi Laju reaksinya = k [C] [D] d[C] = k [C] [D]; bila k[D] tetap maka laju reaksinya = k’ [C] dt d[C] atau = k’ [C] dan k’ = k [D], k’= tetapan laju orde 1 semu dt dan waktu paruhnya (t ½) = 0, 693/k’

Contoh 3 Reaksi radikal OH- dengan metana di atmosfir mempunyai konstanta laju reaksi pada suhu 25 o. C sebesar 6, 3 x 10 -15 mol/L detik. Reaksinya: OH- (g) + CH 4 (g) H 2 O (g) + CH 3 - (g) 1. Tentukan hukum laju reaksi orde pertama semu jika OH- konstan dan hitunglah k’ jika [OH-] = 1, 2 x 106 mol/L 2. Hitunglah waktu paruh metana bila [OH-] = 1, 2 x 106 mol/L
![Penyelesaian 1. Laju reaksi = k [OH-] [CH 4] karena [OH-] konstan maka konstanta Penyelesaian 1. Laju reaksi = k [OH-] [CH 4] karena [OH-] konstan maka konstanta](http://slidetodoc.com/presentation_image/2ca762bf0863bb5d5e2494903823ed20/image-17.jpg)
Penyelesaian 1. Laju reaksi = k [OH-] [CH 4] karena [OH-] konstan maka konstanta laju reaksi = k’ laju reaksi menjadi = k’ [CH 4]; dan k’ = k [OH-] k’ = (6, 3 x 10 -15 mol/L detik) (1, 2 x 106 mol/L) = 7, 6 x 10 -9 detik-1 2. t½ = 0, 693/k’ = 0, 693/ 7, 6 x 10 -9 detik-1 = 2 tahun 11 bulan

4 FAKTOR-FAKTOR LAJU REAKSI 1. Macam zat yang bereaksi 2. Konsentrasi zat yang bereaksi Konsentrasi pereaksi berbanding lurus dengan laju reaksi 3. Tekanan untuk reaksi yang melibatkan gas, karena konsentrasi gas berhubungan dengan tekanan 4. Luas permukaan semakin halus bentuk zat yang bereaksi semakin cepat laju reaksi. Contoh: laju reaksi Alumunium dalam bentuk serbuk > laju reaksi alumunium dalam bentuk batangan

5. Suhu semakin tinggi suhu maka energi kinetik molekul meningkat sehingga frekuensi tumbukan semakin tinggi sehingga laju reaksi meningkat Tetapan laju bervariasi secara eksponensial dengan kebalikan suhu k = A e-Ea/RT ln k = ln A - Ea RT ≈ ln k = ln A - y a ( )( ) Ea R b 1 T x

6. Katalis zat yang mempercepat reaksi kimia tetapi tidak mengalami perubahan yang permanen • Katalis homogen • Katalis heterogen Katalis : fasa sama dengan reaktan : fasa berbeda dengan reaktan >< Inhibitor Contoh: Logam platina (Pt) mengkatalis reaksi hidrogenasi etena menjadi etana H 2 + C 2 H 4 → Pt C 2 H 6
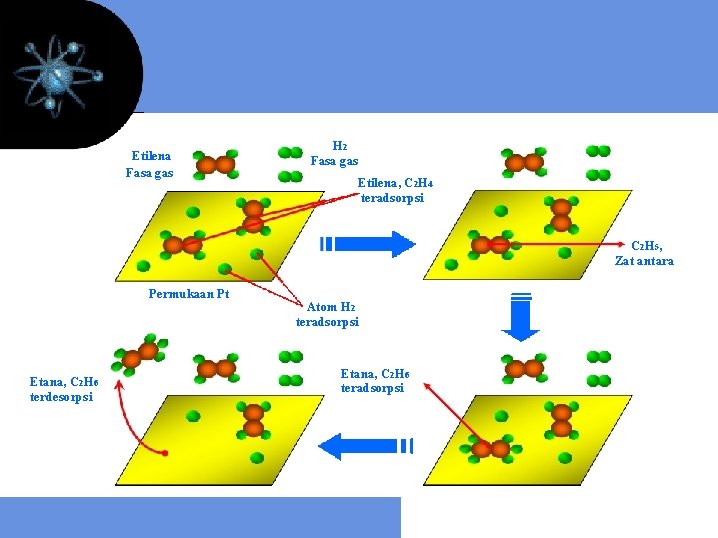
Etilena Fasa gas H 2 Fasa gas Etilena, C 2 H 4 teradsorpsi C 2 H 5, Zat antara Permukaan Pt Etana, C 2 H 6 terdesorpsi Atom H 2 teradsorpsi Etana, C 2 H 6 teradsorpsi
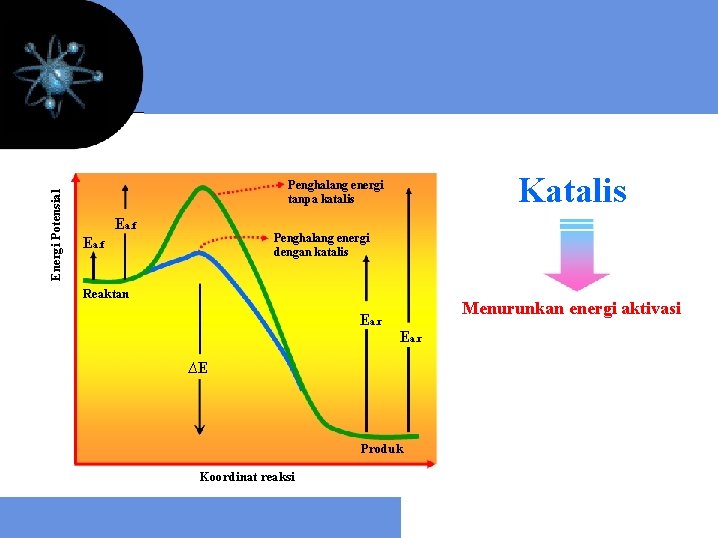
Energi Potensial Katalis Penghalang energi tanpa katalis Ea. f Penghalang energi dengan katalis Ea. f Reaktan Ea. r Menurunkan energi aktivasi Ea. r ∆E Produk Koordinat reaksi

5 MEKANISME REAKSI Mekanisme reaksi menyatakan jenis dan jumlah tahap pada suatu reaksi Reaksi Elementer Unimolekular : N 2 O 5* → NO 2 + NO 3 laju = k [N 2 O 5*] Bimolekular : NO(g) + O 3(g) → NO 2(g) + O 2(g) laju = k [NO] [O 3] Termolekular : I + Ar → I 2 + Ar laju = k [ I ]2 [Ar] laju = k [ I ]2

Contoh 4 Carilah molekularitas pada reaksi satu tahap beikut: a. NO + N 2 O 5 3 NO 2 b. 2 NO + Cl 2 2 NOCl c. Cl + M d. C 6 H 5 – CH NC – CH Cl 2 + M C 6 H 5 – CH (isomer cis trans) CH - CN

Penyelesaian a. bimolekular (2 molekul yaitu NO dan N 2 O 5) b. termokular (3 molekul yaitu 2 molekul NO dan 1 molekul Cl 2) c. termokular (3 molekul yaitu Cl, dan M) d. unimolekular (1 molekul)

6 ENZIM SEBAGAI KATALIS Enzim merupakan protein globular yang dapat mengkatalisis reaksi biokimia spesifik Mekanisme Kerja Enzim E+ S E– S S = substrat; P = produk E– P E+ P

Faktor-faktor yang mempengaruhi kerja enzim a. p. H muatan enzim bergantung pada p. H lingkungannya dan mempengaruhi keaktifan dari sisi aktif enzim b. Suhu suhu dapat merusak struktur tiga dimensi dari enzim (protein) c. Aktivator aktivitas enzim dapat meningkat dengan adanya ion-ion anorganik. Contohnhya: ion Cl- pada enzim amilase air liur
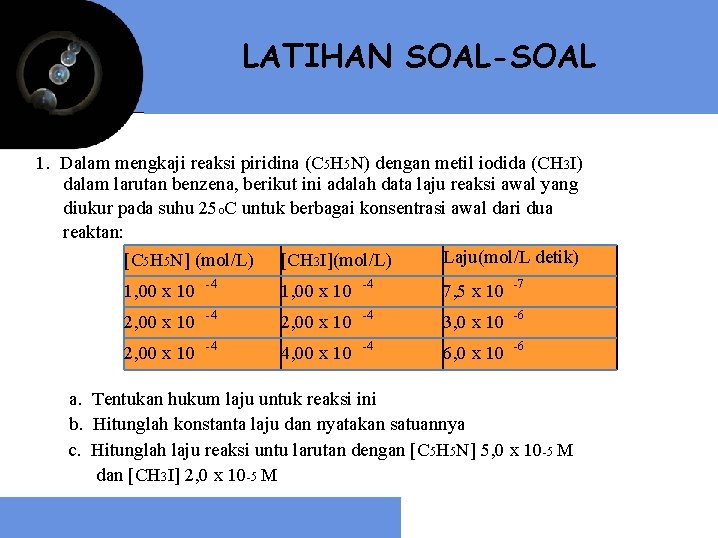
LATIHAN SOAL-SOAL 1. Dalam mengkaji reaksi piridina (C 5 H 5 N) dengan metil iodida (CH 3 I) dalam larutan benzena, berikut ini adalah data laju reaksi awal yang diukur pada suhu 25 o. C untuk berbagai konsentrasi awal dari dua reaktan: Laju(mol/L detik) [C 5 H 5 N] (mol/L) [CH 3 I](mol/L) 1, 00 x 10 -4 7, 5 x 10 -7 2, 00 x 10 -4 3, 0 x 10 -6 2, 00 x 10 -4 4, 00 x 10 -4 6, 0 x 10 -6 a. Tentukan hukum laju untuk reaksi ini b. Hitunglah konstanta laju dan nyatakan satuannya c. Hitunglah laju reaksi untu larutan dengan [C 5 H 5 N] 5, 0 x 10 -5 M dan [CH 3 I] 2, 0 x 10 -5 M

2. Senyawa A terurai membentuk B dan C pada reaksi yang mengikuti ordo pertama. Pada suhu 25 o. C konstanta laju reaksinya adalah 0, 0450 detik-1. Hitunglah waktu paruh zat A pada suhu 25 o. C 3. Dimerisasi tetrafluoroetilena (C 2 F 4) menjadi oktafluorosiklobutana (C 4 F 8) mempunyai orde kedua untuk pereaksi C 2 F 4 dan pada suhu 450 K konstanta lajunya k = 0, 0448 L mol-1 detik-1. Jika konsentrasi awal C 2 F 4 0, 100 M, berapa konsentrasinya sesudah 250 detik 4. Pada suhu 600 K, konstanta laju untuk dekomposisi reaksi ordo pertama nitroetana : CH 3 CH 2 NO 2 (g) C 2 H 4 (g) + HNO 2 (g) adalah 1, 9 x 10 -4 detik-1. Sampel CH 3 CH 2 NO 2 dipanaskan pada suhu 600 K dan pada suhu ini tekanan parsial awalnya adalah 0, 078 atm. Hitunglah tekanan parsialnya setelah 3 jam

5. Identifikasi setiap reaksi elementer berikut sebagai unimolekular, bimolekular, atau termolekular, dan tulislah hukum lajunya a. HCO + O 2 b. CH 3 + O 2 + N 2 c. HO 2 NO 2 HO 2 + CO CH 3 O 2 N 2 HO 2 + NO 2 6. Tetapan laju dari reaksi elementer: BH 4 - (aq) + NH 4+ (aq) BH 3 NH 3 (aq) + H 2 (g) ialah k = 1, 94 x 10 -4 L/mol detik pada suhu 30 o. C dan reaksi memiliki energi aktivasi 161 k. J/mol. Hitunglah tetapan laju reaksi di atas pada suhu 40 o. C
- Slides: 30