Biologick fakulta Jihoesk Univerzity Katedra fyziologie a anatomie

Biologická fakulta Jihočeské Univerzity Katedra fyziologie a anatomie rostlin Kurz fyziologie rostlin Fyziologie fotosyntézy 1 Ivan Šetlík
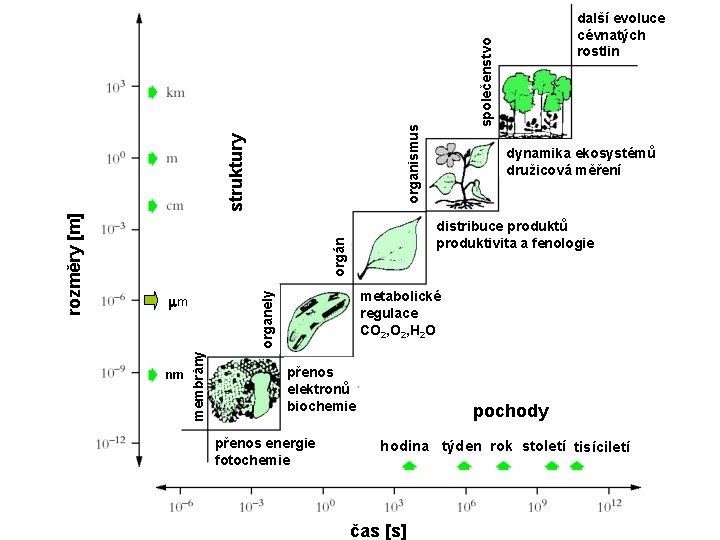
společenstvo organismus struktury dynamika ekosystémů družicová měření distribuce produktů produktivita a fenologie orgán nm metabolické regulace CO 2, H 2 O organely membrány rozměry [m] m další evoluce cévnatých rostlin přenos elektronů biochemie přenos energie fotochemie pochody hodina týden rok století tisíciletí čas [s]
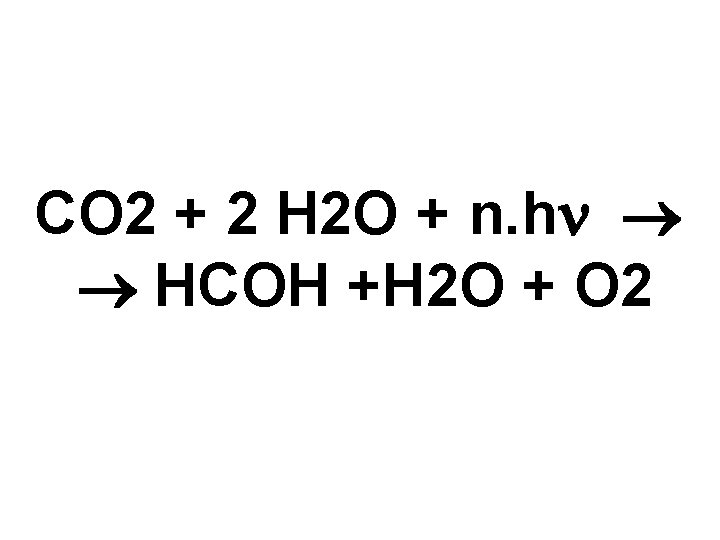
CO 2 + 2 H 2 O + n. h HCOH +H 2 O + O 2

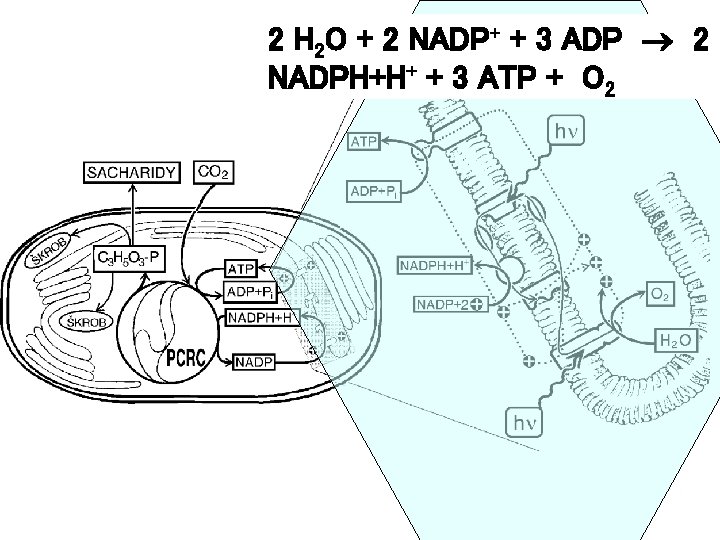
2 H 2 O + 2 NADP+ + 3 ADP 2 NADPH+H+ + 3 ATP + O 2

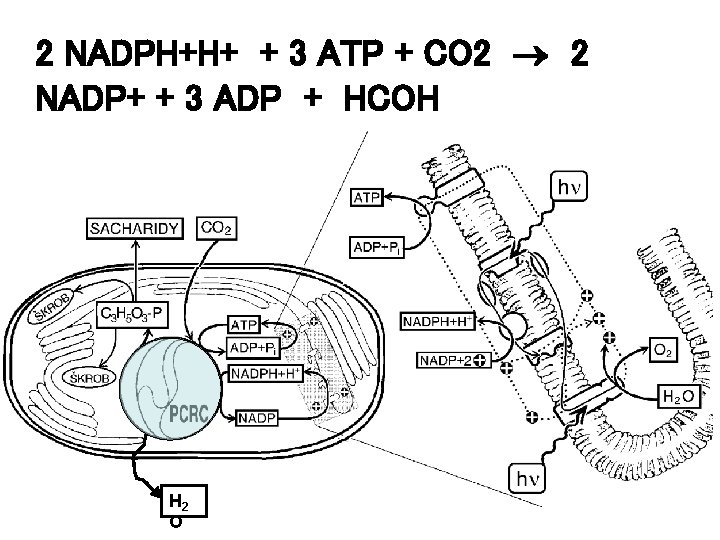
2 NADPH+H+ + 3 ATP + CO 2 2 NADP+ + 3 ADP + HCOH H 2 O


Ozářenost Parciální tlak CO 2 Teplota (Voda)

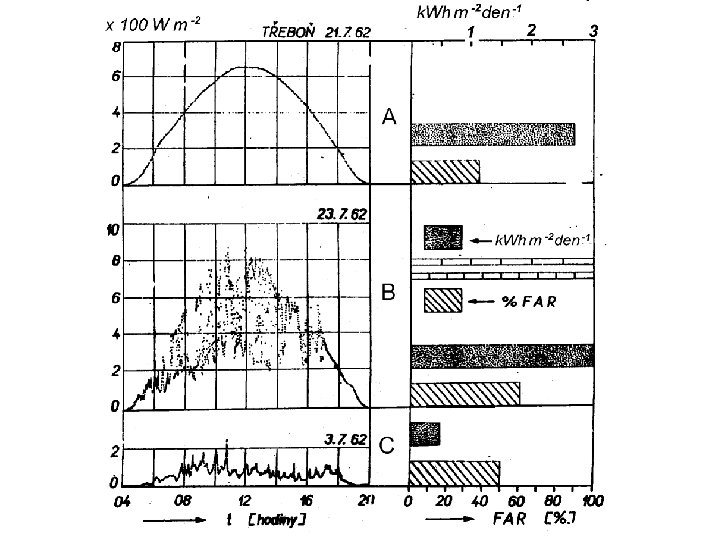
1 2 3 4 5 6
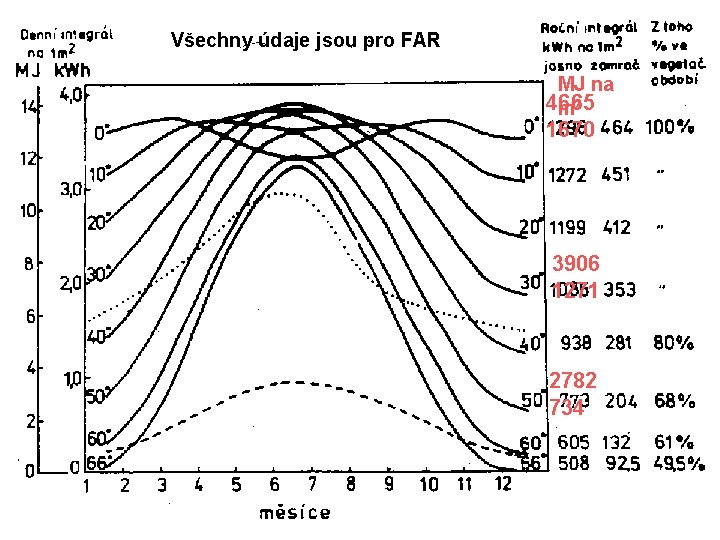
Všechny údaje jsou pro FAR MJ na 4665 m 2 1670 3906 1271 2782 734

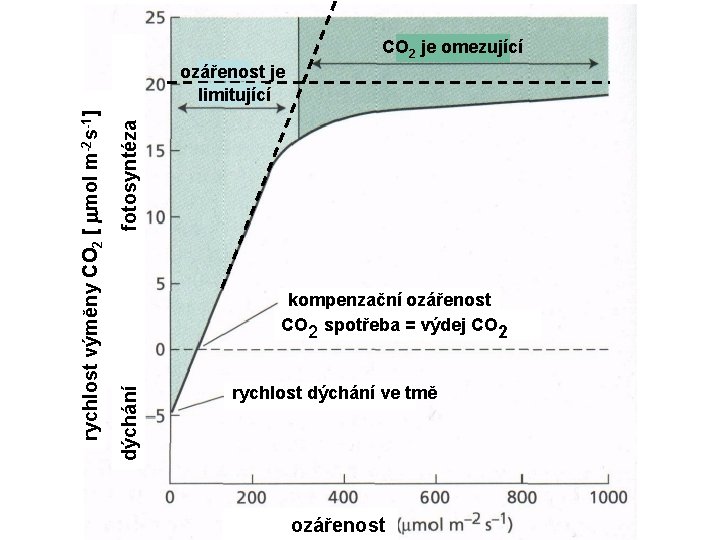
fotosyntéza Compensation irradiance kompenzační ozářenost CO 2 spotřeba = výdej CO 2 dýchání rychlost výměny CO 2 [ mol m-2 s-1] Irradiance ozářenost je limitující CO 2 je omezující rychlost dýchání ve tmě ozářenost Absorbed radiation
![Čistá rychlost fotosyntézy [ mol (O 2)mmol-1 (Chl) s -1] 200 Pa (CO 2) Čistá rychlost fotosyntézy [ mol (O 2)mmol-1 (Chl) s -1] 200 Pa (CO 2)](http://slidetodoc.com/presentation_image_h2/afb1ccb766baaf6b7c5a588a78e8801a/image-15.jpg)
Čistá rychlost fotosyntézy [ mol (O 2)mmol-1 (Chl) s -1] 200 Pa (CO 2) 2000 ppm (CO 2) 40 Pa (CO 2) 400 ppm (CO 2) 20 Pa (CO 2) 200 ppm (CO 2) 0 25 50 75 Ozářenost [ mol(kvant)m-2 s -1 100
![-1 -1 vývoj kyslíku [ mol(O 2)g(Chl) s ] 40 Chlorella 100 Pa CO -1 -1 vývoj kyslíku [ mol(O 2)g(Chl) s ] 40 Chlorella 100 Pa CO](http://slidetodoc.com/presentation_image_h2/afb1ccb766baaf6b7c5a588a78e8801a/image-16.jpg)
-1 -1 vývoj kyslíku [ mol(O 2)g(Chl) s ] 40 Chlorella 100 Pa CO 2 30 20 10 20 30 ozářenost [W. m-2] 40 40 50
![-2 Ozářenost [W [W. m Ozářenost m-2]] Rychlost rychlostfotosyntézy [ mol CO 2 m-2 -2 Ozářenost [W [W. m Ozářenost m-2]] Rychlost rychlostfotosyntézy [ mol CO 2 m-2](http://slidetodoc.com/presentation_image_h2/afb1ccb766baaf6b7c5a588a78e8801a/image-17.jpg)
-2 Ozářenost [W [W. m Ozářenost m-2]] Rychlost rychlostfotosyntézy [ mol CO 2 m-2 s-1]
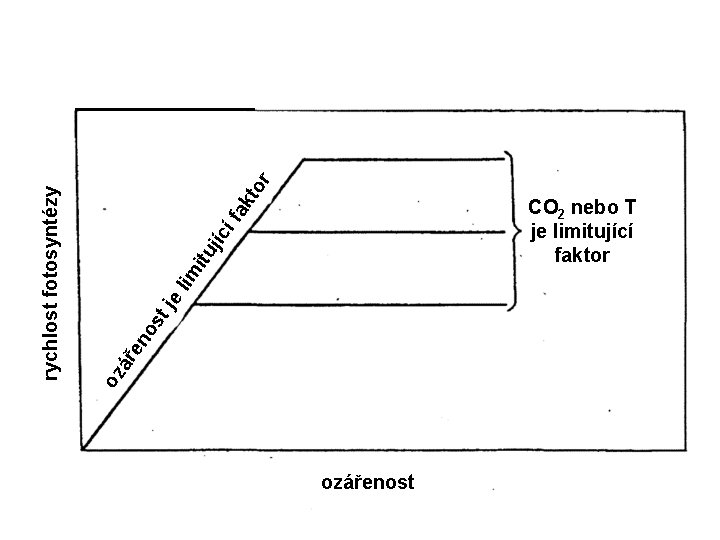
os en oz ář e tj r to íf ak itu jíc lim rychlost fotosyntézy CO 2 nebo T je limitující faktor ozářenost
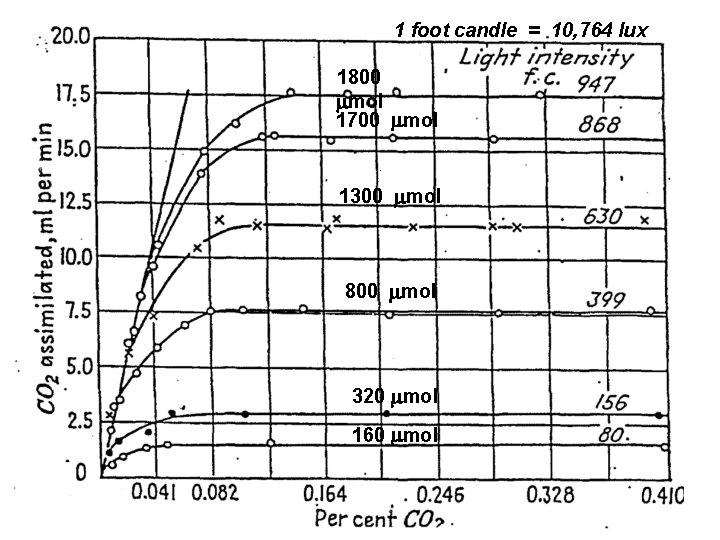
1 foot candle = 10, 764 lux 1800 mol 1700 mol 1300 mol 800 mol 320 mol 160 mol
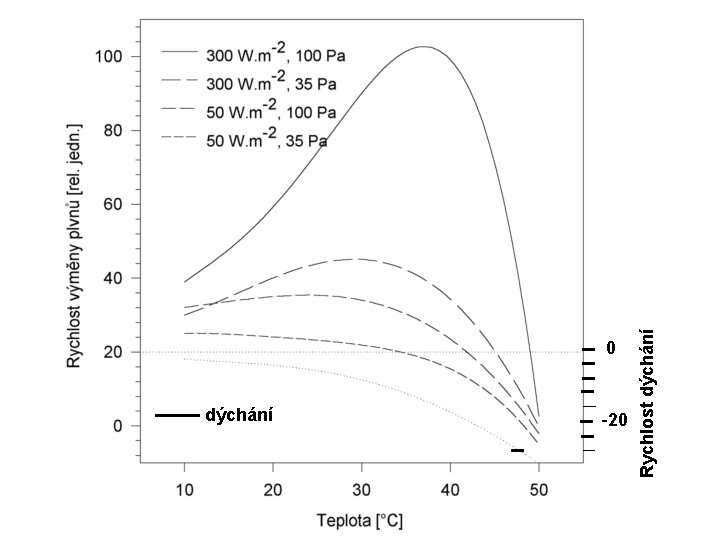
dýchání -20 Rychlost dýchání 0
![% CO 2 2 ob j. 1 100 75 50 25 Ozářenost [W. m-2] % CO 2 2 ob j. 1 100 75 50 25 Ozářenost [W. m-2]](http://slidetodoc.com/presentation_image_h2/afb1ccb766baaf6b7c5a588a78e8801a/image-21.jpg)
% CO 2 2 ob j. 1 100 75 50 25 Ozářenost [W. m-2] 0 Rychlost fotosyntézy [ mol(O 2)mmol-1(Chl)s-1] Rychlost fotosyntézy [g(CO 2)m-2 h-1] 3 40 30 20 10 Te plo ta [°C ] 0 10 40 80 120 200 -2 -1 Ozářenost [ mol(kvant)m s ]
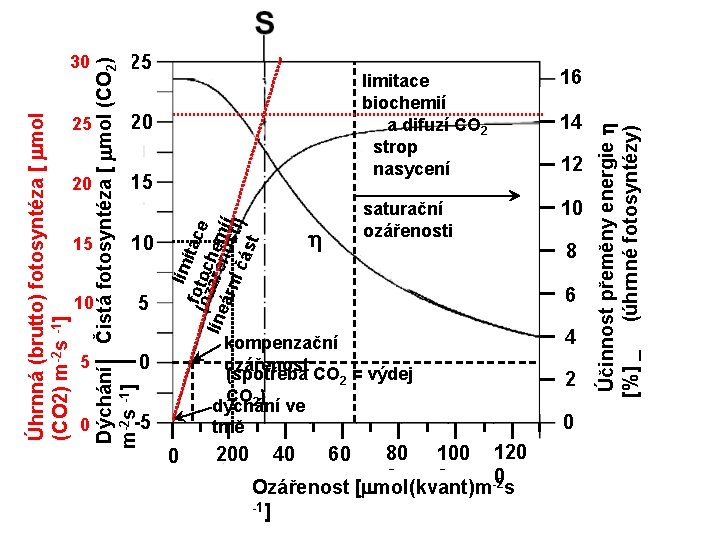
15 15 10 10 5 5 0 h limitace biochemií a difuzí CO 2 strop nasycení 16 saturační ozářenosti 10 kompenzační ozářenost (spotřeba CO 2 = výdej CO 2) dýchání ve tmě 0 -5 0 200 80 100 120 40 60 0 0 [ mol(kvant)m -2 Ozářenost s -1] 14 12 8 6 4 2 0 Účinnost přeměny energie h [%] _ (úhrnné fotosyntézy) 20 20 lim itac t e (ofo o hem line zářecn árn os íí í čá tí) st Čistá fotosyntéza [ mol (CO 2) 25 25 Dýchání m-2 s -1] Úhrnná (brutto) fotosyntéza [ mol (CO 2) m-2 s -1] 30

Pochody omezující ozářeností nasycenou fotosyntézu (1) přenos elektronů přenašeči mezi fotosystémy, (2) přesun NADPH+H+ a ATP k reakcím Calvinova cyklu (3) enzymové reakce Calvinova cyklu (4) rychlost vstupu CO 2 do mezibuněčných prostor listu (5) difúze CO 2 k asimilujícím buňkám a do jejich nitra až ke chloroplastům
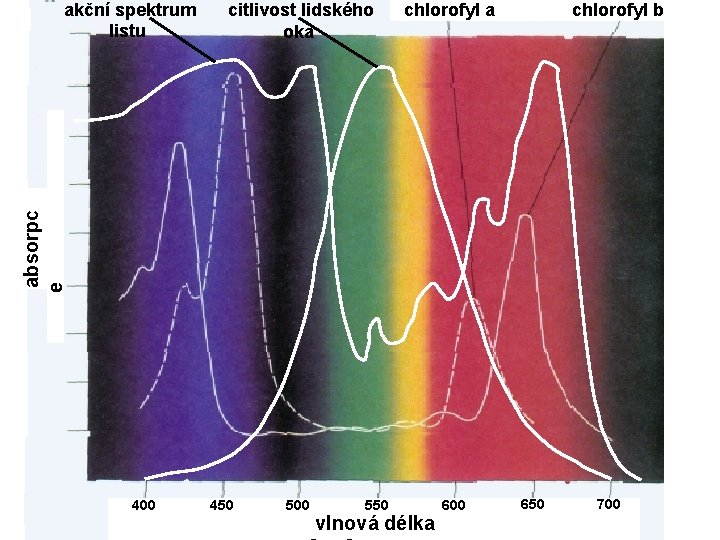
citlivost lidského oka chlorofyl b absorpc e akční spektrum listu 400 450 500 550 vlnová délka 600 650 700
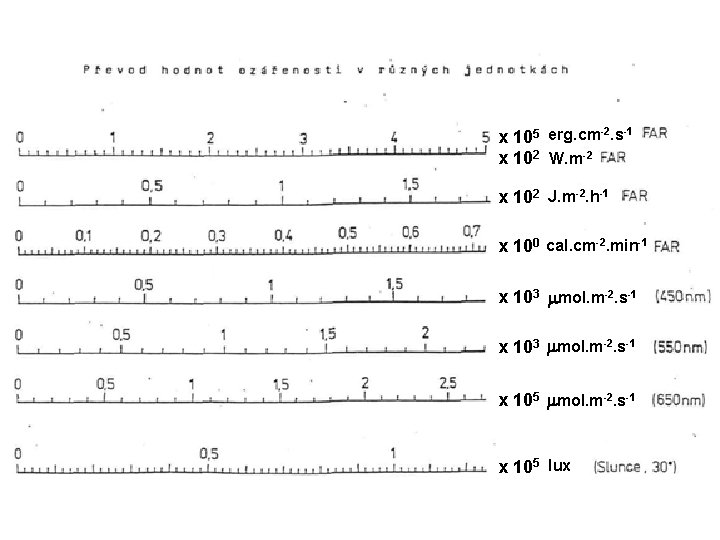
x 105 erg. cm-2. s-1 x 102 W. m-2 x 102 J. m-2. h-1 x 100 cal. cm-2. min-1 x 103 mol. m-2. s-1 x 105 lux

Obsah energie jednoho fotonu je dán vztahem E = h. c / kde h je Planckova konstanta rovná 6, 626 10– 34 J. s nebo 0, 4136 10– 14 e. V. s , je kmitočet záření [s-1] c rychlost světla ve vakuu, tj. 2, 998 108 m. s– 1 [m] je vlnová délka záření o které jde. Pokud při výpočtu použijeme vlnovou délku v nm nabude výpočetní vzorec tvar E = 1240 e. V. nm / nm = 1240/ e. V

Energie, kterou nese jeden mol fotonů, také označovaný jako jeden einstein (1 E, není zákonná jednotka) je dána rovnicí E = N. h. c / J. mol– 1 N je Avogadrovo číslo = (6, 022 1023 mol– 1 h je Planckova konstanta = 6, 626 10– 34 J. s] c rychlost světla ve vakuu = = 2, 998 108 m. s– 1 nebo 2, 998 1017 nm. s– 1]

Vzorec pro výpočet pak je buď E = (6, 022 1023 mol– 1 ) (6, 626 10– 34 J. s ) s– 1 3, 99 10– 10 J. mol– 1 Nebo E = (6, 0 1023 mol– 1 ) (6, 6 10– 34 J. s ) (3, 0 1017 nm. s– 1 ) / nm (1, 196 108 J. mol– 1. nm ) / nm což je přibližně (a lépe se to pamatuje) E = 120 000 / k. J. mol– 1

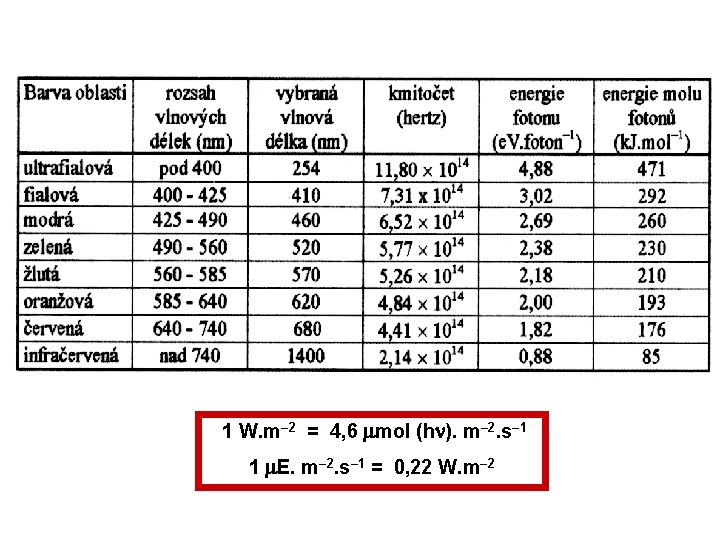
1 W. m– 2 = 4, 6 mol (h ). m– 2. s– 1 1 E. m– 2. s– 1 = 0, 22 W. m– 2
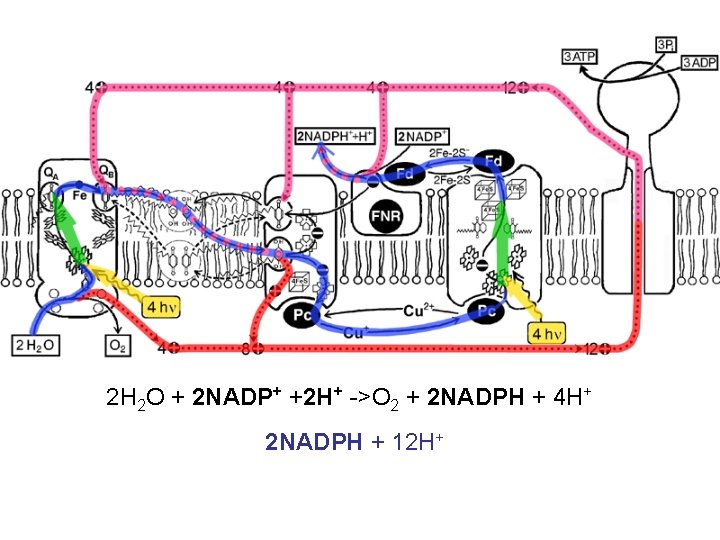
2 H 2 O + 2 NADP+ +2 H+ ->O 2 + 2 NADPH + 4 H+ 2 NADPH + 12 H+

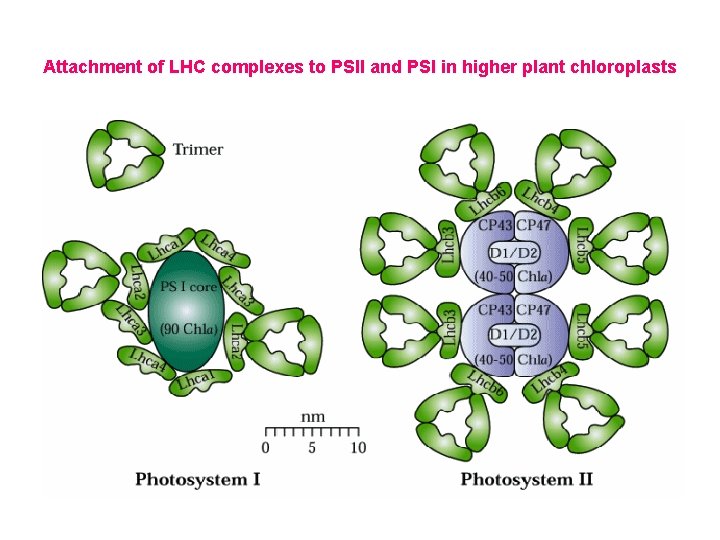
Attachment of LHC complexes to PSII and PSI in higher plant chloroplasts


100 cst. s– 1 reakčního centra a 500 molekul chlorofylu na 1 RC 0, 2(e–). molekula(Chl)– 1. s– 1 tedy 0, 2 meq(e–). mmol– 1(Chl). s– 1 tedy 200 eq(e–). mmol– 1(Chl). s– 1 čili 200 eq(e–). g– 1(Chl). s– 1 pro redukci jedné molekuly CO 2 5 elektronů tedy 200 : 5 = = 40 mol(CO 2). mmol– 1(Chl). s– 1 = = 40 mol(CO 2). g– 1(Chl). s– 1

v listu je 0, 5 mmol(Chl). m– 2 což je 0, 5 g(Chl). m – 2 odpovídající rychlost karboxylace 40 mol(CO 2). g– 1 (Chl). s– 1 : 2 = 20 mol(CO 2). m– 2. s– 1 1 mol(CO 2). m– 2. s-1 ≈ ≈ 2 mol(CO 2). mmol– 1(Chl). s– 1

Kvantová účinnost tj. jaký počet kvant se musí pohltit na asimilaci jedné molekuly CO 2, tedy počet (molů) pohlcených kvant / / počet asimilovaných (molů) molekul CO 2 nebo kvantový výtěžek, což je obrácený poměr počet asimilovaných (molů) molekul CO 2 / / počet (molů) pohlcených kvant

15 mol (CO 2) m-2 s-1 potřebuje 200 mol (h ). m– 2. s– 1 kvantová potřeba ≈ 13, 3 mol kvant na 1 mol CO 2 kvantový výtěžek ≈ 0, 075 mol CO 2. kvantum– 1. 200 mol záření přinese (220 x 103 x 200 x 10 -6) což je (0, 22 200) = 44 J obsah energie v 1 molu {HCOH} je 470 k. J úhrnná uložená energie bude 470 103 k. J. mol-1 15 10 -6 mol = (0, 47 15) = 7, 05 J a energetická účinnost 7, 05 : 44 = 0, 16 čili 16 %. 13, 3 mol kvant o energii 220 k. J mol– 1 je 2926 k. J na 1 mol {HCOH} v němž je vloženo 470 k. J dává 470 : 2493 = 0, 16.

Účinnost energetická, tj. jaký podíl energie, která do reakce vstoupila (příkon záření) je uložen v produktu (výkon), a dá se z něho uvolnit (např. jako spalné teplo HCOH) tedy (energie získaná) k. J/(energie vložená) k. J to je bezrozměrné číslo a často se vyjadřuje v procentech

Pro výpočet maximální možné energetické účinnosti fotosyntézy, musíme znát minimální počet kvant potřebných pro asimilaci jedné molekuly CO 2, případně pro vyloučení jedné molekuly O 2. K tomu je třeba celým řetězcem přenosu elektronů oxygenní fotosyntézy přenést nejméně čtyři elektrony. Řetězec zahrnuje fotosystém 1 a fotosystém 2, je tedy na přenesení čtyř elektronů potřeba osm fotonů, které se pohltily a v reakčních centrech rozdělily náboje. Připočteme-li nutné ztráty, pak jsou důvěryhodné výsledky měření, které udávají 10 až 12 kvant záření na 1 molekulu kyslíku (nebo CO 2). Vypočteme tedy maximální energetickou účinnost fotosyntézy jednak pro teoretický nejnižší počet osmi přeměněných kvant, jednak pro experimentálně podložený počet 12 kvant.

Pro asimilaci jedné molekuly CO 2 Calvinovým cyklem je třeba dodat 2 molekuly NADPH+H+ a 3 ATP. Zda tento nárok mohou splnit čtyři elektrony prošlé řetězcem oxygenní fotosyntézy závisí na tom, pracuje-li v cyt b 6 /f komplexu Q-cyklus nebo ne. Pokud ano, dojde při přenosu dvou elektronů řetězcem k přesunu šesti protonů přes membránu a souběžně s redukcí dvou NADP na NADPH+H+ se přes membránu přepraví 12 protonů, tedy dost pro syntézu 3 ATP. Pokud Q-cyklus nepracuje, sníží se poměr P/2 e na 4 a úhrnný počet přesunutých protonů na 8, což pro syntézu 3 ATP nepostačuje. V tom případě se patrně musí další fotony uplatnit v cyklickém přenosu elektronů kolem fotosystému 1, který vede k tzv. cyklické fosforylaci a zlepší poměr nabídky ATP k NADPH+H+. To může být jedna z příčin vyší potřeby kvant na 1 mol CO 2.

Všechna kvanta, která chlorofyl absorbuje mají stejný fotochemický účinek. Mají však různý obsah energie. Fotochemická reakce nemůže svázat větší množství energie, než které nese foton nejchudší na energii, který ještě excituje chlorofyl. Energie, o kterou jsou fotony vyšších kmitočtů (kratších vlnových délek) bohatší, se ztrácí jako teplo. Energeticky nejúčinnější ve fotosyntéze bude tedy přeměna fotonů nejchudších energií, tedy červených. Chceme-li spočítat teoreticky nejvyšší možnou účinnost fotosyntézy budeme uvažovat tyto fotony. Současně ukážeme, jak se tato účinnost změní, pokud se budou ve fotosyntéze využívat fotony s průměrným obsahem energie, tedy zelené, což přibližně odpovídá průměrné energii jednoho fotonu v bílém (tedy všebarevném) světle.

Elektrony při fotochemickém přenosu v thylakoidu překonávají týž úhrnný rozdíl v oxidoredukčním potenciálu jako elektrony v membráně mitochondrií, od páru voda/kyslík k páru NADPH+H+/NADP, tedy 1, 14 V. Celkem tedy nahromadí 4 96, 5 1, 14 = 440 k. J. K tomu je třeba přičíst ještě energii uloženou v makroergických vazbách tří molů ATP a to je přibližně 3 55 = 165 k. J, takže úhrnem se v těchto membránových pochodech nahromadí 440 + 165 = 605 k. J.

Jaká je maximální možná účinnost membránových pochodů fotosyntézy a účinnost přeměny zářivé energie pro celou fotosyntézu, včetně asimilace CO 2 Calvinovým cyklem ukazuje Tab. 2. V tabulce jsou uvedeny hodnoty, při jejichž výpočtu se počítalo s tím, že obsah energie uložené v sacharidu jako produktu fotosyntézy, je 470 k. J na jednouhlíkový článek sacharidu, který označujeme HCOH nebo CH 2 O. Energie nahromaděná v produktech membránových pochodů, které se využijí na redukci 1 molu CO 2 , tj. 3 ATP a 2 (NADPH+H+) je přibližně 600 k. J, Z toho plyne, že účinnost biochemických pochodů Calvinova cyklu = 470 / 600 = 0, 78 čili 78%.
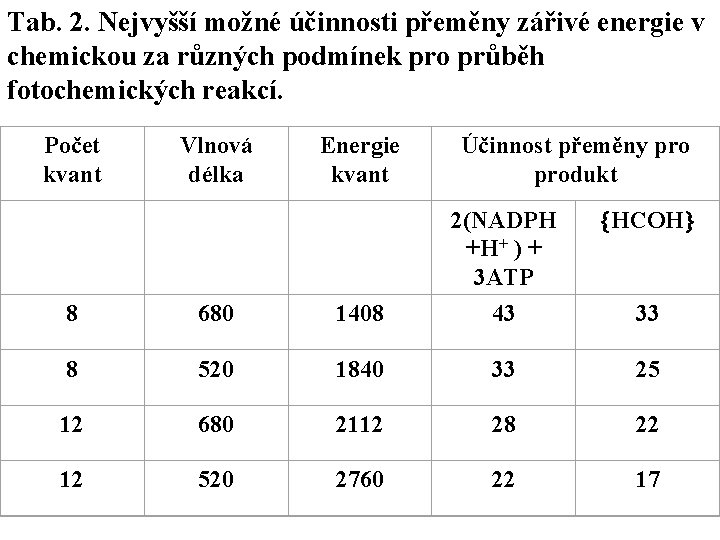
Tab. 2. Nejvyšší možné účinnosti přeměny zářivé energie v chemickou za různých podmínek pro průběh fotochemických reakcí. Počet kvant Vlnová délka Energie kvant Účinnost přeměny produkt 2(NADPH +H+ ) + 3 ATP HCOH 8 680 1408 43 33 8 520 1840 33 25 12 680 2112 28 22 12 520 2760 22 17
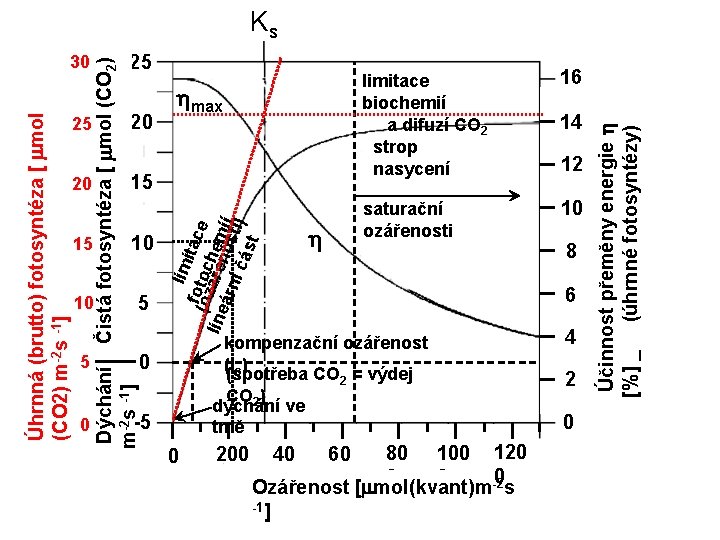
15 15 10 10 5 5 0 h limitace biochemií a difuzí CO 2 strop nasycení 16 saturační ozářenosti 10 kompenzační ozářenost (Ic) (spotřeba CO 2 = výdej CO 2) dýchání ve tmě 0 -5 0 200 80 100 120 40 60 0 0 [ mol(kvant)m -2 Ozářenost s -1] 14 12 8 6 4 2 0 Účinnost přeměny energie h [%] _ (úhrnné fotosyntézy) 20 20 hmax lim itac t e (ofo o hem line zářecn árn os íí í čá tí) st 25 25 Dýchání m-2 s -1] Úhrnná (brutto) fotosyntéza [ mol (CO 2) m-2 s -1] 30 Čistá fotosyntéza [ mol (CO 2) Ks

- Slides: 47