ALKANA 1 2 Alkana senyawa organik yang miskin










![Penentuan bilangan oksidasi ] 1. Untuk setiap atom dalam ikatan, atom elektropositif bilangan oksidasinya Penentuan bilangan oksidasi ] 1. Untuk setiap atom dalam ikatan, atom elektropositif bilangan oksidasinya](https://slidetodoc.com/presentation_image_h2/4847cda4fc8aed5bace9dc93b28fcc60/image-31.jpg)

- Slides: 36

ALKANA 1

2

Alkana : senyawa organik yang miskin gugus fungsi Alkana umumnya non polar dan tak reaktif How to make “alkana” more useful in organic synthesis? Functionalization 3

Review Jenis pemutusan ikatan: - homolitik (terjadi pada pelarut non polar dan fasa gas) - heterolitik (terjadi pada pelarut polar dan terbatas pada situasi di mana keelektronegatifan A dan B dan gugus-gugus yang terikat pada mereka saling menstabilkan muatan (+) dan (-)) Kestabilan radikal menentukan kekuatan ikatan C-H Energi ikatan kekuatan berkurang : CH 4> 1 o. C > 2 o. C > 3 o. C Kestabilan radikal ditentukan oleh delokalisasi elektron di mana orbital p pada pusat radikal overlapping dengan ikatan C-H di sebelahnya ……… hiperkonyugasi >>>struktur hampir planar, dengan posisi elektron tunggal pada orbital p pada posisi tegak lurus terhadap bidang molekul 4

Resonansi dan hiperkonyugasi: - pada keduanya terjadi interaksi elektron pada orbital p yang memberikan delokalisasi elektron stabil - terdapat perbedaan pada tipe orbital: pada resonansi tipe p overlap dengan orbital p pada hiperkonyugasi overlap orbital-orbital ikatan tipe s Kestabilan radikal -pengaruh terjejalnya halangan antara substituen-substituen pada radikal alkil sekunder dan alkil tersier (steric crowding) yang semakin leluasa karena pengaruh perubahan geometri tetrahedral planar (dalam radikal) (pada radikal tersier, substituen-substituen semakin berjauhan halangan sterik makin berkurang, jadi makin stabil) 5

6

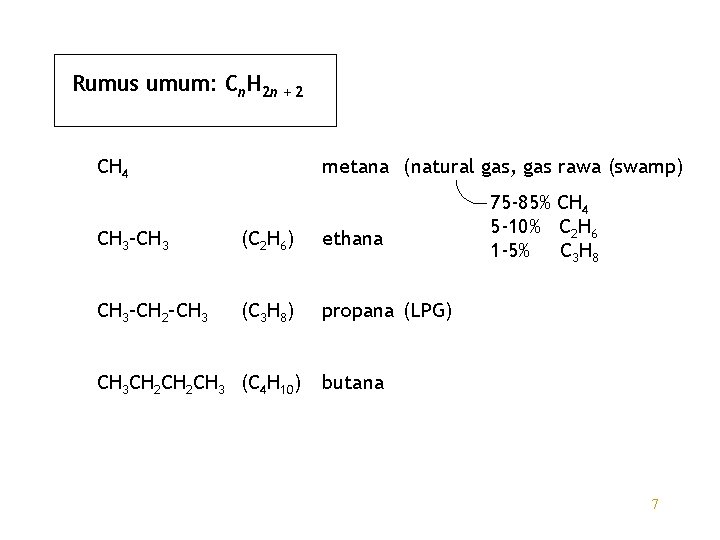
Rumus umum: Cn. H 2 n + 2 CH 4 metana (natural gas, gas rawa (swamp) CH 3–CH 3 (C 2 H 6) ethana CH 3–CH 2–CH 3 (C 3 H 8) propana (LPG) CH 3 CH 2 CH 3 (C 4 H 10) 75 -85% CH 4 5 -10% C 2 H 6 1 -5% C 3 H 8 butana 7

8

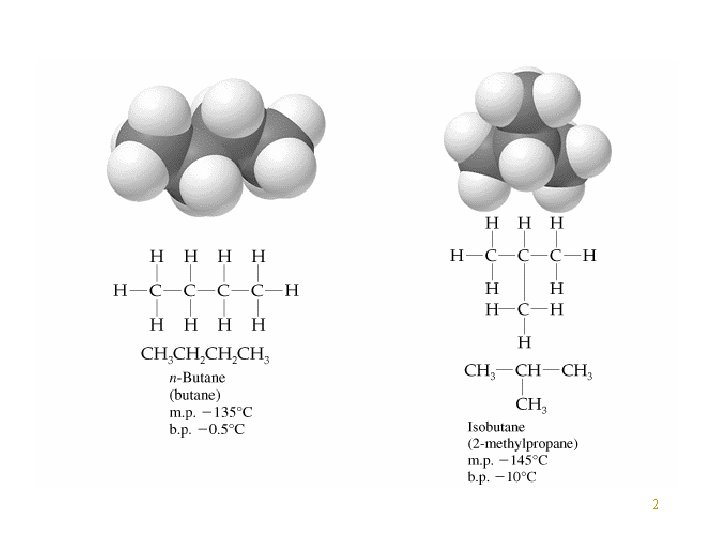
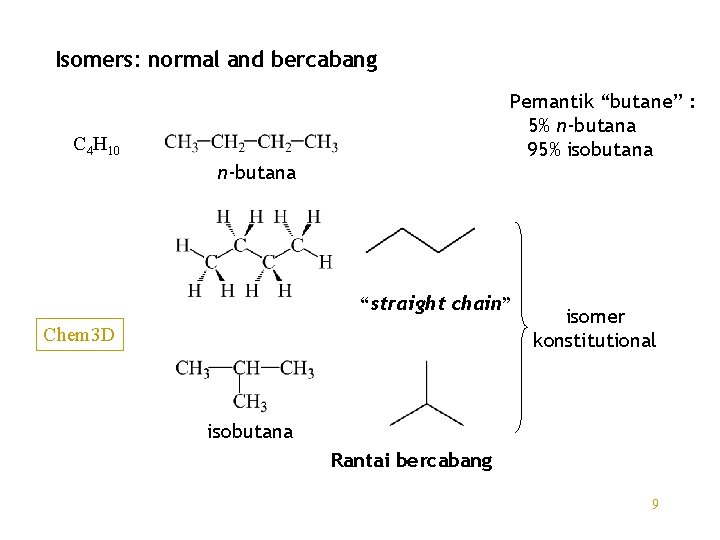
Isomers: normal and bercabang Pemantik “butane” : 5% n-butana 95% isobutana C 4 H 10 n-butana “straight chain” Chem 3 D isomer konstitutional isobutana Rantai bercabang 9

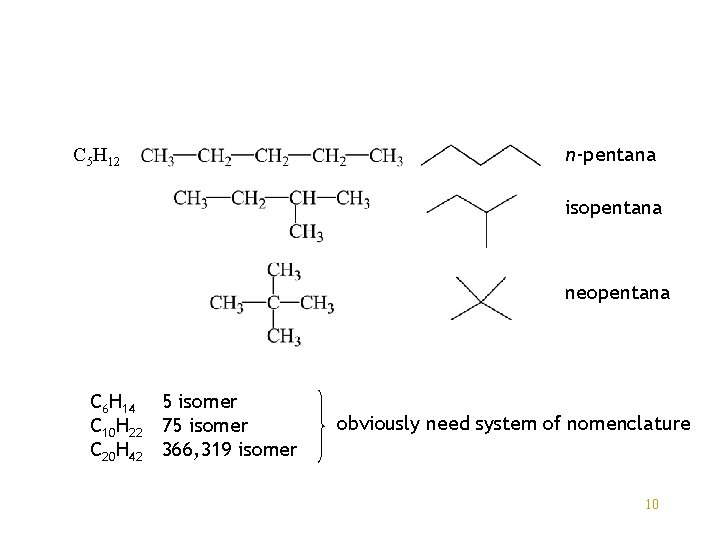
C 5 H 12 n-pentana isopentana neopentana C 6 H 14 5 isomer C 10 H 22 75 isomer C 20 H 42 366, 319 isomer obviously need system of nomenclature 10

Contoh soal: Gambarkan isomer konstitusional berikut. C 6 H 14 (5) C 7 H 16 (9) Check Answer 11

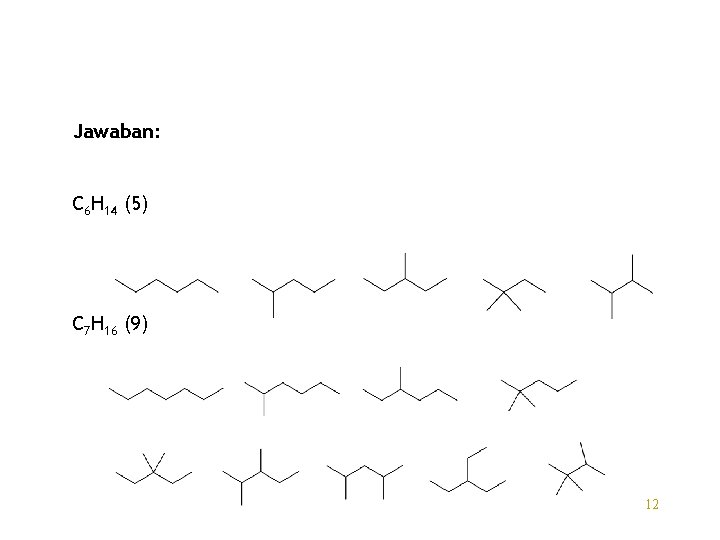
Jawaban: C 6 H 14 (5) C 7 H 16 (9) 12

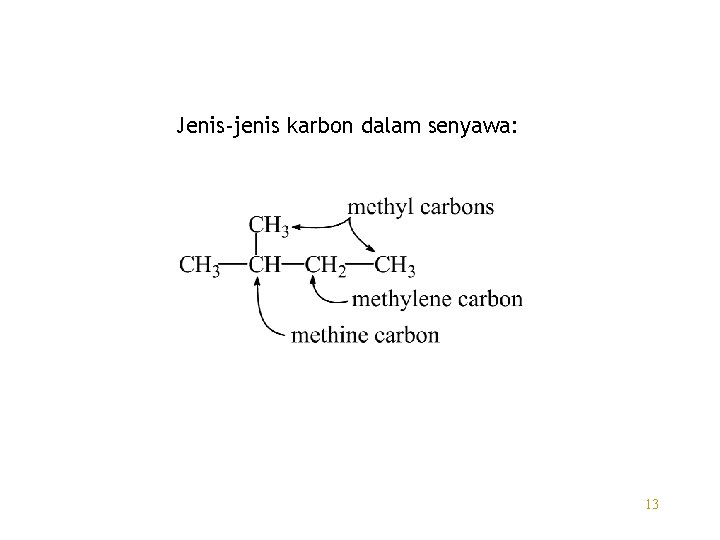
Jenis-jenis karbon dalam senyawa: 13

Senyawa hidrokarbon hanya mengandung karbon dan hidrogen : ikatan tunggal (ikatan s) …………. Alkana Cn. H 2 n+2 Ø Hidrokarbon jenuh Ø Hidrokarbon tak jenuh : mengandung ikatan ganda (ikatan p) ……Cn. H 2 n Ø Hidrokarbon alifatik : rantai terbuka (lurus atau bercabang) Ø Hidrokarbon siklik : Cn. H 2 n Cincin atau ikatan rangkap mengurangi 2 H pada ikatan rangkap atau tiap cincin Contoh: CH 3 CH 2 CH 3 CH 2 CH=CH 2 C 4 H 10 C 4 H 8 Cn. H 2 n C 4 H 8 mengandung 1 double bond equivalen (DBE) atau 1 ikatan rangkap atau 1 cincin Cn. H 2 n-2 mengandung 2 double bond equivalen (DBE) atau 1 ikatan rangkap, 1 cincin, 2 ikatan rangkap, atau 2 cincin 14

15

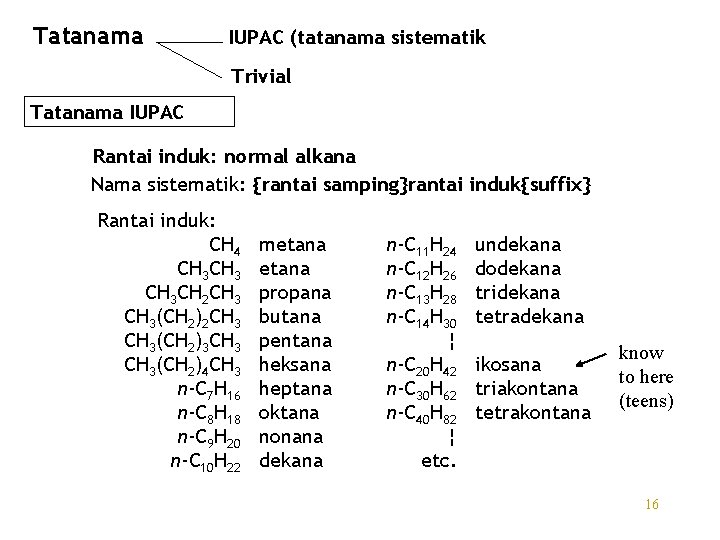
Tatanama IUPAC (tatanama sistematik Trivial Tatanama IUPAC Rantai induk: normal alkana Nama sistematik: {rantai samping}rantai induk{suffix} Rantai induk: CH 4 CH 3 CH 2 CH 3(CH 2)3 CH 3(CH 2)4 CH 3 n-C 7 H 16 n-C 8 H 18 n-C 9 H 20 n-C 10 H 22 metana propana butana pentana heksana heptana oktana nonana dekana n-C 11 H 24 n-C 12 H 26 n-C 13 H 28 n-C 14 H 30 ¦ n-C 20 H 42 n-C 30 H 62 n-C 40 H 82 ¦ etc. undekana dodekana tridekana tetradekana ikosana triakontana tetrakontana know to here (teens) 16

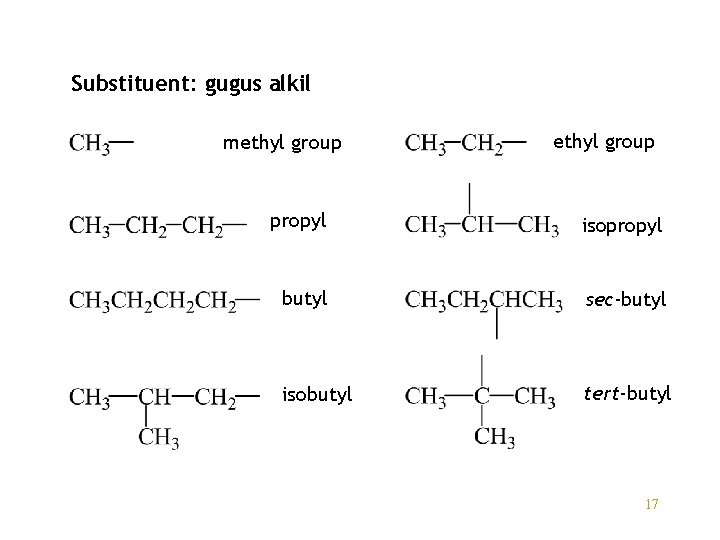
Substituent: gugus alkil methyl group propyl isopropyl butyl sec-butyl isobutyl tert-butyl 17

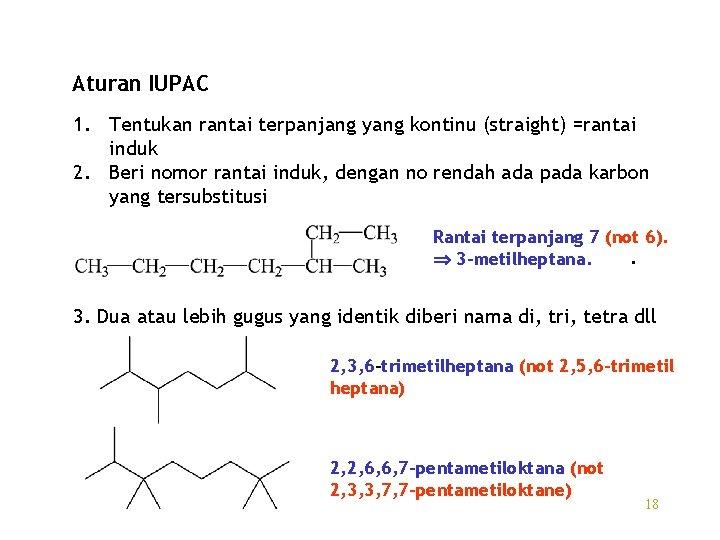
Aturan IUPAC 1. Tentukan rantai terpanjang yang kontinu (straight) =rantai induk 2. Beri nomor rantai induk, dengan no rendah ada pada karbon yang tersubstitusi Rantai terpanjang 7 (not 6). . 3 -metilheptana. 3. Dua atau lebih gugus yang identik diberi nama di, tri, tetra dll 2, 3, 6 -trimetilheptana (not 2, 5, 6 -trimetil heptana) 2, 2, 6, 6, 7 -pentametiloktana (not 2, 3, 3, 7, 7 -pentametiloktane) 18

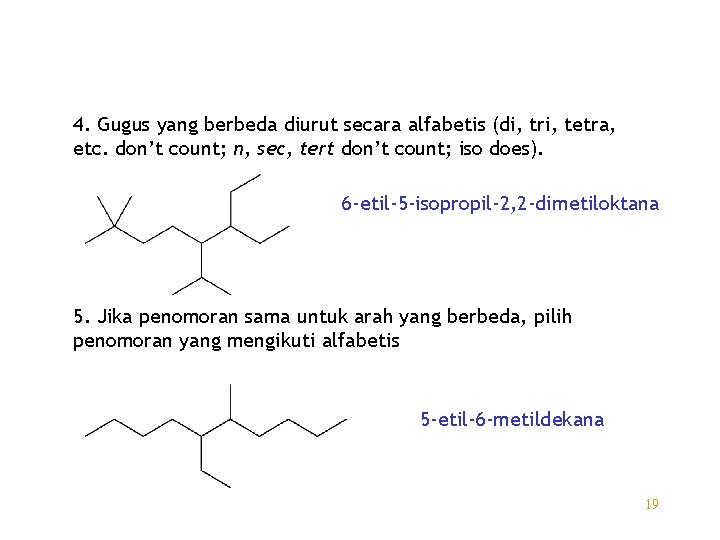
4. Gugus yang berbeda diurut secara alfabetis (di, tri, tetra, etc. don’t count; n, sec, tert don’t count; iso does). 6 -etil-5 -isopropil-2, 2 -dimetiloktana 5. Jika penomoran sama untuk arah yang berbeda, pilih penomoran yang mengikuti alfabetis 5 -etil-6 -metildekana 19

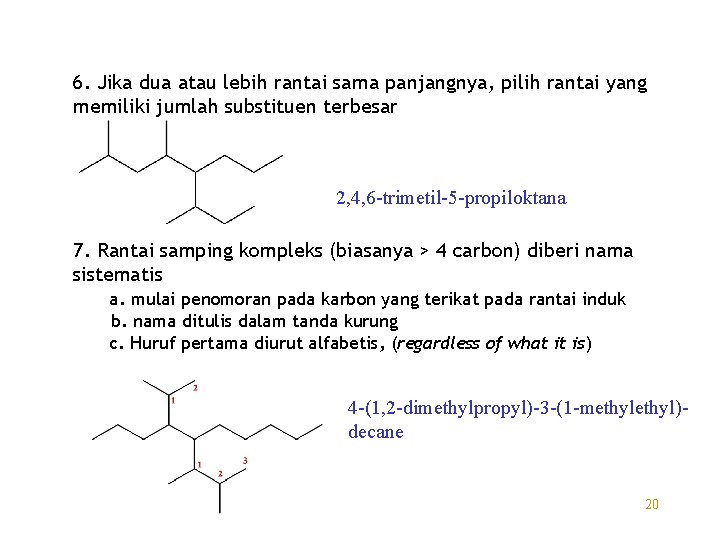
6. Jika dua atau lebih rantai sama panjangnya, pilih rantai yang memiliki jumlah substituen terbesar 2, 4, 6 -trimetil-5 -propiloktana 7. Rantai samping kompleks (biasanya > 4 carbon) diberi nama sistematis a. mulai penomoran pada karbon yang terikat pada rantai induk b. nama ditulis dalam tanda kurung c. Huruf pertama diurut alfabetis, (regardless of what it is) 4 -(1, 2 -dimethylpropyl)-3 -(1 -methyl)decane 20

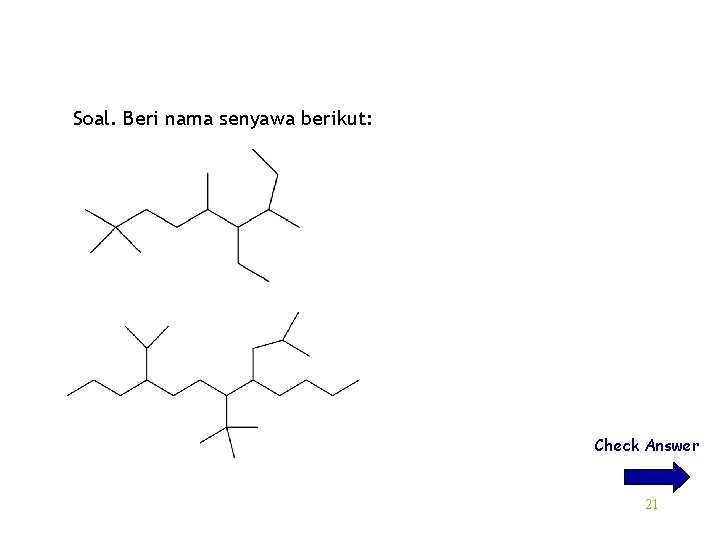
Soal. Beri nama senyawa berikut: Check Answer 21

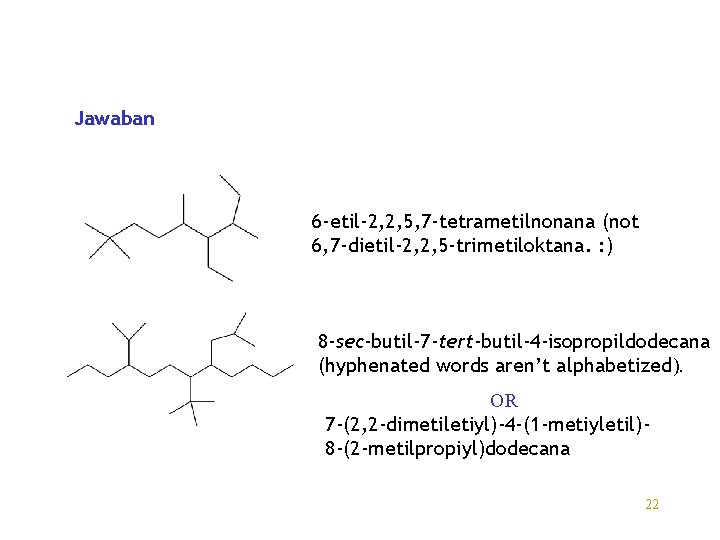
Jawaban 6 -etil-2, 2, 5, 7 -tetrametilnonana (not 6, 7 -dietil-2, 2, 5 -trimetiloktana. : ) 8 -sec-butil-7 -tert-butil-4 -isopropildodecana (hyphenated words aren’t alphabetized). OR 7 -(2, 2 -dimetiletiyl)-4 -(1 -metiyletil)8 -(2 -metilpropiyl)dodecana 22

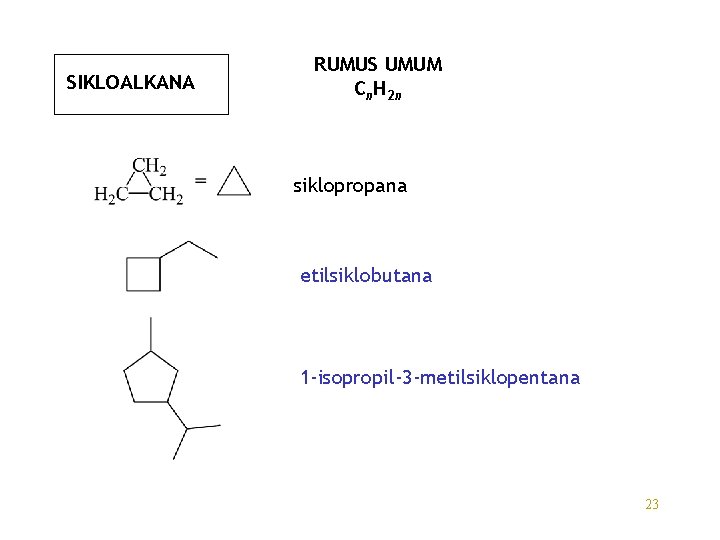
SIKLOALKANA RUMUS UMUM Cn. H 2 n siklopropana etilsiklobutana 1 -isopropil-3 -metilsiklopentana 23

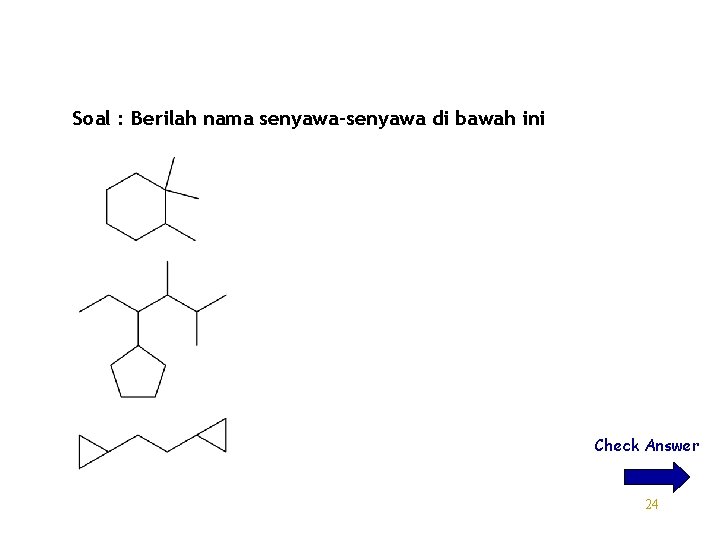
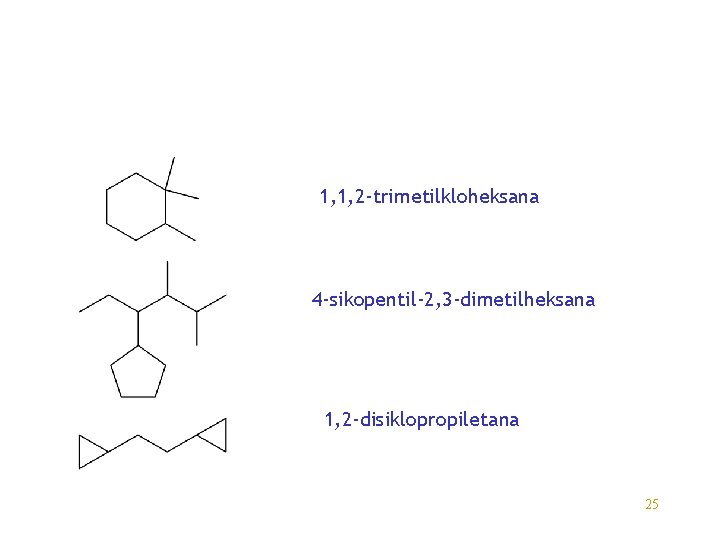
Soal : Berilah nama senyawa-senyawa di bawah ini Check Answer 24

1, 1, 2 -trimetilkloheksana 4 -sikopentil-2, 3 -dimetilheksana 1, 2 -disiklopropiletana 25

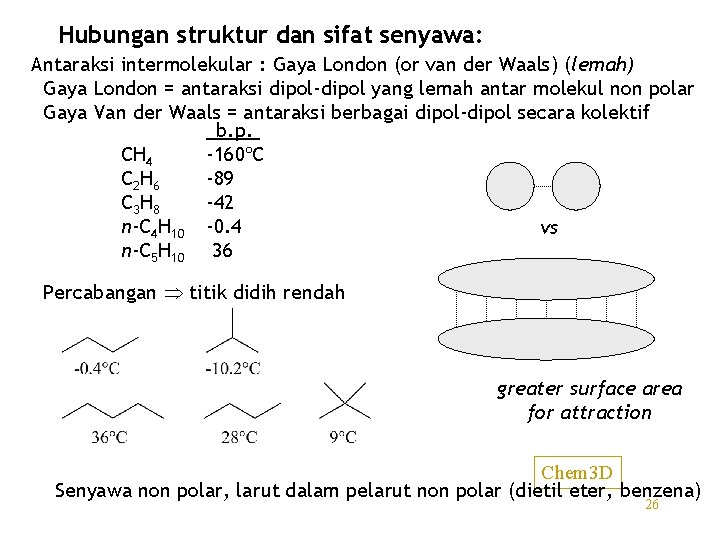
Hubungan struktur dan sifat senyawa: Antaraksi intermolekular : Gaya London (or van der Waals) (lemah) Gaya London = antaraksi dipol-dipol yang lemah antar molekul non polar Gaya Van der Waals = antaraksi berbagai dipol-dipol secara kolektif b. p. CH 4 -160ºC C 2 H 6 -89 C 3 H 8 -42 n-C 4 H 10 -0. 4 vs n-C 5 H 10 36 Percabangan titik didih rendah greater surface area for attraction Chem 3 D Senyawa non polar, larut dalam pelarut non polar (dietil eter, benzena) 26

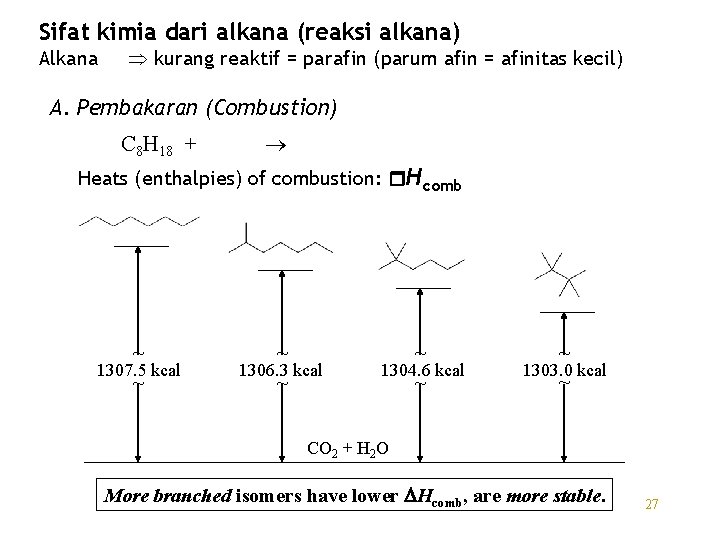
Sifat kimia dari alkana (reaksi alkana) Alkana kurang reaktif = parafin (parum afin = afinitas kecil) A. Pembakaran (Combustion) C 8 H 18 + Heats (enthalpies) of combustion: Hcomb ~ 1307. 5 kcal ~ ~ 1306. 3 kcal ~ ~ 1304. 6 kcal ~ ~ 1303. 0 kcal ~ CO 2 + H 2 O More branched isomers have lower DHcomb, are more stable. 27

B. Reaksi halogenasi 250 o. C – 400 o. C sinar CH 4 + X 2 CH 3 X + HX Reaktivitas X 2 : Cl 2> Br 2 (iodinasi tak terjadi) H : 3 o > 2 o > 1 o 250 o. C – 400 o. C sinar CH 4 + Cl 2 CH 3 Cl + HCl 28

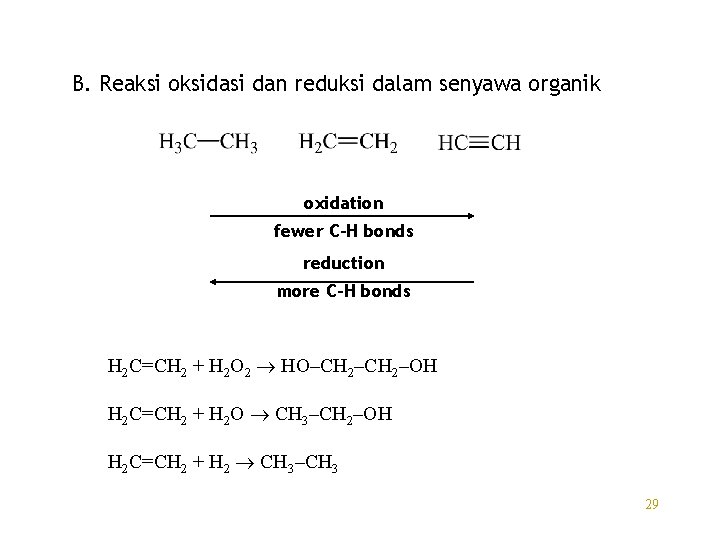
B. Reaksi oksidasi dan reduksi dalam senyawa organik oxidation fewer C-H bonds reduction more C-H bonds H 2 C=CH 2 + H 2 O 2 HO–CH 2–OH H 2 C=CH 2 + H 2 O CH 3–CH 2–OH H 2 C=CH 2 + H 2 CH 3–CH 3 29

30
![Penentuan bilangan oksidasi 1 Untuk setiap atom dalam ikatan atom elektropositif bilangan oksidasinya Penentuan bilangan oksidasi ] 1. Untuk setiap atom dalam ikatan, atom elektropositif bilangan oksidasinya](https://slidetodoc.com/presentation_image_h2/4847cda4fc8aed5bace9dc93b28fcc60/image-31.jpg)
Penentuan bilangan oksidasi ] 1. Untuk setiap atom dalam ikatan, atom elektropositif bilangan oksidasinya +1, dan atom yang elektronegatif bilangan oksidasi -1 (If the atoms are the same, each atom gets a 0. ) 2. Jumlah atom total. Oxidation number of carbon is +1 +1 +1 -1 = +2 31

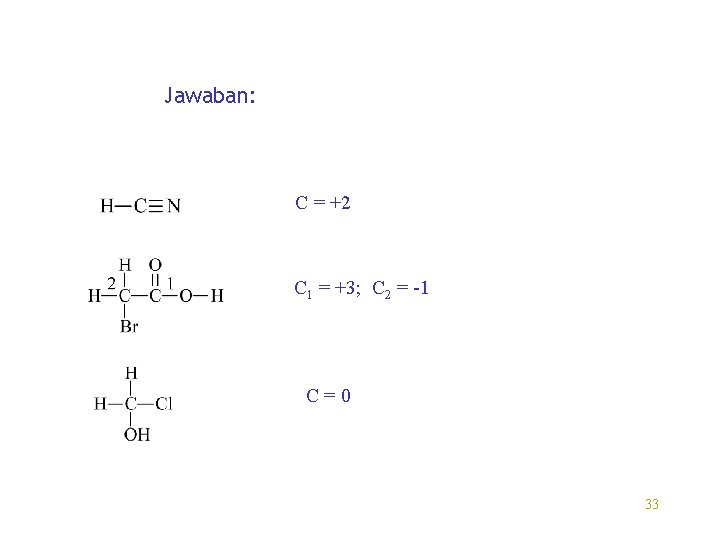
Soal : tentukan bilangan oksidasi untuk karbon dalam tiap molekul Check Answer 32

Jawaban: C = +2 C 1 = +3; C 2 = -1 C=0 33

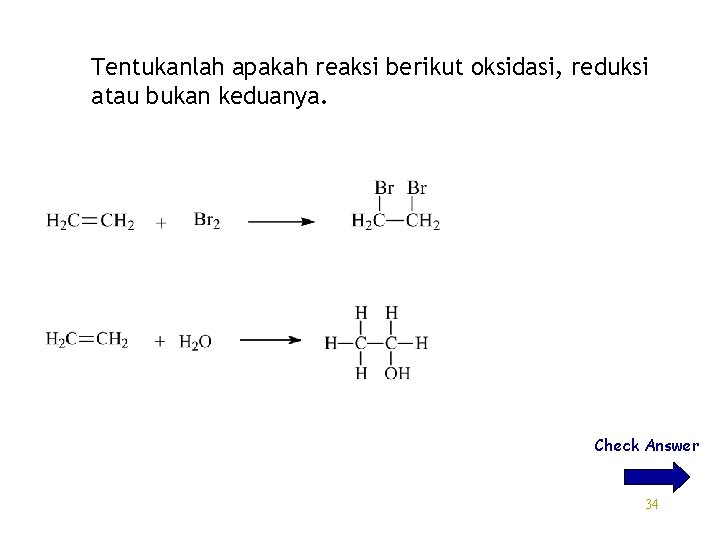
Tentukanlah apakah reaksi berikut oksidasi, reduksi atau bukan keduanya. Check Answer 34

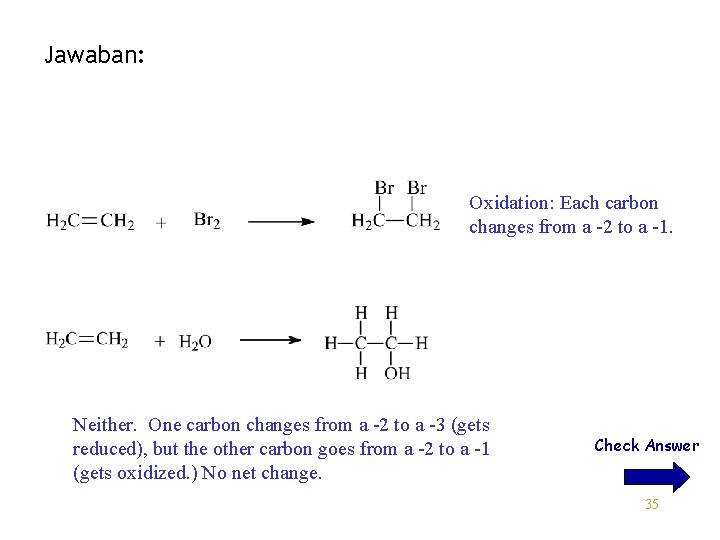
Jawaban: Oxidation: Each carbon changes from a -2 to a -1. Neither. One carbon changes from a -2 to a -3 (gets reduced), but the other carbon goes from a -2 to a -1 (gets oxidized. ) No net change. Check Answer 35

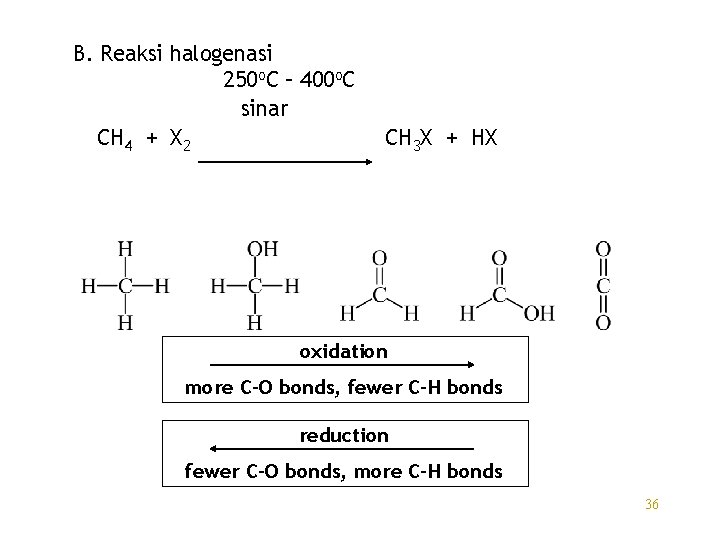
B. Reaksi halogenasi 250 o. C – 400 o. C sinar CH 4 + X 2 CH 3 X + HX oxidation more C-O bonds, fewer C-H bonds reduction fewer C-O bonds, more C-H bonds 36