Aktuality ve farmakoterapii diabetu Marek Honka Diabetologick centrum

Aktuality ve farmakoterapii diabetu Marek Honka Diabetologické centrum FN Ostrava

Přehled sdělení ü Strategie léčby diabetu 2. typu ü Účinky metforminu mimo metabolismus sacharidů ü Léčiva odvozená od účinku inkretinů ü Perspektiva glitazonů po „pádu“ rosiglitazonu

Reflexe výsledků UKPDS-ACCORD-ADVANCE v současné strategii léčby DM 2. typu • prokázán dlouhodobý efekt kompenzace i pro diabetes 2. typu • intenzivní intervence od začátku onemocnění nejefektivnější • opožděná intervence nesmí být spojena nárůstem rizika hypoglykémie s

Intervence ve vztahu ke KVS riziku • přínos jednotlivých intervencí se u DM 2. typu sčítá • účinek intervence narůstá s časem (lineárně - exponenciálně? ) • z intenzivní léčby profitují zejména osoby: • s nižším vstupním Hb. A 1 c • s kratším trváním diabetu • bez přítomnosti mikro a makrovaskulárního postižení
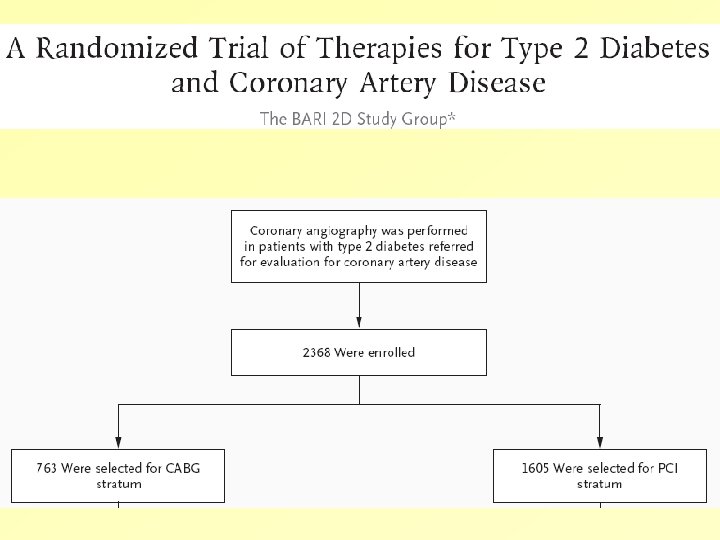

Intervence ve vztahu ke KVS riziku • U osob s poškozeným cévním řečištěm ani sebelepší instrumentální výkon příliš nezlepší prognosu quo ad vitam
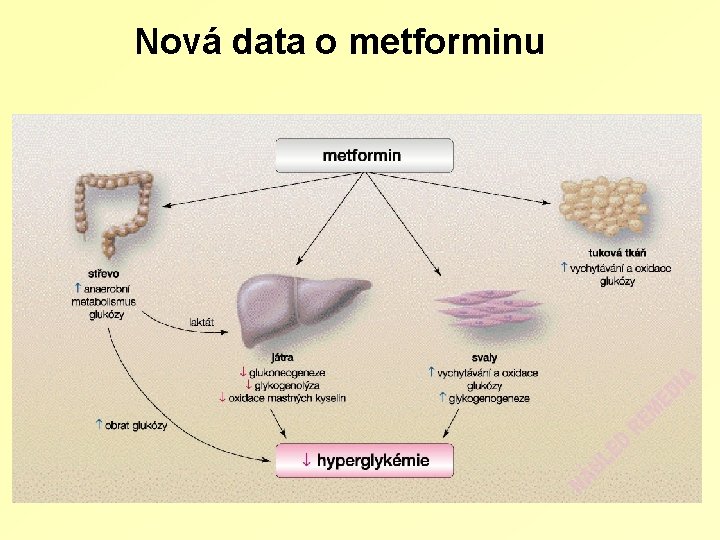
Nová data o metforminu
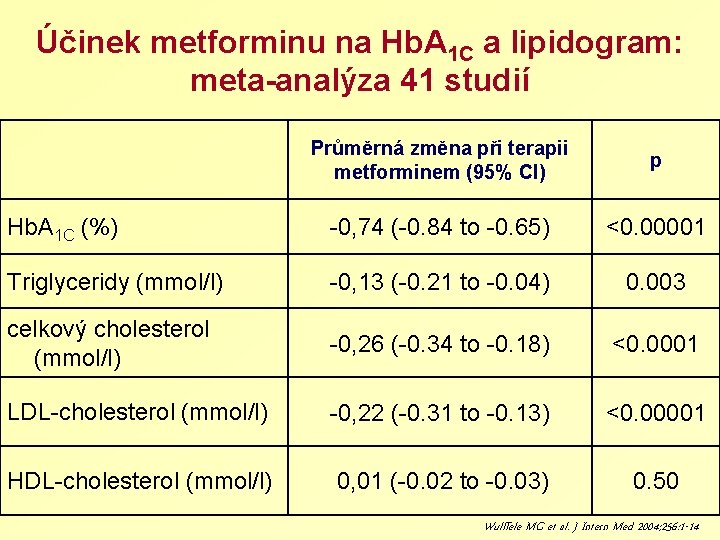
Účinek metforminu na Hb. A 1 C a lipidogram: meta-analýza 41 studií Průměrná změna při terapii metforminem (95% CI) p Hb. A 1 C (%) -0, 74 (-0. 84 to -0. 65) <0. 00001 Triglyceridy (mmol/l) -0, 13 (-0. 21 to -0. 04) 0. 003 celkový cholesterol (mmol/l) -0, 26 (-0. 34 to -0. 18) <0. 0001 LDL-cholesterol (mmol/l) -0, 22 (-0. 31 to -0. 13) <0. 00001 HDL-cholesterol (mmol/l) 0, 01 (-0. 02 to -0. 03) 0. 50 Wulffele MG et al. J Intern Med 2004; 256: 1 -14
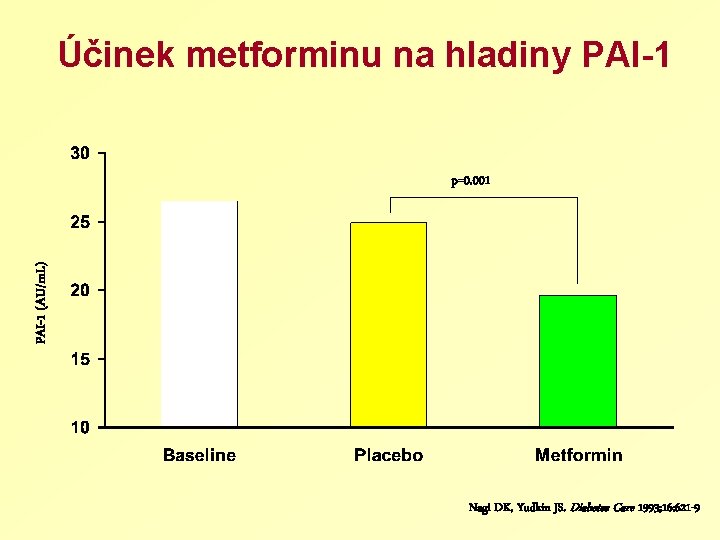
Účinek metforminu na hladiny PAI-1 (AU/m. L) p=0. 001 Nagi DK, Yudkin JS. Diabetes Care 1993; 16: 621 -9
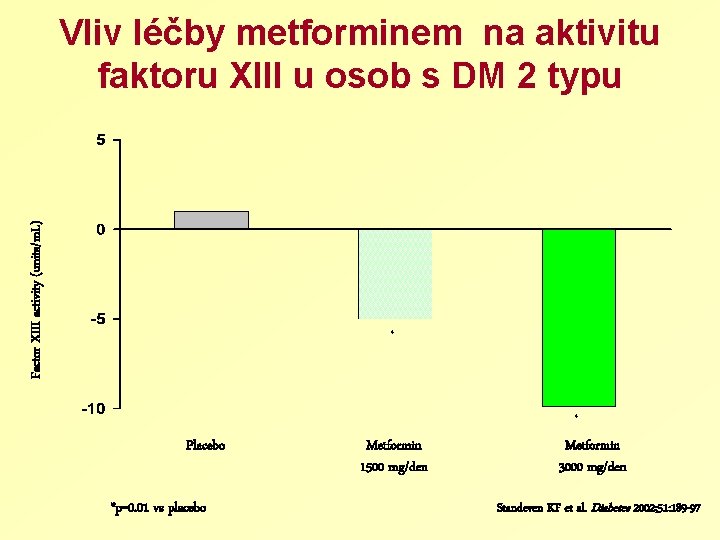
Factor XIII activity (units/m. L) Vliv léčby metforminem na aktivitu faktoru XIII u osob s DM 2 typu * Placebo *p=0. 01 vs placebo Metformin 1500 mg/den * Metformin 3000 mg/den Standeven KF et al. Diabetes 2002; 51: 189 -97
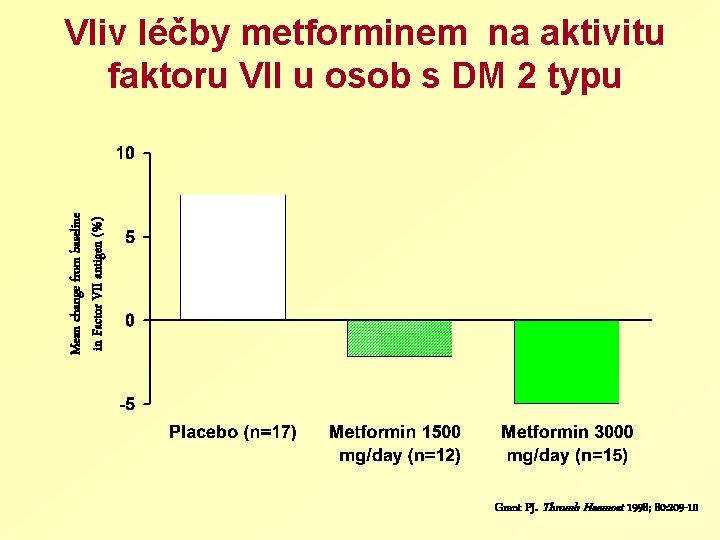
Mean change from baseline in Factor VII antigen (%) Vliv léčby metforminem na aktivitu faktoru VII u osob s DM 2 typu Grant PJ. Thromb Haemost 1998; 80: 209 -10

Další antiaterogenní účinky metforminu Účinek Potenciální přínos Oxidace Apoptózy, oxidativního poškození pozdních produktů glykace zánětu, oxidačního stresu/apoptózy exprese adhezních molekul na povrchu buněk endotelu Aterogeneze aktivace monocytů → makrofágy Aterogeneze vychytávání lipidů makrofágy Aterogeneze Kurukulasuriya R et al. Diabetes 1999; 48 Suppl: A 315; Beisswenger P et al. Diabetes Metab 2003; 29: 6 S 95 -103; Pavlović D et al. Diabetes Obes Metab 2000; 2: 251 -6; Mamputu JC et al. Diabetes Metab 2003; 29: 6 S 71 -6. Wiernsperger NF et al. Diabetes Metab 2003; 29: 6 S 77 -87
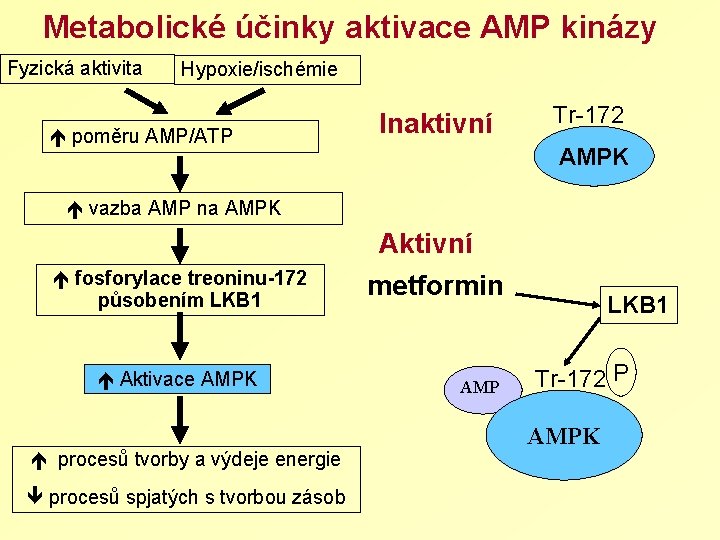
Metabolické účinky aktivace AMP kinázy Fyzická aktivita Hypoxie/ischémie poměru AMP/ATP Inaktivní Tr-172 AMPK vazba AMP na AMPK Aktivní fosforylace treoninu-172 působením LKB 1 Aktivace AMPK procesů tvorby a výdeje energie procesů spjatých s tvorbou zásob metformin AMP LKB 1 Tr-172 P AMPK

Aktivace AMP- kinázy 1) Ve vztahu k diabetu ü výdej glukózy játry ü vychytávání glukózy tkáněmi ü udržuje senzitivitu tkání k inzulínu ü Snižuje hladinu glykémie 2) Ve vztahu k buněčnému růstu? ü antianabolická/prokatabolická úloha ü mediátor přirozených supresorů kancerogeneze ü zpomaluje/zastavuje aberantní buněčný růst
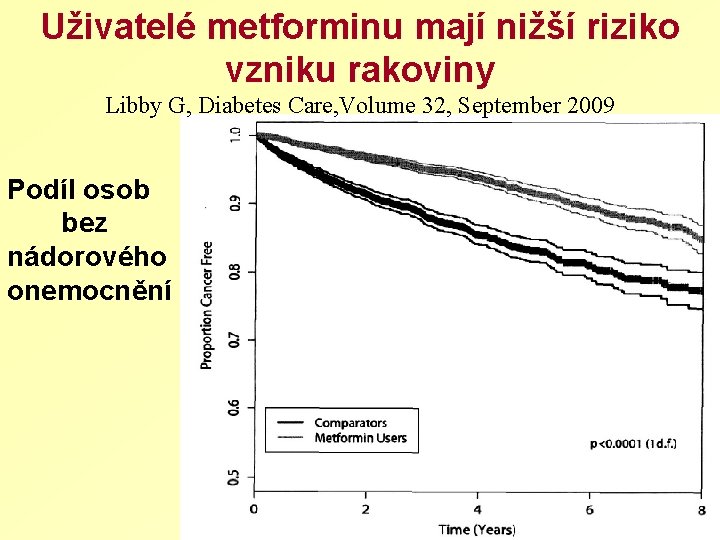
Uživatelé metforminu mají nižší riziko vzniku rakoviny Libby G, Diabetes Care, Volume 32, September 2009 Podíl osob bez nádorového onemocnění
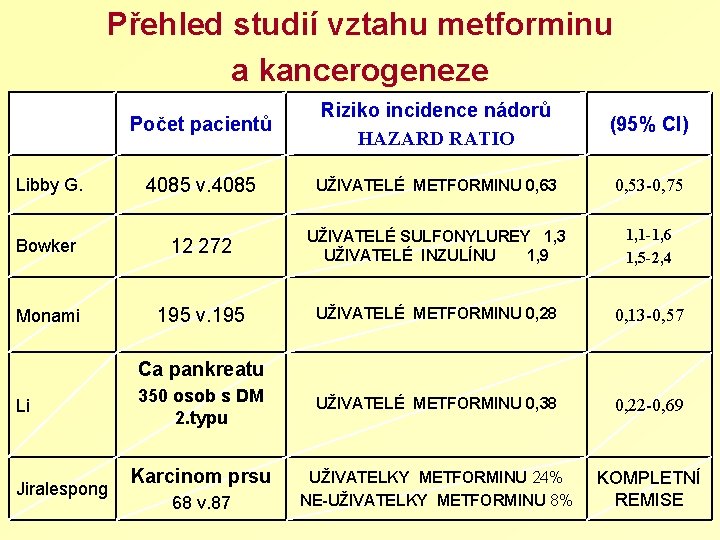
Přehled studií vztahu metforminu a kancerogeneze Počet pacientů Riziko incidence nádorů HAZARD RATIO (95% CI) Libby G. 4085 v. 4085 UŽIVATELÉ METFORMINU 0, 63 0, 53 -0, 75 Bowker 12 272 UŽIVATELÉ SULFONYLUREY 1, 3 UŽIVATELÉ INZULÍNU 1, 9 1, 1 -1, 6 1, 5 -2, 4 Monami 195 v. 195 UŽIVATELÉ METFORMINU 0, 28 0, 13 -0, 57 UŽIVATELÉ METFORMINU 0, 38 0, 22 -0, 69 UŽIVATELKY METFORMINU 24% NE-UŽIVATELKY METFORMINU 8% KOMPLETNÍ REMISE Ca pankreatu Li Jiralespong 350 osob s DM 2. typu Karcinom prsu 68 v. 87
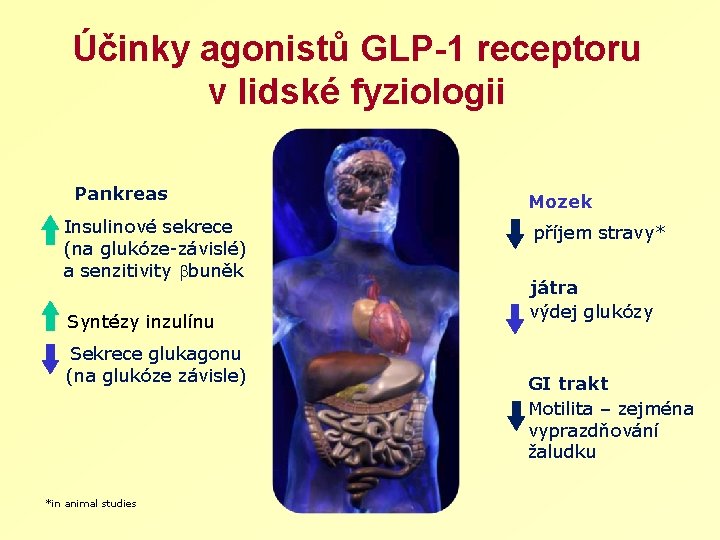
Účinky agonistů GLP-1 receptoru v lidské fyziologii Pankreas Insulinové sekrece (na glukóze-závislé) a senzitivity buněk Syntézy inzulínu Sekrece glukagonu (na glukóze závisle) *in animal studies Mozek příjem stravy* játra výdej glukózy GI trakt Motilita – zejména vyprazdňování žaludku

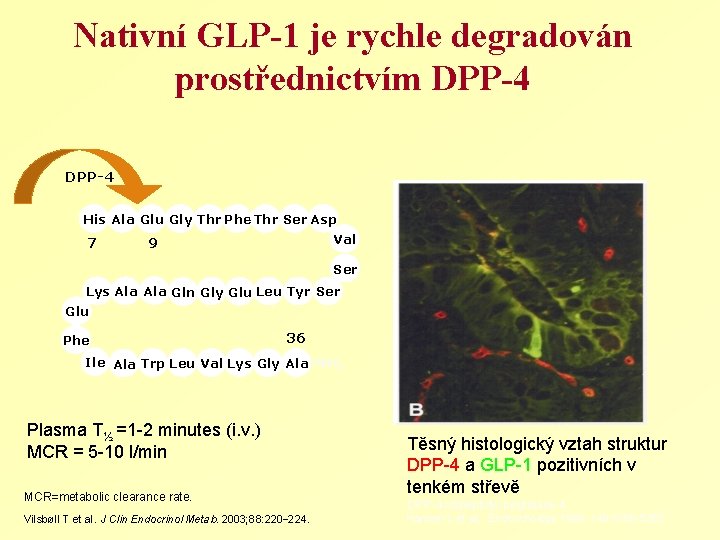
Nativní GLP-1 je rychle degradován prostřednictvím DPP-4 His Ala Glu Gly Thr Phe Thr Ser Asp 7 Val 9 Ser Lys Ala Gln Gly Glu Leu Tyr Ser Glu Phe 36 Ile Ala Trp Leu Val Lys Gly Ala -NH 2 Plasma T½ =1 -2 minutes (i. v. ) MCR = 5 -10 l/min MCR=metabolic clearance rate. Vilsbøll T et al. J Clin Endocrinol Metab. 2003; 88: 220– 224. Těsný histologický vztah struktur DPP-4 a GLP-1 pozitivních v tenkém střevě DPP-4=dipeptidyl peptidase 4 Hansen L et al, Endocrinology 1999; 140: 5356 -5363
Struktura dipeptidyl peptidázy - 4
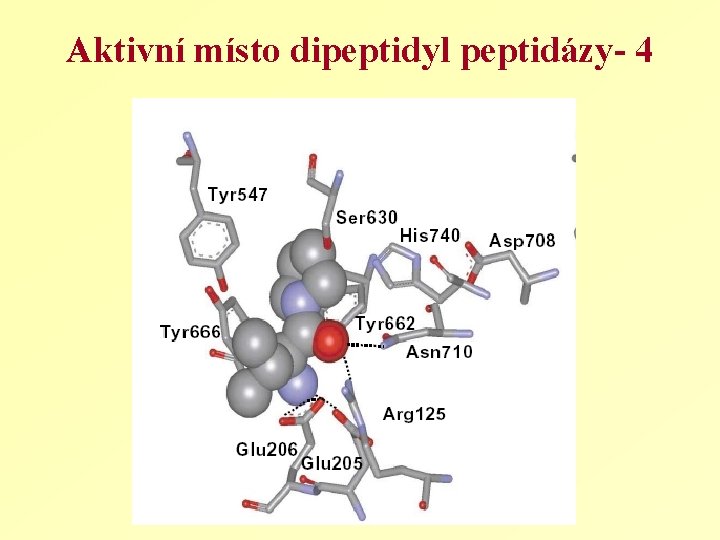
Aktivní místo dipeptidyl peptidázy- 4
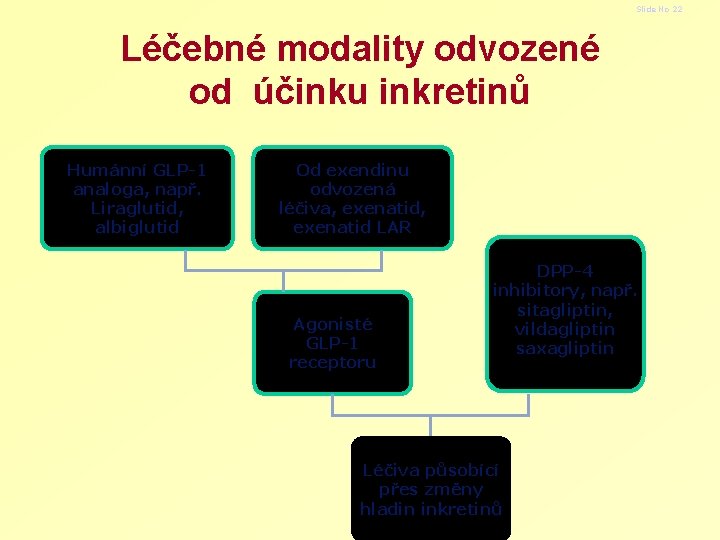
Slide No 22 Léčebné modality odvozené od účinku inkretinů Humánní GLP-1 analoga, např. Liraglutid, albiglutid Od exendinu odvozená léčiva, exenatid LAR Agonisté GLP-1 receptoru DPP-4 inhibitory, např. sitagliptin, vildagliptin saxagliptin Léčiva působící přes změny hladin inkretinů
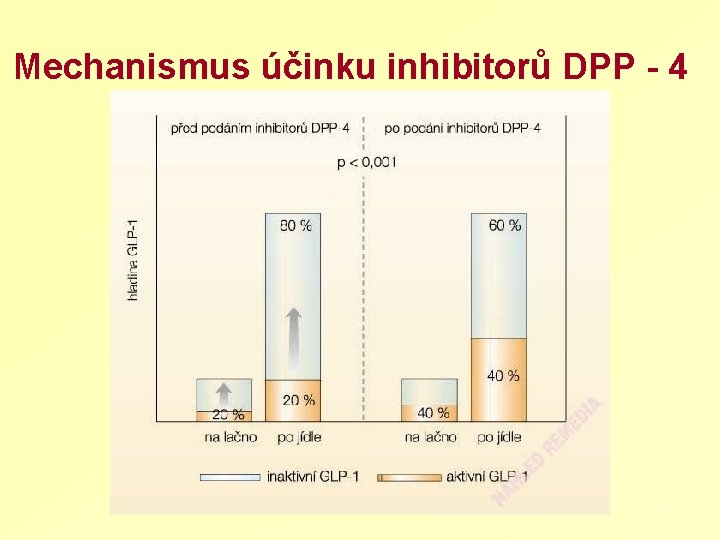
Mechanismus účinku inhibitorů DPP - 4
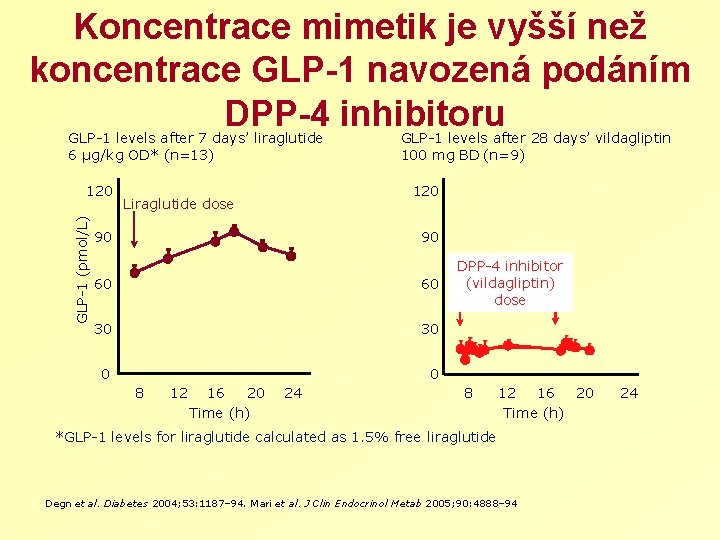
Koncentrace mimetik je vyšší než koncentrace GLP-1 navozená podáním DPP-4 inhibitoru GLP-1 levels after 7 days’ liraglutide 6 µg/kg OD* (n=13) GLP-1 (pmol/L) 120 GLP-1 levels after 28 days’ vildagliptin 100 mg BD (n=9) 120 Liraglutide dose 90 90 60 60 30 30 0 0 8 12 16 20 Time (h) 24 DPP-4 inhibitor (vildagliptin) dose 8 12 16 20 Time (h) *GLP-1 levels for liraglutide calculated as 1. 5% free liraglutide Degn et al. Diabetes 2004; 53: 1187– 94. Mari et al. J Clin Endocrinol Metab 2005; 90: 4888– 94 24
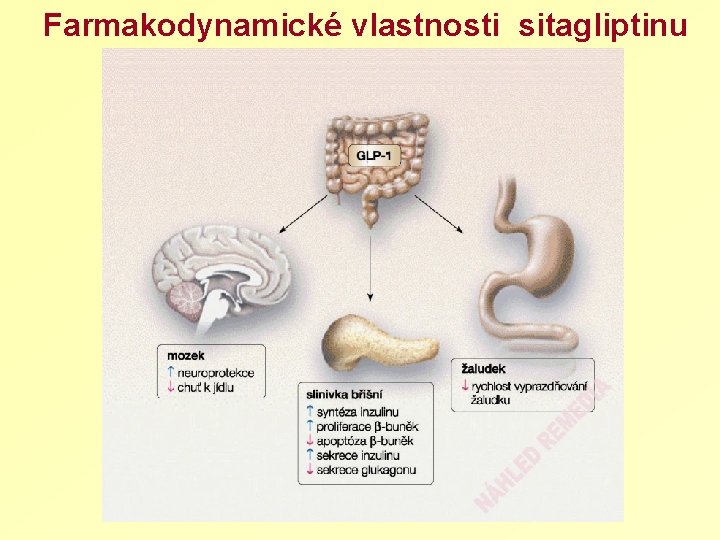
Farmakodynamické vlastnosti sitagliptinu
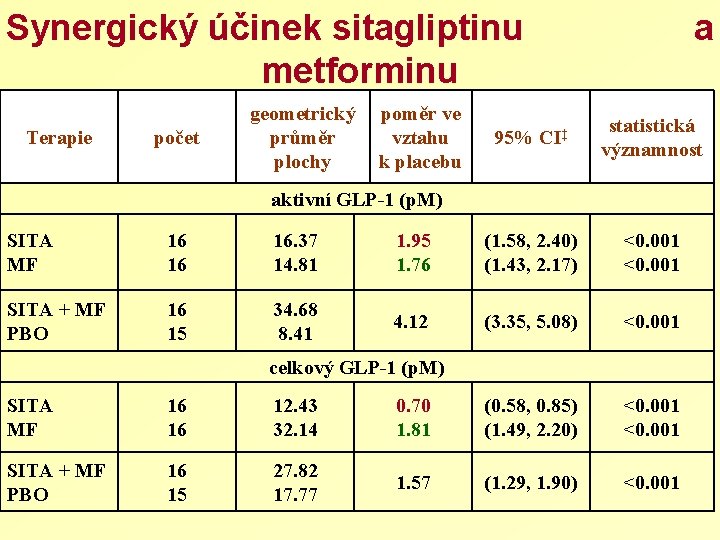
Synergický účinek sitagliptinu metforminu Terapie počet geometrický průměr plochy poměr ve vztahu k placebu a 95% CI‡ statistická významnost aktivní GLP-1 (p. M) SITA MF 16 16 16. 37 14. 81 1. 95 1. 76 (1. 58, 2. 40) (1. 43, 2. 17) <0. 001 SITA + MF PBO 16 15 34. 68 8. 41 4. 12 (3. 35, 5. 08) <0. 001 celkový GLP-1 (p. M) SITA MF 16 16 12. 43 32. 14 0. 70 1. 81 (0. 58, 0. 85) (1. 49, 2. 20) <0. 001 SITA + MF PBO 16 15 27. 82 17. 77 1. 57 (1. 29, 1. 90) <0. 001
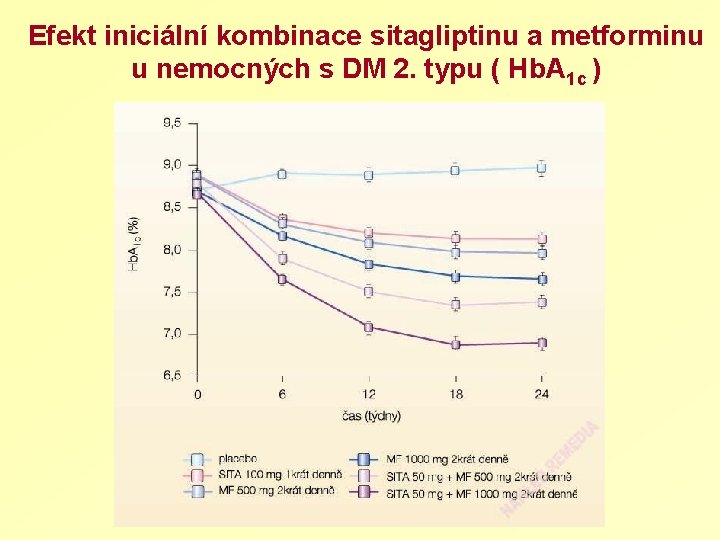
Efekt iniciální kombinace sitagliptinu a metforminu u nemocných s DM 2. typu ( Hb. A 1 c )
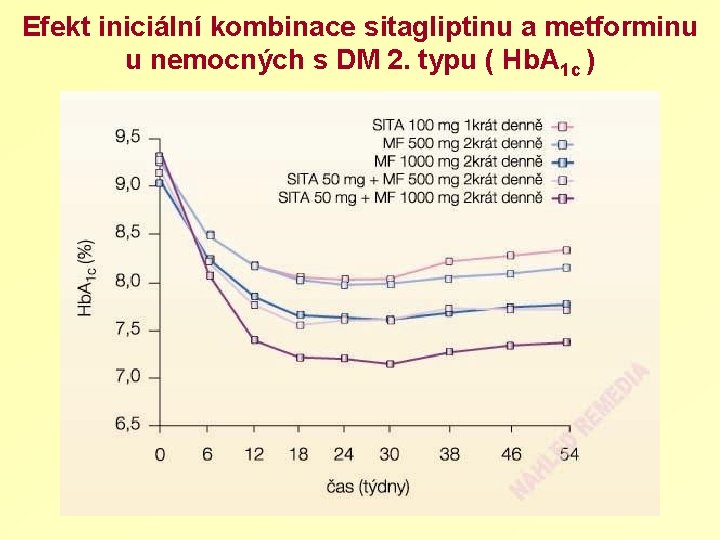
Efekt iniciální kombinace sitagliptinu a metforminu u nemocných s DM 2. typu ( Hb. A 1 c )
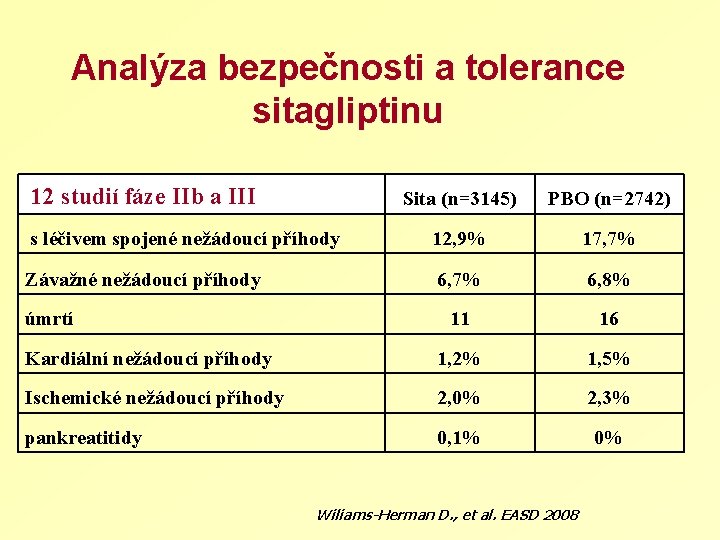
Analýza bezpečnosti a tolerance sitagliptinu 12 studií fáze IIb a III Sita (n=3145) PBO (n=2742) s léčivem spojené nežádoucí příhody 12, 9% 17, 7% Závažné nežádoucí příhody 6, 7% 6, 8% 11 16 Kardiální nežádoucí příhody 1, 2% 1, 5% Ischemické nežádoucí příhody 2, 0% 2, 3% pankreatitidy 0, 1% 0% úmrtí Wiliams-Herman D. , et al. EASD 2008

Nežádoucí účinky při léčbě sitagliptinem 1. Frekvence přerušení léčby sitagliptinem byla podobná jako u placeba üIncidence hypoglykemií při léčbě sitagliptinem byla podobná jakou u placeba (1. 2% vs 0. 9%) üIncidence GIT nežádoucích příhod při léčbě sitagliptinem byla podobná ve srovnání s placebem: – bolesti břicha (2. 3%, 2. 1%) – nausea (1. 4%, 0. 6%) – průjem (3. 0%, 2. 3%) – zvracení (0. 8%, 0. 9%) 47
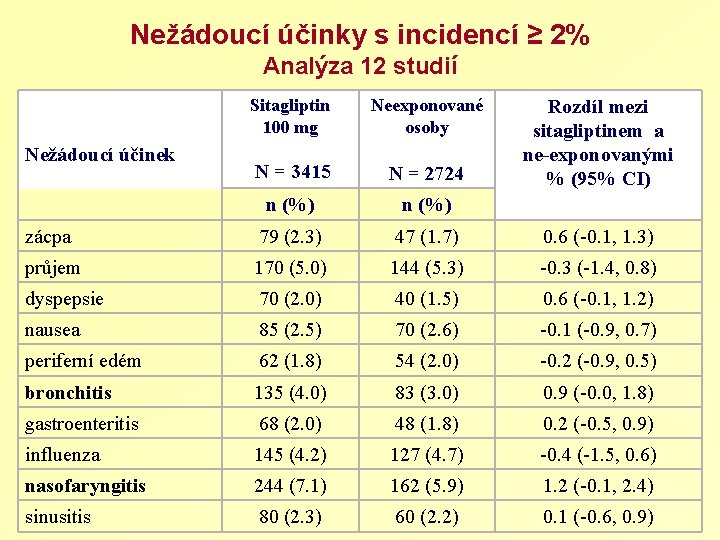
Nežádoucí účinky s incidencí ≥ 2% Analýza 12 studií Sitagliptin 100 mg Neexponované osoby N = 3415 N = 2724 n (%) zácpa 79 (2. 3) 47 (1. 7) 0. 6 (-0. 1, 1. 3) průjem 170 (5. 0) 144 (5. 3) -0. 3 (-1. 4, 0. 8) dyspepsie 70 (2. 0) 40 (1. 5) 0. 6 (-0. 1, 1. 2) nausea 85 (2. 5) 70 (2. 6) -0. 1 (-0. 9, 0. 7) periferní edém 62 (1. 8) 54 (2. 0) -0. 2 (-0. 9, 0. 5) bronchitis 135 (4. 0) 83 (3. 0) 0. 9 (-0. 0, 1. 8) gastroenteritis 68 (2. 0) 48 (1. 8) 0. 2 (-0. 5, 0. 9) influenza 145 (4. 2) 127 (4. 7) -0. 4 (-1. 5, 0. 6) nasofaryngitis 244 (7. 1) 162 (5. 9) 1. 2 (-0. 1, 2. 4) sinusitis 80 (2. 3) 60 (2. 2) 0. 1 (-0. 6, 0. 9) Nežádoucí účinek Rozdíl mezi sitagliptinem a ne-exponovanými % (95% CI)
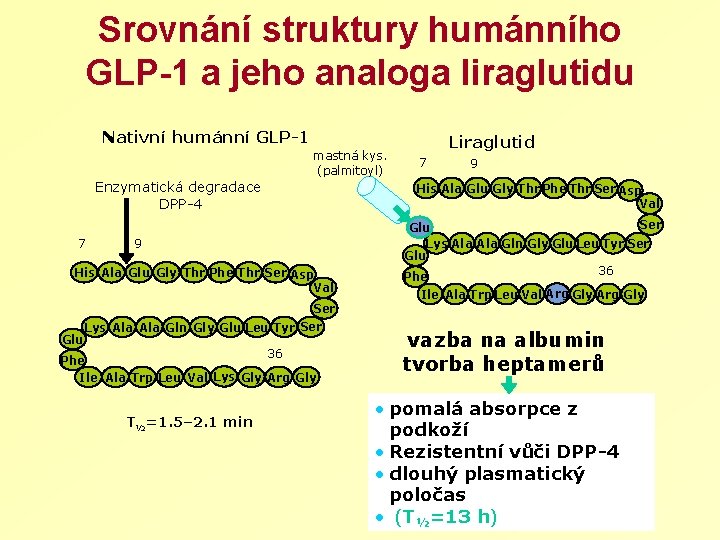
Srovnání struktury humánního GLP-1 a jeho analoga liraglutidu Nativní humánní GLP-1 mastná kys. (palmitoyl) Enzymatická degradace DPP-4 7 7 9 His Ala Glu Gly Thr Phe Thr Ser Asp Val Ser Lys Ala Gln Gly Glu Leu Tyr Ser Glu 36 Phe Ile Ala Trp Leu Val Lys Gly Arg Gly T½=1. 5– 2. 1 min Liraglutid Ser Glu Lys Ala Gln Gly Glu Leu Tyr Ser Glu 36 Phe Ile Ala Trp Leu Val Arg Gly vazba na albumin tvorba heptamerů • pomalá absorpce z podkoží • Rezistentní vůči DPP-4 • dlouhý plasmatický poločas • (T½=13 h)
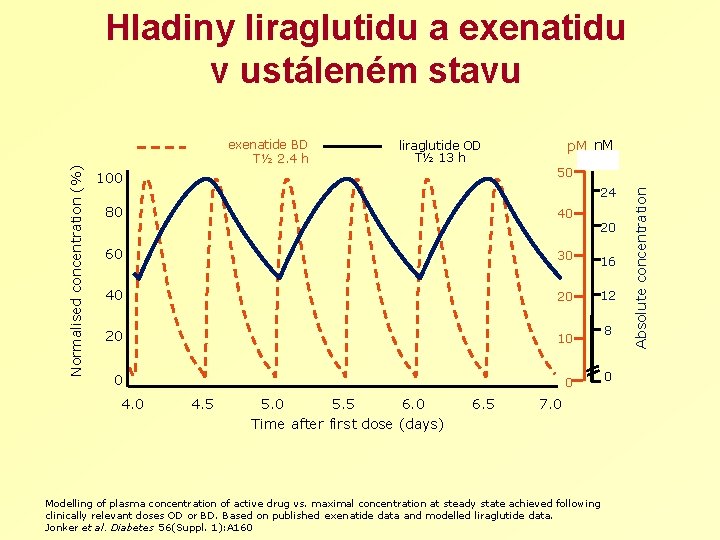
liraglutide OD T½ 13 h p. M n. M 28 exenatide BD T½ 2. 4 h 100 50 80 40 60 30 40 20 20 10 0 0 4. 0 24 4. 5 5. 0 5. 5 6. 0 Time after first dose (days) 6. 5 20 16 12 7. 0 Modelling of plasma concentration of active drug vs. maximal concentration at steady state achieved following clinically relevant doses OD or BD. Based on published exenatide data and modelled liraglutide data. Jonker et al. Diabetes 56(Suppl. 1): A 160 8 0 Absolute concentration Normalised concentration (%) Hladiny liraglutidu a exenatidu v ustáleném stavu
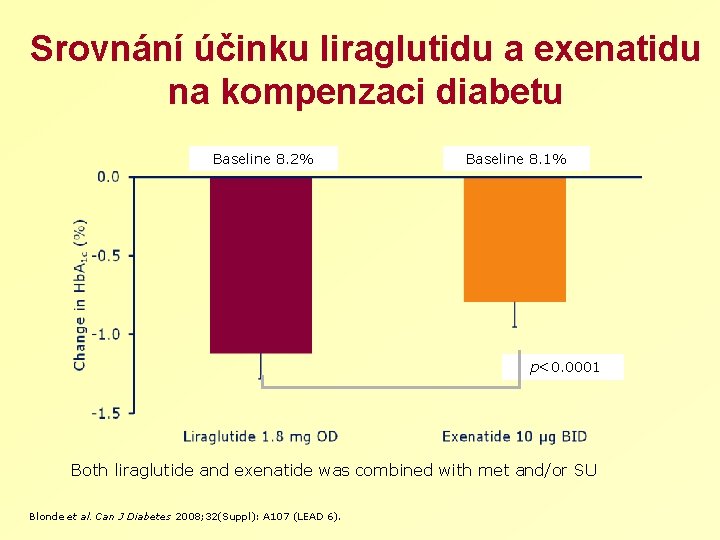
Srovnání účinku liraglutidu a exenatidu na kompenzaci diabetu Baseline 8. 2% Baseline 8. 1% p<0. 0001 Both liraglutide and exenatide was combined with met and/or SU Blonde et al. Can J Diabetes 2008; 32(Suppl): A 107 (LEAD 6).
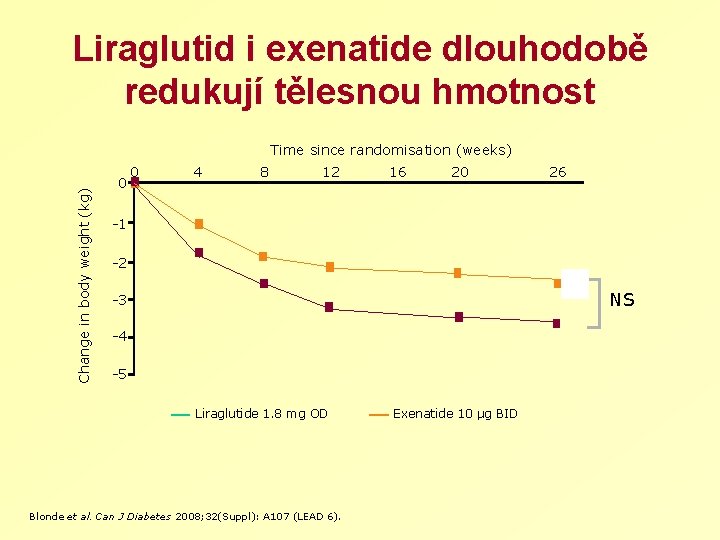
Liraglutid i exenatide dlouhodobě redukují tělesnou hmotnost Change in body weight (kg) Time since randomisation (weeks) 0 0 4 8 12 16 20 26 -1 -2 NS -3 -4 -5 Liraglutide 1. 8 mg OD Blonde et al. Can J Diabetes 2008; 32(Suppl): A 107 (LEAD 6). Exenatide 10 μg BID
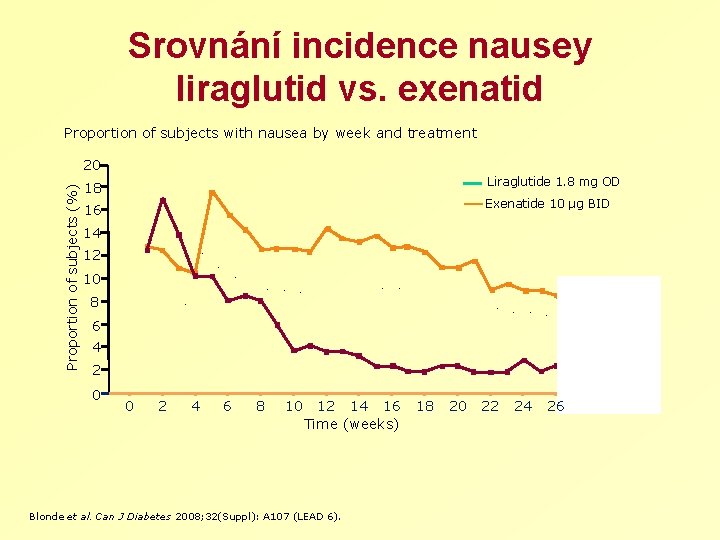
Srovnání incidence nausey liraglutid vs. exenatid Proportion of subjects with nausea by week and treatment Proportion of subjects (%) 20 18 Liraglutide 1. 8 mg OD 16 Exenatide 10 μg BID 14 12 10 8 6 4 2 0 0 2 4 6 8 10 12 14 16 Time (weeks) Blonde et al. Can J Diabetes 2008; 32(Suppl): A 107 (LEAD 6). 18 20 22 24 26 28
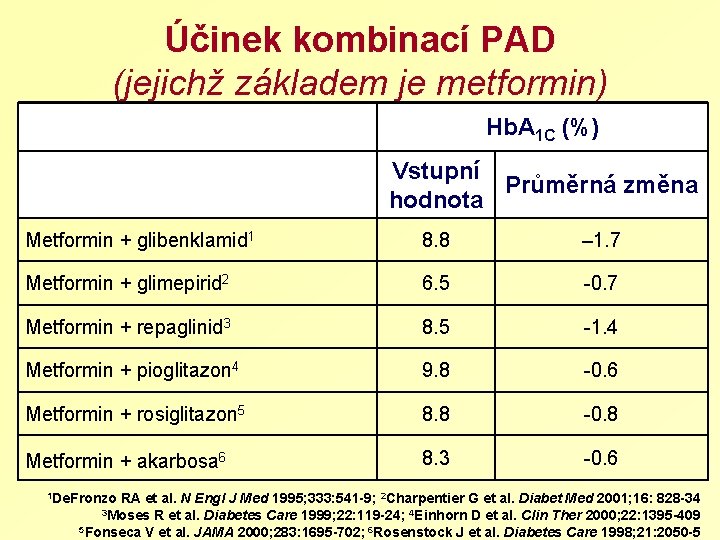
Účinek kombinací PAD (jejichž základem je metformin) Hb. A 1 C (%) Vstupní Průměrná změna hodnota Metformin + glibenklamid 1 8. 8 – 1. 7 Metformin + glimepirid 2 6. 5 -0. 7 Metformin + repaglinid 3 8. 5 -1. 4 Metformin + pioglitazon 4 9. 8 -0. 6 Metformin + rosiglitazon 5 8. 8 -0. 8 Metformin + akarbosa 6 8. 3 -0. 6 1 De. Fronzo RA et al. N Engl J Med 1995; 333: 541 -9; 2 Charpentier G et al. Diabet Med 2001; 16: 828 -34 3 Moses R et al. Diabetes Care 1999; 22: 119 -24; 4 Einhorn D et al. Clin Ther 2000; 22: 1395 -409 5 Fonseca V et al. JAMA 2000; 283: 1695 -702; 6 Rosenstock J et al. Diabetes Care 1998; 21: 2050 -5
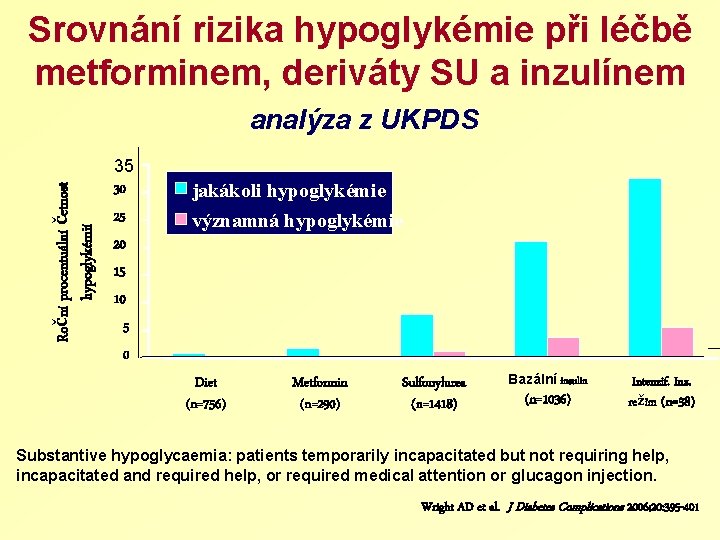
Srovnání rizika hypoglykémie při léčbě metforminem, deriváty SU a inzulínem Roční procentuální četnost hypoglykémií analýza z UKPDS 35 30 jakákoli hypoglykémie 25 významná hypoglykémie 20 15 10 5 0 Diet (n=756) Metformin (n=290) Sulfonylurea (n=1418) Bazální insulin (n=1036) Intenzif. Inz. režim (n=38) Substantive hypoglycaemia: patients temporarily incapacitated but not requiring help, incapacitated and required help, or required medical attention or glucagon injection. Wright AD et al. J Diabetes Complications 2006; 20: 395 -401


Design studie RECORD Osoby léčené monoterapií metformin sulfonylurea Náhodně zařazeny k určité alternativě kombinace PAD přidán rosiglitazon (pokračuje metformin) přidána sulfonylurea (pokračuje metformin) přidán rosiglitazon (pokračuje sulfonylurea) přidán metformin (pokračuje sulfonylurea)
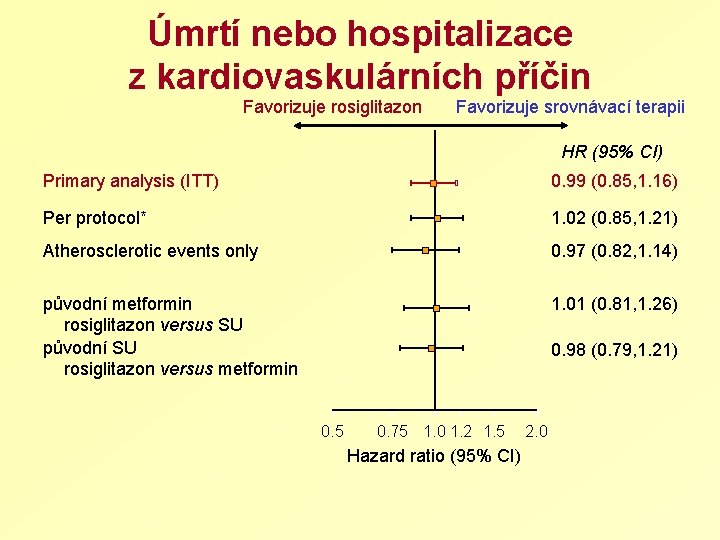
Úmrtí nebo hospitalizace z kardiovaskulárních příčin Favorizuje rosiglitazon Favorizuje srovnávací terapii HR (95% CI) Primary analysis (ITT) 0. 99 (0. 85, 1. 16) Per protocol* 1. 02 (0. 85, 1. 21) Atherosclerotic events only 0. 97 (0. 82, 1. 14) původní metformin rosiglitazon versus SU původní SU rosiglitazon versus metformin 1. 01 (0. 81, 1. 26) 0. 98 (0. 79, 1. 21) 0. 5 0. 75 1. 0 1. 2 1. 5 Hazard ratio (95% CI) 2. 0

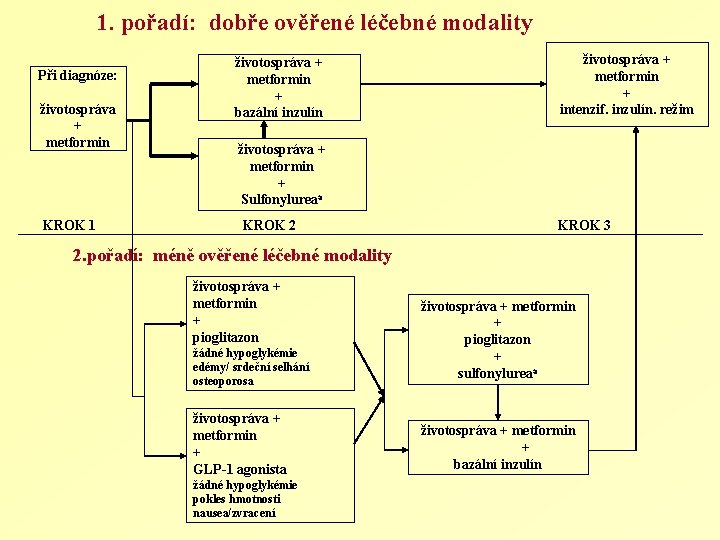
1. pořadí: dobře ověřené léčebné modality Při diagnóze: životospráva + metformin KROK 1 životospráva + metformin + bazální inzulín životospráva + metformin + intenzif. inzulín. režim životospráva + metformin + Sulfonylureaa KROK 2 KROK 3 2. pořadí: méně ověřené léčebné modality životospráva + metformin + pioglitazon žádné hypoglykémie edémy/ srdeční selhání osteoporosa životospráva + metformin + GLP-1 agonista žádné hypoglykémie pokles hmotnosti nausea/zvracení životospráva + metformin + pioglitazon + sulfonylureaa životospráva + metformin + bazální inzulín
- Slides: 44