AGNCIA NACIONAL DE VIGIL NCIA SANITRIA Gerncia Geral
























- Slides: 25

AGÊNCIA NACIONAL DE VIGIL NCIA SANITÁRIA Gerência Geral de Medicamentos Gerência de Avaliação de Segurança e Eficácia Coordenação de Produtos Biológicos Regulamentação dos medicamentos biológicos no Brasil Simpósio anual de Pesquisa e Atualização Departamento de Oftalmologia Universidade Federal de São Paulo Março, 2012 Agência Nacional de Vigilância Sanitária Marcelo Moreira www. anvisa. gov. br

Registro de Medicamentos Bases legais Lei nº 6360/76 “ Art. 12. Nenhum dos produtos de que trata esta Lei, inclusive os importados, poderá ser industrializado, exposto à venda ou entregue ao consumo antes de registrado no Ministério da Saúde” Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Registro de Medicamentos Bases legais Lei nº 6360/76 “Art. 16. O registro de drogas, medicamentos, insumos farmacêuticos e correlatos, dadas as suas características sanitárias, medicamentosas ou profiláticas, curativas, paliativas, ou mesmo para fins de diagnóstico, fica sujeito, além do atendimento das exigências próprias, aos seguintes requisitos específicos: (Redação dada pela Lei nº 10. 742, de 6 de outubro de 2003) Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Registro de Medicamentos Bases legais Lei nº 6360/76 “Art. 16. (. . . ) II - que o produto, através de comprovação científica e de análise, seja reconhecido como seguro e eficaz para o uso a que se propõe, e possua a identidade, atividade, qualidade, pureza e inocuidade necessárias; ”. (Redação dada pela Lei nº 10. 742, de 6 de outubro de 2003) Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Registro de Medicamentos Bases legais Lei nº 6360/76 - VALIDADE: 5 anos e poderá ser revalidado por períodos iguais e sucessivos, mantido o número do registro inicial; - REVALIDAÇÃO: 6 meses antes de expirar a validade. Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Registro de Medicamentos Bases legais Decreto nº 79. 094/77 “Art. 17 - O registro dos produtos submetidos ao sistema de vigilância sanitária fica sujeito à observância dos seguintes requisitos: . . . X - Comprovação, por intermédio de inspeção sanitária, de que o estabelecimento de produção cumpre as boas práticas de fabricação e controle. ” Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Evolução da Legislação de Registro de Medicamentos - Mesmos critérios para diferentes categorias de medicamentos; - Criação da ANVISA em 1999 (Lei 9. 782/99); Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Evolução da Legislação de Registro de Medicamentos - Medicamentos Genéricos – Lei 9. 787/99; - Hemoderivados – RDC 46/00; Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Evolução da Legislação de Registro de Produtos Biológicos - Produtos Biológicos – RDC 80/02 (primeiro marco normativo); - Produtos Biológicos – RDC 315/2005 (segundo marco normativo); - Produtos Biológicos – RDC 55/2010 e RDC 49/2011 (resoluções vigentes). Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Regulamentação de Produtos Biológicos O que é registrado como produto biológico no Brasil? 1. Vacinas; 2. Soros Hiperimunes; 3. Hemoderivados; 4. Biomedicamentos: derivados de fluidos biológicos ou de tecidos de origem animal, procedimentos biotecnológicos; Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Regulamentação de Produtos Biológicos O que é registrado como medicamento biológico no Brasil? 5. Anticorpos monoclonais; 6. Medicamentos contendo microorganismos vivos, atenuados ou mortos; 7. Probióticos; 8. Alergênicos. Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

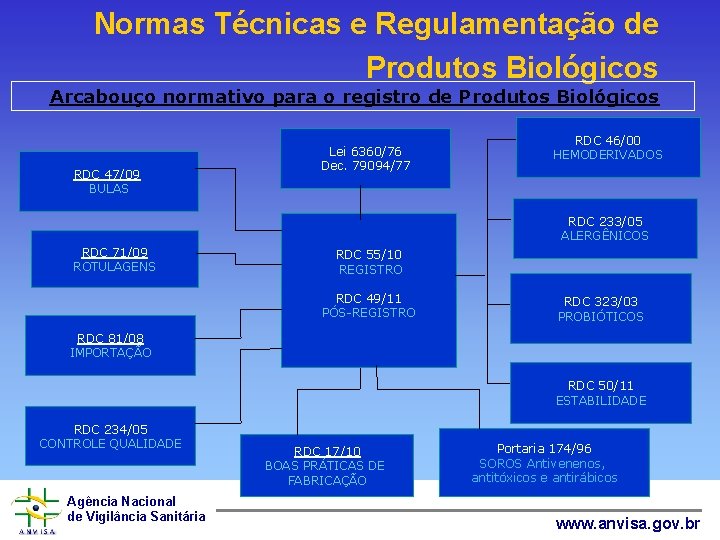
Normas Técnicas e Regulamentação de Produtos Biológicos Arcabouço normativo para o registro de Produtos Biológicos RDC 47/09 BULAS Lei 6360/76 Dec. 79094/77 RDC 46/00 HEMODERIVADOS RDC 233/05 ALERGÊNICOS RDC 71/09 ROTULAGENS RDC 55/10 REGISTRO RDC 49/11 PÓS-REGISTRO RDC 323/03 PROBIÓTICOS RDC 81/08 IMPORTAÇÃO RDC 50/11 ESTABILIDADE RDC 234/05 CONTROLE QUALIDADE Agência Nacional de Vigilância Sanitária RDC 17/10 BOAS PRÁTICAS DE FABRICAÇÃO Portaria 174/96 SOROS Antivenenos, antitóxicos e antirábicos www. anvisa. gov. br

Registro de Produtos Biológicos Resolução da Diretoria Colegiada – RDC nº. 55/2010 Dispõe sobre o registro de produtos biológicos novos e produtos biológicos e dá outras providências. Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Registro de Produtos Biológicos Resolução da Diretoria Colegiada – RDC nº. 55/2010 Definições (capítulo I, Seção II, Art. 2º) XX - Produto biológico novo: medicamento biológico que contém molécula com atividade biológica conhecida, ainda não registrado no Brasil e que tenha passado por todas as etapas de fabricação. Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Registro de Produtos Biológicos Resolução da Diretoria Colegiada – RDC nº. 55/2010 Definições (capítulo I, Seção II, Art. 2º) XV - Produto biológico: medicamento biológico não novo ou conhecido que contém molécula com atividade biológica conhecida, já registrado no Brasil e (. . . ) etapas de fabricação. Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Registro de Produtos Biológicos Resolução da Diretoria Colegiada – RDC nº. 55/2010 Art. 16. O registro de produto fabricado em outros países somente poderá ser concedido pela Anvisa se o medicamento estiver registrado e liberado para uso em seu país de fabricação. Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Registro de Produtos Biológicos Resolução da Diretoria Colegiada – RDC nº. 55/2010 Art. 17. Todas as empresas envolvidas na fabricação de um produto biológico novo ou produto biológico devem cumprir as boas práticas de fabricação, e apresentar o Certificado de Boas Práticas de Fabricação (CBPF) emitido pela Anvisa. Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Registro de Produtos Biológicos Resolução da Diretoria Colegiada – RDC nº. 55/2010 Art. 18. Todas as indicações terapêuticas solicitadas no registro, para o produto biológico novo ou produto biológico, devem estar documentalmente demonstradas nos relatórios dos estudos clínicos. Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Alterações Pós-Registro de Produtos Biológicos Área: Medicamento Assunto: 1519 - PRODUTO BIOLÓGICO - Inclusão de Nova Apresentação Comercial Relação de Documentos de Instrução 1 - Formulários de petição FP 1 e FP 2 devidamente preenchidos 2 - Via original do comprovante de pagamento da taxa de fiscalização de vigilância sanitária - GRU 3 - Justificativa do requerimento, contemplando a descrição detalhada e as razões de ordem técnica, de acordo com o modelo constante na RDC nº 49/2011. 4 - 1(um) CD-ROM com a mesma informação documentada gravada em linguagem eletrônica tipo pdf 5 - Cópia da Licença de Funcionamento da Empresa e/ou Alvará Sanitário Atualizado 6 - Cópia do Certificado de Autorização de Funcionamento da Empresa ou de sua publicação em D. O. U Fundamentação Legal Lei nº 6360, de 23/09/1976; Decreto nº 79. 094, de 05/01/1977; RDC nº 305, de 14/11/2022; RDC nº 68, de 28/03/2003; RDC nº 222, de 28/12/2006; RDC nº 49, de 22/09/2011, RDC nº 50, de 22/09/2011 Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Alterações Pós-Registro de Produtos Biológicos Área: Medicamento Assunto: 1519 - PRODUTO BIOLÓGICO - Inclusão de Nova Apresentação Comercial Relação de Documentos de Instrução 7 - Código de barras GTIN para as apresentações 8 - Relatório dos estudos de estabilidade para produtos líquidos ou liofilizados, no caso de alteração da proporção de volume ou peso por embalagem, respectivamente 9 - Modelos de rotulagem e embalagem, conforme RDC nº. 71/2009, e suas posteriores atualizações. 10 - Modelo de texto de bula atualizado, conforme RDC nº. 47/2009 e suas posteriores atualizações. 11 - Cópia do CBPF, expedido pela ANVISA para todos os fabricantes do princípio ativo, do produto biológico a granel, do produto biológico em sua embalagem primária, do produto biológico terminado, do diluente e do adjuvante. Fundamentação Legal Lei nº 6360, de 23/09/1976; Decreto nº 79. 094, de 05/01/1977; RDC nº 305, de 14/11/2022; RDC nº 68, de 28/03/2003; RDC nº 222, de 28/12/2006; RDC nº 49, de 22/09/2011, RDC nº 50, de 22/09/2011 Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Alterações Pós-Registro de Produtos Biológicos Área: Medicamento Assunto: 1615 - PRODUTO BIOLÓGICO - Inclusão de Nova Indicação Terapêutica no País Relação de Documentos de Instrução 1 - Formulários de petição FP 1 e FP 2 devidamente preenchidos 2 - Via original do comprovante de pagamento da taxa de fiscalização de vigilância sanitária (GRU) 3 - Justificativa do requerimento, contemplando a descrição detalhada e as razões de ordem técnica, de acordo com o modelo constante na RDC nº 49/2011. 4 - 1(um) CD-ROM com a mesma informação documentada gravada em linguagem eletrônica tipo pdf 5 - Cópia da Licença de Funcionamento da Empresa e/ou Alvará Sanitário Atualizado 6 - Cópia do certificado de autorização de funcionamento da empresa ou de sua publicação em Diário Oficial da União (DOU) Fundamentação Legal Lei nº 6360, de 23/09/1976; Decreto nº 79. 094, de 05/01/1977; RDC nº 305, de 14/11/2022; RDC nº 68, de 28/03/2003; RDC nº 222, de 28/12/2006; RDC nº 49, de 22/09/2011, RDC nº 50, de 22/09/2011 Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Alterações Pós-Registro de Produtos Biológicos Área: Medicamento Assunto: 1615 - PRODUTO BIOLÓGICO - Inclusão de Nova Indicação Terapêutica no País Relação de Documentos de Instrução 7 - Relatório de Experimentação Terapêutica 8 - Modelo de texto de bula atualizado, conforme RDC nº. 47/2009 e suas posteriores atualizações. 9 - Cópia do CBPF, expedido pela ANVISA para todos os fabricantes do princípio ativo, do produto biológico a granel, do produto biológico em sua embalagem primária, do produto biológico terminado, do diluente e do adjuvante. Fundamentação Legal Lei nº 6360, de 23/09/1976; Decreto nº 79. 094, de 05/01/1977; RDC nº 305, de 14/11/2022; RDC nº 68, de 28/03/2003; RDC nº 222, de 28/12/2006; RDC nº 49, de 22/09/2011, RDC nº 50, de 22/09/2011 Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Alterações Pós-Registro de Produtos Biológicos Área: Medicamento Assunto: 1948 - PRODUTO BIOLÓGICO - Inclusão da Via de Administração Relação de Documentos de Instrução 1 - Formulários de petição FP 1 e FP 2 devidamente preenchidos 2 - Via original do comprovante de pagamento da Taxa de Fiscalização de Vigilância Sanitária (GRU) 3 - Justificativa do requerimento, contemplando a descrição detalhada e as razões de ordem técnica, de acordo com o modelo constante na RDC nº 49/2011. 4 - 1(um) CD-ROM com a mesma informação documentada gravada em linguagem eletrônica tipo pdf 5 - Cópia da Licença de Funcionamento da Empresa e/ou Alvará Sanitário Atualizado 6 - Cópia do certificado de autorização de funcionamento da empresa ou de sua publicação em Diário Oficial da União (DOU) Fundamentação Legal Lei nº 6360, de 23/09/1976; Decreto nº 79. 094, de 05/01/1977; RDC nº 305, de 14/11/2022; RDC nº 68, de 28/03/2003; RDC nº 222, de 28/12/2006; RDC nº 49, de 22/09/2011, RDC nº 50, de 22/09/2011 Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Alterações Pós-Registro de Produtos Biológicos Área: Medicamento Assunto: 1948 - PRODUTO BIOLÓGICO - Inclusão da Via de Administração Relação de Documentos de Instrução 7 - Relatório de experimentação terapêutica para a nova via de administração. 8 - Modelos de rotulagem e embalagem, conforme RDC nº. 71/2009, e suas posteriores atualizações. 9 - Modelo de texto de bula atualizado, conforme RDC nº. 47/2009 e suas posteriores atualizações. 10 - Cópia do CBPF, expedido pela ANVISA para todos os fabricantes do princípio ativo, do produto biológico a granel, do produto biológico em sua embalagem primária, do produto biológico terminado, do diluente e do adjuvante. Fundamentação Legal Lei nº 6360, de 23/09/1976; Decreto nº 79. 094, de 05/01/1977; RDC nº 305, de 14/11/2022; RDC nº 68, de 28/03/2003; RDC nº 222, de 28/12/2006; RDC nº 49, de 22/09/2011, RDC nº 50, de 22/09/2011 Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

“É sempre muito cedo parar. ” Norman Vincent Peale Obrigado, produtos. biologicos@anvisa. gov. br Agência Nacional de Vigilância Sanitária www. anvisa. gov. br