AGHWIMi R wykad z chemii oglnej Chemia Oglna






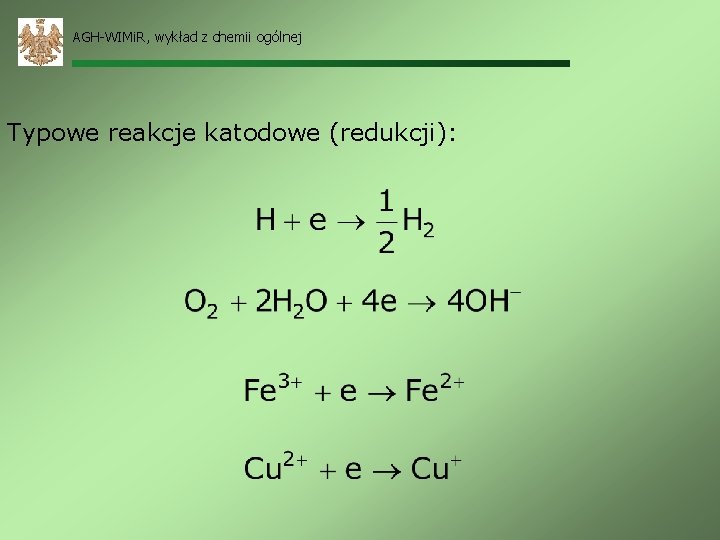










- Slides: 34

AGH-WIMi. R, wykład z chemii ogólnej Chemia Ogólna Wykład 7

AGH-WIMi. R, wykład z chemii ogólnej KOROZJA Korozja – osłabienie podstawowych własności materiału w wyniku reakcji z otoczeniem. Korozja metalu Korozja cegieł

AGH-WIMi. R, wykład z chemii ogólnej Rodzaje korozji • korozja ogólna, • korozja lokalna: wżerowa, międzykrystaliczna, • korozja naprężeniowa, • procesy korozyjno–erozyjne, • kawitacja, • korozja atmosferyczna, • korozja w betonie, • korozja w glebie, • korozja biologiczna, • korozja wysokotemperaturowa. szczelinowa,

AGH-WIMi. R, wykład z chemii ogólnej Środowiska korozyjne • kwaśne, • alkaliczne, • woda morska, • solanka, • środowiska organiczne, • stopione sole.

AGH-WIMi. R, wykład z chemii ogólnej Korozja elektrochemiczna najczęściej podczas zetknięcia potencjałach ogniwo występujący (glawaniczna) typ dwóch korozji. metali elektrochemicznych. galwaniczne, gdzie metal o – Zachodzi różnych Tworzą o one niższym potencjale stanowi anodę, zaś metal o wyższym potencjale – katodę.

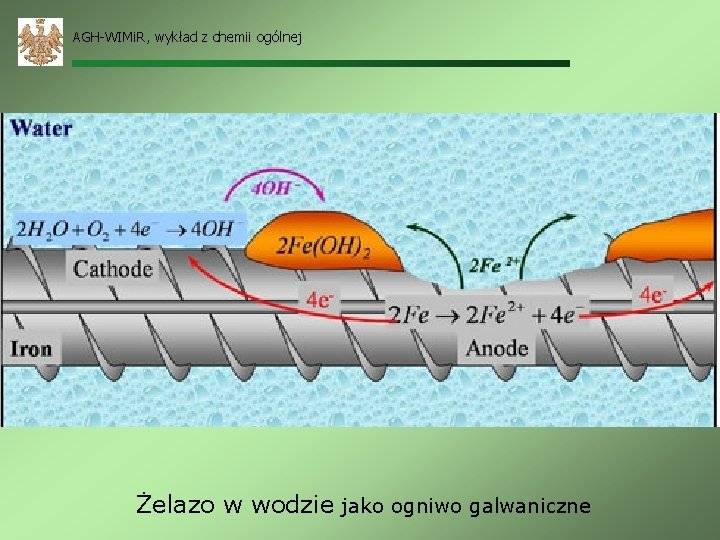
AGH-WIMi. R, wykład z chemii ogólnej Żelazo w wodzie jako ogniwo galwaniczne

AGH-WIMi. R, wykład z chemii ogólnej Mechanizm korozji elektrochemicznej Zniszczenie metalu następuje anodowej: sprzężonej z procesem katodowym: w wyniku reakcji
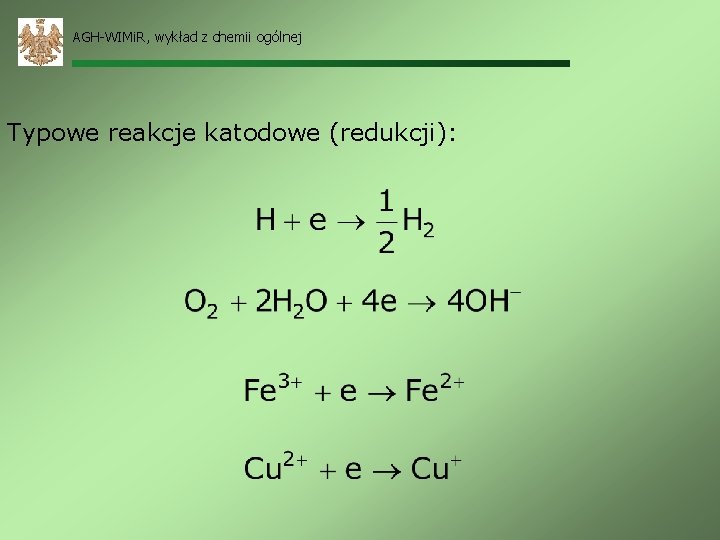
AGH-WIMi. R, wykład z chemii ogólnej Typowe reakcje katodowe (redukcji):

AGH-WIMi. R, wykład z chemii ogólnej Ogniwa galwaniczne Rodzaj procesu korozyjnego związany jest z: • występowaniem naprężeń, • obecnością wtrąceń, • różnicą stężeń.

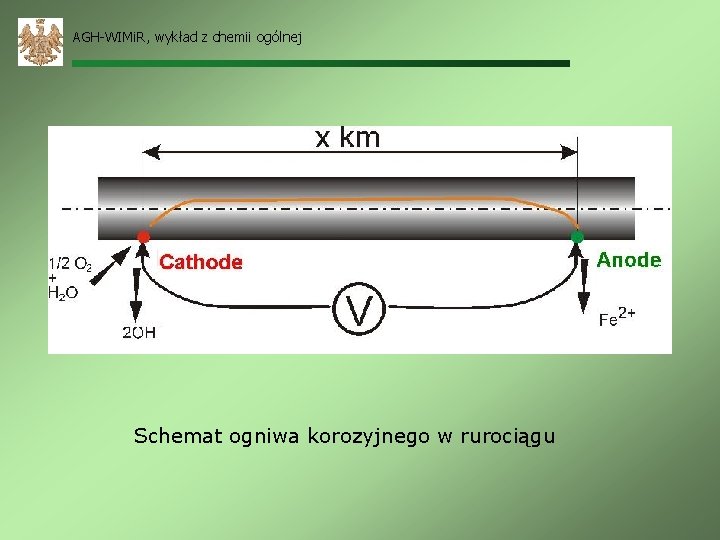
AGH-WIMi. R, wykład z chemii ogólnej Schemat ogniwa korozyjnego w rurociągu

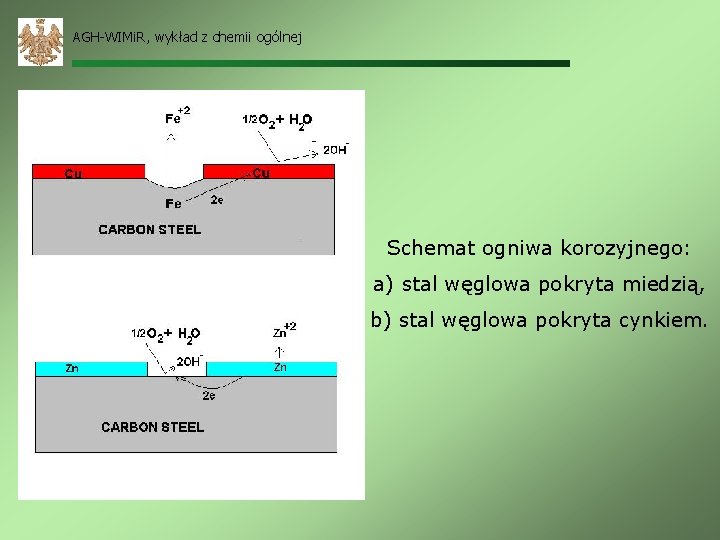
AGH-WIMi. R, wykład z chemii ogólnej Schemat ogniwa korozyjnego: a) stal węglowa pokryta miedzią, b) stal węglowa pokryta cynkiem.

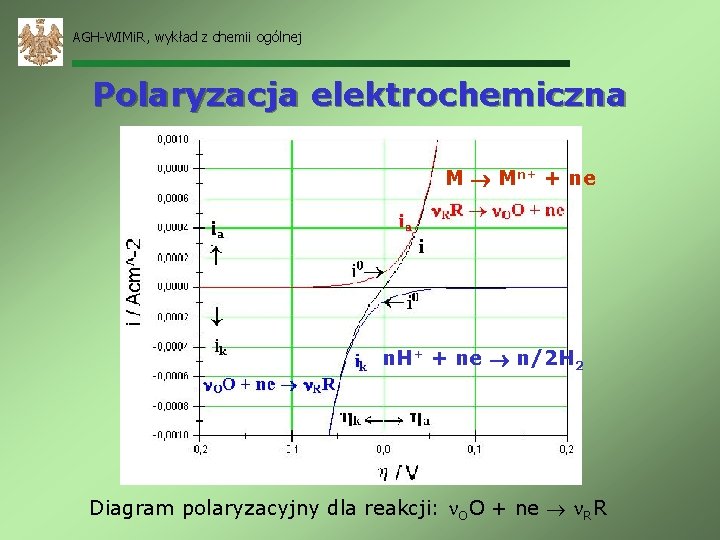
AGH-WIMi. R, wykład z chemii ogólnej Polaryzacja elektrochemiczna M Mn+ + ne n. H+ + ne n/2 H 2 Diagram polaryzacyjny dla reakcji: OO + ne RR

AGH-WIMi. R, wykład z chemii ogólnej Pasywacja – stan odporności korozyjnej aktywnego metalu w wyniku utworzenia odpornej warstwy powierzchniowej inhibitującej proces korozji w określonym środowisku i określonych warunkach p. H.

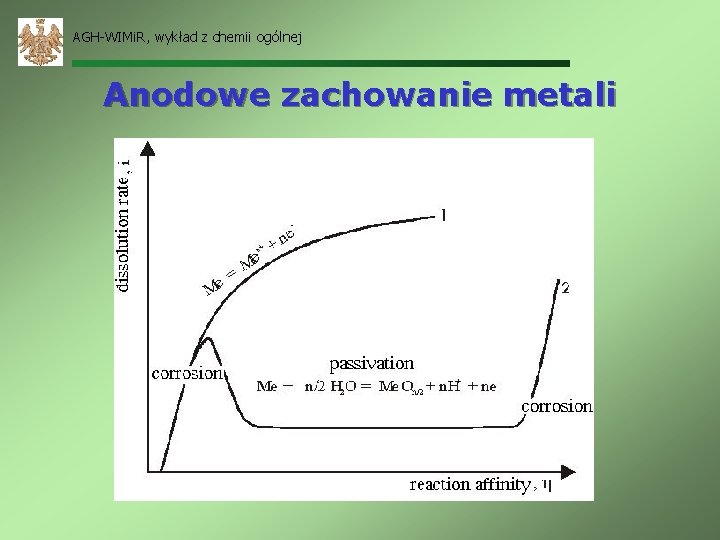
AGH-WIMi. R, wykład z chemii ogólnej Anodowe zachowanie metali

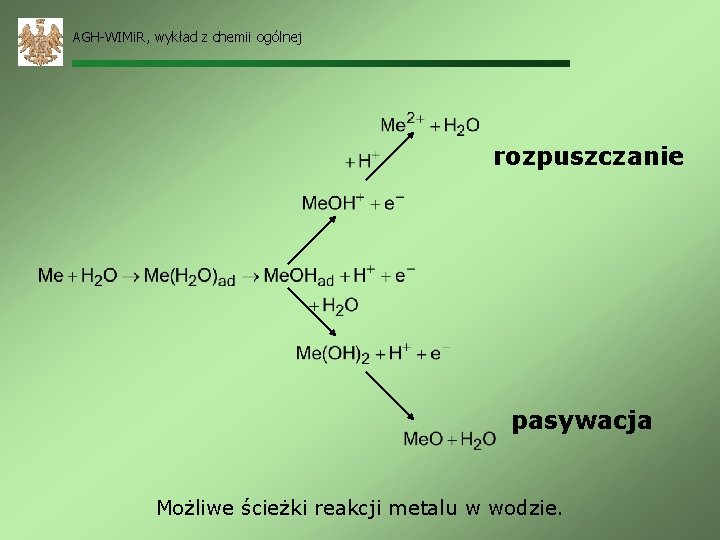
AGH-WIMi. R, wykład z chemii ogólnej rozpuszczanie pasywacja Możliwe ścieżki reakcji metalu w wodzie.

AGH-WIMi. R, wykład z chemii ogólnej Mechanizm pasywacji Źródłem tlenu, niezbędnego dla powstania warstwy pasywnej, mogą być: - w środowisku wodnym: • cząsteczki wody, • rozpuszczony tlen. - w środowiskach bezwodnych: • cząsteczki kwasów tlenowych (H 2 SO 4, H 3 PO 4, HNO 3, HCOOH), • aniony zawierające tlen (Cr. O 4 -2, Cr 2 O 7 -2, Mn. O 4 -), • cząsteczki rozpuszczalnika (CH 3 OH).

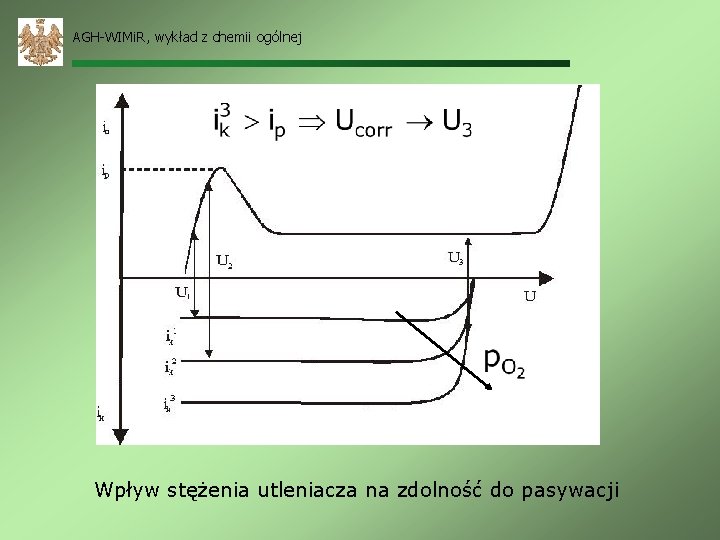
AGH-WIMi. R, wykład z chemii ogólnej Wpływ stężenia utleniacza na zdolność do pasywacji

AGH-WIMi. R, wykład z chemii ogólnej Pasywacja stopów Odporność korozyjna stopów zależy od obecności i ilości składników stopowych posiadających wysokie powinowactwo do tlenu i zdolności tworzenia warstwy pasywnej. Najważniejszym pierwiastkiem odpowiedzialnym za pasywację jest chrom. stopowym

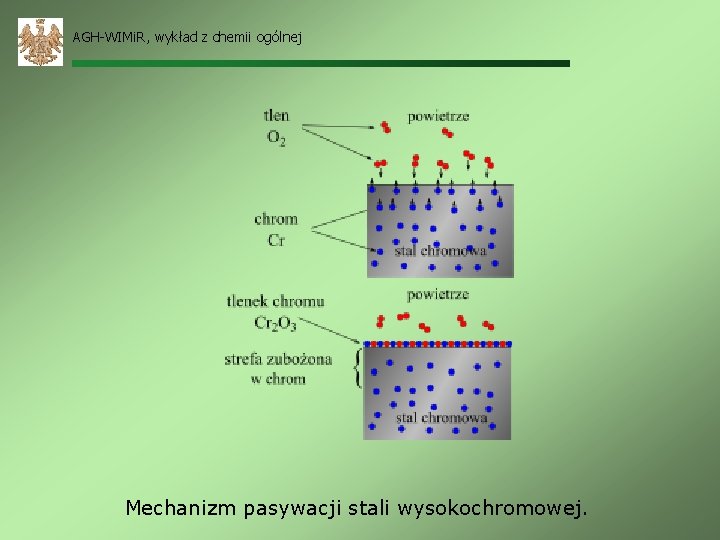
AGH-WIMi. R, wykład z chemii ogólnej Mechanizm pasywacji stali wysokochromowej.

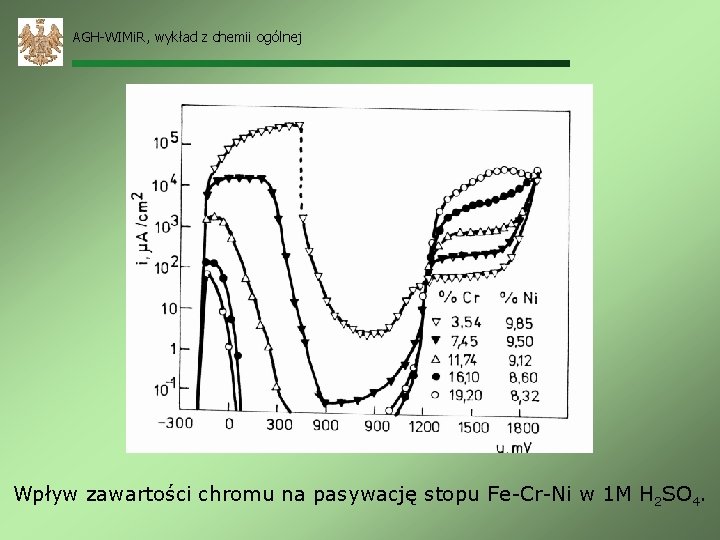
AGH-WIMi. R, wykład z chemii ogólnej Wpływ zawartości chromu na pasywację stopu Fe-Cr-Ni w 1 M H 2 SO 4.

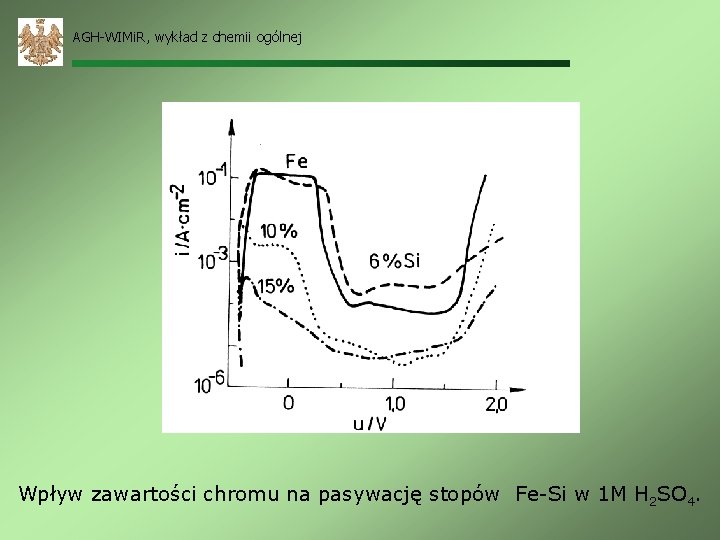
AGH-WIMi. R, wykład z chemii ogólnej Wpływ zawartości chromu na pasywację stopów Fe-Si w 1 M H 2 SO 4.

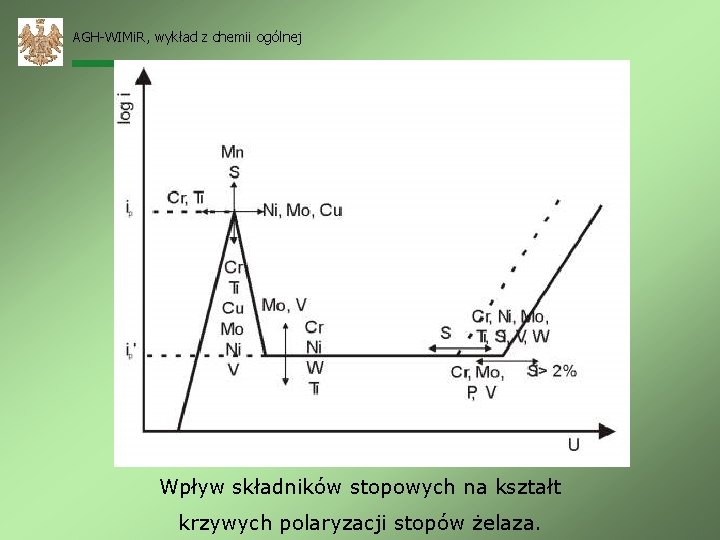
AGH-WIMi. R, wykład z chemii ogólnej Wpływ składników stopowych na kształt krzywych polaryzacji stopów żelaza.

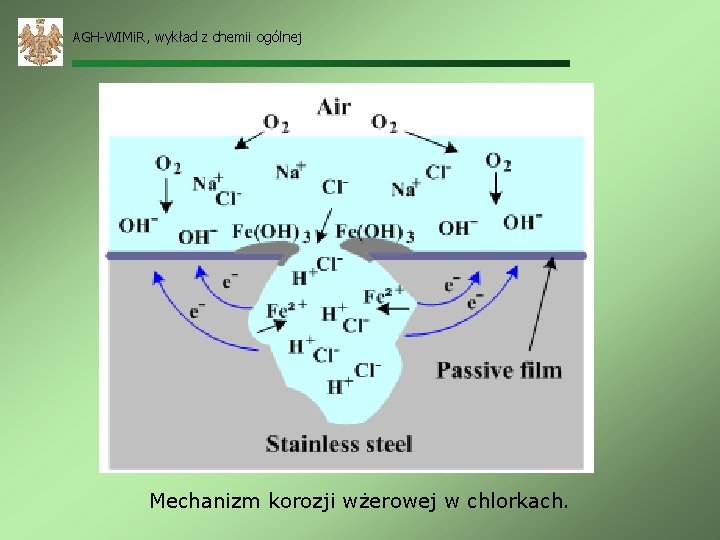
AGH-WIMi. R, wykład z chemii ogólnej Korozja wżerowa – rodzaj korozji lokalnej w wyniku której powstają „dziury” w materiale. Jest bardziej niebezpieczna od korozji ogólnej, ponieważ trudniej ją przewidzieć i jej przeciwdziałać. Występuje na metalach i stopach ulegających pasywacji.

AGH-WIMi. R, wykład z chemii ogólnej Mechanizm korozji wżerowej w chlorkach.

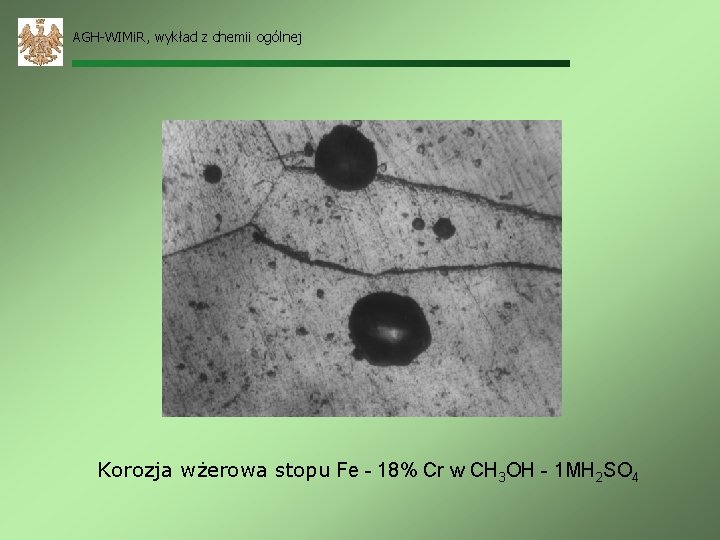
AGH-WIMi. R, wykład z chemii ogólnej Korozja wżerowa stopu Fe - 18% Cr w CH 3 OH - 1 MH 2 SO 4

AGH-WIMi. R, wykład z chemii ogólnej Korozja międzykrystaliczna – korozja zachodzą wzdłuż granic ziaren mechaniczne metalu stopu. osłabiająca Korozja znacząco właściwości międzykrystaliczna stali chromowych jest związana ze zjawiskiem wydzielania się węglików chromu na granicach ziaren i ze zubożeniem przygranicznych obszarów ziaren w chrom.

AGH-WIMi. R, wykład z chemii ogólnej Korozja międzykrystaliczna części samolotu wykonana ze stopu aluminum 7075 -T 6

AGH-WIMi. R, wykład z chemii ogólnej Korozja naprężeniowa spowodowane korozyjnym. – naprężeniami pęknięcia oraz materiału środowiskiem

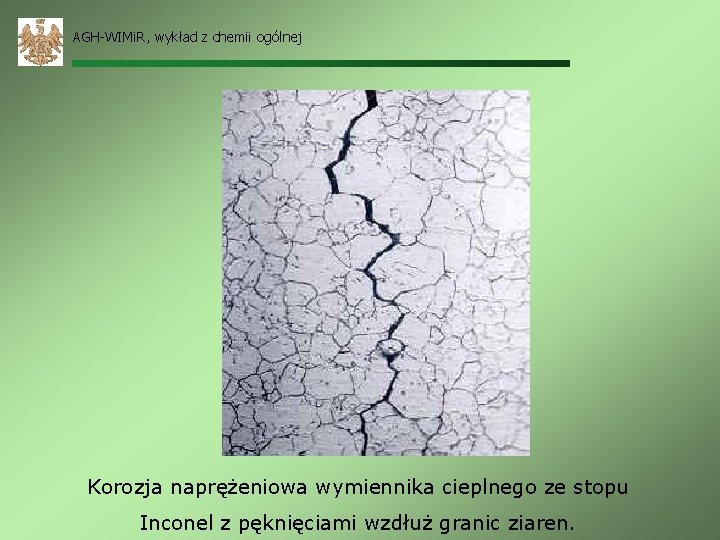
AGH-WIMi. R, wykład z chemii ogólnej Korozja naprężeniowa wymiennika cieplnego ze stopu Inconel z pęknięciami wzdłuż granic ziaren.

AGH-WIMi. R, wykład z chemii ogólnej Ochrona przed korozją • stopy odporne na korozję, • kompozyty, • powłoki ochronne, • ochrona katodowa, • ochrona anodowa, • inhibitory.

AGH-WIMi. R, wykład z chemii ogólnej Powłoki ochronne metaliczne Przykłady: Zn 2+ + 2 e Zn 0 Cu 2+ + 2 e Cu 0 Ni 2+ + 2 e Ni 0 Cr 3+ + 3 e Cr 0 Ag+ + e Ag 0 Au 3+ + 3 e Au 0

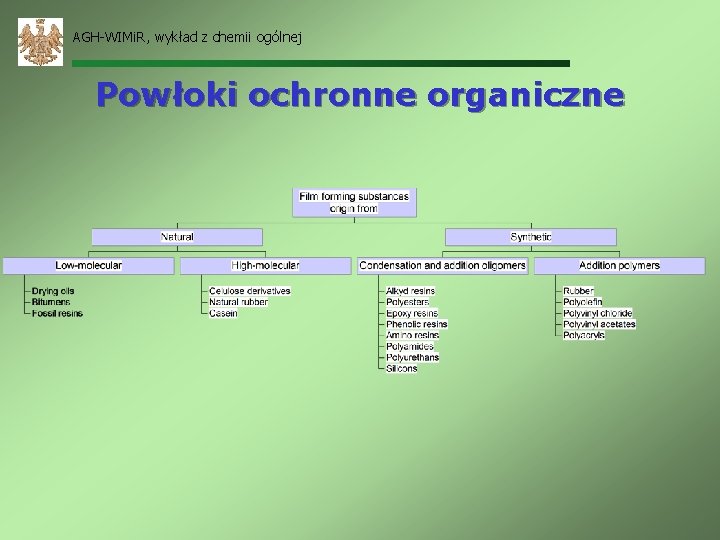
AGH-WIMi. R, wykład z chemii ogólnej Powłoki ochronne organiczne

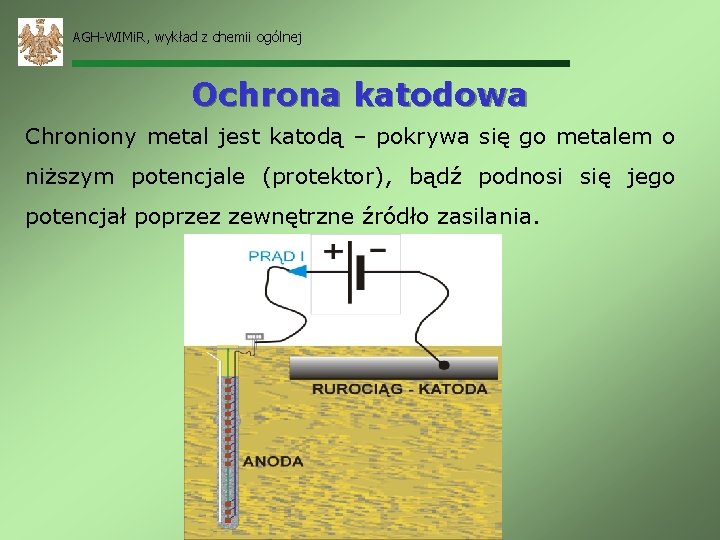
AGH-WIMi. R, wykład z chemii ogólnej Ochrona katodowa Chroniony metal jest katodą – pokrywa się go metalem o niższym potencjale (protektor), bądź podnosi się jego potencjał poprzez zewnętrzne źródło zasilania.

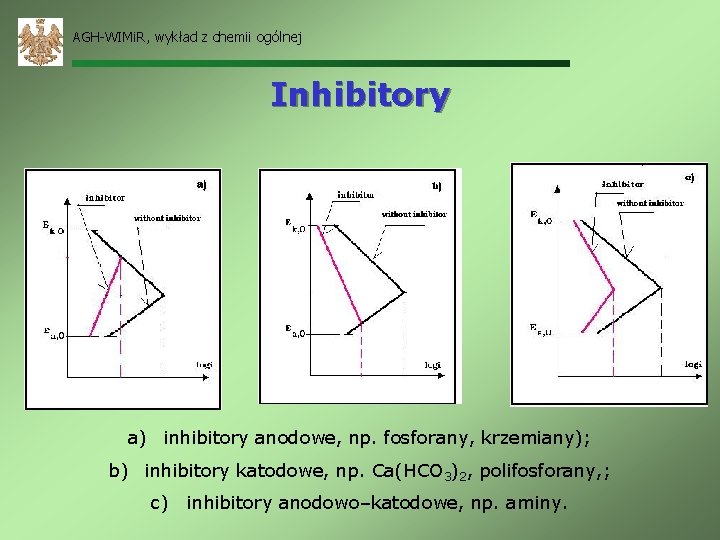
AGH-WIMi. R, wykład z chemii ogólnej Inhibitory a) inhibitory anodowe, np. fosforany, krzemiany); b) inhibitory katodowe, np. Ca(HCO 3)2, polifosforany, ; c) inhibitory anodowo–katodowe, np. aminy.