PODSTAWY CHEMII INYNIERIA BIOMEDYCZNA Wykad 1 PODSTAWY CHEMII

PODSTAWY CHEMII INŻYNIERIA BIOMEDYCZNA Wykład 1

PODSTAWY CHEMII Wykładowca Prof. dr hab. inż. Marta Radecka, n B-6, III p. 306, tel (12) (617) 25 -26 n e-mail: radecka@agh. edu. pl n Strona www: http: //galaxy. uci. agh. edu. pl/~radecka/ n http: //www. agh. edu. pl/ Pracownicy Strony domowe pracowników Marta Radecka 10/31/2020 Inżynieria Biomedyczna, I rok 2

PODSTAWY CHEMII n n n Do czego służą wykłady i jak się zdaje egzamin? Program wykładów i laboratorium odpowiada dokładnie „zawartości” egzaminu Egzamin pisemny ü żeby do niego przystąpić, trzeba zaliczyć laboratorium ü każdy ma prawo zdawać egzamin trzykrotnie Student ma prawo do trzykrotnego przystąpienia do egzaminu w zaplanowanych terminach, w tym jeden raz w terminie podstawowym i dwa razy w terminie poprawkowym. Nieusprawiedliwiona nieobecność na egzaminie w danym terminie powoduje utratę tego terminu. Student, który nie uzyskał zaliczenia w terminie podstawowym ma prawo po jego uzyskaniu przystąpić do egzaminu w terminach poprawkowych. Jeżeli student nie uzyskał zaliczenia do czasu terminów poprawkowych egzaminu, brak zaliczenia nie usprawiedliwia nieobecności na egzaminie i skutkuje utratą wszystkich terminów egzaminów, które odbyły się przed uzyskaniem zaliczenia. Jeżeli z przyczyn losowych student nie wykorzystał przysługujących mu terminów, Dziekan w porozumieniu z prowadzącym przedmiot, wyznacza dodatkowe terminy egzaminów. Regulamin studiów akademii Górniczo-Hutniczej Im. Stanisława Staszica (obowiązujący od 1 października 2012 r) 10/31/2020 Inżynieria Biomedyczna, I rok 3
Zaliczenie przedmiotu n Skala ocen Przy zaliczeniach zajęć i egzaminach oraz wystawianiu oceny końcowej stosuje się i wpisuje do indeksu następujące oceny: a) 91 – 100% bardzo dobry (5. 0); b) 81 – 90% plus dobry (4. 5); c) 71 – 80% dobry (4. 0); d) 61 – 70% plus dostateczny (3. 5); e) 50 – 60% dostateczny (3. 0); f) poniżej 50% niedostateczny (2. 0). n Ocena końcowa 0. 6 oceny egzaminu + 0. 4 oceny laboratorium 10/31/2020 Inżynieria Biomedyczna, I rok 4

Najważniejsze podręczniki * * * A. Bielański - Chemia ogólna i nieorganiczna A. Bielański - Podstawy chemii nieorganicznej F. A. Cotton, G. Wilkinson, P. L. Gaus - Chemia nieorganiczna. Podstawy. J. D. Lee - Zwięzła chemia nieorganiczna P. A. Cox – Chemia nieorganiczna. Krótkie wykłady * * dla bardziej ambitnych: R. G. Wells - Strukturalna chemia nieorganiczna L. Jones, P. Atkins – Chemia ogólna Wszelkie inne podręczniki mające w nazwie - chemia ogólna lub chemia nieorganiczna 10/31/2020 Inżynieria Biomedyczna, I rok 5

Chemia jest nauką przyrodniczą Definicja: chemia jest nauką, która zajmuje się składem, strukturą i właściwościami substancji oraz reakcjami, w których jedna substancja zmienia się w inną Zasady nowoczesnej chemii: poszukiwanie prawidłowości w zachowaniu się różnych substancji poszukiwanie modeli, które tłumaczą obserwacje modele powinny tłumaczyć zachowanie innych substancji i jeśli to możliwe obejmować relacje ilościowe modele powinno dać się weryfikować doświadczalnie 10/31/2020 Inżynieria Biomedyczna, I rok 6

Program wykładów n n Równowagi w roztworach elektrolitów Elementy termodynamiki Elementy elektrochemii Trochę mechaniki kwantowej n n n budowa atomu, cząsteczki, wiązania chemiczne Stany materii, reguła faz Kinetyka reakcji Koloidy 10/31/2020 Inżynieria Biomedyczna, I rok 7

Program laboratorium n n n n Stężenia roztworów + stechiometria Równowaga chemiczna, Kolokwium nr 1, Dysocjacja elektrolityczna + p. H roztworu, Kolokwium nr 2 Równowagi w roztworach związków trudnorozpuszczalnych, Kolokwium nr 3 Roztwory buforowe, hydroliza , Kolokwium nr 4 Kolokwium nr 5, elementy analizy chemicznej, pobranie szła i przygotowanie szła Elementy analizy jakościowej Elementy analizy ilościowej 10/31/2020 Inżynieria Biomedyczna, I rok 8

HARMONOGRAM ZAJĘĆ http: //galaxy. uci. agh. edu. pl/~radecka/ Zajęcia nr 1 -6: 06. 10; 13. 10; 20. 10; 27. 10; 03. 11; 10. 11. 2015 Grupy 1, 2, 3 godzina 8. 00 -9. 30 Grupy 4, 5, 6 godzina 9. 45 -11. 15 Grupy 7, 8, 9 godzina 11. 30 -13. 00 Grupy 10, 11 godzina 13. 15 -14. 45 Grupa 1, 2, 3, 7, 8, 9 Zajęcia nr 7 -10: 17. 11; 01. 12; 15. 12 2015; 12. 01 2016 n Grupa 1, 2, 3 godzina 8. 00 -11. 00 n Grupa 7, 8, 9 godzina 11. 30 -14. 30 Grupa 4, 5, 6, 10, 11 Zajęcia nr 7 -10: 24. 11; 08. 12. 22. 12 2015; 19. 01 2016 n Grupa 4, 5, 6 godzina 8. 00 -11. 00 n Grupa 10, 11 godzina 11. 30 -14. 30 Inżynieria Biomedyczna, I rok 10/31/2020 9

Podział reakcji n Wszystkie reakcje chemiczne można podzielić na odwracalne i nieodwracalne: n Reakcja nieodwracalna przebiega tylko w jednym kierunku - od substratów do produktów ( ) n Reakcja odwracalna może przebiegać w obu kierunkach ( ) c 10/31/2020 Reakcjenieodwracalne przebiegają tak długo, aż wyczerpie się jeden lub kilka substratów Inżynieria Biomedyczna, I rok 10

A reakcje odwracalne ? Równowaga 10/31/2020 Inżynieria Biomedyczna, I rok 11

Szybkość reakcji chemicznej Dla reakcji chemicznej opisanej równaniem: Szybkość reakcji: Gdzie szybkość zmian stężenia reagenta i Szybkość reakcji często można przedstawić za pomocą równania (empirycznego) kinetycznego: 10/31/2020 Inżynieria Biomedyczna, I rok k- stała reakcji, , - rząd reakcji 12

SZYBKOŚĆ REAKCJI Szybkość reakcji odwracalnej gdzie k 1 i k 2 - stałe szybkości reakcji, zależne tylko od rodzaju reakcji, temperatury i ciśnienia całkowitego (dla reakcji w fazie gazowej) CZAS 10/31/2020 Inżynieria Biomedyczna, I rok 13

Prawo równowagi W stanie równowagi termodynamicznej ustala się stan równowagi dynamicznej: prędkość reakcji prostej i odwrotnej jest taka sama Stężenie reagenta i w stanie równowagi 10/31/2020 Inżynieria Biomedyczna, I rok 14
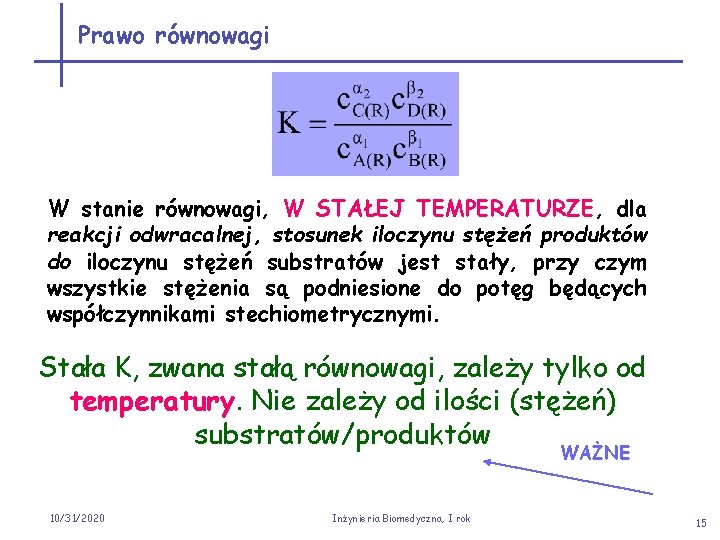
Prawo równowagi W stanie równowagi, W STAŁEJ TEMPERATURZE, dla reakcji odwracalnej, stosunek iloczynu stężeń produktów do iloczynu stężeń substratów jest stały, przy czym wszystkie stężenia są podniesione do potęg będących współczynnikami stechiometrycznymi. Stała K, zwana stałą równowagi, zależy tylko od temperatury. Nie zależy od ilości (stężeń) substratów/produktów WAŻNE 10/31/2020 Inżynieria Biomedyczna, I rok 15

Stała równowagi K (różny zapis) to jest ogólne prawo równowagi. . . (prawo działania mas, a-aktywność) to jest prawo równowagi dla reakcji w gazach, przy niezbyt wysokich ciśnieniach (p. A, p. B, p. C, p. D –ciśnienia cząstkowe poszczególnych gazów) to jest prawo równowagi dla reakcji w mieszaninach (roztworach), przy niezbyt wysokich stężeniach ([A], [B], [C], [D] stężenia poszczególnych składników) 10/31/2020 Inżynieria Biomedyczna, I rok 16
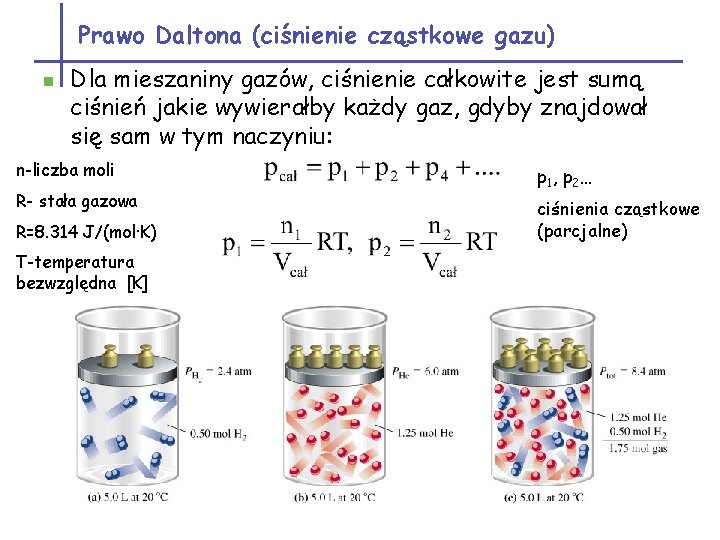
Prawo Daltona (ciśnienie cząstkowe gazu) n Dla mieszaniny gazów, ciśnienie całkowite jest sumą ciśnień jakie wywierałby każdy gaz, gdyby znajdował się sam w tym naczyniu: n-liczba moli R- stała gazowa R=8. 314 J/(mol·K) T-temperatura bezwzględna [K] p 1 , p 2… ciśnienia cząstkowe (parcjalne)
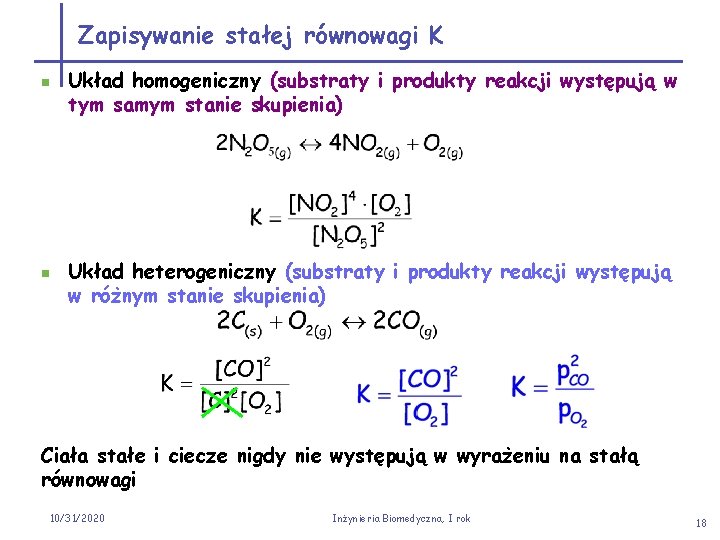
Zapisywanie stałej równowagi K n n Układ homogeniczny (substraty i produkty reakcji występują w tym samym stanie skupienia) Układ heterogeniczny (substraty i produkty reakcji występują w różnym stanie skupienia) Ciała stałe i ciecze nigdy nie występują w wyrażeniu na stałą równowagi 10/31/2020 Inżynieria Biomedyczna, I rok 18

Własności równowagi Układy w równowadze są n DYNAMICZNE (stała i taka sama prędkość reakcji prostej i odwrotnej) n ODWRACALNE n Równowagę można osiągnąć z każdego kierunku n n n W stanie równowagi występują wszystkie reagenty Jeżeli K>>1 w stanie równowagi dominują produkty Jeżeli znamy wartość K i stężenia aktualne to można określić: n n 10/31/2020 Czy układ jest w stanie równowagi W którą stronę biegnie reakcja Inżynieria Biomedyczna, I rok 19
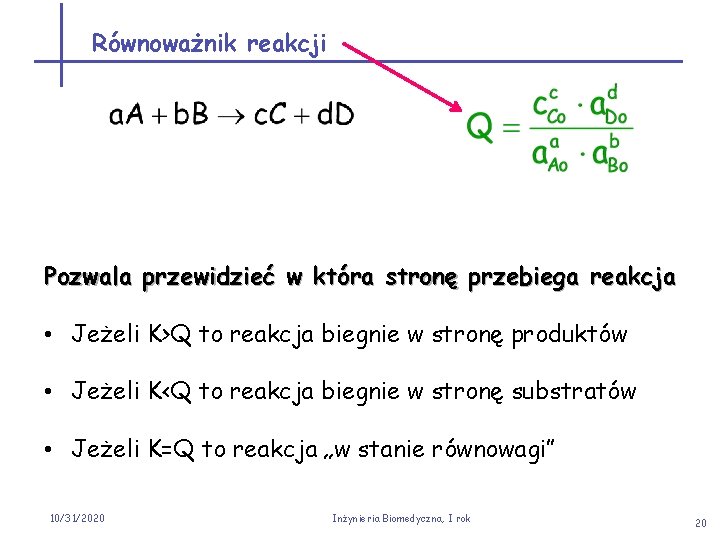
Równoważnik reakcji Pozwala przewidzieć w która stronę przebiega reakcja • Jeżeli K>Q to reakcja biegnie w stronę produktów • Jeżeli K<Q to reakcja biegnie w stronę substratów • Jeżeli K=Q to reakcja „w stanie równowagi” 10/31/2020 Inżynieria Biomedyczna, I rok 20
![Jeszcze o stałej równowagi n n Jednostki stężenia: 3 n [ ] mol/dm otrzymujemy Jeszcze o stałej równowagi n n Jednostki stężenia: 3 n [ ] mol/dm otrzymujemy](http://slidetodoc.com/presentation_image/34273318353abb26cb022e863a475ac3/image-21.jpg)
Jeszcze o stałej równowagi n n Jednostki stężenia: 3 n [ ] mol/dm otrzymujemy Kc n Dla składników gazowych, p=(n/V)·RT p jest proporcjonalne do stężenia, Jeżeli p wyrażone jest w atmosferach otrzymujemy Kp n Kc i Kp mają różne wartości (chociaż ilości składników są takie same) Jednostka stałej K zależy od współczynników stechiometrycznych reakcji oraz sposobu wyrażenia koncentracji składników 10/31/2020 Inżynieria Biomedyczna, I rok 21
![Jaka jest relacja pomiędzy Kc i Kp ? [A] [B] [C] [D] gdzie ∆n=(c+d)-(a+b) Jaka jest relacja pomiędzy Kc i Kp ? [A] [B] [C] [D] gdzie ∆n=(c+d)-(a+b)](http://slidetodoc.com/presentation_image/34273318353abb26cb022e863a475ac3/image-22.jpg)
Jaka jest relacja pomiędzy Kc i Kp ? [A] [B] [C] [D] gdzie ∆n=(c+d)-(a+b) Jeżeli ∆n=0 to Kp=Kc 10/31/2020 Inżynieria Biomedyczna, I rok 22
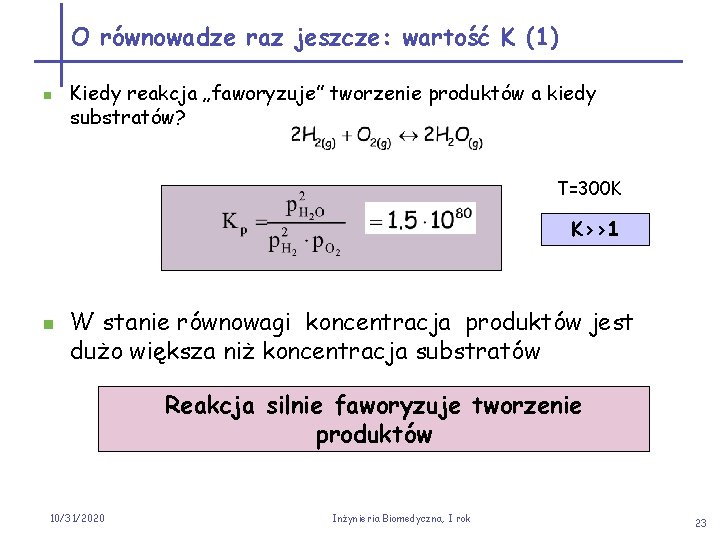
O równowadze raz jeszcze: wartość K (1) n Kiedy reakcja „faworyzuje” tworzenie produktów a kiedy substratów? T=300 K K>>1 n W stanie równowagi koncentracja produktów jest dużo większa niż koncentracja substratów Reakcja silnie faworyzuje tworzenie produktów 10/31/2020 Inżynieria Biomedyczna, I rok 23

O równowadze raz jeszcze (2) K<<1 W stanie równowagi koncentracja produktów jest mniejsza niż substratów Reakcja silnie faworyzuje tworzenie substratów …. . a w przypadku reakcji odwrotnej? Reakcja silnie faworyzuje tworzenie produktów 10/31/2020 Inżynieria Biomedyczna, I rok 24

Równowaga i bodźce zewnętrzne n Stan równowagi może być przesunięty jeżeli zmienimy: n koncentrację składników n ciśnienie zewnętrzne (w przypadku reagentów gazowych) n temperaturę Reguła przekory Le Chateliera Jeśli w warunkach równowagi zmienimy jeden z parametrów reakcji (temperaturę lub ciśnienie), to równowaga reakcji przesunie się w taki sposób, by zmniejszyć działanie bodźca (układ przeciwstawi się zmianie). . . 10/31/2020 Inżynieria Biomedyczna, I rok Henri Le Chatelier 1850 -1936 25
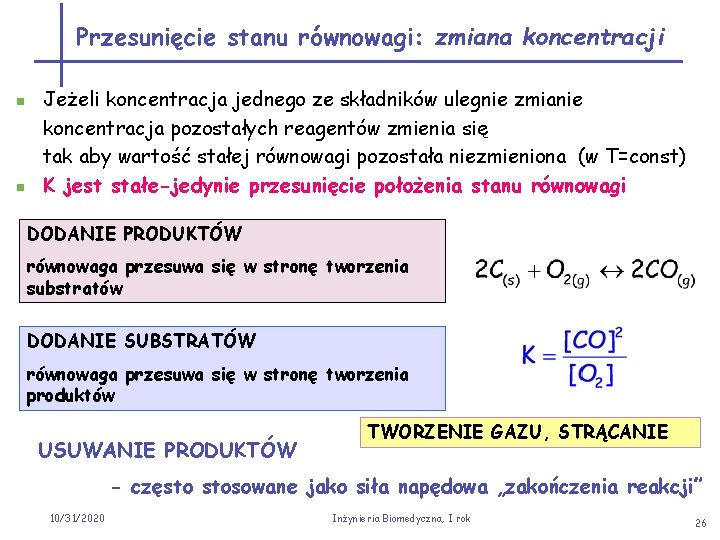
Przesunięcie stanu równowagi: zmiana koncentracji n n Jeżeli koncentracja jednego ze składników ulegnie zmianie koncentracja pozostałych reagentów zmienia się tak aby wartość stałej równowagi pozostała niezmieniona (w T=const) K jest stałe-jedynie przesunięcie położenia stanu równowagi DODANIE PRODUKTÓW równowaga przesuwa się w stronę tworzenia substratów DODANIE SUBSTRATÓW równowaga przesuwa się w stronę tworzenia produktów USUWANIE PRODUKTÓW TWORZENIE GAZU, STRĄCANIE - często stosowane jako siła napędowa „zakończenia reakcji” 10/31/2020 Inżynieria Biomedyczna, I rok 26

Efekt zmiany ciśnienia (równowaga w gazach) Wzrost ciśnienia (zmniejszenie objętości) 4 mole gazu 2 mole gazu przesunięcie w prawo w stronę mniejszej ilości 10/31/2020 moli gazów 27

Efekt zmiany ciśnienia (równowaga w gazach) spadek ciśnienia (zwiększenie objętości) 4 mole gazu 2 mole gazu przesunięcie w lewo 10/31/2020 w stronę większej ilości moli gazów 28
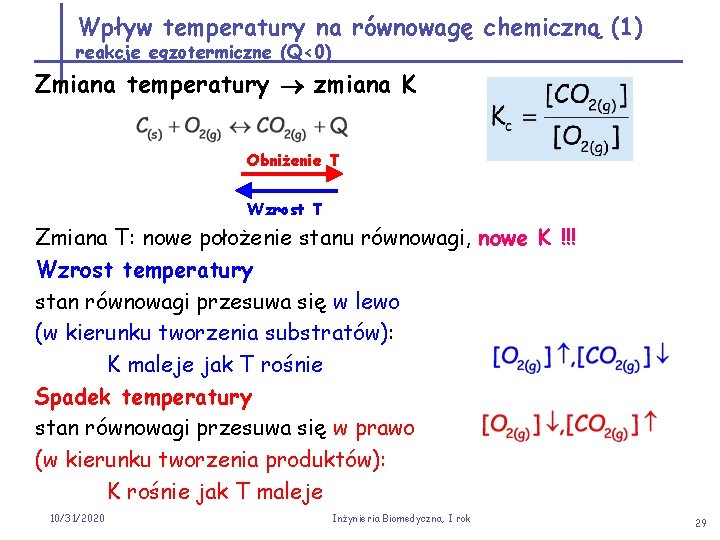
Wpływ temperatury na równowagę chemiczną (1) reakcje egzotermiczne (Q<0) Zmiana temperatury zmiana K Obniżenie T Wzrost T Zmiana T: nowe położenie stanu równowagi, nowe K !!! Wzrost temperatury stan równowagi przesuwa się w lewo (w kierunku tworzenia substratów): K maleje jak T rośnie Spadek temperatury stan równowagi przesuwa się w prawo (w kierunku tworzenia produktów): K rośnie jak T maleje 10/31/2020 Inżynieria Biomedyczna, I rok 29
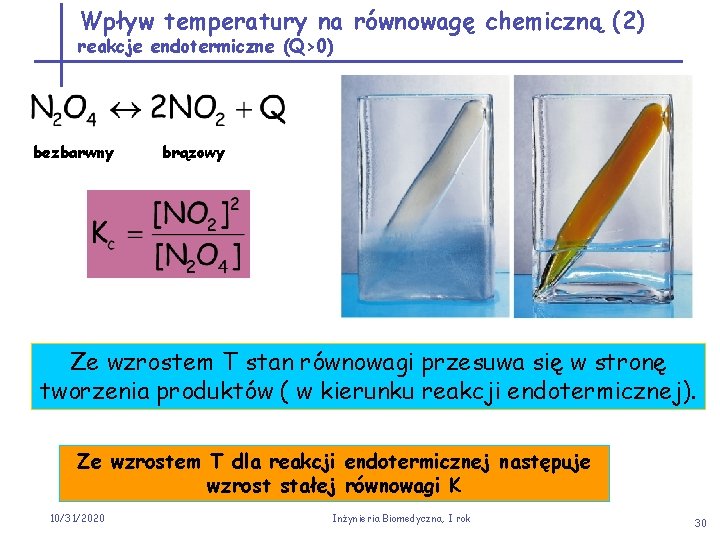
Wpływ temperatury na równowagę chemiczną (2) reakcje endotermiczne (Q>0) bezbarwny brązowy Ze wzrostem T stan równowagi przesuwa się w stronę tworzenia produktów ( w kierunku reakcji endotermicznej). Ze wzrostem T dla reakcji endotermicznej następuje wzrost stałej równowagi K 10/31/2020 Inżynieria Biomedyczna, I rok 30
- Slides: 30