Akademia GrniczoHutnicza WIMi R wykad z chemii oglnej


















![AGH-University of Science and Technology, lecture on General Chemistry Przykład: K 4[Fe(CN)6] – sześciocyjanożelazian AGH-University of Science and Technology, lecture on General Chemistry Przykład: K 4[Fe(CN)6] – sześciocyjanożelazian](https://slidetodoc.com/presentation_image_h2/948b9e019d029e3e26d7a5a386d7980a/image-24.jpg)





















- Slides: 45

Akademia Górniczo-Hutnicza, WIMi. R, wykład z chemii ogólnej CHEMIA OGÓLNA Wykład 1

AGH-University of Science and Technology, lecture on General Chemistry Katedra Chemii i Korozji Metali Wydziału Odlewnictwa ul. Reymonta 23 budynek D 8 wykładowca - prof. dr hab. Jacek Banaś, ćwiczenia laboratoryjne: dr E. Wisła (IMi. R), dr hab. H. Krawiec, dr J. Zawada, dr inż. K. Moskwa, dr inż. M. Starowicz, dr U. Lelek-Borkowska, mgr inż. A. Łukaszczyk

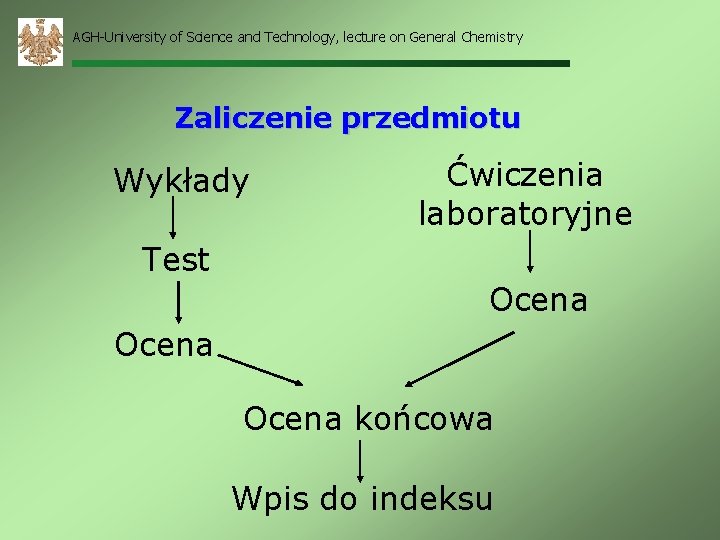
AGH-University of Science and Technology, lecture on General Chemistry Zaliczenie przedmiotu Wykłady Ćwiczenia laboratoryjne Test Ocena końcowa Wpis do indeksu

Akademia Górniczo-Hutnicza, WIMi. R, wykład z chemii ogólnej KLASYFIKACJA ZWIĄZKÓW NIEORGANICZNYCH • tlenki, • kwasy, • wodorotlenki, • sole, • wodorki, • związki kompleksowe, • inne.

AGH-University of Science and Technology, lecture on General Chemistry TLENKI n – wartościowość pierwiastka O – stopień utlenienia: – 2 (– 1 w nadtlenkach). Wszystkie pierwiastki tworzą tlenki, zarówno metale, metaloidy (pierwiastki amfoteryczne) jak i niemetale.

AGH-University of Science and Technology, lecture on General Chemistry Nazewnictwo tlenków: tlenek + nazwa pierwiastka i jego wartościowość w nawiasie (jeśli więcej niż jedna możliwa). Przykład: stopień utlenienia sodu - +1, stopień utlenienia tlenu - -2, ostatecznie: tlenek sodu

AGH-University of Science and Technology, lecture on General Chemistry nazwa systematyczna: tlenek dwuwodoru nazwa zwyczajowa: woda stopień utlenienia węgla - +4, nazwa systematyczna: dwutlenek węgla (IV), tlenek węgla (IV) nazwa zwyczajowa: dwutlenek węgla

AGH-University of Science and Technology, lecture on General Chemistry Przykład: K 2 O – tlenek potasu, Ca. O – tlenek wapnia, Al 2 O 3 – tlenek glinu, N 2 O – tlenek dwuazotu (I), tlenek azotu (I), podtlenek azotu, NO - tlenek azotu (II), N 2 O 3 - trójtlenek dwuazotu (III), tlenek azotu (III), NO 2 – dwutlenek azotu (IV), N 2 O 5 - pięciotlenek dwuazotu (V), tlenek azotu (V), Cl 2 O 7 – siedmiotlenek dwuchloru (VII), tlenek chloru(VII).

AGH-University of Science and Technology, lecture on General Chemistry KWASY n – wartościowość reszty kwasowej H– stopień utlenienia: +1 (– 1 w wodorkach). Kwasy tworzą niemetale. Rodzaje kwasów: • beztlenowe, • tlenowe.

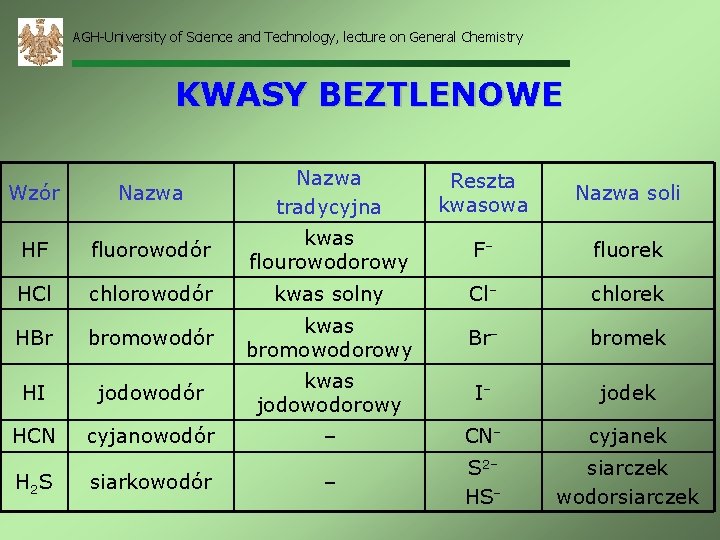
AGH-University of Science and Technology, lecture on General Chemistry KWASY BEZTLENOWE Wzór Nazwa tradycyjna Reszta kwasowa Nazwa soli HF fluorowodór kwas flourowodorowy F– fluorek HCl chlorowodór kwas solny Cl– chlorek HBr bromowodór kwas bromowodorowy Br– bromek HI jodowodór kwas jodowodorowy I– jodek HCN cyjanowodór – CN– cyjanek – S 2– HS– siarczek wodorsiarczek H 2 S siarkowodór

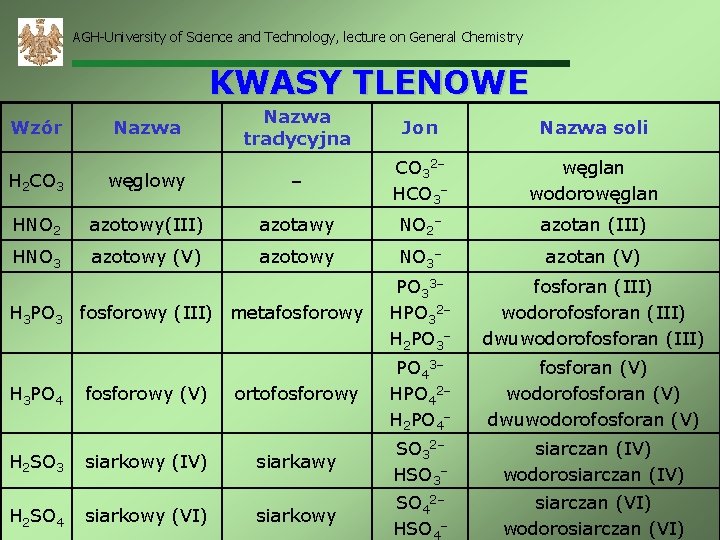
AGH-University of Science and Technology, lecture on General Chemistry KWASY TLENOWE Wzór Nazwa tradycyjna Jon Nazwa soli węglan wodorowęglan H 2 CO 3 węglowy – CO 32– HCO 3– HNO 2 azotowy(III) azotawy NO 2– azotan (III) HNO 3 azotowy (V) azotowy NO 3– azotan (V) H 3 PO 3 fosforowy (III) metafosforowy PO 33– HPO 32– H 2 PO 3– fosforan (III) wodorofosforan (III) dwuwodorofosforan (III) H 3 PO 4 ortofosforowy PO 43– HPO 42– H 2 PO 4– fosforan (V) wodorofosforan (V) dwuwodorofosforan (V) siarkawy SO 32– HSO 3– siarczan (IV) wodorosiarczan (IV) siarkowy SO 42– HSO 4– siarczan (VI) wodorosiarczan (VI) H 2 SO 3 H 2 SO 4 fosforowy (V) siarkowy (IV) siarkowy (VI)

AGH-University of Science and Technology, lecture on General Chemistry KWASY TLENOWE Wzór Nazwa tradycyjna Jon Nazwa soli HCl. O chlorowy (I) podchlorawy Cl. O– chloran (I) HCl. O 2 chlorowy (III) chlorawy Cl. O 2– chloran (III) HCl. O 3 chlorowy (V) chlorowy Cl. O 3– chloran (V) nadchlorowy Cl. O 4– chloran (VII) HCl. O 4 chlorowy (VII) HBr. O 3 bromowy (V) – Br. O 3– bromian (V) HIO 4 jodowy (VII) – IO 4– jodan (VII)

AGH-University of Science and Technology, lecture on General Chemistry WODOROTLENKI n – wartościowość metalu. Wodorotlenki tworzą metale i metaloidy.

AGH-University of Science and Technology, lecture on General Chemistry Przykład: Li. OH – wodorotlenek litu, Ca(OH)2 – wodorotlenek wapnia, Al(OH)3 – wodorotlenek glinu, Fe(OH)2 – wodorotlenek żelaza (II), Fe(OH)3 - wodorotlenek żelaza (III), Sn(OH)2 - wodorotlenek cyny (II), Sn(OH)4 - wodorotlenek cyna (IV).

AGH-University of Science and Technology, lecture on General Chemistry SOLE n – wartościowość metalu, m – wartościowość reszty kwasowej. WODOROSOLE HYDROKSYSOLE

AGH-University of Science and Technology, lecture on General Chemistry Przykład: Na. Cl – chlorek sodu (sól kuchenna), Ca(HCO 3)2 – wodorowęglan wapnia, Mg 3(PO 3)2 – fosforan (V) magnezu, Fe 2 S 3 – siarczek żelaza (III), KNO 3 – azotan (V) potasu (saletra potasowa), (NH 4)(H 2 PO 4)- dwuwodorofosforan (V) amonu, Al(OH)2 Cl - dwuhydroksochlorek glinu.

AGH-University of Science and Technology, lecture on General Chemistry WODORKI n – wartościowość pierwiastka (grupy 1 -15), n – wartościowość pierwiastka (grupy 16, 17).

AGH-University of Science and Technology, lecture on General Chemistry Przykład: Li. H – wodorek litu, BH 3 – wodorek boru, CH 4 - metan, PH 3 – wodorek fosforu, Si. H 4 – wodorek krzemu, H 2 S - siarkowodór, H 2 Se - selenowodór, HF - fluorowodór, HCl - chlorowodór.

AGH-University of Science and Technology, lecture on General Chemistry ZWIĄZKI AMFOTERYCZNE Amfoteryzm – zdolność pierwiastka do zachowania się jak metal, bądź niemetal w zależności od środowiska. Pierwiastki o charakterze amfoterycznym: Zn, Pb, Sn, Al, Be, As, Sb, Cr, Mn. Przykład: 1) W kwasach: Zn. O + 2 HCl Zn. Cl 2 + H 2 O w zasadach: Zn. O + 2 Na. OH + H 2 O Na 2[Zn(OH)4] 2) W kwasach: Al(OH)3 + 3 HCl Al. Cl 3 + 3 H 2 O w zasadach: Al(OH)3 + Na. OH Na[Al(OH)4]

AGH-University of Science and Technology, lecture on General Chemistry Dla pierwiastków amfoterycznych istnieje równowaga pomiędzy formą zasadową, a kwasową: A(OH)m Hm. AOm A – pierwiastek amfoteryczny. Przykład: Sn(OH)4 H 4 Sn. O 4 4 H+ + Sn. O 44 Al(OH)3 H 3 Al. O 3 3 H+ + Al. O 33 -

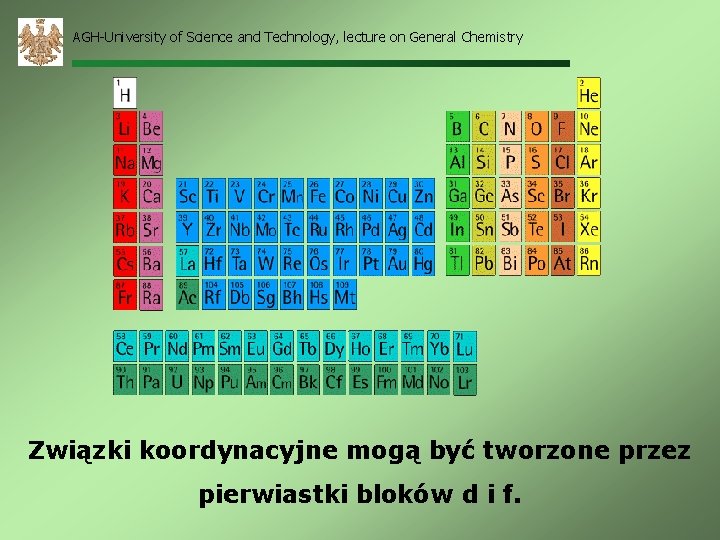
AGH-University of Science and Technology, lecture on General Chemistry ZWIĄZKI KOMPLEKSOWE KOMPLEKSY METALICZNE (związki koordynacyjne) – atom lub jon metalu z wolnymi orbitalami d, zdolnymi do przyjęcia pary elektronów, otoczony ligandami – jonami lub cząsteczkami z wolną parą elektronów.

AGH-University of Science and Technology, lecture on General Chemistry Związki koordynacyjne mogą być tworzone przez pierwiastki bloków d i f.

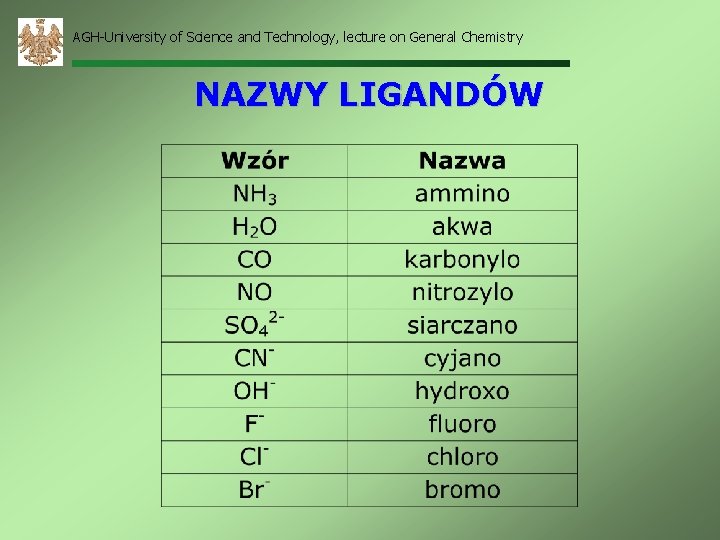
AGH-University of Science and Technology, lecture on General Chemistry NAZWY LIGANDÓW
![AGHUniversity of Science and Technology lecture on General Chemistry Przykład K 4FeCN6 sześciocyjanożelazian AGH-University of Science and Technology, lecture on General Chemistry Przykład: K 4[Fe(CN)6] – sześciocyjanożelazian](https://slidetodoc.com/presentation_image_h2/948b9e019d029e3e26d7a5a386d7980a/image-24.jpg)
AGH-University of Science and Technology, lecture on General Chemistry Przykład: K 4[Fe(CN)6] – sześciocyjanożelazian (II) potasu, K 3[Fe(CN)6]– sześciocyjanożelazian (III) potasu, Fe(CO)5 – pięciokarbonylek żelaza(0), [Cr(NH 3)3(H 2 O)3]Cl – chlorek trójamminotrójakwachromu(III), [Ni. Cl 4]2 - - jon czterochloroniklanowy (II), [Co(SO 4)(NH 3)5]+–jon pięcioamminosiarczanocobaltu(III), [Fe(OH)(H 2 O)5]2+ – jon pięcioakwahydroksożelaza (III).

AGH-University of Science and Technology, lecture on General Chemistry REAKCJE CHEMICZNE Równanie reakcji jest symbolicznym rzeczywistej reakcji chemicznej substraty produkty a, b, c, d – współczynniki stechiometryczne. zapisem

AGH-University of Science and Technology, lecture on General Chemistry Odczytywanie równania reakcji Powyższe równanie można odczytać na dwa sposoby: 1) dwie cząsteczki wodoru reagują z jedną cząsteczką tlenu dając dwie cząsteczki wody, lub 2) dwa mole wodoru reagując z jednym molem tlenu dają 2 mole wody.

AGH-University of Science and Technology, lecture on General Chemistry Obydwie strony równania muszą się zgadzać, czyli ilość atomów każdego pierwiastka musi być taka sama po obydwu stronach równania. Przykład: Ponieważ po stronie produktów są dwa atomy sodu, Na. OH musi zostać przemnożone przez 2. Teraz, aby zgadzała się ilośc wodoru należy wziąć dwie cząsteczki wody po stronie produktów.

AGH-University of Science and Technology, lecture on General Chemistry TYPY REAKCJI CHEMICZNYCH SYNTEZA – dwa lub więcej substratów tworzy jeden produkt. Przykład:

AGH-University of Science and Technology, lecture on General Chemistry ANALIZA – jeden substrat rozkłada się na produkty. Przykład:

AGH-University of Science and Technology, lecture on General Chemistry REAKCJA WYMIANY POJEDYNCZEJ – tylko jeden pierwiastek ulega wymianie w związku podczas reakcji. Przykład:

AGH-University of Science and Technology, lecture on General Chemistry REAKCJA WYMIANY PODWÓJNEJ – dwa pierwiastki ulegają wymianie. Przykład:

AGH-University of Science and Technology, lecture on General Chemistry REACJE REDOX – nazwa pochodzi od procesów redukcji i utleniania: Utlenianie jest związane z utratą elektronu przez atom lub cząsteczkę, czyli podwyższeniem stopnia utlenienia. Redukcja związana jest z przyjęciem obniżeniem (redukcją) stopnia utlenienia. elektronu i

AGH-University of Science and Technology, lecture on General Chemistry Przykład: Teraz można uzgodnić równanie reakcji:

AGH-University of Science and Technology, lecture on General Chemistry

AGH-University of Science and Technology, lecture on General Chemistry EFFEKT CIEPLNY REAKCJI Układ – reagenty, to co poddajemy obserwacji, Otoczenie- wszystko poza układem, Ciepło (Q) – energia wymieniona z otoczeniem.

AGH-University of Science and Technology, lecture on General Chemistry I ZASADA TERMODYNAMIKI U – zmiana energi wewnętrznej układu, Q - ciepło, W – praca.

AGH-University of Science and Technology, lecture on General Chemistry Jedynym znaczącym rodzajem pracy wykonywanej przez układ, bądź na układzie jest praca objętościowa: p – ciśnienie zewnętrzne, V = V 2 - V 1 – zmiana objętości. Znak ujemny znaczy, że praca została wykonana przez układ, znak dodatni – praca została wykonana na układzie.

AGH-University of Science and Technology, lecture on General Chemistry W warunkach izobarycznych: definiując entalpię jako: otrzymujemy:

AGH-University of Science and Technology, lecture on General Chemistry Entalpia – ciepło procesu chemicznego w warunkach izobarycznych. Entalpia jest funkcją stanu, tzn. że zmiana entalpii zależy wyłącznie od stanu początkowego i końcowego układy, a nie zależy od drogi przemiany.

AGH-University of Science and Technology, lecture on General Chemistry PRAWO HESS’A n – współczynniki stechiometryczne, H 0 - standardowa entalpia tworzenia, warunki standardowe: T=298 K (25 o. C) , p=101325 Pa(1 atm. ).

AGH-University of Science and Technology, lecture on General Chemistry H tworzenia pierwiastka zawsze 0. H 0 <0 – reakcja egzotermiczna – ciepło oddawane jest z układu do otoczenia, H 0>0 – reakcja endotermiczna – ciepło pobierane jest przez układ z otoczenia. Przykład:

AGH-University of Science and Technology, lecture on General Chemistry Przykład: Ile ciepła wydzieli się podczas spalania 1 m 3 acetylenu? Krok 1: zapisujemy i uzgadniamy równanie reakcji:

AGH-University of Science and Technology, lecture on General Chemistry Krok 2: Zapisujemy wyrażenie na standardową entalpię reakcji zgodnie z prawem Hessa: Krok 3: Wstawiamy do wyrażenia wartości standardowych entalpii tworzenia produktów i substratów: Podczas spalania 1 mola acetylenu wydziela się 2601 k. J ciepła.

AGH-University of Science and Technology, lecture on General Chemistry Krok 4: Wyliczamy ile moli acetylenu znajduje się w 1 m 3:

AGH-University of Science and Technology, lecture on General Chemistry Krok 5: Mnożymy ilość cipeła wyliczoną dla 1 mola przez ilość moli znajdującą się w 1 m 3: Odpowiedź: Podczas spalania 1 m 3 acetylenu wydziela się 116. 1 MJ ciepła.