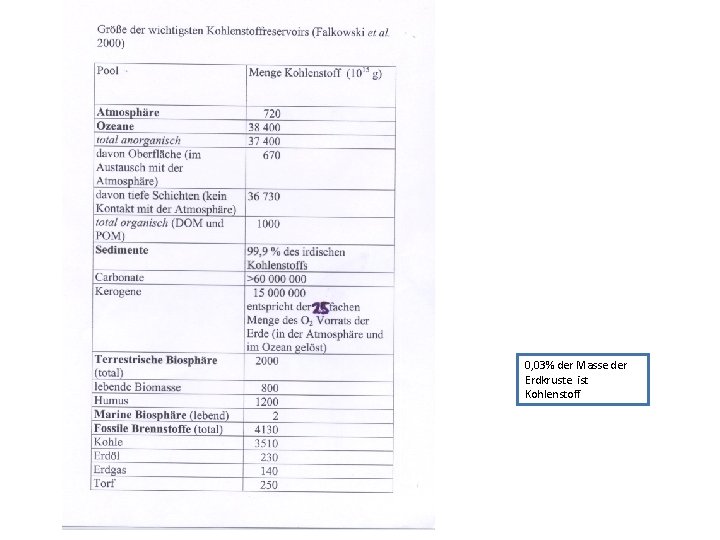
0 03 der Masse der Erdkruste ist Kohlenstoff























- Slides: 36

0, 03% der Masse der Erdkruste ist Kohlenstoff



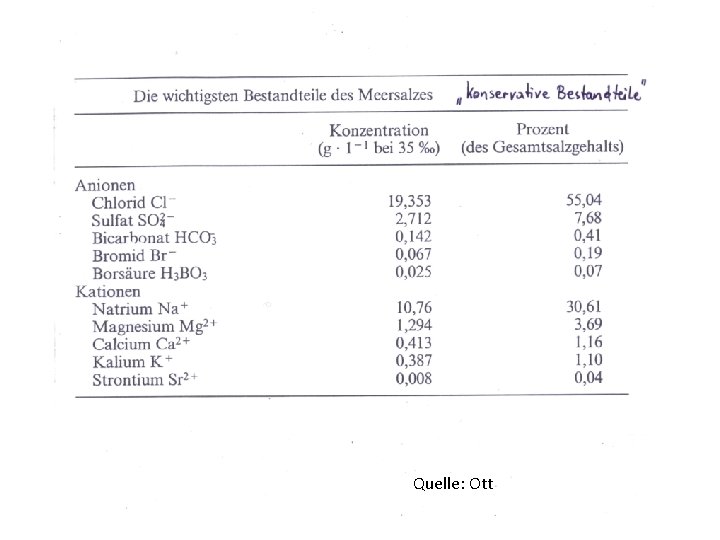
Quelle: Ott


Bei der Verwitterung der Silicate der Erdkruste wird CO 2 verbraucht: z. B. Kalkfeldspat (Anorthit) Ca. Al 2 Si 2 O 8 + 2 H 2 O + 2 CO 2 = H 2 Al 2 Si 2 O 8 + Ca(HCO 3)2 (gelöst) Beim Ausfallen der Carbonate im Ozean wird die Hälfte des bei der Verwitterung der Silicate verbrauchten CO 2 wieder frei: Ca 2+ + 2 HCO 3 - = Ca. CO 3 + H 2 O + CO 2

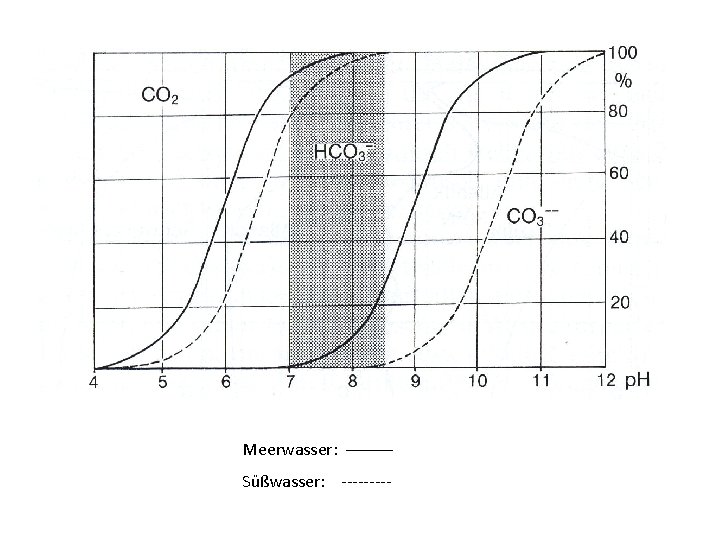
Meerwasser: ____ Süßwasser: -----

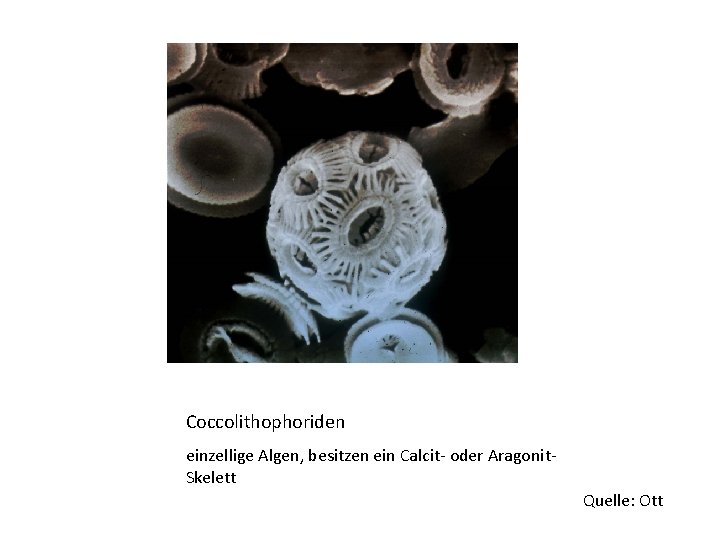
Coccolithophoriden einzellige Algen, besitzen ein Calcit- oder Aragonit. Skelett Quelle: Ott

Geochemischer Carbonat-Silicat Kreislauf Verwitterung von Kalk- oder Silicatgestein verbraucht CO 2 Ca 2 Si. O 4+4 H 2 O+4 CO 2→ 2 Ca(HCO 3)2+Si(OH)4 (gelöst) Im Meer scheidet sich Kalk ab 2 Ca(HCO 3)2→ 2 Ca. CO 3↓+2 H 2 O+2 CO 2↑ Es bilden sich Kalksedimente. In diesem Reservior verbleibt der Kohlenstoff Jahrmillionen. An den Kontinentalrändern schiebt sich der Meeresboden unter die Landmassen (Subduktion), unter hohen Drucken und Temperaturen reagiert dort das Calciumcarbonat mit Quarz 2 Ca. CO 3+Si. O 2→Ca 2 Si. O 4+2 CO 2↑

Hydrothermale Quellen in der Tiefsee an aktiven Spreizungsachsen: Ca 2+ + 2 HCO 3 - + Si(OH)4 = Ca. Si. O 3 + 2 CO 2 + 3 H 2 O (Wollastonit, Kettensilicat) Quelle: Ott

Verwitterung: Ursache der Wasserhärte und der Fruchtbarkeit von Boden und Gewässern • „Temporäre Härte“ (= Carbonathärte): Anteil an Calcium- und Magnesiumhydrogencarbonat • „Permanente Härte“ (=Sulfathärte): erfasst die gelösten Calciumund Magnesiumsalze der Salzsäure, Schwefelsäure, Salpetersäure u. a. • Pflanzennährstoffe werden freigesetzt: Sulfat, Phosphat, Kieselsäure, K+, Mg 2+, Cl-, Fe 2+/3+, Mn 2+, Zn 2+, Cu 2+ u. a.

mol L-1 atm-1

Verwitterung von Calcit, offenes System (bei 101 325 Pa = Normaldruck) • 0. 038% v/v CO 2 in der Atmosphäre p. H=8. 3 [Ca 2+] = 5 x 10 -4 mol/L entspricht 2. 8°d. H • 3% v/v CO 2 in der Bodenluft p. H = 7. 02 [Ca 2+] = 2. 8 x 10 -3 mol/L entspricht 15. 7°d. H


Effekt der Landpflanzen auf die Verwitterung • Durch den (mikrobiellen) Abbau von Pflanzenresten im Boden wird CO 2 produziert und in der Bodenlösung angereichert • Die Anwesenheit der Vegetation beschleunigt die CO 2 -Verwitterung daher um das 100 – 150 fache • Dadurch entzieht ein Wald-Ökosystem in Österreich der Atmosphäre im Jahr ca. 20 g C/m 2 also 200 kg C/ha • Dieser Kohlenstoff wird als Ca(HCO 3)2 ins Meer transportiert und dort als Ca. CO 3 ausgefällt. Die Hälfte des gebundenen CO 2 wird dabei frei, die andere Hälfte in den Carbonatsedimenten dauerhaft gespeichert.

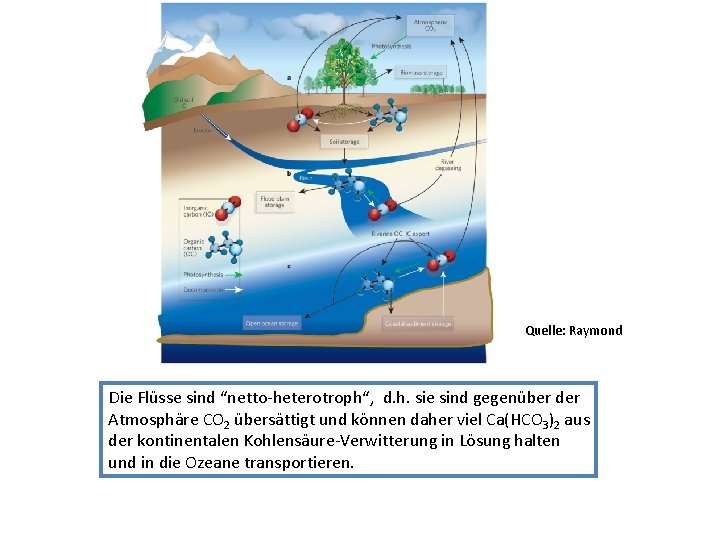
Quelle: Raymond Die Flüsse sind “netto-heterotroph“, d. h. sie sind gegenüber der Atmosphäre CO 2 übersättigt und können daher viel Ca(HCO 3)2 aus der kontinentalen Kohlensäure-Verwitterung in Lösung halten und in die Ozeane transportieren.


Carbonatsystem der Gewässer: Geschwindigkeit der Gleichgewichtseinstellung • Thermodynamisches Gleichgewicht stellt sich in der wässrigen Lösung im Allgemeinen rasch ein • Gewässer sind meist nicht im Gleichgewicht mit der Atmosphäre, weil biologische Prozesse im Wasser CO 2 schneller produzieren oder konsumieren als der CO 2 Transfer zwischen der Atmosphäre und dem Wasser erfolgt. • Bildung und Auflösung von Ca. CO 3 können verzögert erfolgen • Metastabile Gleichgewichte: Aragonit (orthorhombisch) ist in einem natürlichen Wasser thermodynamisch weniger stabil als Calcit (trigonal). Unter bestimmten Bedingungen kann sich Aragonit gegenüber Calcit metastabil verhalten.

Metallionen in Gewässern • Durch die zivilisatorischen Tätigkeiten sind die geochemischen Kreisläufe einer Anzahl metallischer Elemente beschleunigt • natürlichen Flüsse: durch Verwitterung der Gesteine, vulkanische Emissionen, Verbreitung natürlicher Aerosole aus Böden und Meerwasser • Die anthropogenen Flüsse übersteigen oft die natürlichen Flüsse. Die Gewässer sind dadurch besonders betroffen • Anthropogene Quellen für Schwermetalle sind z. B. Erzgewinnung, metallverarbeitende Industrien, Verbrennung fossiler Brennstoffe, Zementproduktion • Durch die Verbrennung fossiler Brennstoffe werden z. B. die Flüsse von As, Cd, Se, Hg, Zn in die Atmosphäre stark erhöht. Dadurch werden auch die Konzentrationen dieser Elemente im Wasser und in den Böden erhöht.


Schwermetall-Entgiftungsstrategien der Organismen • • • Enzymatische Umwandlungen von toxischen zu weniger toxischen oder flüchtigen Spezies: Hg 2+→Hg 0 As(OH)3→(CH 3)3 As+-CH 2 COO- “Arsenobetain“ • Spezielle Membranen können den Durchtritt von Metallionen in besonders gefährdete Bereiche wie Gehirn, Fetus verhindern • Hochmolekulare Verbindungen wie z. B. die Metallthionein-Proteine (=kleine Proteine mit hohem Cysteinanteil von 20 -30%) können toxische Metallionen binden und damit aus dem Verkehr ziehen

Speziierung der Schwermetalle in der Umwelt • Gelöst oder an feste bzw. kolloidale Phasen gebunden • Komplexbildung mit verschiedenen Liganden in Lösung • Verschiedene Redoxzustände • Metallorganische Verbindungen • Das Schicksal von Schwermetallen in den Gewässern hängt von der Speziierung ab (z. B. Transport in die Sedimente, Mobilisierung aus Sedimenten, Infiltration ins Grundwasser, Anreicherung in Organismen) • Die Toxizität ist stark von der jeweiligen chemischen Spezies abhängig.

Hg als umweltrelevantes Schwermetall 4 x 10 -5 Massen% Hg in der Erdkruste Hg 22+ ↔Hg 0 + Hg 2+ sehr schwerlösliche Minerale: Hg 2 Cl 2 und Hg. S HSAB-Prinzip → Thiophilie des Quecksilbers: Starke Wechselwirkung mit schwefelhaltigen Liganden z. B. Thiole = „Mercaptane“ = Quecksilberfänger

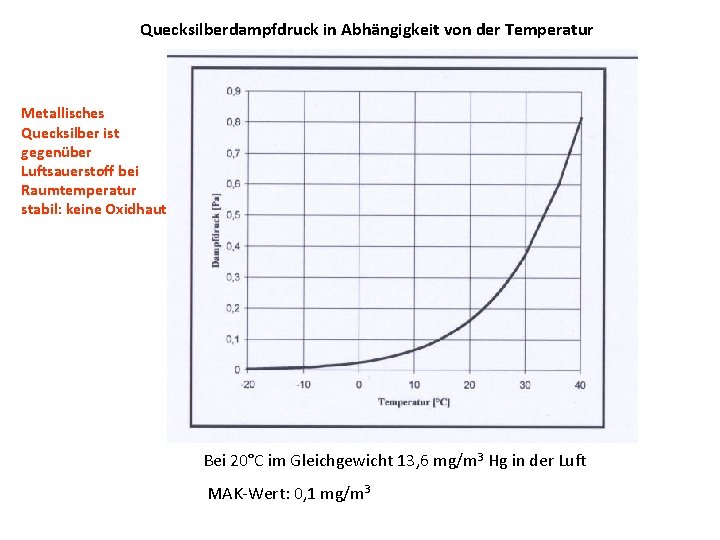
Quecksilberdampfdruck in Abhängigkeit von der Temperatur Metallisches Quecksilber ist gegenüber Luftsauerstoff bei Raumtemperatur stabil: keine Oxidhaut Bei 20°C im Gleichgewicht 13, 6 mg/m 3 Hg in der Luft MAK-Wert: 0, 1 mg/m 3

Chronische Quecksilbervergiftung z. B. durch Einatmen von Quecksilberdämpfen oder Stäuben : • Durchblutungsstörungen • Beeinträchtigung der Koordination z. B. beim Schreiben • Erregbarkeit “Mad Hatter Syndrom“ der verwendenden Hutmacher im 18. und 19. Jh (vgl. Lewis Carrols Alice im Wunderland) • Gedächtnisverlust • Bei extrem hoher Belastung: Lähmung, Taubheit, Blindheit, Tod

The United States public Health Service banned the use of mercury in the felt industry in December 1941. The levels of exposure were up to 0. 7 mg per cubic meter of air.

Quecksilberverbindungen haben nur mit sehr harten Basen wie Fluorid und Nitrat den Charakter von Ionenkristallen. In anderen Fällen besitzen die Bindungen des Quecksilbers einen ungewöhnlich hohen kovalenten Anteil → geringe elektrische Leitfähigkeit der wässrigen Lösungen, gute Löslichkeit auch in organischen Lösungsmitteln, z. B. Löslichkeit von Hg. Cl 2: Quelle: Heiko Potgeter

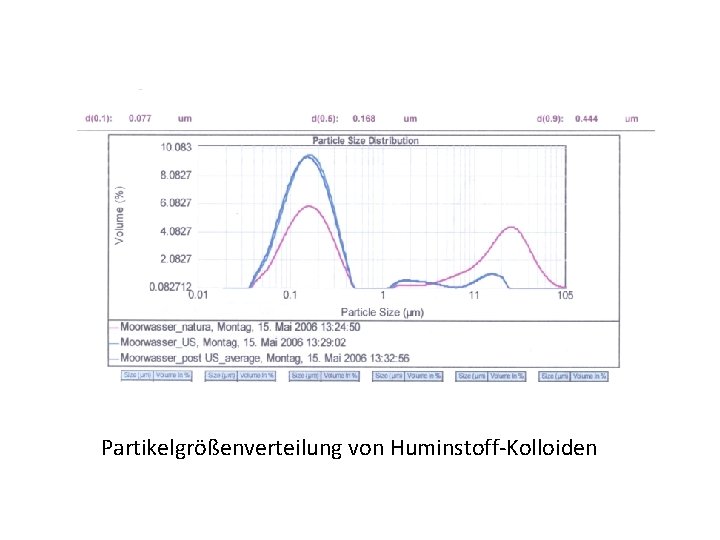
Quecksilber(II)verbindungen bilden mit vielen in Gewässern vorkommenden Anionen stabile Komplexe, dadurch kann die Wasserlöslichkeit stark erhöht werden. mit Halogenidionen: Hg. X 3 -, Hg. X 42 - (vor allem im Meerwasser) Ungewöhnlich stabile Komplexe mit Huminstoffen („gelöste“ kolloidale Phase in Fließgewässern, Seen, Grundwasser)

Partikelgrößenverteilung von Huminstoff-Kolloiden

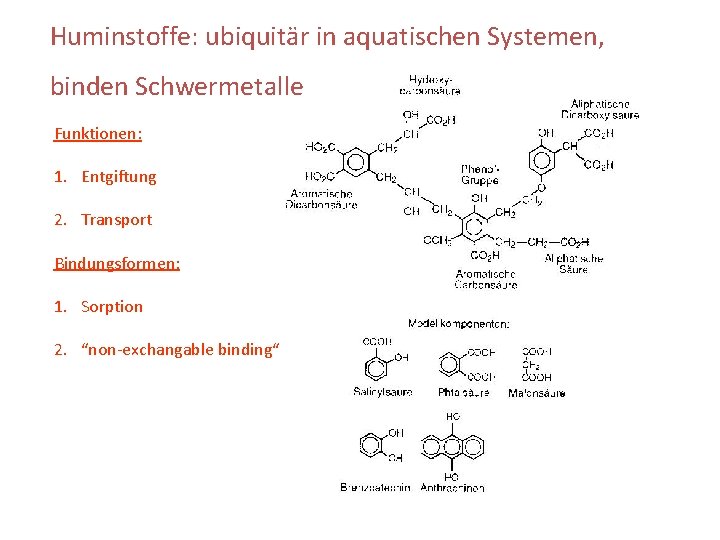
Huminstoffe: ubiquitär in aquatischen Systemen, binden Schwermetalle Funktionen: 1. Entgiftung 2. Transport Bindungsformen: 1. Sorption 2. “non-exchangable binding“

Organische Quecksilberverbindungen Wichtig ist ausschließlich die Oxidationsstufe +II Monoorganyle RHg. X, Diorganyle R 2 Hg linear gebaut Kovalente Bindung Hg-C relativ geringe Bindungsenergien 50 – 200 k. J/mol kann leicht homolytisch unter Bildung von Radikalen gespalten werden (thermische oder photolytische Zersetzung) → Lebensdauer in der Atmosphäre nur wenige Stunden

Synthesechemie: die einfach durchzuführende homolytische Spaltung der Hg-C Bindung wird für die Bildung von Radikalen ausgenutzt. In der Umwelt ist die Hg-C Bindung gegenüber Wasser und Luft weitgehend inert (aus kinetischen Gründen) Charakteristische Abbaureaktionen in der Umwelt: Acidolyse: RHg. X + HA → RH + AHg. X Reduktion: RHg. X + 2 H 2 O + 2 e- → RH + HX + 2 OH- + Hg 0 Homolyse: R 2 Hg → 2 R· + Hg 0

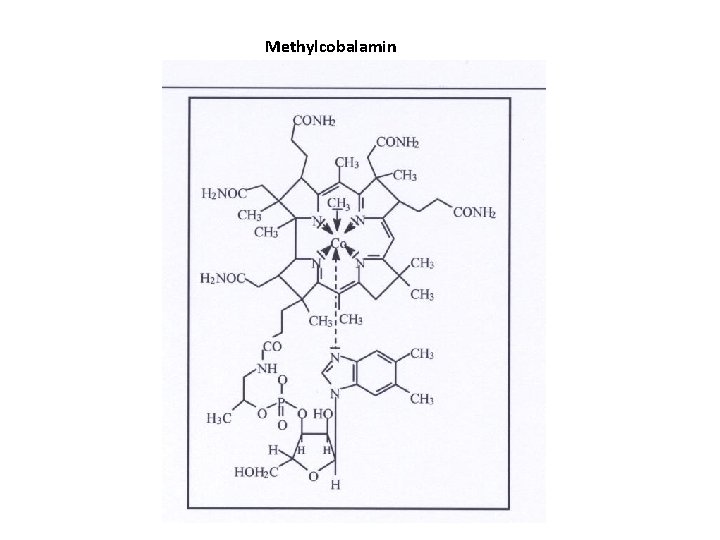
Methylcobalamin

Entstehung von Dimethylquecksilber bei der Zersetzung von Monomethylquecksilber in Anwesenheit von H 2 S (H 2 S wird durch die mikrobielle Sulfatreduktion in reduzierenden Sedimenten gebildet): 2 CH 3 Hg+ + S 2 - → CH 3 Hg-S-Hg. CH 3 → (CH 3)2 Hg + Hg. S

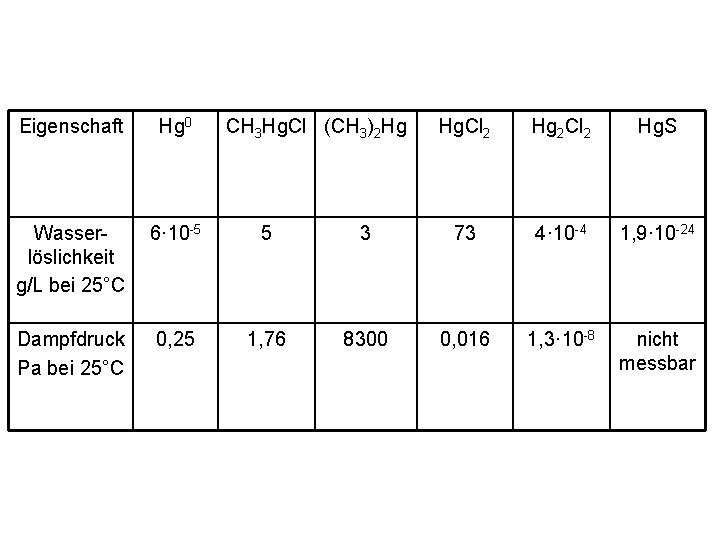
Eigenschaft Hg 0 CH 3 Hg. Cl (CH 3)2 Hg Wasserlöslichkeit g/L bei 25°C 6· 10 -5 5 Dampfdruck Pa bei 25°C 0, 25 1, 76 Hg. Cl 2 Hg 2 Cl 2 Hg. S 3 73 4· 10 -4 1, 9· 10 -24 8300 0, 016 1, 3· 10 -8 nicht messbar

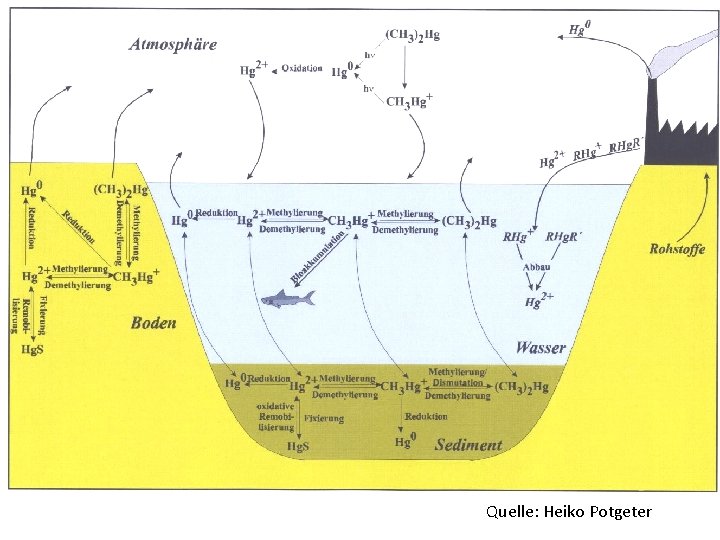
Quelle: Heiko Potgeter