Znaczenie zmian epigenetycznych w chorobach metabolicznych Marta Podolska

Znaczenie zmian epigenetycznych w chorobach metabolicznych Marta Podolska Klinika Chorób Wewnętrznych, Diabetologii i Farmakologii Klinicznej

Dutch famine hunger winter

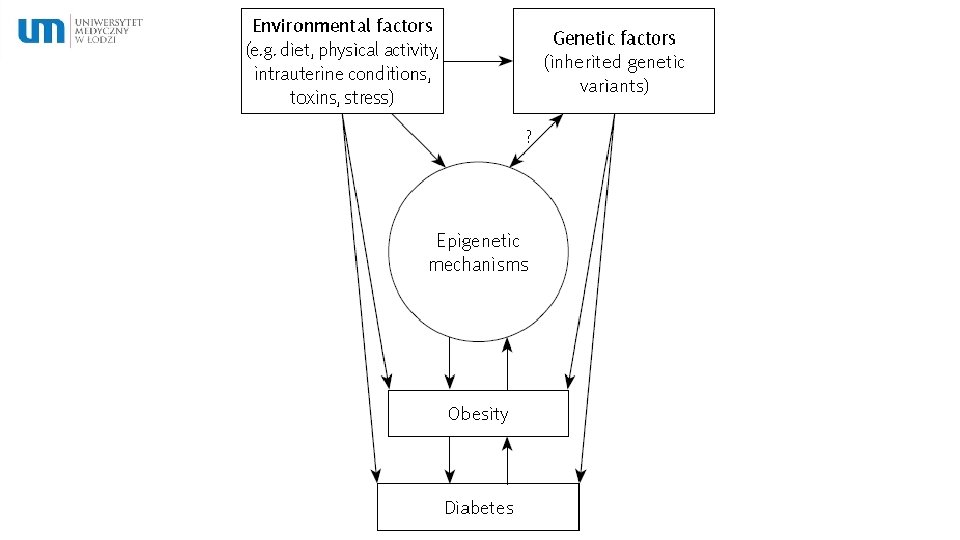
Znaczenie epigenetyki – „Dutch famine study” Dzieci kobiet, które doświadczały głodu w dwóch pierwszych trymestrach ciąży częściej rozwijały otyłość i choroby układu krążenia w dorosłym życiu niż dzieci kobiet narażonych na głód w późniejszym okresie ciąży lub kobiet nienarażonych na głód W póżniejszym okresie ciąży – większe ryzyko rozwoju insulinooporności i nadciśnienia w dorosłym życiu

Hertfordshire cohort study Mężczyźni urodzeni pomiędzy 1911 a 1930 o niskiej wadze urodzeniowej (LBW- low birth weight) częściej wykazywali upośledzoną tolerancję glukozy, nieprawidłowe ciśnienie skurczowe oraz rozwijali niedokrwienną chorobę serca LBW men 18 -krotnie częściej rozwijali zespół metaboliczny
Obszar genetyki Badanie cech komórkowych oraz fizjologicznych, które spowodowane są czynnikami zewnętrznymi/środowiskowymi zmieniającymi ekspresję genów Epigenetyka Dotyczy sposobu odczytania danego genu, a nie zmiany w jego sekwencji!

Mogą być dziedziczone Mogą również podlegać ciągłym zmianom w wyniku działania określonych czynników środowiskowych, tj. : Mechanizmy epigenetyczne Sposób odżywiania Zaburzenia równowagi hormonalnej Działanie ksenobiotyków

Metylacja DNA Główne mechanizmy epigenetyczne Metylacja, acetylacja histonów Interferencja mi. RNA

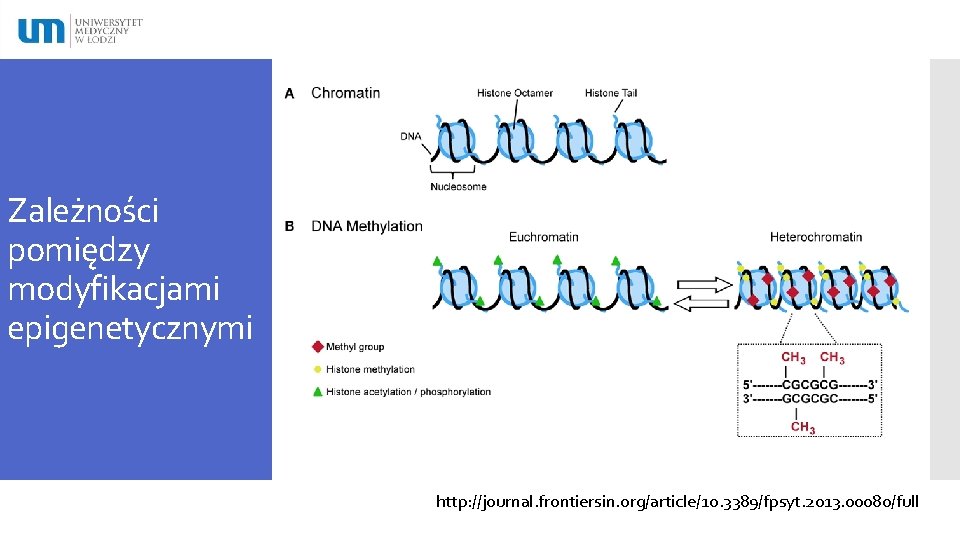
Zależności pomiędzy modyfikacjami epigenetycznymi http: //journal. frontiersin. org/article/10. 3389/fpsyt. 2013. 00080/full
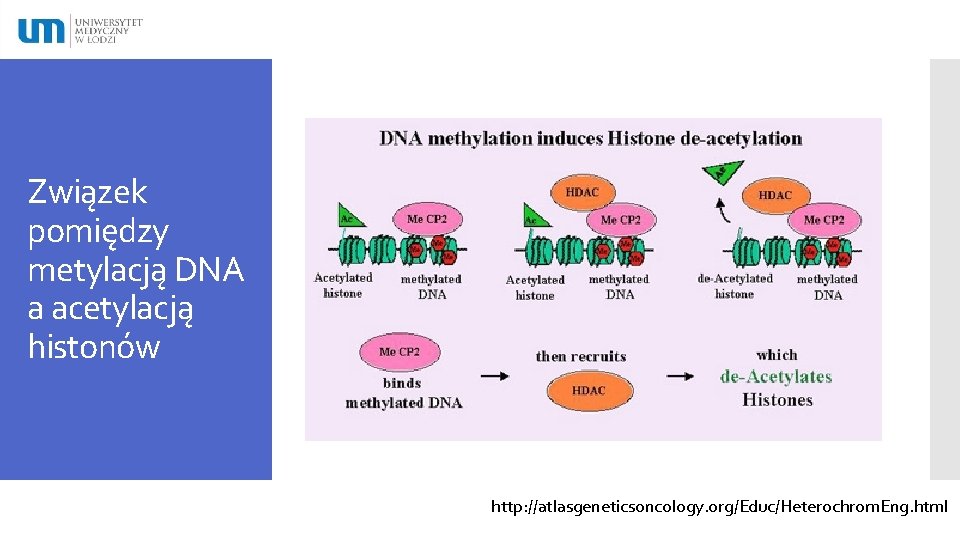
Związek pomiędzy metylacją DNA a acetylacją histonów http: //atlasgeneticsoncology. org/Educ/Heterochrom. Eng. html

Różnicowanie komórek Znaczenie epigenetyki Pośrednik między środowiskiem (bodziec) a efektem fenotypowym U roślin i mikrobów zmiany epigenetyczne pośredniczą w ewolucji
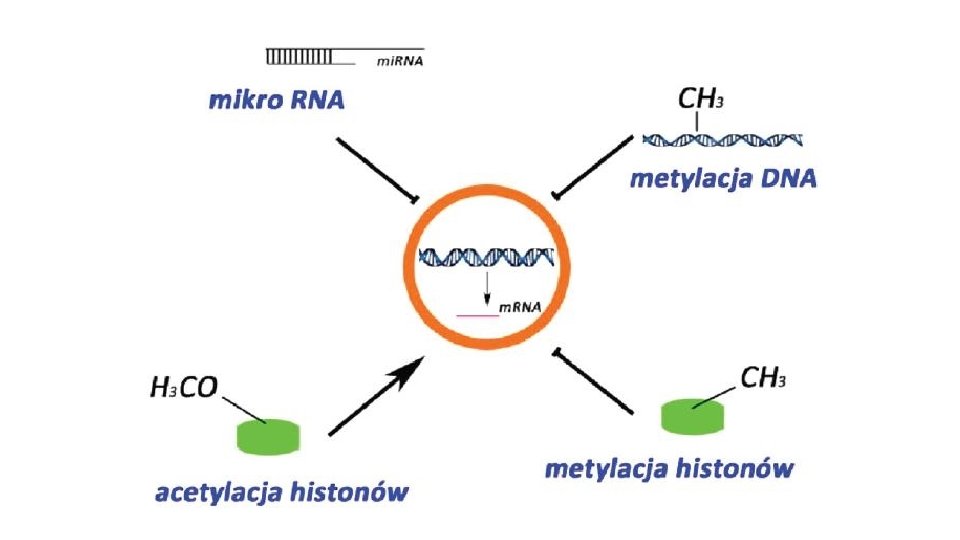

Aktywne wyciszanie tych genów i tych regionów DNA, których transkrypcja nie jest pożądana Metylacja DNA Wysoki poziom metylacji w telomerach, centromerach, nieaktywnych chromosomach X Kluczowa dla rozwoju i różnicowania -> brak DNMTs prowadzi do letalności embrionalnej Zaburzenia prowadzą do powstawania nowotworów
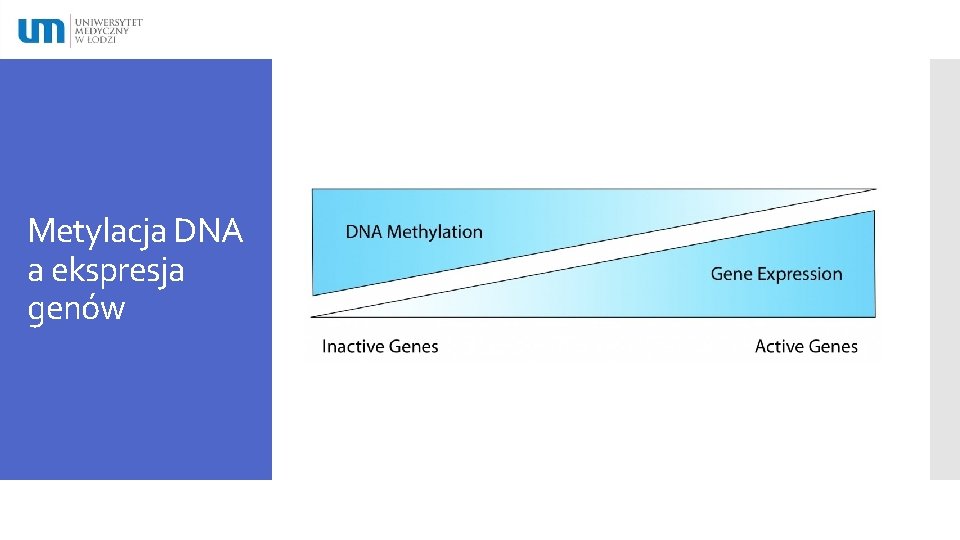
Metylacja DNA a ekspresja genów

Kształtowanie trzustki Micro. RNA Różnicowanie komórek tłuszczowych Wpływ na signaling insuliny
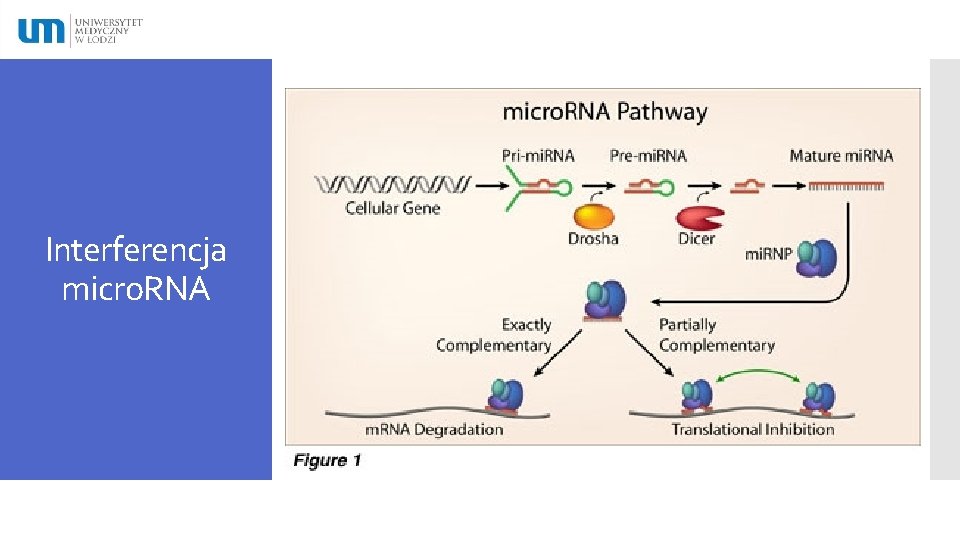
Interferencja micro. RNA
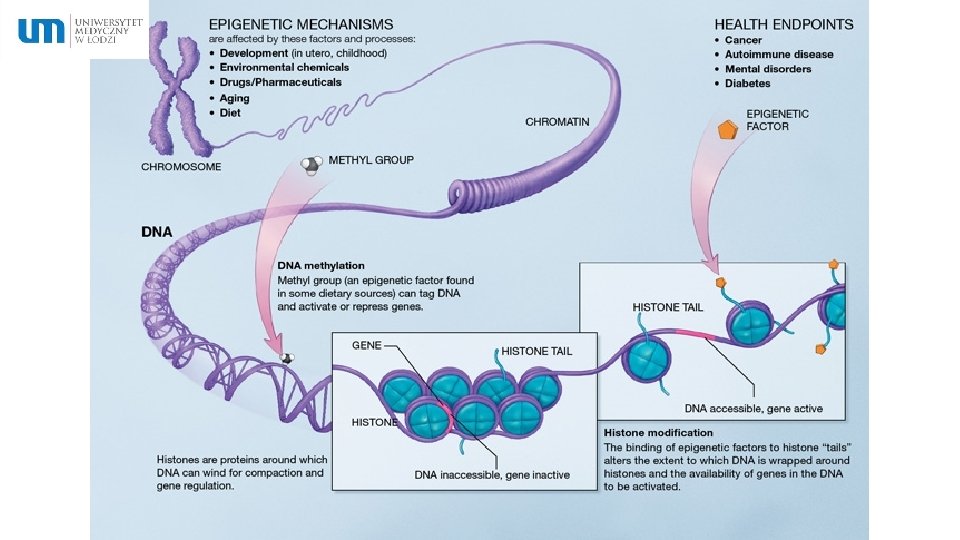
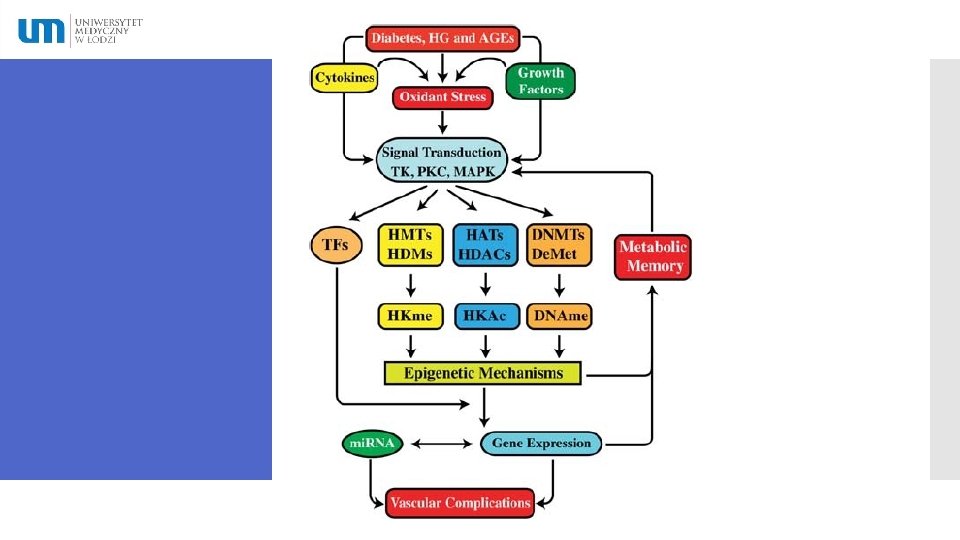

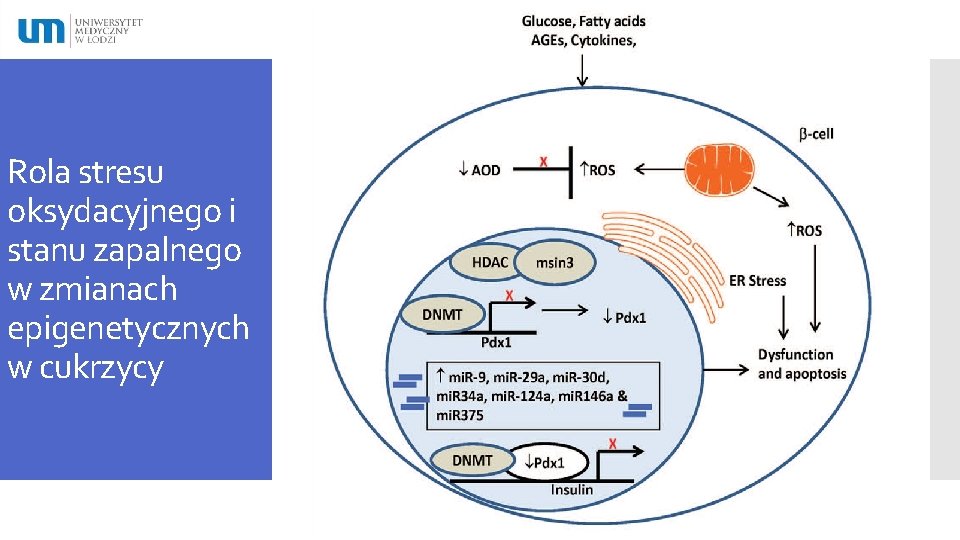
Rola stresu oksydacyjnego i stanu zapalnego w zmianach epigenetycznych w cukrzycy

Przykłady zmian epigenetycznych w chorobach metabolicznych z piśmiennictwa

Wpływ hiperglikemii na zmiany epigenetyczne Hodowla komórek monocytarnych w warunkach hiperglikemii zwiększa aktywność HATs w regionie promotorowym podjednostki p 65 Nfk. B Indukcja Set 7 (HMT) powoduje stałe zmiany ekspresji genów biorących udział w inicjowaniu procesu zapalnego w komórkach śródbłonka i monocytach Delecja tego enzymu powodowała hamowanie ekspresji Nfk. B i zależnych od niego cytokin prozapalnych (TNFa, Il 1 b)

Metylacja DNA w chorobach metabolicznych Badanie wzoru metylacji DNA u bliźniąt monozygotycznych ujawniło, że wzory te są podobne w dzieciństwie, zaś wraz z wiekiem zaczynają coraz bardziej różnić się między sobą (Kirchner) Steegers-Theunissen et al. – wyraźnie odmienny stopień metylacji u osób eksponowanych na obniżoną podaż kalorii w porównaniu z grupą przyjmującą zalecaną podaż kalorii

Metylacja DNA w chorobach metabolicznych Ling i wsp. - zaobserwowali, że stopień ekspresji PGC-1 -alpha (kluczowa rola w regulacji biogenezy i zużycia energii w tkankach aktywnych metabolicznie) jest obniżony u pacjentów z T 2 DM Poziom ekspresji korelował z 2 -krotnym zwiększeniem stopnia metylacji w promotorze PGC-1 -alpha Dodatkowo upośledzenie funkcji wydzielania insuliny przez komórki beta trzustki

Kutoda et al. , - ekspresja insuliny jest zależna od modyfikacji epigenetycznych Metylacja DNA w chorobach metabolicznych Osoby z T 2 D wykazują zwiększoną metylację w czterech Cp. G w promotorze dla insuliny w wyspach trzustkowych, co odwrotnie koreluje z poziomem m. RNA insuliny Komórki beta eksponowane na wysokie stężenia glukozy wykazują zwiększoną metylację w promotorze insuliny Brak związku pomiędzy wiekiem i stopniem metylacji DNA; korelacja pomiędzy otyłością a metylacją DNA

Metylacja DNA w chorobach metabolicznych Ronn et al. – wpływ 6 -miesięcznych ćwiczeń fizycznych na wzór metylacji DNA w tkance tłuszczowej zdrowych mężczyzn wcześniej prezentujących niski stopień aktywności fizycznej Interwencja znacznie zmieniła wzór metylacji, wpłynęła na ekspresję genów związanych z otyłością i T 2 DM – głównie tych odpowiedzialnych za metabolizm glukozy, metabolizm tłuszczów i adipogenezę

Posttranslacyjne modyfikacje histonów w chorobach metabolicznych Abu-Farha i wsp. przeprowadzili analizę proteomu w PBMCs i podskórnej tkance tłuszczowej pobranych od osób szczupłych i otyłych przed i po 3 -miesięcznych ćwiczeniach fizycznych Znaczące różnice w poziomie 47 białek w PBMCs otyłych w porównaniu do szczupłych (↓HDAC 4 u otyłych) Po ćwiczeniach zmiana w poziomie 38 białek u otyłych Zmiana poziomu HDAC 4 do poziomu obserwowanego u szczupłych Poziom ekspresji HDAC 4 korelował z parametrami fizycznymi, klinicznymi i metabolicznymi – potencjalne właściwości protekcyjne przeciw otyłości

Ferland-Mc-Collough i wsp. zidentyfikowali rolę mi. R 483 -3 p w związku pomiędzy żywieniem we wczesnych latach życia a rozwojem zaburzeń metabolicznych w późniejszych latach mi. RNA w chorobach metabolicznych ↑mi. R-483 -3 p u młodych mężczyzn o niskiej wadze urodzeniowej GDF 3 - zaangażowany w regulację wzrostu adipocytów, rozwój otyłości i przemiany energetyczne ↑mi. R-483 -3 p - ↓GDF 3, PPAR-gamma „increased mi. R-483 -3 p expression in vivo, programmed by early-life nutrition, limits storage of lipids in adipose tissue, causing lipotoxicity and insulin resistance and thus increasing susceptibility to metabolic disease”

Powikłania cukrzycy – zagadnienie pamięci metabolicznej Wiele ważnych biochemicznych mechanizmów zostaje aktywowanych w obecności występującego w cukrzycy wysokiego stężenia glukozy. W wielu randomizowanych badaniach wykazano, że wczesna intensywna kontrola glikemii redukuje ryzyko powikłań cukrzycy. To zjawisko określa się jako „pamięć metaboliczna”. Sugeruje się, że wczesna normalizacja glikemii może zatrzymać powodowane hiperglikemią patologiczne procesy potęgujące stres oksydacyjny i glikację białek komórkowych i lipidów. Zjawisko „pamięci metabolicznej” sugeruje, że wczesne agresywne leczenie i dokładna kontrola glikemii mogą być wykorzystane w prewencji przewlekłych powikłań cukrzycy. Pamięć metaboliczna” — znaczenie w cukrzycy Ewa Otto-Buczkowska Forum Medycyny Rodzinnej 2014; 8(2): 51 -55.
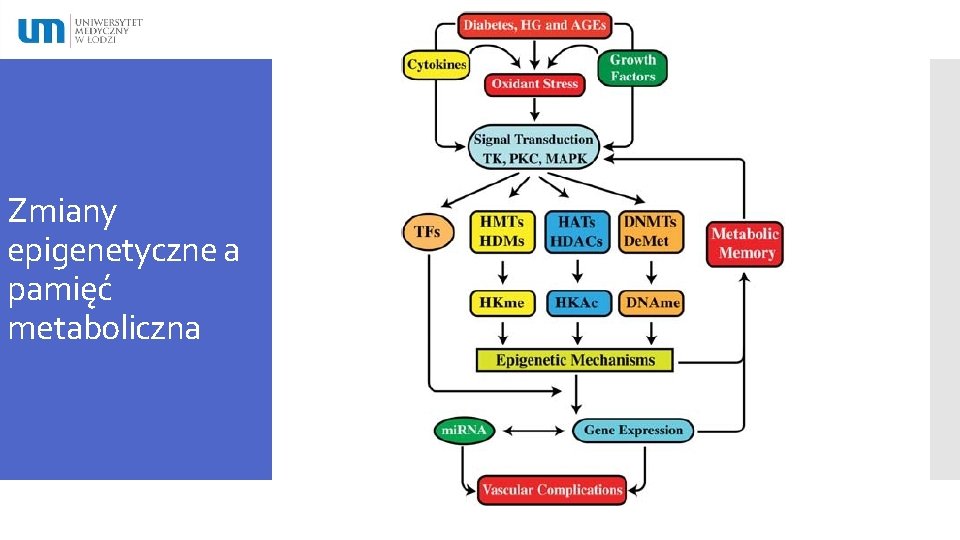
Zmiany epigenetyczne a pamięć metaboliczna

Zmiany epigenetyczne a pamięć metaboliczna DCCT (1993) – intensywna kontrola glikemii zmniejsza ryzyko wystąpienia i rozwoju powikłań naczyniowych w T 1 D UKPDS (1977 -1997) – kontrola glikemii i poprawa ciśnienia tętniczego zmniejsza ryzyko rozwoju powikłań naczyniowych w T 2 D

Zmiany epigenetyczne a powikłania cukrzycowe Zmiana ekspresji szeregu genów zaangażowanych w powstawanie i utrzymywanie się przewlekłego procesu zapalnego Nfk. B TNFa IL 6 MCP 1 prowadzi do uszkodzenia komórek śródbłonka

Rola epigenetyki w retinopatii cukrzycowej Metylacja genów Sod 2 i MMP-9, zwiększenie transkrypcji LSD 1 (demetylaza H 3 K 4 i H 3 K 9) oraz innych DNMTs, zwiększenie poziomu mi. RNAs dla czynników transkrypcyjnych i VEGF Potencjalne targety dla farmakoterapii inhibicja metylacji Sod 2 i MMP-9 - 5 -azacytydyna, 5 aza-20 -deoxycytydyna zmniejszenie poziomu mi. RNA inhibitory acetylotransferaz histonów – galusan epigallokatechiny, kwas suberanilohydroksamowy, Romidepsin

Rola epigenetyki w nefropatii cukrzycowej Istotne różnice w metylacji promotorów 19 genów u pacjentów z T 1 D i DN w porównaniu z pacjentami z T 1 D, ale bez DN Hipermetylacja genu UNC 13 B u pacjentów z DN

Rola epigenetyki w neuropatii cukrzycowej Hipermetylacja Pdx 1 prowadzi do zaburzenia funkcji wysp trzustkowych i rozwoju cukrzycy u szczurów Wyciszenie poprzez metylację DNA prowadzi do zmniejszenia liczby komórek beta, co powoduje rozwój insulinooporności, a także niezdolność komórek wydzielania peptydów zaangażowanych w zapobieganiu niszczenia naczyń i neuropatii spowodowanych stanem zapalnym

Rola epigenetyki w kardiomiopatii cukrzycowej Przerost i apoptoza kardiomiocytów, zwłóknienie mięśnia sercowego mi. R-133 – dwoista rola ↑ - zaburzenia przewodnictwa mięśnia sercowego ↓ - przerost mięśnia sercowego

Patogeneza Co dalej? Diagnostyka Terapia

Leczenie z wykorzystaniem wiedzy z badań nad epigenetyką micro. RNA antagoniści (inhibitory) lub oligonukleotydy naśladujące micro. RNA - choroby serca - nowotwory - zapalenie wątroby C ( II faza badań klinicznych) - choroby metaboliczne: mi. R-33 – poprawa metabolizmu tłuszczów, zmniejszenie ryzyka rozwoju miażdzycy mi. R-103/107 – poprawa metabolizmu glukozy i zwiększenie insulinowrażliwości

Zmiany epigenetyczne mogą być zaangażowane w patogenezę wielu chorób metabolicznych oraz w rozwój ich powikłań Podsumowanie Zmiany epigenetyczne wpływają na ekspresję genów zaangażowanych w metabolizm, magazynowanie tłuszczu, remodeling komórkowy, odpowiedź immunologiczną oraz adipogenezę W przyszłości możliwe zidentyfikowanie epigenetycznych targetów dla prewencji i leczenia chorób metabolicznych
- Slides: 41
































































