SEMANA 4 REACCIN Y ECUACIN QUMICA 2021 1



















- Slides: 28

SEMANA 4 REACCIÓN Y ECUACIÓN QUÍMICA 2021 1

SEMANA 04 REACCIÓN Y ECUACIÓN QUÍMICA • Partes e interpretación de símbolos. • Manifestaciones de las reacciones. • Tipos de reacciones: - Combinación o Síntesis, Análisis o descomposición, Sustitución simple, Doble sustitución, Neutralización y Combustión - Exotérmicas y endotérmicas - Reversibles e irreversibles • Balanceo de ecuaciones por el método de tanteo. • Número de oxidación, reglas de asignación. Aplicación de los conceptos en la salud y el ambiente. Lecturas en libro de texto. La Química en la Salud: “Compresas frías y compresas calientes” LABORATORIO: REACCIONES QUÍMICAS 2

Reacción Química • Es un cambio ó fenómeno químico en donde los átomos de una sustancia se han transformado en una o más sustancias nuevas y con propiedades diferentes. • Generalmente se presentan manifestaciones. • Ejemplo: El hierro en contacto con el oxígeno del aire se oxida y produce como manifestación un óxido de color rojo café. • Esta reacción la podemos escribir utilizando las fórmulas químicas de los compuestos que reaccionan y de los que se producen. (El hierro puede formar dos tipos de óxidos) Fe + O 2 → Fe 2 O 3 y también Fe + O 2 → Fe. O 3

Ecuación Química • Es la reacción química que se encuentra Balanceada para que cumpla la Ley de la Conservación de la Materia. • Se balancea utilizando coeficientes que igualan la cantidad de átomos de los Reactivos con la cantidad de átomos de los Productos. Fe + O 2 Fe 2 O 3 (balanceada: 4 Fe + 3 O 2 2 Fe 2 O 3) Fe + O 2 → Fe. O (balanceada: 2 Fe + O 2 2 Fe. O) 4

Partes y símbolos de un Ecuación Química • Reactivos: átomos ó compuestos que reaccionan. • Productos: átomos ó compuestos que se forman. • Catalizador (sustancia que altera la velocidad de reacción pero no reacciona. Se coloca encima de la flecha. • Se utilizan →, ↔, +, # o coeficientes antes de la fórmula, subíndices después del símbolo, estado físico entre paréntesis (s), (l), (g) ó ↑, (ac), precipitado , calor ∆, catalizador. 5

Manifestaciones de las reacciones (es lo que se percibe por los sentidos) • Cambio de color • Cambio de temperatura • Formación o desprendimiento de gas ó burbujas • Formación de un sólido ó precipitado • Cambio de p. H • Liberación de olor • Producción de energía lumínica 6

Tipos de Reacciones Reacción de Síntesis ó Combinación A + B → AB 2 Mg(s) + O 2(g) → 2 Mg. O(s) H 2(g)+ Br 2(g) → 2 HBr(g) Ca. O(s) + CO 2 (g) → Ca. CO 3 (s) 7

Reacción de Análisis ó Descomposición AB → A + B Ca. CO 3 (s) → Ca. O (s) + CO 2 (g) 2 Hg. O(s) → 2 Hg (l) + O 2 (g) 2 Al 2 O 3(s) → 4 Al(s) + 3 O 2(g) 2 Cu(NO 3)2 (s) → 2 Cu. O(s) + 4 NO 2(g)+ O 2(g) 8

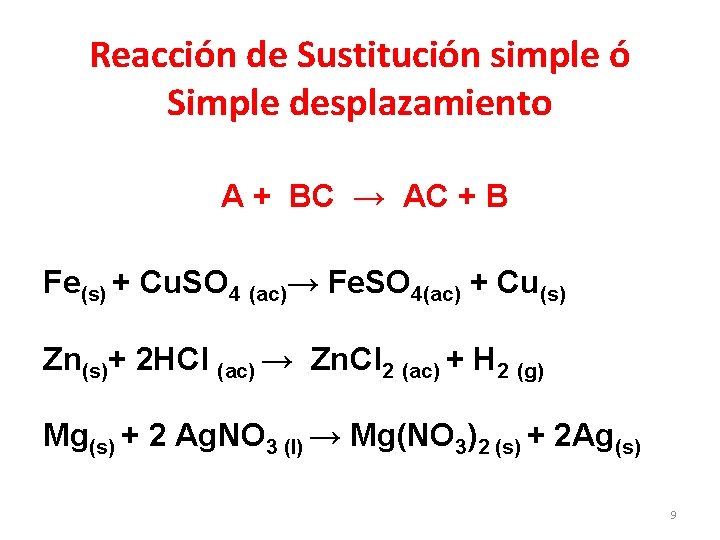
Reacción de Sustitución simple ó Simple desplazamiento A + BC → AC + B Fe(s) + Cu. SO 4 (ac)→ Fe. SO 4(ac) + Cu(s) Zn(s)+ 2 HCl (ac) → Zn. Cl 2 (ac) + H 2 (g) Mg(s) + 2 Ag. NO 3 (l) → Mg(NO 3)2 (s) + 2 Ag(s) 9

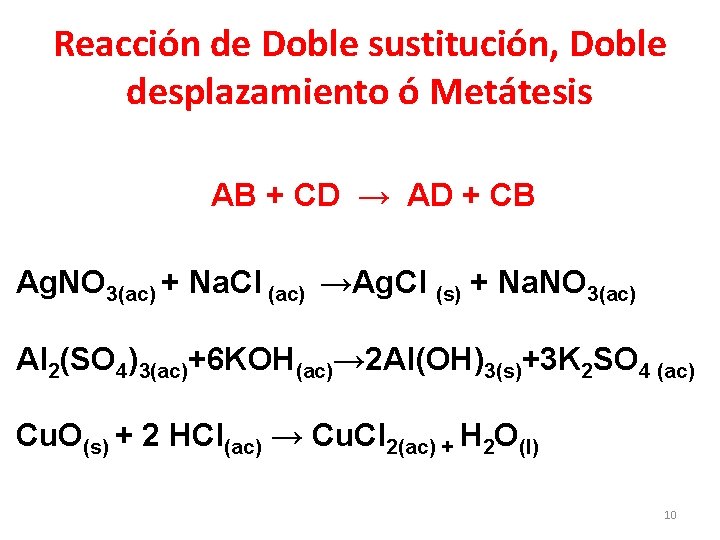
Reacción de Doble sustitución, Doble desplazamiento ó Metátesis AB + CD → AD + CB Ag. NO 3(ac) + Na. Cl (ac) →Ag. Cl (s) + Na. NO 3(ac) Al 2(SO 4)3(ac)+6 KOH(ac)→ 2 Al(OH)3(s)+3 K 2 SO 4 (ac) Cu. O(s) + 2 HCl(ac) → Cu. Cl 2(ac) + H 2 O(l) 10

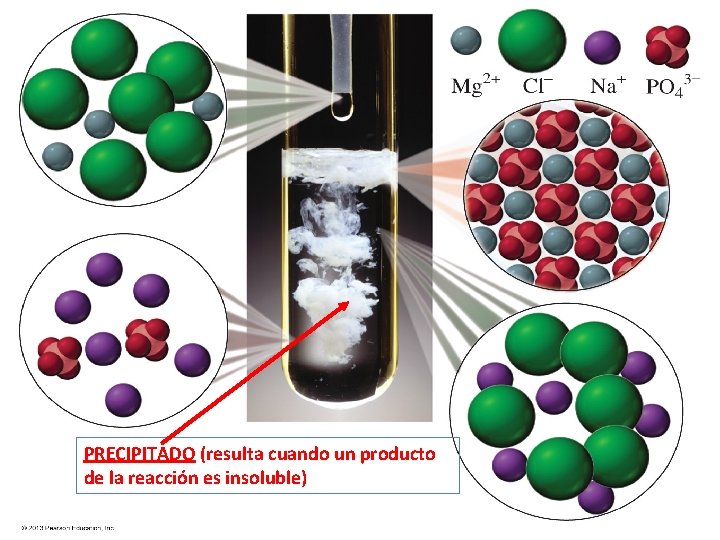
PRECIPITADO (resulta cuando un producto de la reacción es insoluble) 11

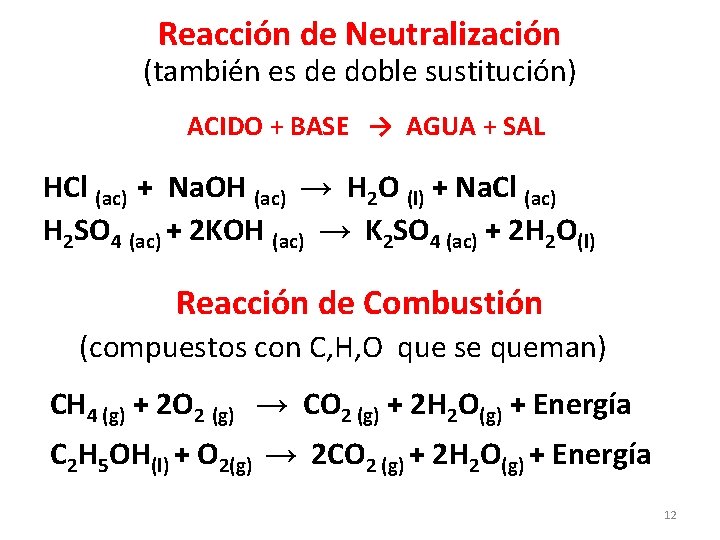
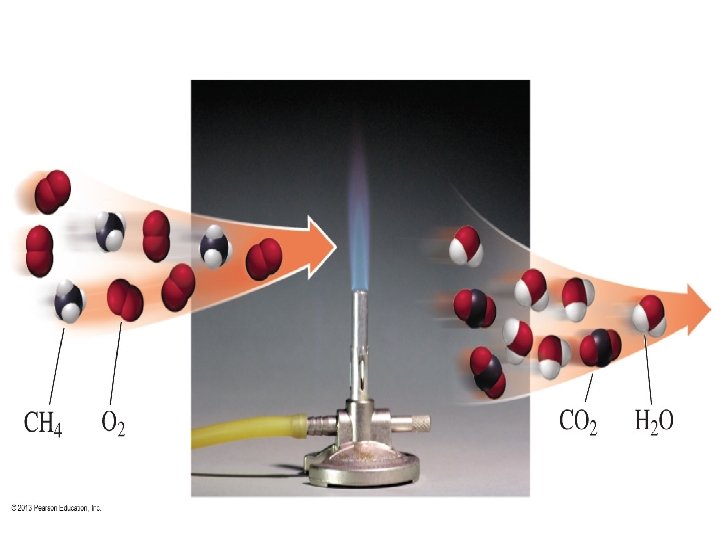
Reacción de Neutralización (también es de doble sustitución) ACIDO + BASE → AGUA + SAL HCl (ac) + Na. OH (ac) → H 2 O (l) + Na. Cl (ac) H 2 SO 4 (ac) + 2 KOH (ac) → K 2 SO 4 (ac) + 2 H 2 O(l) Reacción de Combustión (compuestos con C, H, O que se queman) CH 4 (g) + 2 O 2 (g) → CO 2 (g) + 2 H 2 O(g) + Energía C 2 H 5 OH(l) + O 2(g) → 2 CO 2 (g) + 2 H 2 O(g) + Energía 12


Reacción Endotérmica • Necesita energía y se representa en los reactivos con ∆, Kcal o Energía o con △H+ H 2(g) + ½ O 2(g) + ∆ → H 2 O H 2(g) + ½ O 2(g) + 283 Kcal → H 2 O (l) H 2(g) + ½ O 2(g) → H 2 O(l) △H =+283 Kcal 14

Reacción Exotérmica • Libera energía y se representa en los productos con ∆, Kcal o Energía o con △HCH 4(g) + 2 O 2(g) → CO 2(g)+ 2 H 2 O(g) + ∆ CH 4(g) + 2 O 2(g) → CO 2(g)+ 2 H 2 O(g) + 192 Kcal CH 4(g) + 2 O 2(g) → CO 2(g)+2 H 2 O(g) △H=192 Kcal 15

Reacción Irreversible Se realiza solo en una dirección. Directa A → B 2 Al 2 O 3(s) → 4 Al(s) + 3 O 2(g) Reacción Reversible Se realiza en dos direcciones. Directa A → B A⇄B Inversa A ← B CS 2 (g) + 4 H 2 (g) ⇄ CH 4 (g) + 2 H 2 S (g) 16

Balanceo de Ecuaciones • Procedimiento utilizado para igualar el # total de átomos ó moléculas presentes en los Reactivos y los Productos, para que se cumpla la Ley de la Conservación de la Materia. • Se balancea utilizando coeficientes que son # enteros que se escriben adelante de las fórmulas de los compuestos) NO SE DEBEN DE CAMBIAR LOS SUBÍNDICES DE LAS FÓRMULAS PARA BALANCEAR. • Utilizaremos los métodos de TANTEO y REDOX 17

Balanceo por Tanteo No balanceada Fe + O 2 Fe 2 O 3 • Se colocan coeficientes que igualen el # de átomos entre los Reactivos y los Productos. Se recomienda balancear siguiendo en este orden: 1º Metales 2º No metales 3º Hidrógenos 4º Oxígenos Balanceada 4 Fe + 3 O 2 2 Fe 2 O 3 • coeficientes de los reactivos 4 y 3 y del producto 2. (Si el coeficiente es 1, no se debe escribir). 18

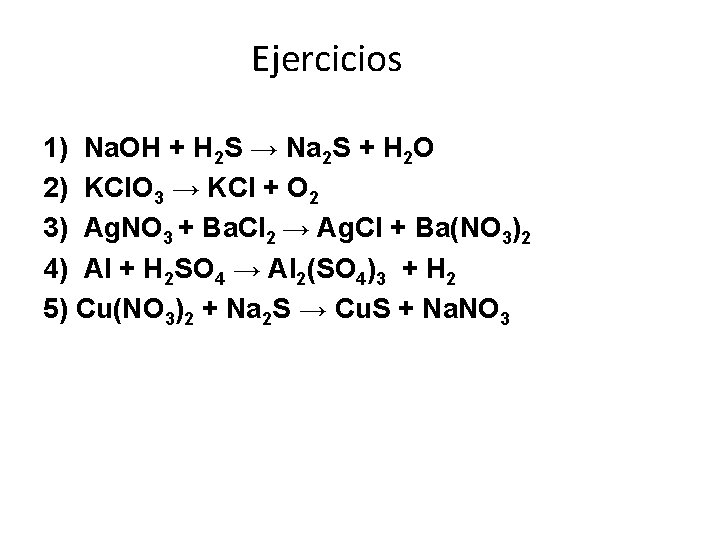
Ejercicios 1) Na. OH + H 2 S → Na 2 S + H 2 O 2) KCl. O 3 → KCl + O 2 3) Ag. NO 3 + Ba. Cl 2 → Ag. Cl + Ba(NO 3)2 4) Al + H 2 SO 4 → Al 2(SO 4)3 + H 2 5) Cu(NO 3)2 + Na 2 S → Cu. S + Na. NO 3 19

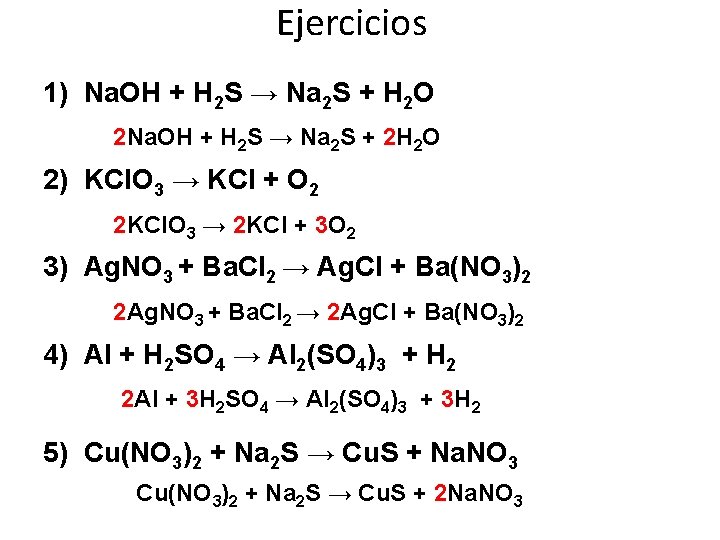
Ejercicios 1) Na. OH + H 2 S → Na 2 S + H 2 O 2 Na. OH + H 2 S → Na 2 S + 2 H 2 O 2) KCl. O 3 → KCl + O 2 2 KCl. O 3 → 2 KCl + 3 O 2 3) Ag. NO 3 + Ba. Cl 2 → Ag. Cl + Ba(NO 3)2 2 Ag. NO 3 + Ba. Cl 2 → 2 Ag. Cl + Ba(NO 3)2 4) Al + H 2 SO 4 → Al 2(SO 4)3 + H 2 2 Al + 3 H 2 SO 4 → Al 2(SO 4)3 + 3 H 2 5) Cu(NO 3)2 + Na 2 S → Cu. S + Na. NO 3 Cu(NO 3)2 + Na 2 S → Cu. S + 2 Na. NO 3 20

Número ó Estado de Oxidación • Es un número entero positivo ó negativo que se le asigna a cada átomo de un compuesto, ión ó elemento. • Este número indicará cuantos electrones ha ganado, perdido ó compartido ese átomo al formar parte de ese compuesto. • Para asignar los números de oxidación se siguen algunas reglas: 21

Reglas para asignar los números de oxidación de los átomos 1. Los elementos libres (que no forman compuestos) y los diatómicos, tienen # de oxidación = 0 Ej: H 2 (H= 0) Cl 2 (Cl= 0) Zn (Zn= 0) Ag (Ag= 0) 2. El Hidrogeno en compuestos, # de oxid. = +1 (excepto en (HM) hidruros = -1) Ej: H 2 S (H 2+1 S-2) NH 3 (N-3 H 3+1) 3. El Oxigeno en compuestos, # de oxid. =-2 (excepto en (H 2 O 2) peróxidos = -1) Ej: CO 2 (C+4 O-22) SO 3 (S+6 O-23) 22

4. Elementos con # de oxidación únicos. Los de columna IA # oxid= +1; IIA # oxid= +2; IIIA # oxid= +3 5. La suma de todos los números de oxidación de todos los átomos de un compuesto debe=0 Ej: H 3 BO 3 (H=+1 x 3=+3) (B=+3 x 1=+3) (O=-2 x 3=-6) (+3+3 -6= 0) 6. Para un ión monoatómico su # oxid=su carga Ej: Na+(Na=+1) Ca+2(Ca=+2) S-2(S=-2) Cl-(Cl=-1) 23

7. En un ión poliatómico, la suma de los # de oxidación de todos sus átomos debe ser igual a la carga del ión. Ej: (PO 4)-3 (P=+5) (O=-2 x 4=-8); (+5 -8=-3) 8. Para compuestos binarios Xx. Yy, el subíndice x es la carga de Y. El subíndice y es la carga de X Ej: Fe 2 S 3 (Fe=+3 ; S=-2) PCl 5 (P=+5 ; Cl=-1) Fe(NO 3)3 (Fe=+3) (O=-2 x 9=-18); (N=+5 x 3=+15) 24

9. Si un no-metal es de columna par, puede trabajar principalmente con # de oxidación pares, que no sean mayores a su número de columna. Si es de columna impar trabaja con # de oxidación impares que no sean mayores a su # de la columna. 25

Ejemplos de asignación de # de oxidación: H 2 SO 4 H=+1 O=-2 S= +6 H 2 SO 3 H=+1 O=-2 S= +4 HCl. O 4 H=+1 O=-2 Cl=+7 Ni 2(CO 3)3 Ni=+3 y todo el (CO 3)= -2 Entonces C=+4 O=-2 22226299229

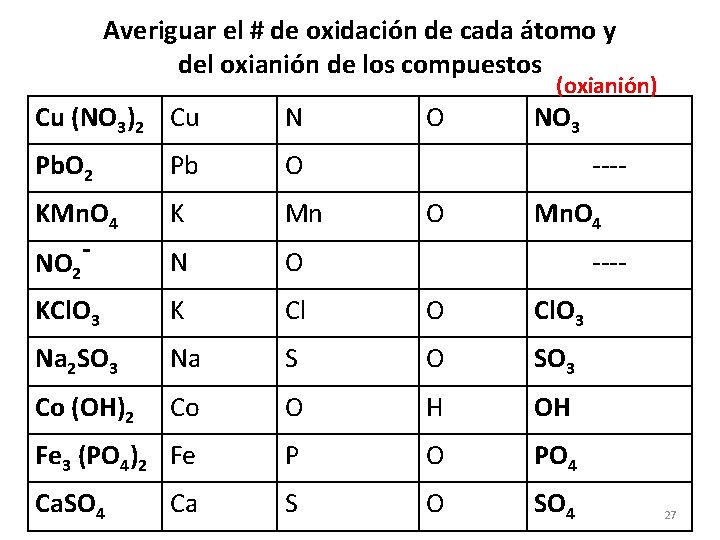
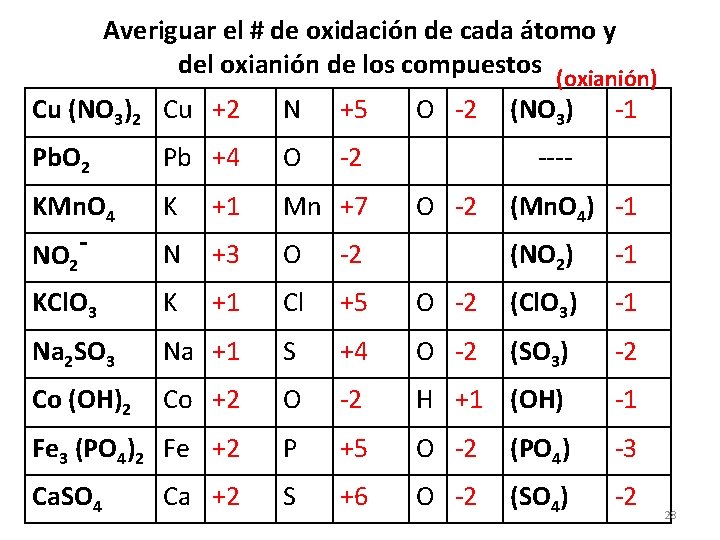
Averiguar el # de oxidación de cada átomo y del oxianión de los compuestos Cu (NO 3)2 Cu N Pb. O 2 Pb O KMn. O 4 NO - K Mn N O KCl. O 3 K Cl O Cl. O 3 Na 2 SO 3 Na S O SO 3 Co (OH)2 Co O H OH Fe 3 (PO 4)2 Fe P O PO 4 Ca. SO 4 S O SO 4 2 Ca O (oxianión) NO 3 ---O Mn. O 4 ---- 27

Averiguar el # de oxidación de cada átomo y del oxianión de los compuestos (oxianión) Cu (NO 3)2 Cu +2 N +5 Pb. O 2 Pb +4 O -2 KMn. O 4 NO K +1 Mn +7 N +3 O -2 KCl. O 3 K +1 Cl +5 Na 2 SO 3 Na +1 S Co (OH)2 Co +2 O -2 (NO 3) -1 ---O -2 (Mn. O 4) -1 (NO 2) -1 O -2 (Cl. O 3) -1 +4 O -2 (SO 3) -2 O -2 H +1 (OH) -1 Fe 3 (PO 4)2 Fe +2 P +5 O -2 (PO 4) -3 Ca. SO 4 S +6 O -2 (SO 4) -2 2 Ca +2 28