Reaccin y Ecuacin Qumica Semana 4 2019 Isabel

Reacción y Ecuación Química Semana 4 – 2019 Isabel Fratti de del Cid Diseño de diapositivas, imágenes e ilustraciones cortesía de Licda : Lilian Guzmán. 1

Reacción Química • Una reacción constituye una transformación de la materia, que genera sustancias con características diferentes de las sustancias de donde se originaron. A esto se le conoce como cambio ó fenómeno Quimico lo que constituye una reacción quimica. Si la materia no genera sustancias diferentes, sino que mantiene su composición y estructura, se dice que experimento un cambio o fenómeno físico. 2

Reacción Química Es un proceso en el cuál, uno o mas elementos o compuestos reaccionan entre si para formar uno o mas elementos o compuestos con características y propiedades diferentes a las sustancias originales. Es decir ocurre un cambio químico. Ejemplo: Oxidación del Hierro 4 Fe (s) + 3 O 2 (g) 2 Fe 2 O 3 (s) (sólido gris) ( gas incoloro) (Sólido café-anaranjado) Note: los átomos mantienen su identidad y número en ambos lados de la ecuación pero formando compuestos diferentes. 3

Manifestaciones de una reacción química Entre los cambios detectables se pueden dar: § Liberación de gas * § Cambio de color * § Formación de precipitado* § Cambio de temperatura * § Cambio de p. H § Liberación de olor * * Estas pueden percibirse a través de nuestros sentidos(tacto, olfato, vista) 4

Una reacción química corresponde a un cambio Quimico o Fenómeno Quimico, ya que las sustancias formadas poseen propiedades físicas y químicas diferentes. En una reacción química ordinaria, la identidad de los átomos no cambia. ( Es decir el número de protones en el núcleo no CAMBIA). Los electrones si pueden afectarse ya que pueden compartirse o transferirse de un átomo a otro, afectándose la carga de la partícula y su número de oxidación. Los 5

Ecuación Química Es la representación de una reacción química, usando símbolos y formulas de los reactivos usados y los productos formados. En ésta podemos indicar al pie de los símbolos y fórmulas el estado físico en el que se encuentran al momento de reaccionar y formarse. Como una ecuación es una identidad: debe balancearse de modo que la cantidad de átomos participantes sea igual del lado de los reactivos y productos. 6

Partes de una Ecuación A+B → C+D REACTIVOS PRODUCTOS REACTIVOS Elementos ó compuestos que van a participar en la reacción ( se colocan del lado izquierdo) PRODUCTOS Son las sustancias que se forman durante la reacción. ( se colocan del lado derecho) 7

Catalíticos o catalizadores • En algunos casos las reacciones requieren de un catalítico o catalizador para que la reacción ocurra más rápido. CATALIZADOR Es una sustancia que altera la velocidad de la reacción sin ser consumido en la reacción. La mayoría de las reacciones NO requiere catalíticos. Si una reacción requiere agente catalítico, esta sustancia ( su símbolo ó fórmula) se coloca generalmente sobre la flecha de la reacción. • • Ejemplo Pt • C 2 H 4 (g) + H 2 (g) C 2 H 6 (g) • El Pt actúa como catalizador 8

Símbolos usados en las ecuaciones y sus significados Una flecha sencilla entre reactivos y productos (→) indica que la reacción es irreversible. Cu. O (s) + 2 HCl (ac) Cu. Cl 2 (ac) + H 2 O (l) Una doble flecha (⇄), indica que la reacción es reversible. 2 NH 3 + ⇄ N 2 (g) 3 H 2 (g) Nota : al pie de las fórmulas o símbolos de las sustancias participantes, puede indicarse el estado físico en el que se hallan o se producen las sustancias participantes. En la próxima diapositiva se indica la simbología más usada. 9

(g) Gas o estado gaseoso ( del lado de los productos indica liberación de gas) (l) Líquido (s) Sólido ( del lado de los productos, indica formación de precipitado, es decir el producto formado es poco soluble en agua) (ac) Solución Acuosa del lado de los productos o (aq) reactivos nos indica que se hallan en solución acuosa. ( ) Si el producto es un gas ( simbología poco usada) ( ) Si el producto es un precipitado ( simbología poco usada) (∆) Calor: a) Si se escribe sobre las flechas o al lado izquierdo, indica que la reacción es endotérmica. b) Escrito a la izquierda indica que la reacción es 10 exotérmica)

Tipos de Reacciones de Síntesis o Combinación Reaccionan dos o más sustancias y se obtiene un solo producto. La forma general de éstas reacciones es : A + B → AB Ejemplos : 2 Mg(s) + O 2(g) → 2 Mg. O(s) H 2(g)+ Br 2(g) → 2 HBr(g) Ca. O (s) + CO 2 (g) Ca. CO 3 (s) * *Proceso natural de la formación de la piedra caliza. 11

Síntesis y combinación Moléculas de O 2 12

Reacción de Análisis o Descomposición Reacción en la que un solo compuesto genera 2 o más sustancias simples o compuestas. Este tipo de reacción se representa : AB→A+B Ejemplo : Ca. CO 3 (s) → Ca. O(s) + CO 2(g) 2 Hg. O (s) → 2 Hg (S) + O 2 2 Al 2 O 3(s) → 4 Al(s) + 3 O 2(g) 2 Cu (NO 3)2 (s) 2 Cu. O(s) + 4 NO 2(g)+ O 2(g) 13
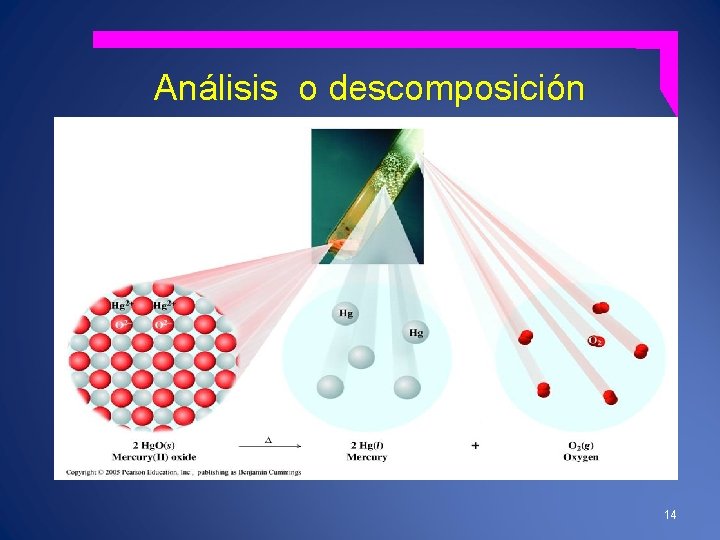
Análisis o descomposición 14

Reacción de Sustitución simple o Simple Desplazamiento Reacción en la cual un elemento desplaza a otro elemento en un compuesto. Representación A+ BC → AC +B Ejemplos : Fe(s) + Cu. SO 4 (ac)→ Fe. SO 4(ac) + Cu (s) Zn (s)+ 2 HCl(ac) → Zn. Cl 2 (ac) + H 2 (g) Mg + 2 Ag. NO 3 → Mg(NO 3)2 + 2 Ag 15

Simple desplazamiento Aquí se observa al zinc, desplazando al Hidrogeno y combinándose con el cloro. . 16

Reacciones de Doble sustitución, doble desplazamiento o Metátesis Reacción donde un elemento de un compuesto, sustituye a otro elemento de otro compuesto, Por lo tanto los reactivos y los productos siempre son sustancias compuestas. Representación AB+ CD → AD + CB Ejemplos: Ag. NO 3(ac) + Na. Cl (ac) →Ag. Cl (s) + Na. NO 3(ac) Al 2(SO 4)3 (ac) + 6 KOH (ac) → 2 Al(OH)3(s) + 3 K 2 SO 4 (ac) Cu. O(s) + 2 HCl(ac) → Cu. Cl 2(ac) + H 2 O e

Reacciones de Doble sustitución o Metátesis El Na+, desplaza al Ba+2 y se combina con el Cl -, y el Ba+2, se combina con el SO 4 -2. Note como el SO 4 -2, posee 2 cargas negativas, necesita 2 iones sodio Na+, para formar Na 2 SO 4 18

Reacciones de Neutralización En esta reacción uno de los reactivos es un ácido y el otro es una base, los productos generalmente son una sal y agua. Pertenecen a las reacciones de doble desplazamiento. Representación ACIDO + BASE → AGUA + SAL HCl (ac) + Na. OH (ac) → H 2 O + Na. Cl (ac) Acido Base H 2 SO 4 (ac) + 2 KOH (ac) Agua sal K 2 SO 4 (ac) + 2 H 2 O 19

Reacciones de Combustión Los compuestos que contienen como mínimo Carbono, Hidrógeno arden con el aire (consumiendo Oxígeno) y forman CO 2*+H 2 O+energía. La gasolina en los automotores al quemarse es un ejemplo de combustión, igual que el gas en las estufas, el alcohol en los mecheros, la cera de las velas, Etc. * Se forma cuando hay suficiente oxígeno disponible. • Ejemplo combustión del metano y el Etanol: CH 4 (g) + 2 O 2 (g) CO 2 (g) + 2 H 2 O (g) + Energía 20

REACCIÓN ENDOTERMICA Estas necesitan energía, ya que la energía de los productos es mayor que la energía de los reactivos ( generalmente la energía se les da en forma de calor, por eso el laboratorio se indica: caliente en baño María, estufa, mechero). El valor de △H tiene un signo positivo (+). Se pueden indicar de las siguientes formas: H 2(g) + ½ O 2(g) +283 Kcal → H 2 O (l) H 2(g) + ½ O 2(g) → H 2 O (l) △H =+283 Kcal H 2 (g) + ½ O 2 (g) + H 2 O (l) 21

REACCIÓN EXOTERMICA En éstas se libera energía ya que la energía de los reactivos es mayor que la energía del producto. El calor o la energía fluye afuera del sistema , hacia los alrededores. En el laboratorio, se siente que el tubo de ensayo se pone caliente o se genera luz o llamas. El valor △H tiene un signo negativo(-). Pueden representarse así: CH 4(g) + 2 O 2(g) → CO 2(g)+2 H 2 O(g) + 192 Kcal CH 4(g) + 2 O 2(g) → CO 2(g)+2 H 2 O(g) △H= -192 Kcal CH 4(g) + 2 O 2(g) → CO 2(g)+2 H 2 O(g) + calor 22

REACCIONES REVERSIBLES Pueden realizarse en una u otra dirección. Reacción directa : A → B ( hacia la derecha) Reacción inversa: A B ( hacia la izquierda) Se representan con una Doble flecha que apunta en ambas direcciones (⇄) para indicar que la reacción es reversible. A ⇄ B Flecha a la derecha: Reacción directa Flecha a la izquierda: ← Reacción inversa CS 2 (g) + 4 H 2 (g) ⇄ CH 4 (g) + 2 H 2 S (g) 23

Balanceo de Ecuaciones Este procedimiento, consiste en buscar los coeficientes ( Números enteros en su mayoría que se colocan delante de la formula ó símbolos de las sustancias participantes) que permiten que en una ecuación química se hallen exactamente el mismo número de átomos a cada lado de la ecuación. Recuerde una ecuación es una igualdad. Además debe cumplirse con la ley de la conservación de la masa ( igual numero de átomos en ambos lados de la ecuación). 24

• Ejemplos: • A- Ecuación NO balanceada: • NH 3 N 2 + H 2 • Balanceada : 2 NH 3 N 2 + 3 H 2 • Los coeficientes que balancean la ecuación: • Del lado de los reactivos : 2 • Del lado de los productos: 1, 3 25

Métodos para balancear una ecuación • Existen varias formas entre ellas : • A- Método Algebraico ( no se verá) • B- Método del ión electrón ( no se verá ) • C- Método Redox ó de Oxido. Reducción ( se verá sem. 5) • D- Balanceo por tanteo( se verá sem. 4) 26

Balanceo por Tanteo Se coloca los coeficientes delante de las fórmulas ó símbolos de las sustancias participantes , hasta lograr igualar el número de cada átomo en el lado de reactivos y productos. Se recomienda seguir el siguiente orden al balancear la ecuación : 1) METALES 2) NO METALES 3)HIDROGENOS 4)OXIGENOS 27

Ejercicios: Balancee por tanteo las siguientes ecuaciones. a) Na. OH + H 2 S → Na 2 S + H 2 O b) KCl. O 3 → KCl + O 2 c) Mg(s) + N 2 (g) → Mg 3 N 2(s) a) Ag. NO 3+ Ba. Cl 2 → Ag. Cl+ Ba(NO 3)2 28
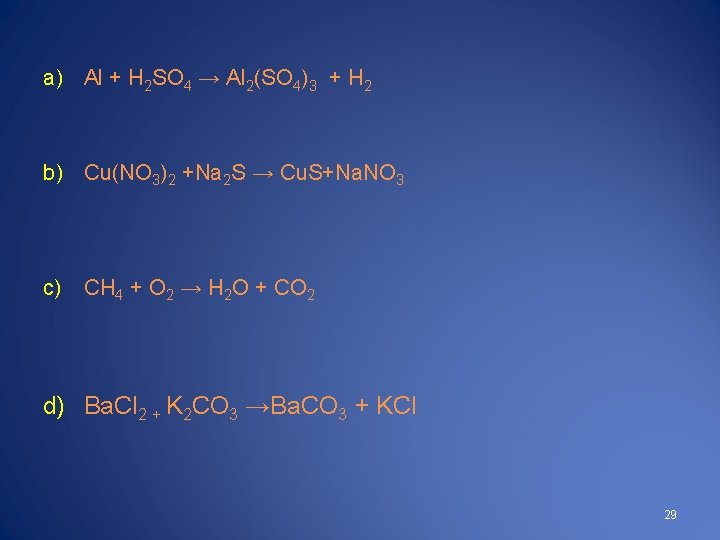
a) Al + H 2 SO 4 → Al 2(SO 4)3 + H 2 b) Cu(NO 3)2 +Na 2 S → Cu. S+Na. NO 3 c) CH 4 + O 2 → H 2 O + CO 2 d) Ba. Cl 2 + K 2 CO 3 →Ba. CO 3 + KCl 29

NÚMERO Ó ESTADO DE OXIDACIÓN un número que se le asigna a Es los átomos presentes en un compuesto ó en estado elemental, o también a iones. Reglas para asignar números de oxidación 1. A todo elemento no combinado o unido consigo mismo se le asigna un número de oxidación de cero. H 2 : H combinado con el mismo se le asigna # de oxidación Cero. Igual con otros combinados con ellos mismos Cl 2 : Cl = 0 Zn : No esta combinado se le asigna cero. Zn = 0 igual a la plata si no se halla combinada se le 30

2 -El Hidrógeno en la mayoría de sus compuestos, se le asigna un numero de Oxidación de +1. • Excepción Hidruros ( Hidrógeno + Metal) en cuyo caso el Hidrógeno se le asigna, -1. Estos casos NO se verán durante el curso. Recordar que si está en forma de H 2 , se le asigna 0. • Ejemplo: Asigne los números ó estados de oxidación del H y S en el H 2 S y en el NH 3 : Cargas totales de los H +2* cargas

• Al Oxígeno en la mayoría de sus compuestos , se le asigna un número de oxidación -2. Excepción : Peróxidos, donde se le asigna -1. Ejemplo: Peroxido de Hidrogeno H 2 O 2 : H+1 O -1 H : +1 O: -1 • En el resto de sus compuestos se le asigna -2. Ej: CO 2 C +4 O-2 2 C: +4 O: -2 Cargas totales del oxígeno : -4 entonces el 32

3 -Para las siguientes familias, el número de oxidación predominante al combinarse: Columna IA No. de oxidación = + 1 Columna IIA No. de oxidación = + 2 Columna IIIA No. de oxidación = + 3 Excepción : Ta : +1, +3 El Flúor siempre que forma compuestos con átomos diferentes se le asigna Número de oxidación -1. 4 -En un compuesto, la suma de todos los números de oxidación es cero. Ej: H 3 BO 3 H= +1 B= +3 O= -2 5 -En un ión poli atómico, la suma de los números de oxidación de todos los átomos es igual a la carga del ión. Ej: PO 4 -3 : O = -2 x 4 = - 8 ; P = +5 Total carga del ión = -3 33

6 -A todos los iones monoatómicos se les asigna números de oxidación iguales a la carga de los iones en esos compuestos : Na + : Na = +1 Ca +2 : Ca : +2 S -2 : S = -2 Cl - : Cl = -1 7 - Para compuestos binarios de la siguiente forma: Ax. By : si X es diferente de Y ( , El número de Oxidación de A será «y» y el de B será «X» Se le debe colocar signo positivo al átomo de menor electronegatividad y signo negativo al de mayor electronegatividad: Ejemplo : Fe 2 S 3 : Fe = +3 S = -2 PCl 5 : P = +5 Cl = -1 34

• Si el elemento se halla en columna par, puede presentar principalmente números de oxidación pares, que no sobrepasen su número de columna. Igual los de Elemen No. Columna Nos. Oxidación más comunes columnas impares. to IV (par) ± 2, 4 S VI ( par) ± 2, 4, 6 As V ( impar) ± Cl VII ( impar ) ± 1, 3, 5, 7 C 3, 5 35

Recordar que: Para encontrar los números de oxidación de los elementos en un compuesto , BASESE en las normas vistas, NO es necesario recurrir a la tabla periódica pues alli no encontrará todos los números de oxidación. Por ejemplo : No aparece el -1, que posee el oxígeno en los peróxidos, ni el 0 ( cero) que se le asigna a los elementos No combinados ó combinados con ellos mismos. 36
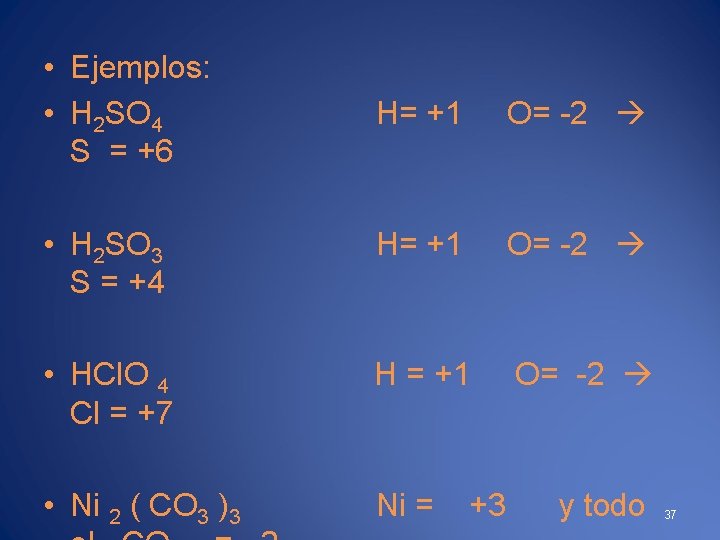
• Ejemplos: • H 2 SO 4 S = +6 H= +1 O= -2 • H 2 SO 3 S = +4 H= +1 O= -2 • HCl. O 4 Cl = +7 H = +1 O= -2 • Ni 2 ( CO 3 )3 Ni = +3 y todo 37
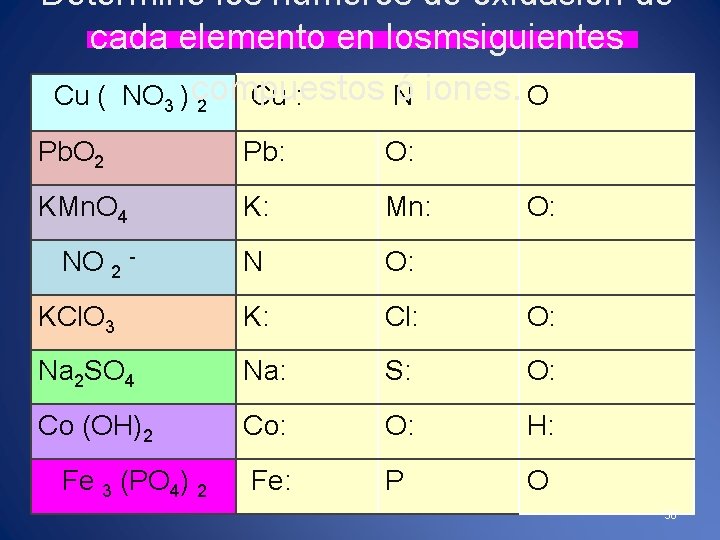
Determine los números de oxidación de cada elemento en losmsiguientes ó iones. Cu ( NO 3 ) compuestos Cu : N O 2 Pb: O: KMn. O 4 K: Mn: NO 2 - N O: KCl. O 3 K: Cl: O: Na 2 SO 4 Na: S: O: Co (OH)2 Co: O: H: Fe: P O Fe 3 (PO 4) 2 O: 38

Resuelva los siguientes ejercicios de la guía de estudio: Ejercicios : 6. 1 y 6. 2 , 7, 9, 10 , 13, 16 39
- Slides: 39