Precorsi Test AMMISSIONE Medicina e Chirurgia Professioni Sanitarie









- Slides: 37

Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia CARBOIDRATI a. a. 2018/2019

Con il nome generico di CARBOIDRATI (o zuccheri o glucidi) si individua un gruppo di composti con peso molecolare variabile da 100 a più di un milione

CARBOIDRATI MONOSACCARIDI zuccheri semplici non scindibili per idrolisi OLIGOSACCARIDI costituiti da 2 a 10 unità monosaccaridiche uguali o diverse POLISACCARIDI costituiti da centinaia o migliaia di unità monosaccaridiche uguali o diverse

CARBOIDRATI Molteplicità di funzioni Il ruolo macroscopico consiste nel costituire una delle forme di immagazzinamento dell’energia Legati a proteine e lipidi si ritrovano nella membrana plasmatica Le strutture glucidiche sono presenti in coenzimi e acidi nucleici

MONOSACCARIDI Cn(H 2 O)n Chimicamente: poliidrossialdeidi poliidrossichetoni 1 funzionalità CARBONILICA n= almeno 3 e raramente > 7 aldeidica ( ALDOSI ) chetonica ( CHETOSI ) 1 gruppo ALCOLICO in ognuno dei restanti atomi di C

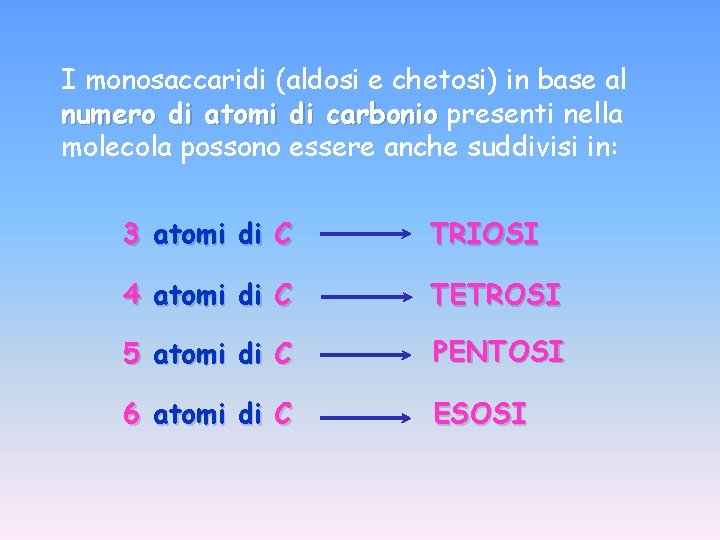
I monosaccaridi (aldosi e chetosi) in base al numero di atomi di carbonio presenti nella molecola possono essere anche suddivisi in: 3 atomi di C TRIOSI 4 atomi di C TETROSI 5 atomi di C PENTOSI 6 atomi di C ESOSI

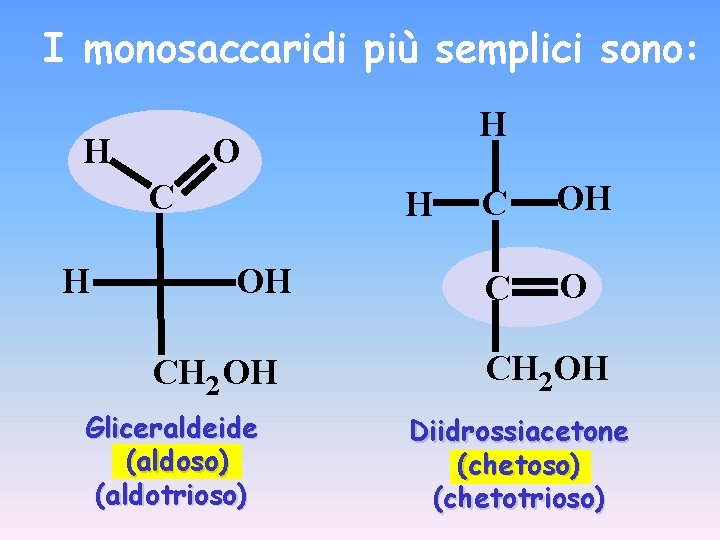
I monosaccaridi più semplici sono: H O C H H H OH CH 2 OH Gliceraldeide (aldoso) (aldotrioso) C OH C O CH 2 OH Diidrossiacetone (chetoso) (chetotrioso)

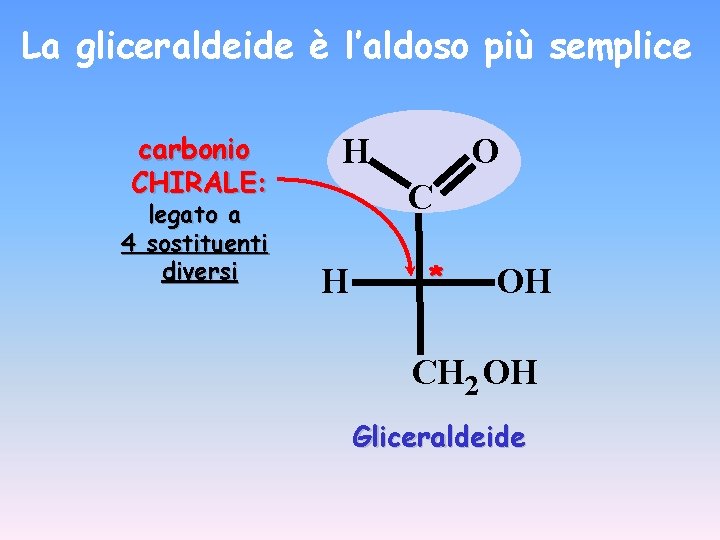
La gliceraldeide è l’aldoso più semplice carbonio CHIRALE: legato a 4 sostituenti diversi H O C H * OH CH 2 OH Gliceraldeide

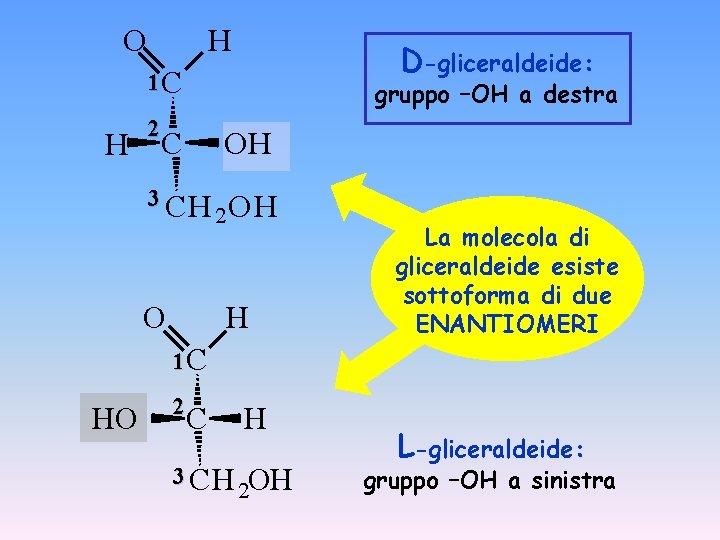
O H D-gliceraldeide: 1 C H 2 gruppo –OH a destra C OH 3 CH O 2 OH H La molecola di gliceraldeide esiste sottoforma di due ENANTIOMERI 1 C HO 2 C 3 CH H 2 OH L-gliceraldeide: gruppo –OH a sinistra

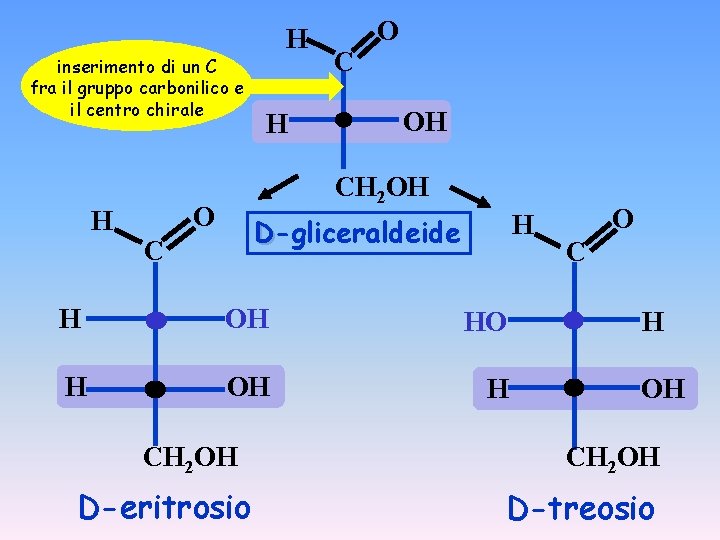
inserimento di un C fra il gruppo carbonilico e il centro chirale H H H O C OH CH 2 OH O H D-gliceraldeide C H OH HO H OH H CH 2 OH D-eritrosio O C H OH CH 2 OH D-treosio

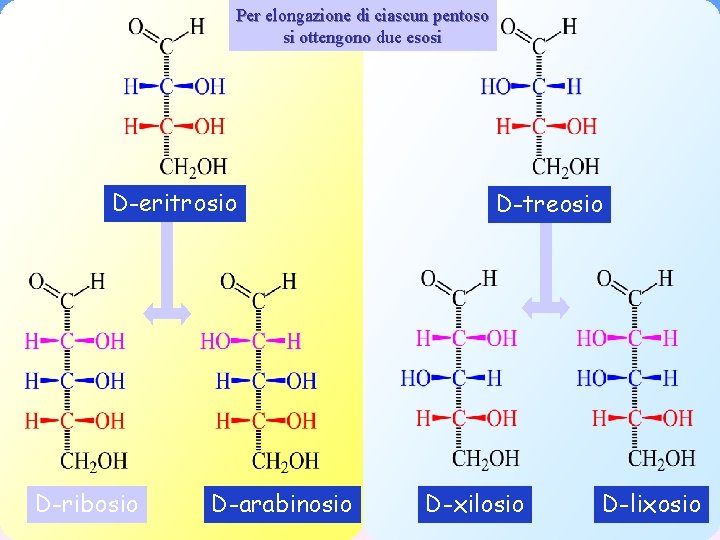
Per elongazione di ciascun pentoso si ottengono due esosi D-eritrosio D-ribosio D-arabinosio D-treosio D-xilosio D-lixosio

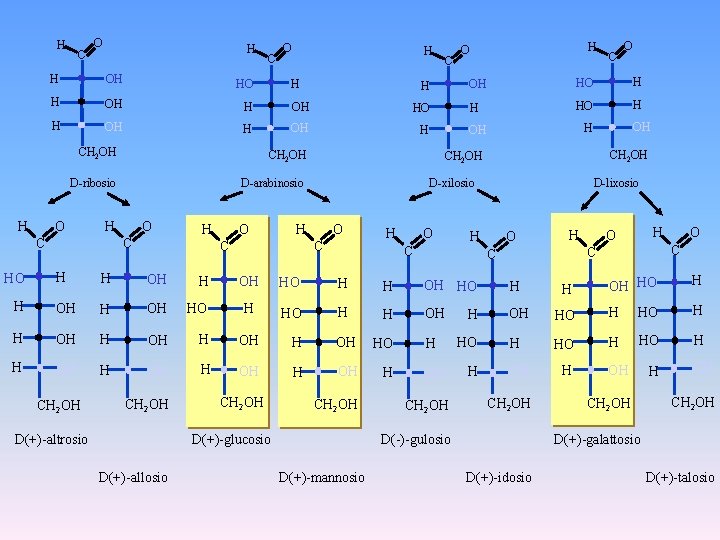
H H C O H H OH HO H OH CH 2 OH D-ribosio D-arabinosio O H C O C H O C C H H OH HO H OH H OH H D(+)-altrosio H H OH CH 2 OH O D-lixosio H O H H HO H H OH OH HO H CH 2 OH OH CH 2 OH HO H OH CH 2 OH D(-)-gulosio D(+)-mannosio C H H H O OH HO H H H O C C HO CH 2 OH OH D(+)-glucosio D(+)-allosio HO C OH CH 2 OH HO D-xilosio H HO H CH 2 OH O O HO H H C OH H CH 2 OH C H O H CH 2 OH H OH CH 2 OH D(+)-galattosio D(+)-idosio D(+)-talosio

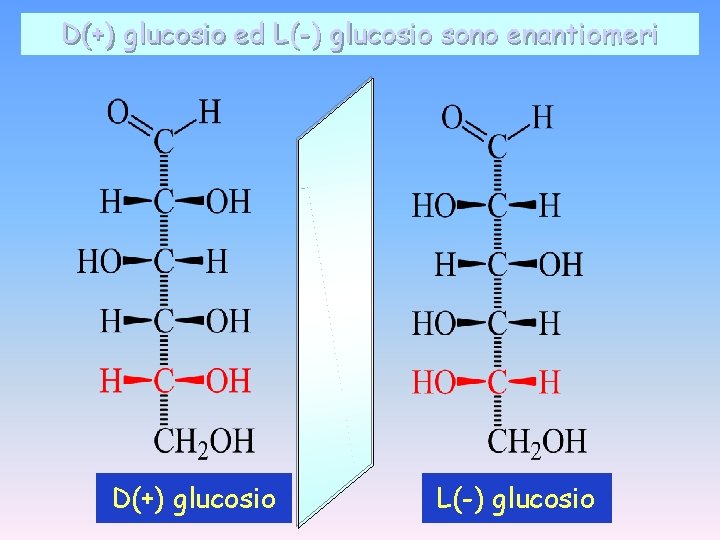
D(+) glucosio ed L(-) glucosio sono enantiomeri D(+) glucosio L(-) glucosio

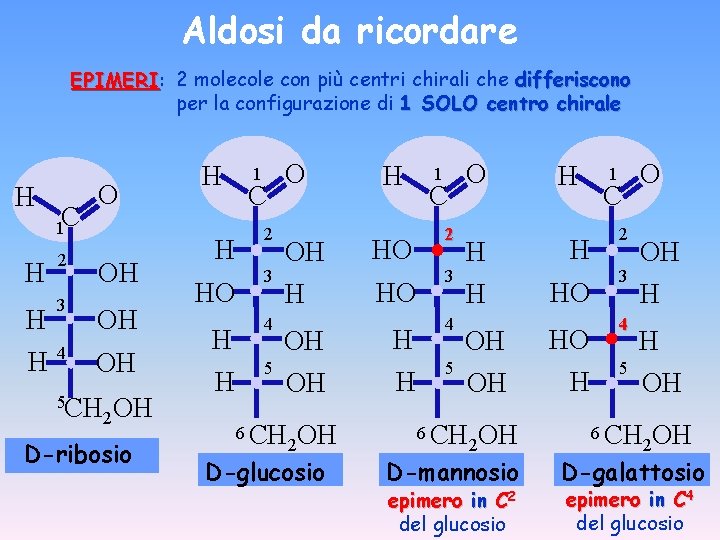
Aldosi da ricordare EPIMERI: EPIMERI 2 molecole con più centri chirali che differiscono per la configurazione di 1 SOLO centro chirale H 1 C H 2 H 3 H 4 O OH OH OH 5 CH 2 OH D-ribosio H H HO H H 1 C 2 3 4 5 O H OH HO OH OH 6 CH 2 OH D-glucosio H H 1 C 2 3 4 5 O H H HO OH OH 6 CH 2 OH D-mannosio epimero in C 2 del glucosio HO H 1 C 2 3 4 5 O OH H H OH 6 CH 2 OH D-galattosio epimero in C 4 del glucosio

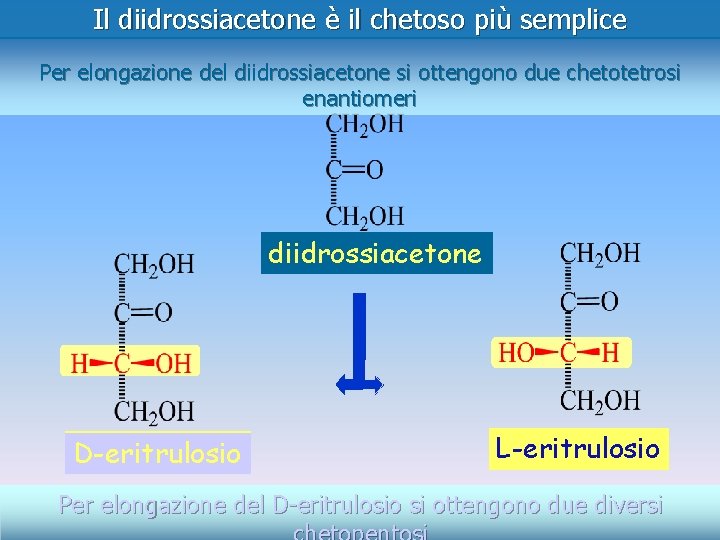
Il diidrossiacetone è il chetoso più semplice Per elongazione del diidrossiacetone si ottengono due chetotetrosi enantiomeri diidrossiacetone D-eritrulosio L-eritrulosio Per elongazione del D-eritrulosio si ottengono due diversi

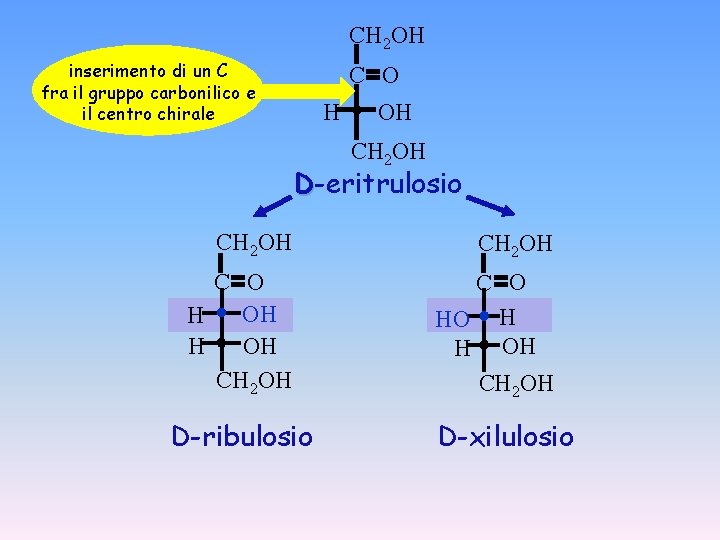
CH 2 OH inserimento di un C fra il gruppo carbonilico e il centro chirale C O H OH CH 2 OH D-eritrulosio CH 2 OH C O OH H CH 2 OH C O HO H H OH CH 2 OH D-ribulosio D-xilulosio

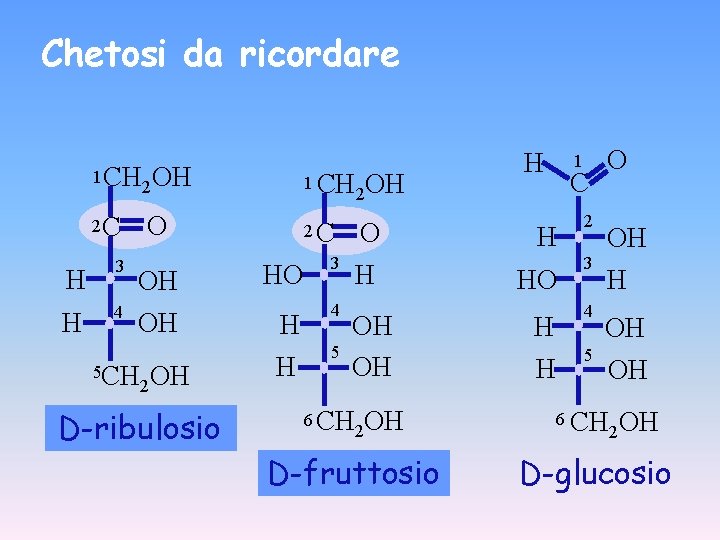
Chetosi da ricordare 1 CH 2 OH 1 CH 2 C O 2 C H 3 H 4 OH OH 5 CH 2 OH D-ribulosio HO 3 H 4 H 5 2 OH O H OH OH 6 CH 2 OH D-fruttosio H 1 C H HO 2 3 4 H H 5 O OH H OH OH 6 CH 2 OH D-glucosio

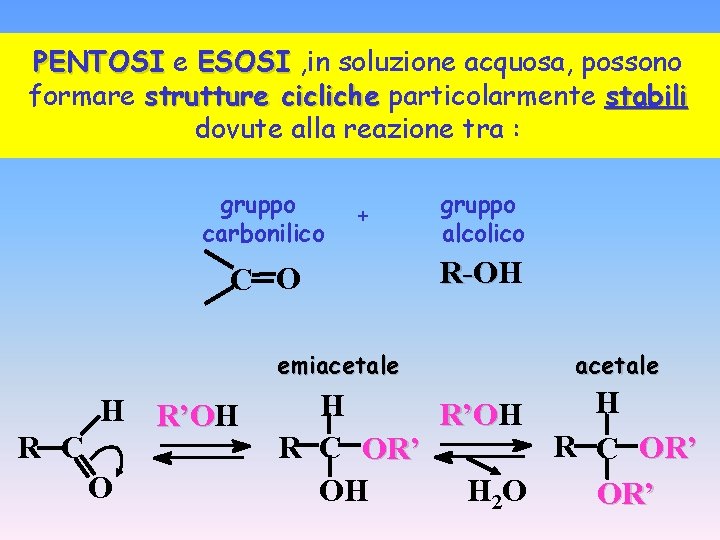
PENTOSI e ESOSI , in soluzione acquosa, possono formare strutture cicliche particolarmente stabili dovute alla reazione tra : gruppo carbonilico + C O emiacetale R C H R’O O gruppo alcolico R-OH R-O acetale H H R’O R C OR’ OH H 2 O OR’

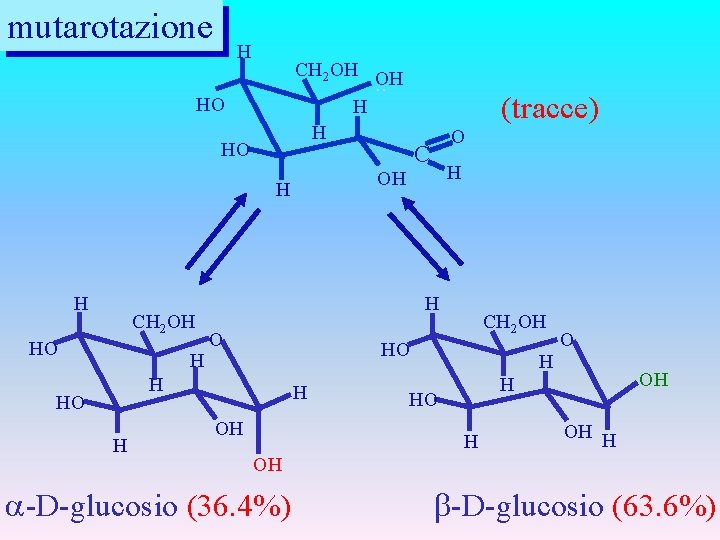
mutarotazione H CH 2 OH OH. . H H HO HO CH 2 OH HO H H O CH 2 OH HO O C OH H H (tracce) H OH H O OH H HO H OH -D-glucosio (36. 4%) -D-glucosio (63. 6%)

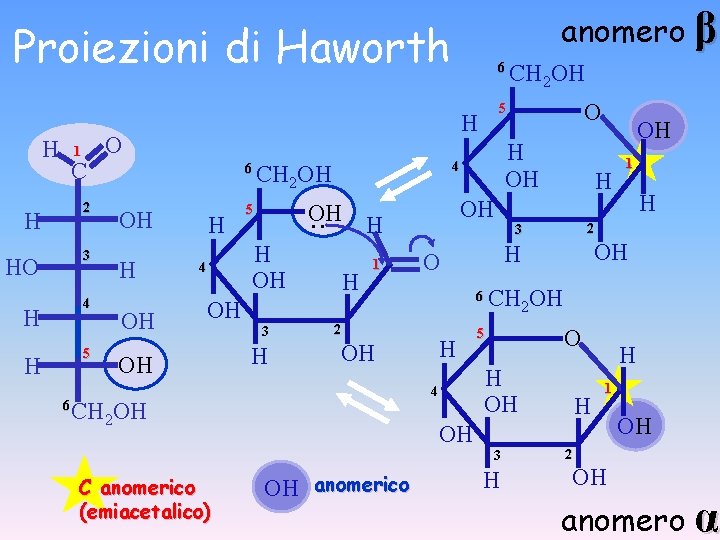
anomero β Proiezioni di Haworth H 1 C 2 H 3 HO 4 H 5 H 6 6 OH OH H H OH 4 OH OH 3 H H 1 6 H OH OH OH anomerico 1 H 2 3 OH CH 2 OH O 5 H OH 4 OH H H O 2 CH 2 OH C anomerico (emiacetalico) OH OH. . H 5 O H OH 4 CH 2 OH 5 H O H 6 3 H H H 1 OH 2 OH anomero α

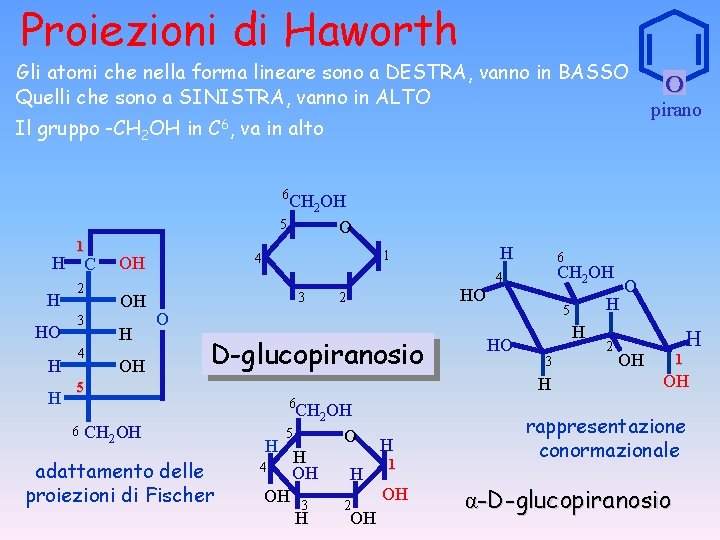
Proiezioni di Haworth Gli atomi che nella forma lineare sono a DESTRA, vanno in BASSO Quelli che sono a SINISTRA, vanno in ALTO Il gruppo -CH 2 OH in C 6, va in alto O pirano 6 CH 2 OH 5 O H H HO H H 1 C 2 3 4 OH H OH 3 2 HO 6 CH 2 OH 4 D-glucopiranosio CH 2 OH adattamento delle proiezioni di Fischer HO H 3 H 6 CH 2 OH 5 O H H H 1 4 OH H OH OH 3 2 H OH H 5 O 5 6 H 1 4 OH 2 O H OH 1 OH rappresentazione conormazionale α-D-glucopiranosio

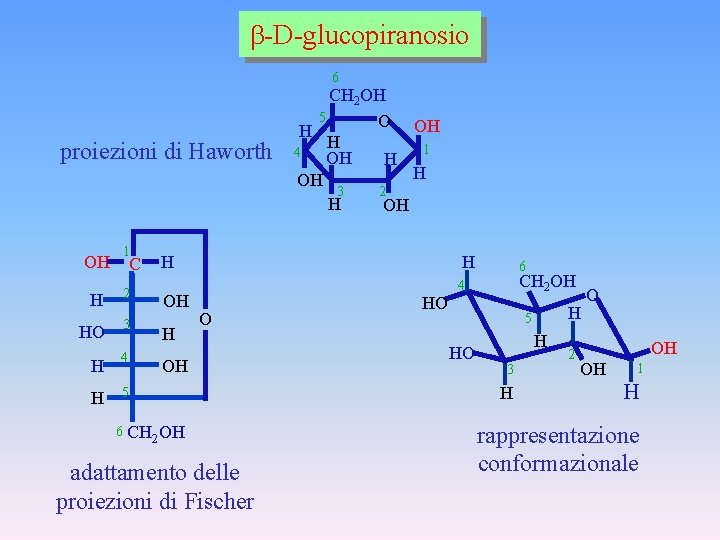
-D-glucopiranosio 6 proiezioni di Haworth 1 OH C H 2 HO 3 H 4 H 5 6 CH 2 OH 5 O OH H H 1 4 OH H H OH 3 2 H OH H O OH CH 2 OH adattamento delle proiezioni di Fischer HO 6 CH 2 OH 4 H 5 HO H 3 H 2 O OH OH 1 H rappresentazione conformazionale

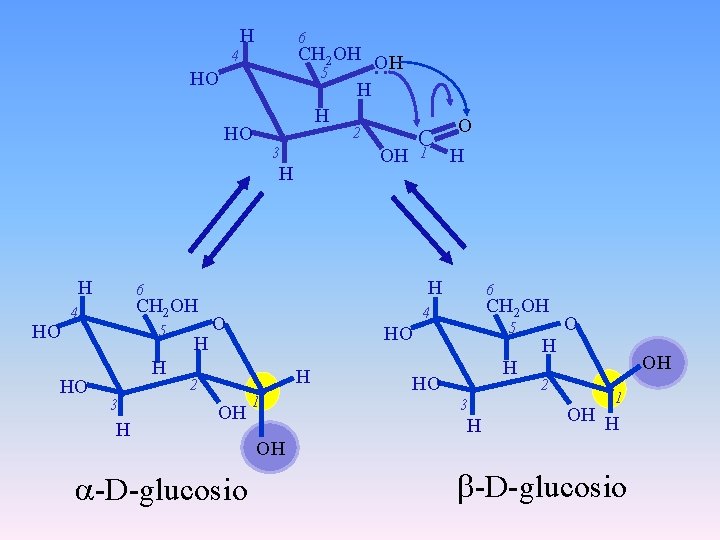
H 6 HO HO 2 3 HO 1 CH 2 OH 5 H 3 H H O H H 6 4 HO C OH H H . . CH 2 OH OH 5 H H 4 -D-glucosio 5 HO H OH CH 2 OH 4 O 2 6 1 H HO 3 H H 2 O OH 1 OH H OH -D-glucosio

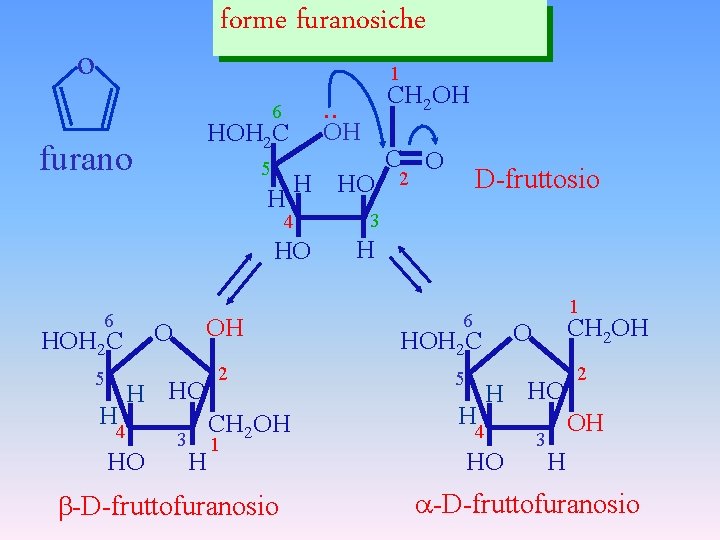
forme furanosiche o 1 . . 6 OH HOH 2 C furano 5 H H HO 4 HO 6 HOH 2 C 5 H OH O H HO 4 HO 3 2 CH 2 OH H 1 -D-fruttofuranosio CH 2 OH C O D-fruttosio 2 3 H 1 6 5 H CH 2 OH O HOH 2 C H HO 4 HO 3 2 OH H -D-fruttofuranosio

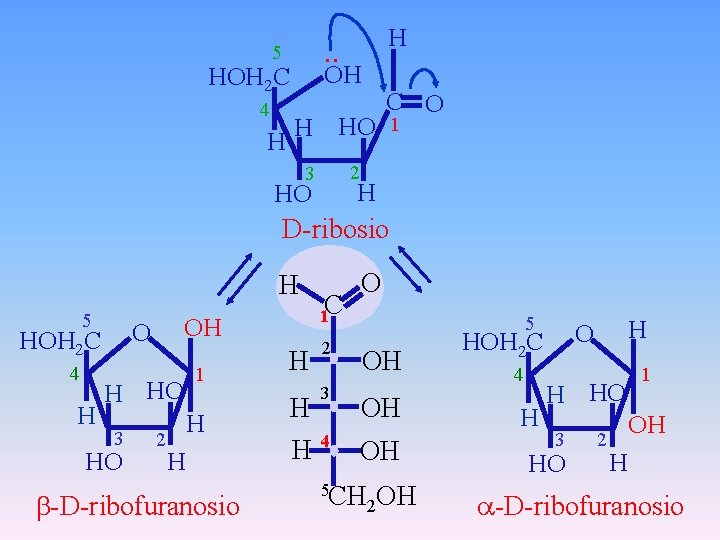
OH HOH 2 C 4 H H . . 5 H HO C O 1 2 3 H HO D-ribosio H 5 HOH 2 C 4 H OH O H HO 3 HO 2 1 H H -D-ribofuranosio 1 C H 2 H 3 H 4 O 5 OH OH OH 5 CH 2 OH 4 H H O HOH 2 C H HO 3 HO 2 1 OH H -D-ribofuranosio

DISACCARIDI

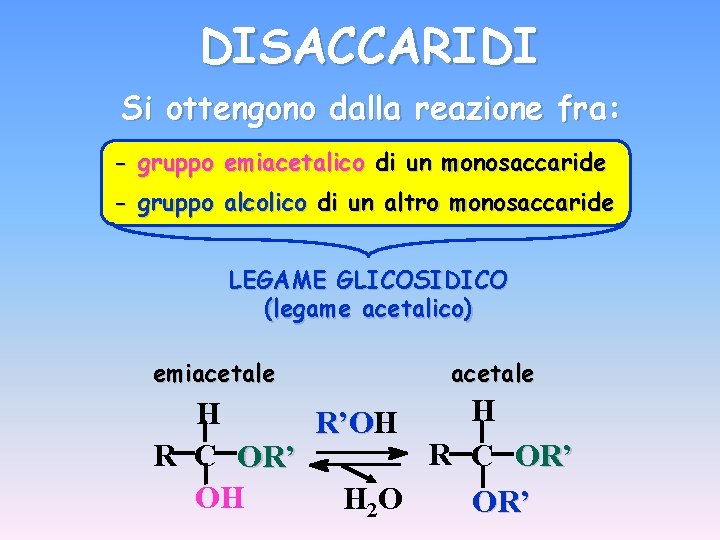
DISACCARIDI Si ottengono dalla reazione fra: - gruppo emiacetalico di un monosaccaride - gruppo alcolico di un altro monosaccaride LEGAME GLICOSIDICO (legame acetalico) emiacetale H H R’O R C OR’ OH H 2 O OR’

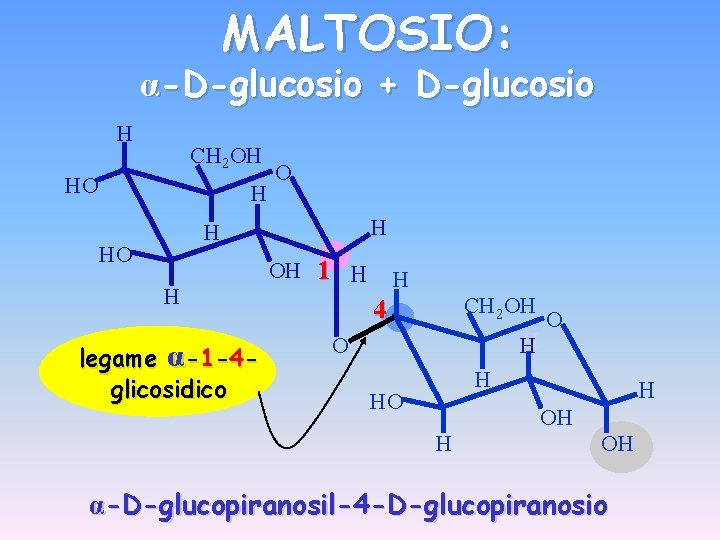
MALTOSIO: α-D-glucosio + D-glucosio H CH 2 OH HO H legame α-1 -4 glicosidico OH 1 H H CH 2 OH 4 H H O O H HO H OH α-D-glucopiranosil-4 -D-glucopiranosio

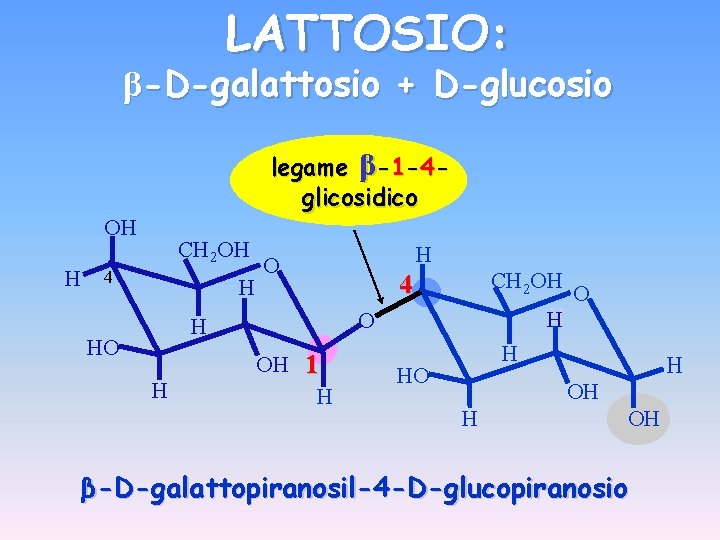
LATTOSIO: β-D-galattosio + D-glucosio legame β-1 -4 glicosidico OH H CH 2 OH 4 H H O H HO H O OH 1 H O H HO H OH β-D-galattopiranosil-4 -D-glucopiranosio

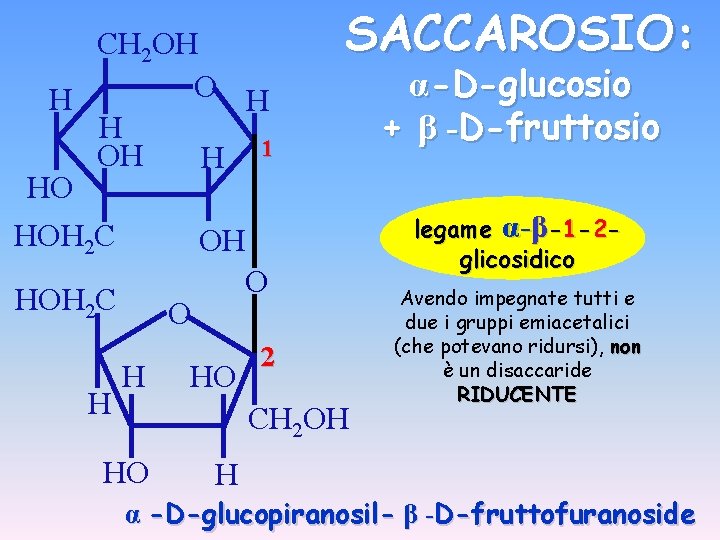
CH 2 OH O H H H OH H 1 HO HOH 2 C H O H SACCAROSIO: OH O HO 2 CH 2 OH HO α-D-glucosio + β -D-fruttosio legame α-β-1 -2 glicosidico Avendo impegnate tutti e due i gruppi emiacetalici (che potevano ridursi), non è un disaccaride RIDUCENTE H α -D-glucopiranosil- β -D-fruttofuranoside

POLISACCARIDI

POLISACCARIDI: polimeri costituiti da un numero elevato di unità monosaccaridiche - AMIDO GLICOGENO CELLULOSA - ACIDO IALURONICO - EPARINA - CONDROITINSOLFATO costituiti SOLO da GLUCOSIO (OMOPOLISACCARIDI) formati da unità monosaccaridiche DIVERSE (ETEROPOLISACCARIDI)

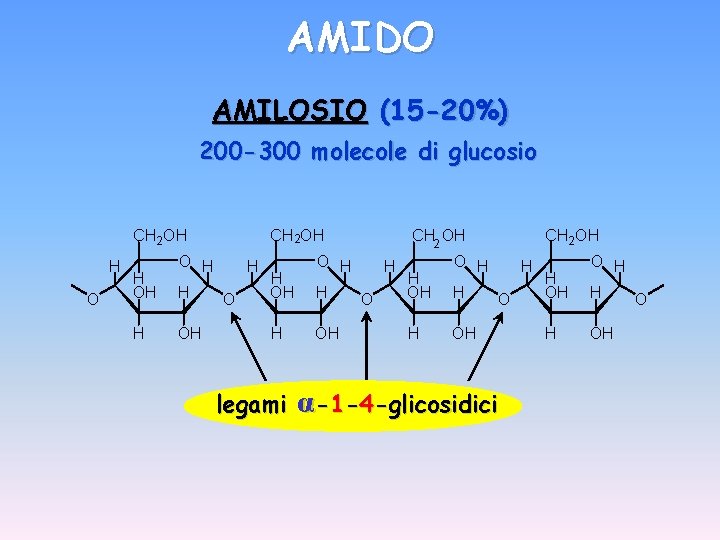
AMIDO polisaccaride di RISERVA dei VEGETALI Contiene 2 unità distinte: - AMILOSIO (15 -20%) costituito da catene lineari di D-glucosio (200 -300 molecole) legami α-1 -4 -glicosidici - AMILOPECTINA (80 -85%) α-1 -4 -glicosidici legami α-1 -6 -glicosidici legami per la parte lineare nei punti di RAMIFICAZIONE (ogni 24 -30 unità di glucosio)

AMIDO AMILOSIO (15 -20%) 200 -300 molecole di glucosio CH 2 OH H O CH 2 OH O H H OH H O O H H OH legami CH 2 OH CH 2 OH H O O H H OH H O α-1 -4 -glicosidici O H H OH O

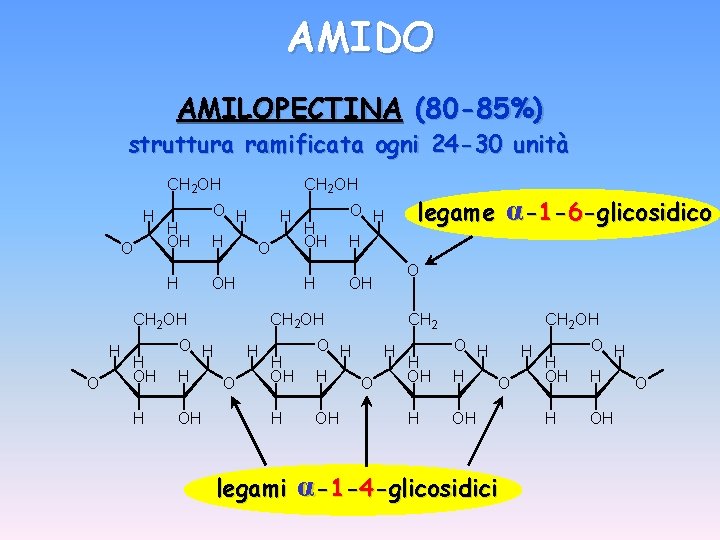
AMIDO AMILOPECTINA (80 -85%) struttura ramificata ogni 24 -30 unità CH 2 OH H O CH 2 OH O H H OH H O CH 2 OH H O H H OH legami CH 2 O H H OH α-1 -6 -glicosidico legame O CH 2 OH O H H OH H O α-1 -4 -glicosidici O H H OH O

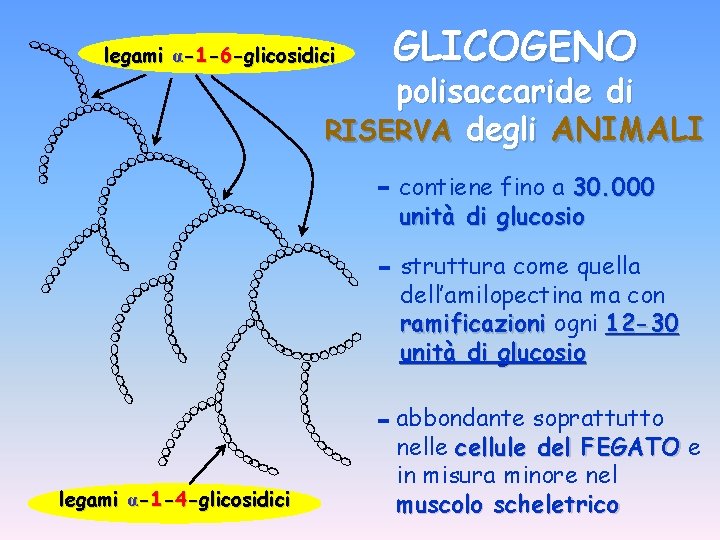
legami α-1 -6 -glicosidici GLICOGENO polisaccaride di RISERVA degli ANIMALI - contiene fino a 30. 000 unità di glucosio - struttura come quella dell’amilopectina ma con ramificazioni ogni 12 -30 unità di glucosio - abbondante soprattutto legami α-1 -4 -glicosidici nelle cellule del FEGATO e in misura minore nel muscolo scheletrico

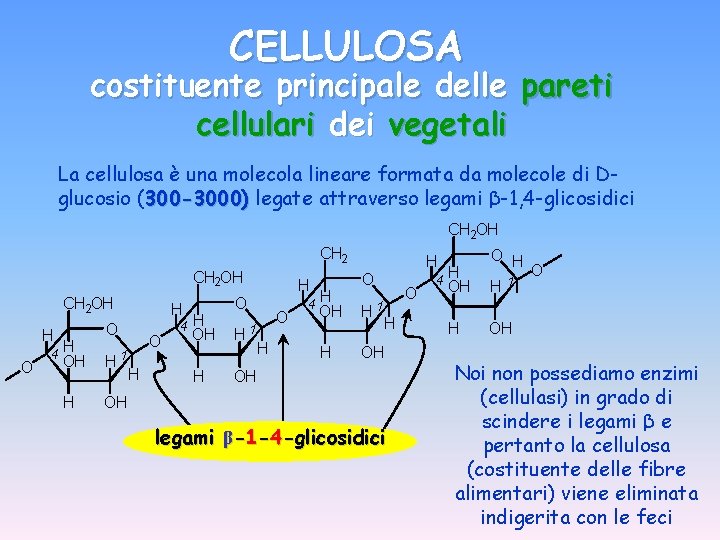
CELLULOSA costituente principale delle pareti cellulari dei vegetali La cellulosa è una molecola lineare formata da molecole di Dglucosio (300 -3000) legate attraverso legami β-1, 4 -glicosidici CH 2 OH H O 4 H O OH H 1 H H O 4 H H O OH H 1 H OH O H 4 H OH H H O H 1 H OH legami β-1 -4 -glicosidici O 4 H O H OH H 1 H OH O Noi non possediamo enzimi (cellulasi) in grado di scindere i legami β e pertanto la cellulosa (costituente delle fibre alimentari) viene eliminata indigerita con le feci