Metody studia a charakterizace nanomateril Termick analza a



















- Slides: 51

Metody studia a charakterizace nanomateriálů Termická analýza a kalorimetrie Aplikace při charakterizaci nanomateriálů J. Leitner ÚIPL VŠCHT Praha

Obsah přednášky 1. Termická analýza a kalorimetrie … 2. Teoretické základy (termochemie a přenos tepla) … 3. Termogravimetrie … 4. Kalorimetrická měření … 5. Tepelné kapacity … 6. Teplota a entalpie tání … 7. Spalná tepla a molární entalpie 8. Povrchová energie/entalpie … 9. Adsorpční tepla … 10. Speciální kalorimetrické metody …

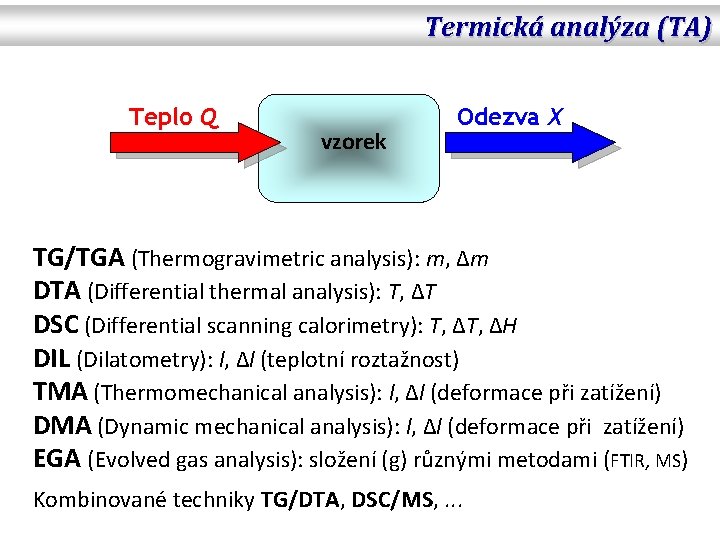
Termická analýza (TA) Teplo Q vzorek Odezva X TG/TGA (Thermogravimetric analysis): m, ∆m DTA (Differential thermal analysis): T, ∆T DSC (Differential scanning calorimetry): T, ∆H DIL (Dilatometry): l, ∆l (teplotní roztažnost) TMA (Thermomechanical analysis): l, ∆l (deformace při zatížení) DMA (Dynamic mechanical analysis): l, ∆l (deformace při zatížení) EGA (Evolved gas analysis): složení (g) různými metodami (FTIR, MS) Kombinované techniky TG/DTA, DSC/MS, . . .

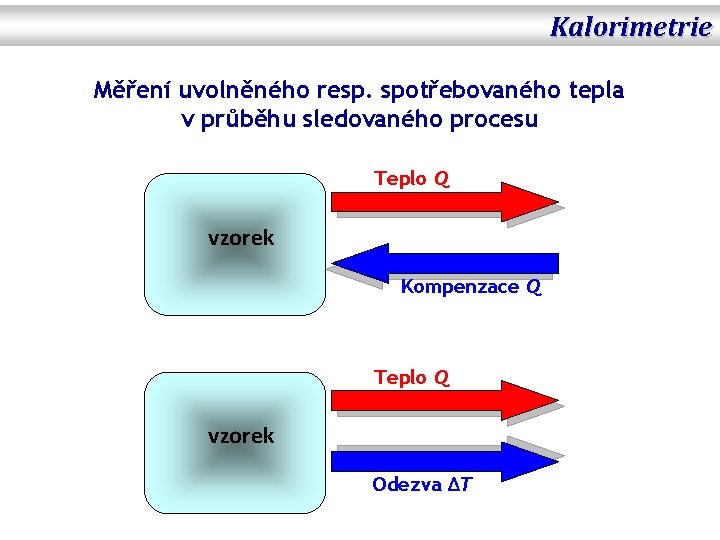
Kalorimetrie Měření uvolněného resp. spotřebovaného tepla v průběhu sledovaného procesu Teplo Q vzorek Kompenzace Q Teplo Q vzorek Odezva ∆T

Současné aplikace TA a kalorimetrie • Stanovení energetického obsahu v palivech a biomase • Stanovení základních termofyzikálních vlastností čistých látek (tepelné kapacity, teploty a tepla fázových přeměn) • Stanovení reakčních tepel (dehydratace, tepelný rozklad, spalná tepla, slučovací tepla) • Stanovení rozpouštěcích a směšovacích tepel • Stanovení adsorpčních tepel • Studium kinetiky heterogenních chemických reakcí materiálové inženýrství - geochemie - chemie biochemie – potravinářská chemie - farmacie

Energie, entalpie, tepelné kapacity

Entalpie fázových přeměn, reakční entalpie Kirchhoffův zákon Hessův zákon

Směšovací a rozpouštěcí entalpie

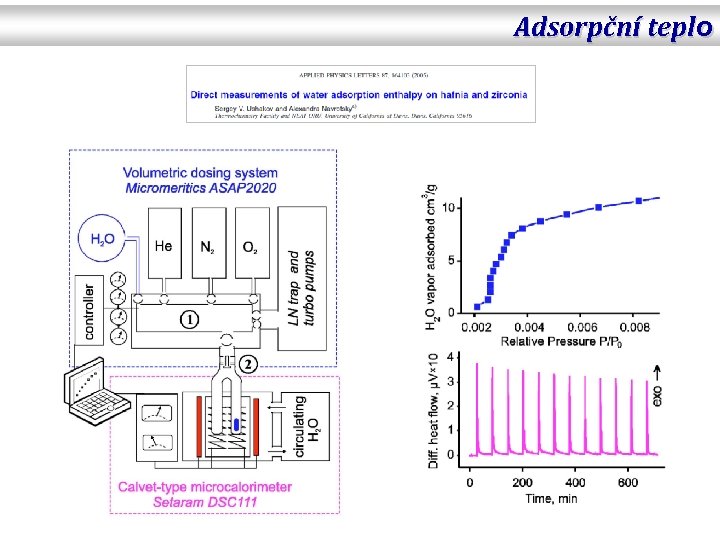
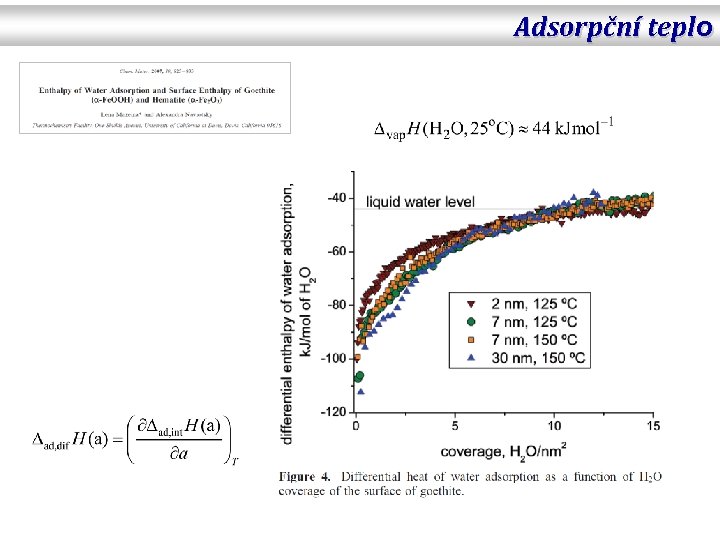
Adsorpční teplo Adsorbované množství a, θ Povrchová koncentrace Γ Diferenciální (izosterické) adsorpční teplo – Adsorpce 1 molu A při stálé teplotě a tlaku na daném povrchu při stálém adsorbovaném množství a(T, p). S rostoucí hodnotou a se snižuje a v limitě se blíží kondenzačnímu teplu adsorbátu. Intergrální adsorpční teplo – Adsorpce 1 molu A při stálé teplotě a tlaku na daném povrchu, jehož velikost je taková, že výsledné adsorbované množství je právě a(T, p).

Povrchová energie Vytvoření nového povrchu a=1 a = 1/2 (γsurf) - Reversibilně vykonaná práce při vzniku jednotkové plochy nového povrchu bez elastické deformace (skalární veličina). Jsou přerušeny vazby mezi atomy, na novém povrchu se objeví nové atomy, jsou zachovány délky vazeb, nemění se atomová hustota povrchu.

Transport tepla Vedení tepla v nehybném prostředí Fourierův zákon Fourierova-Kirchhoffova rovnice

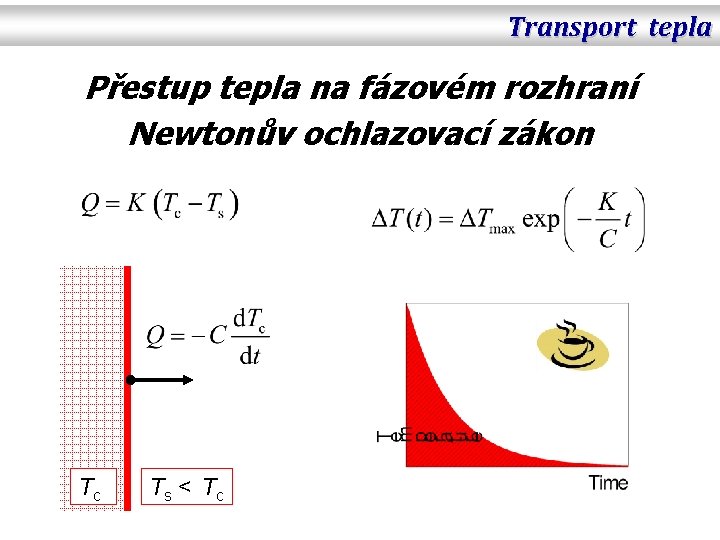
Transport tepla Přestup tepla na fázovém rozhraní Newtonův ochlazovací zákon Tc Ts < Tc

Termogravimetrie STA 449 F 1 Jupiter® (Netzsch) TG/DSC

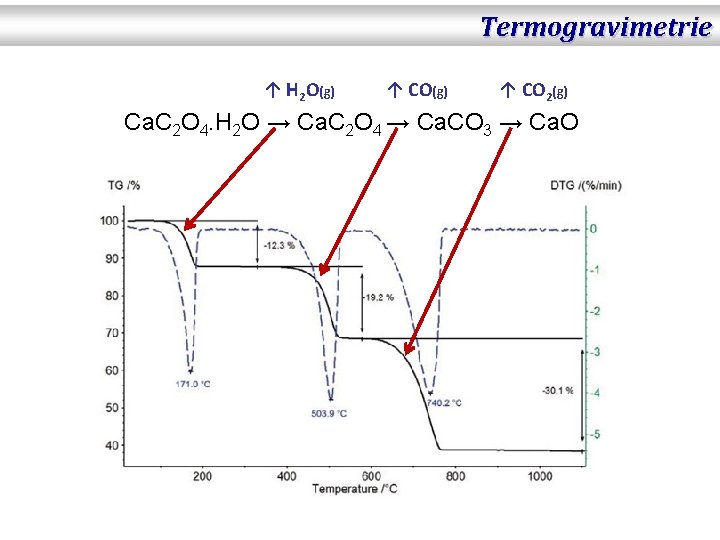
Termogravimetrie ↑ H 2 O(g) ↑ CO 2(g) Ca. C 2 O 4. H 2 O → Ca. C 2 O 4 → Ca. CO 3 → Ca. O

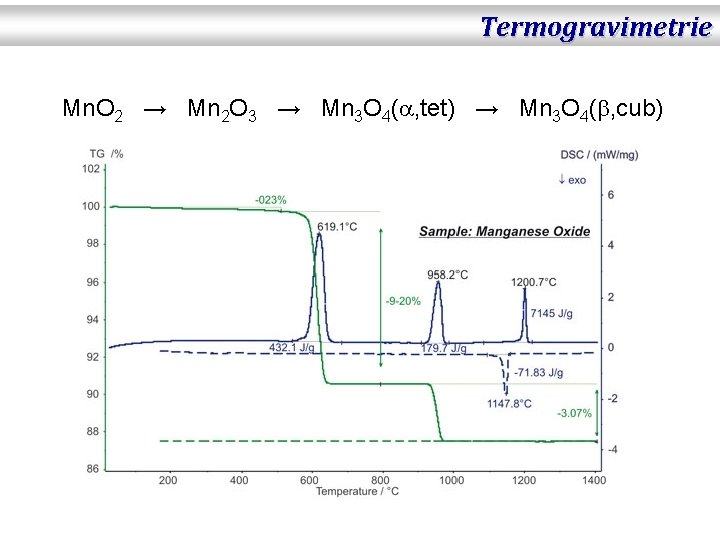
Termogravimetrie Mn. O 2 → Mn 2 O 3 → Mn 3 O 4( , tet) → Mn 3 O 4( , cub)

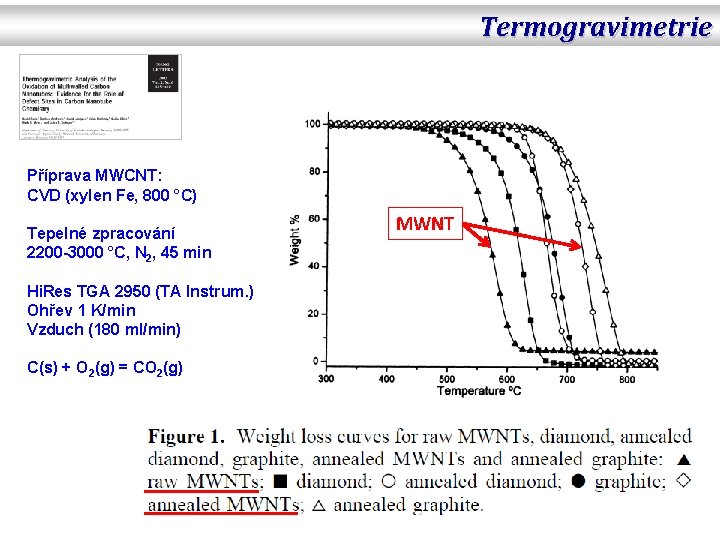
Termogravimetrie Příprava MWCNT: CVD (xylen Fe, 800 °C) Tepelné zpracování 2200 -3000 °C, N 2, 45 min Hi. Res TGA 2950 (TA Instrum. ) Ohřev 1 K/min Vzduch (180 ml/min) C(s) + O 2(g) = CO 2(g) MWNT

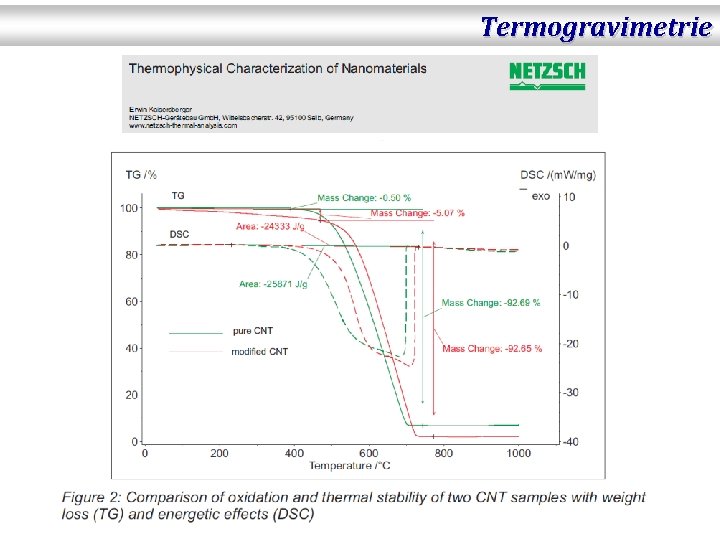
Termogravimetrie

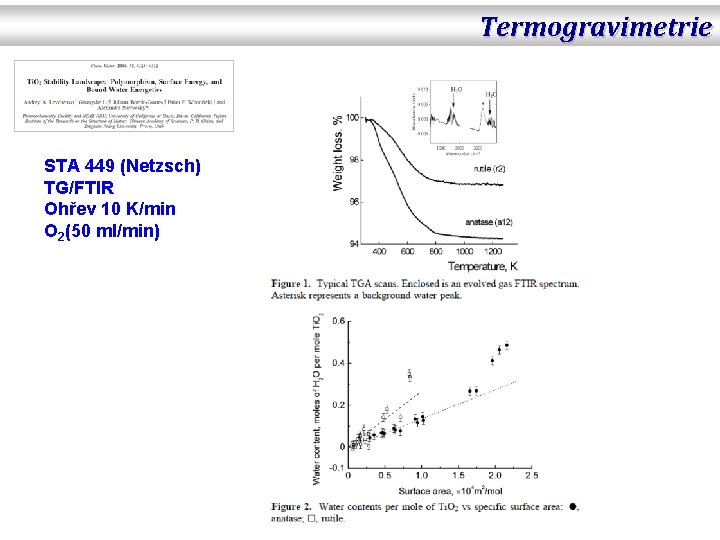
Termogravimetrie STA 449 (Netzsch) TG/FTIR Ohřev 10 K/min O 2(50 ml/min)

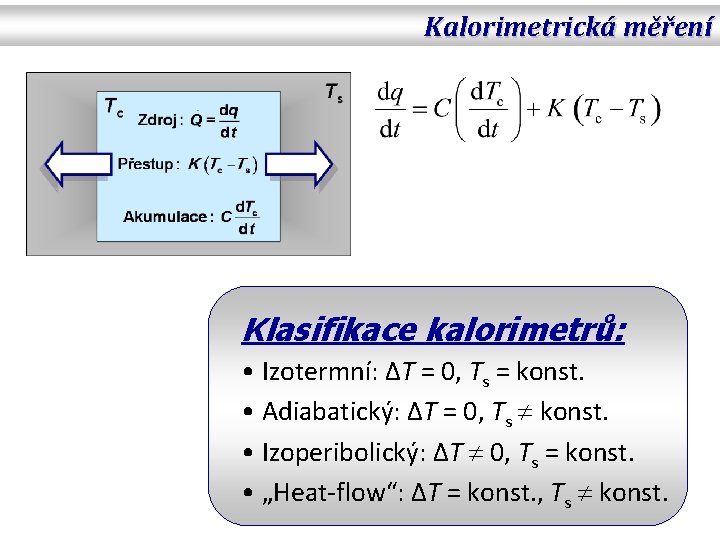
Kalorimetrická měření Klasifikace kalorimetrů: • Izotermní: ΔT = 0, Ts = konst. • Adiabatický: ΔT = 0, Ts konst. • Izoperibolický: ΔT 0, Ts = konst. • „Heat-flow“: ΔT = konst. , Ts konst.

Kalorimetrická měření Vlastnost Jak na to Tepelné kapacity Cpm → Sm = ∫(Cpm/T)d. T Tepelně pulzní kalorimetrie Adiabatická kalorimetrie (AC) Diferenční scanovací kalorimetrie (DSC) Relativní entalpie ΔTHm = Hm(T) – Hm(Tref) Vhazovací kalorimetrie (DROP) Entalpie fázových přeměn I. řádu Δtr. H, Δfus. H Diferenční scanovací kalorimetrie (DSC) Rozpouštěcí kalorimetrie Slučovací entalpie Δsl. H Reakční kalorimetrie • přímé slučování • jiná reakce (spalování, …) Rozpouštěcí kalorimetrie Směšovací entalpie Δmix. H Směšovací kalorimetrie Rozpouštěcí kalorimetrie Povrchová energie/entalpie γsurf Rozpouštěcí kalorimetrie http: //www. vscht. cz/ipl/osobni/leitner/prednasky/Chemrovnovah/FCHR_T 6. ppt

Tepelné kapacity Metoda Tepelně pulzní kalorimetrie Adiabatická kalorimetrie DSC Vhazovací kalorimetrie 10– 1 K 100 K 101 K 102 K 103 K

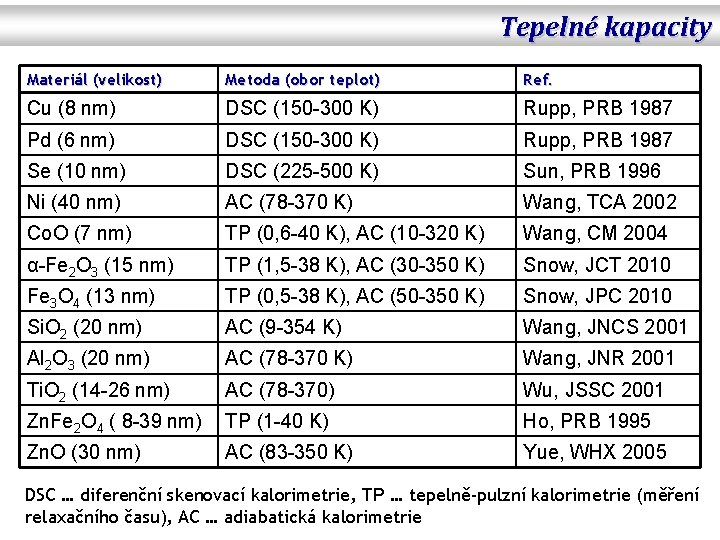
Tepelné kapacity Materiál (velikost) Metoda (obor teplot) Ref. Cu (8 nm) DSC (150 -300 K) Rupp, PRB 1987 Pd (6 nm) DSC (150 -300 K) Rupp, PRB 1987 Se (10 nm) DSC (225 -500 K) Sun, PRB 1996 Ni (40 nm) AC (78 -370 K) Wang, TCA 2002 Co. O (7 nm) TP (0, 6 -40 K), AC (10 -320 K) Wang, CM 2004 α-Fe 2 O 3 (15 nm) TP (1, 5 -38 K), AC (30 -350 K) Snow, JCT 2010 Fe 3 O 4 (13 nm) TP (0, 5 -38 K), AC (50 -350 K) Snow, JPC 2010 Si. O 2 (20 nm) AC (9 -354 K) Wang, JNCS 2001 Al 2 O 3 (20 nm) AC (78 -370 K) Wang, JNR 2001 Ti. O 2 (14 -26 nm) AC (78 -370) Wu, JSSC 2001 Zn. Fe 2 O 4 ( 8 -39 nm) TP (1 -40 K) Ho, PRB 1995 Zn. O (30 nm) AC (83 -350 K) Yue, WHX 2005 DSC … diferenční skenovací kalorimetrie, TP … tepelně-pulzní kalorimetrie (měření relaxačního času), AC … adiabatická kalorimetrie

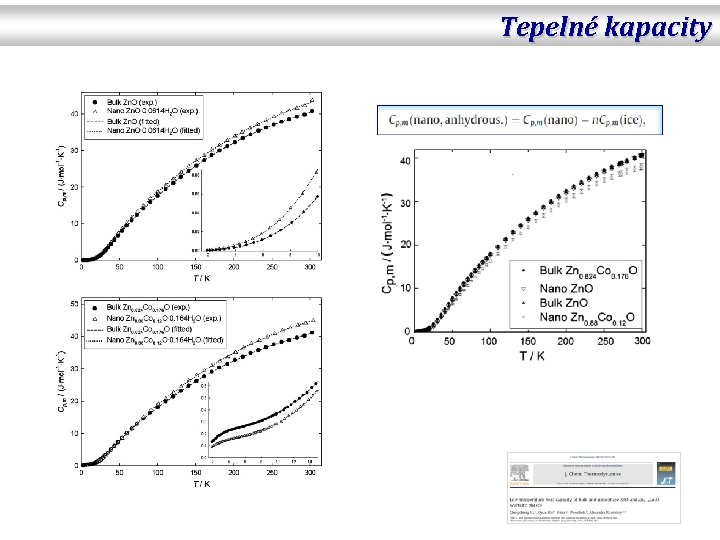
Tepelné kapacity

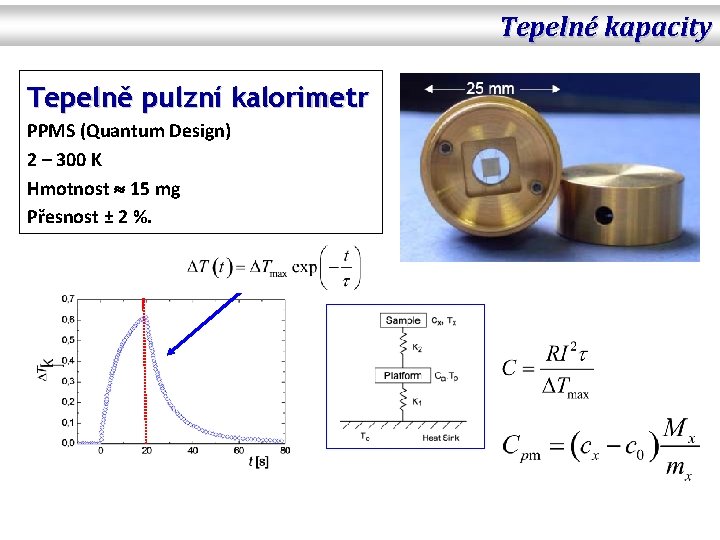
Tepelné kapacity Tepelně pulzní kalorimetr PPMS (Quantum Design) 2 – 300 K Hmotnost 15 mg Přesnost ± 2 %.

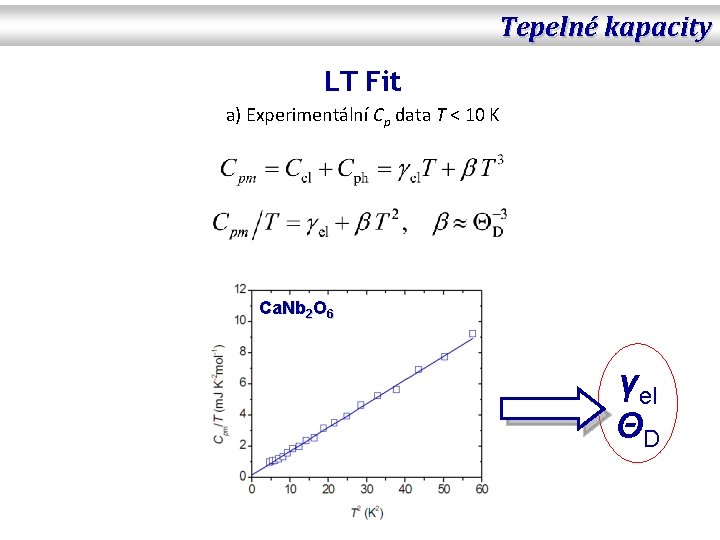
Tepelné kapacity LT Fit a) Experimentální Cp data T < 10 K Ca. Nb 2 O 6 γel ΘD

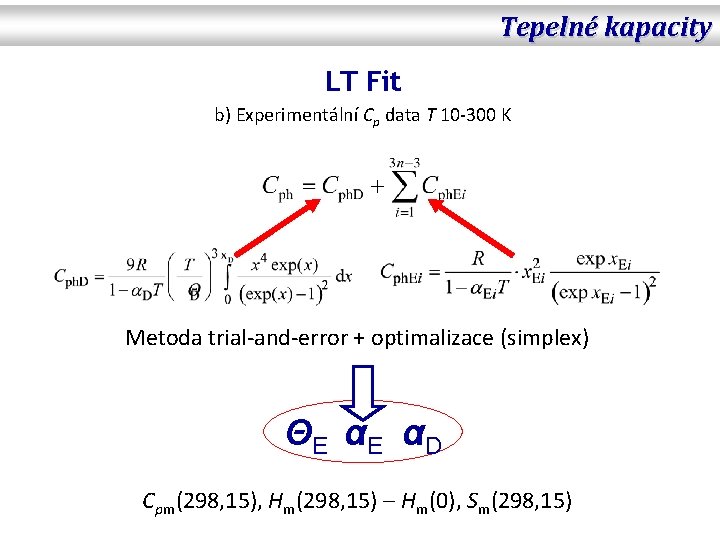
Tepelné kapacity LT Fit b) Experimentální Cp data T 10 -300 K Metoda trial-and-error + optimalizace (simplex) Θ E αE αD Cpm(298, 15), Hm(298, 15) Hm(0), Sm(298, 15)

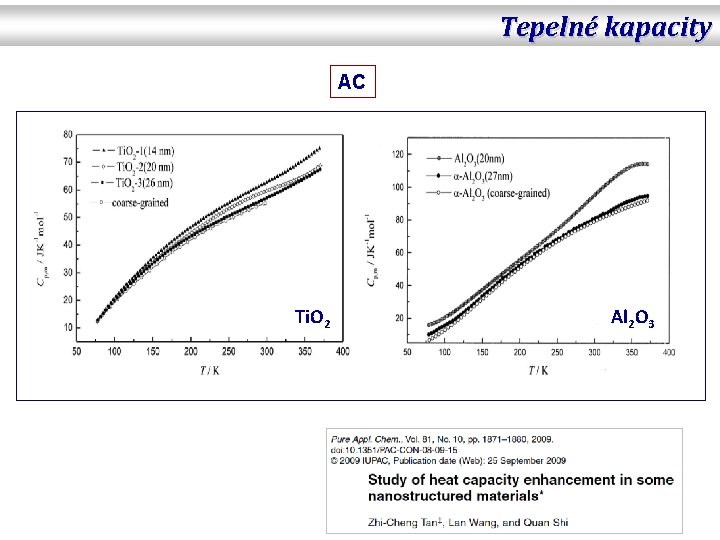
Tepelné kapacity AC Ti. O 2 Al 2 O 3

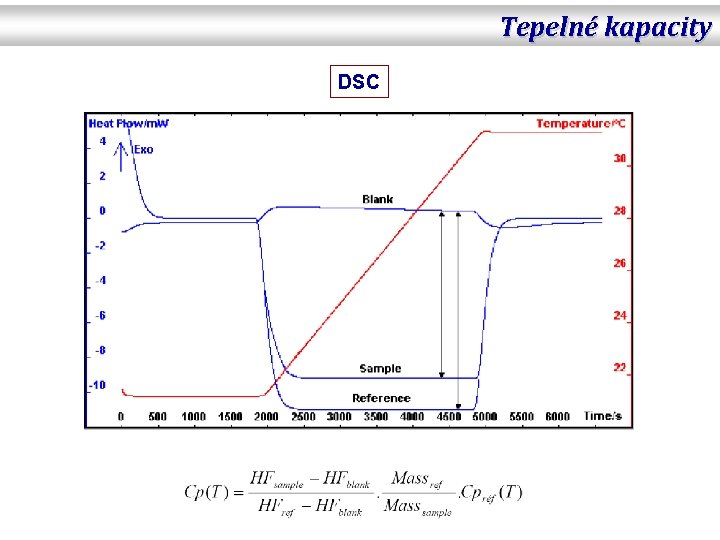
Tepelné kapacity DSC

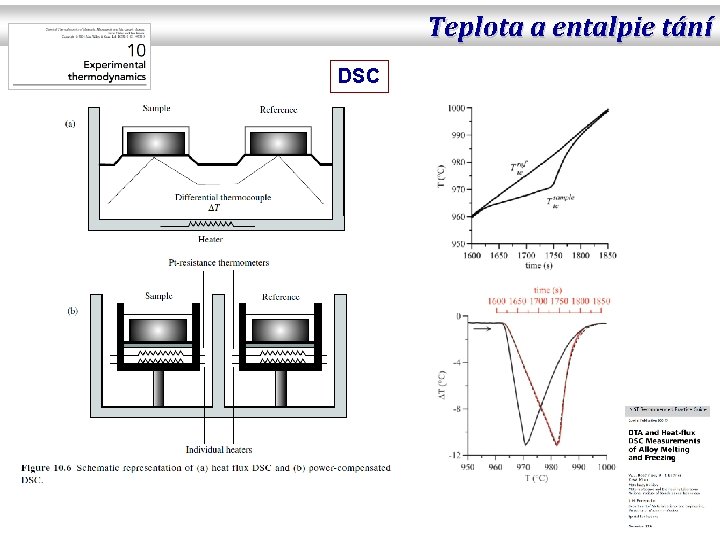
Teplota a entalpie tání DSC

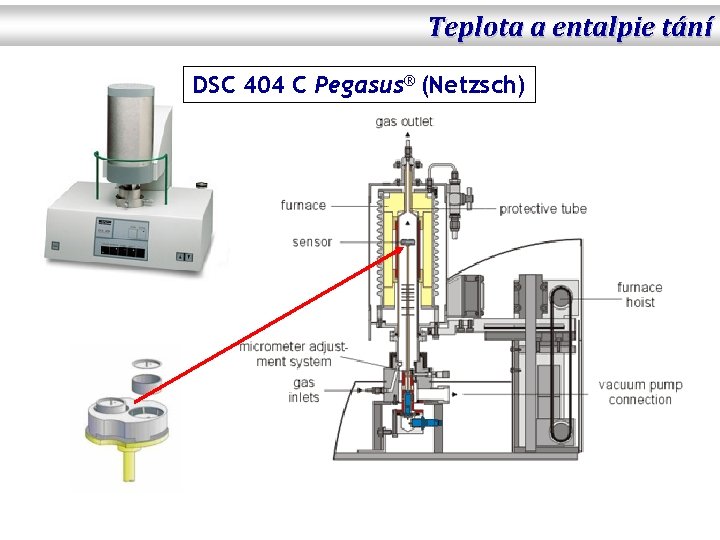
Teplota a entalpie tání DSC 404 C Pegasus® (Netzsch)

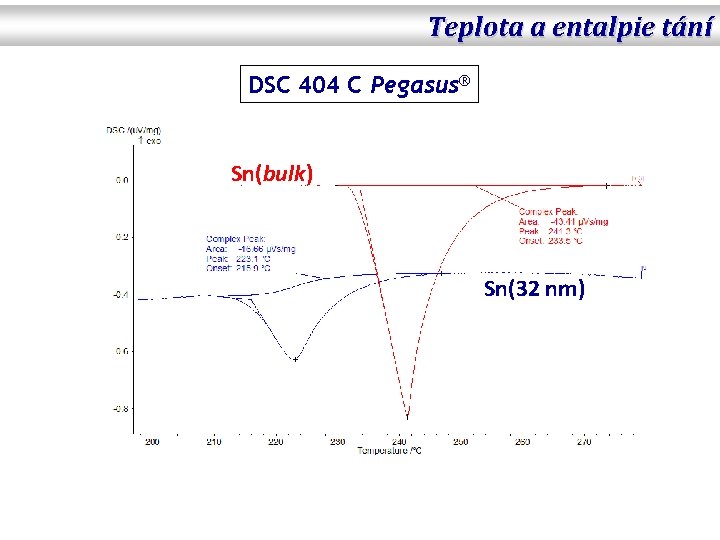
Teplota a entalpie tání DSC 404 C Pegasus® Sn(bulk) Sn(32 nm)

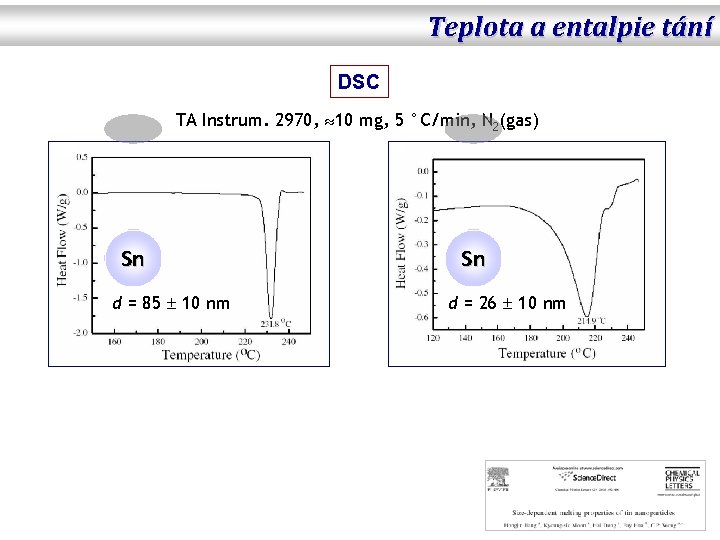
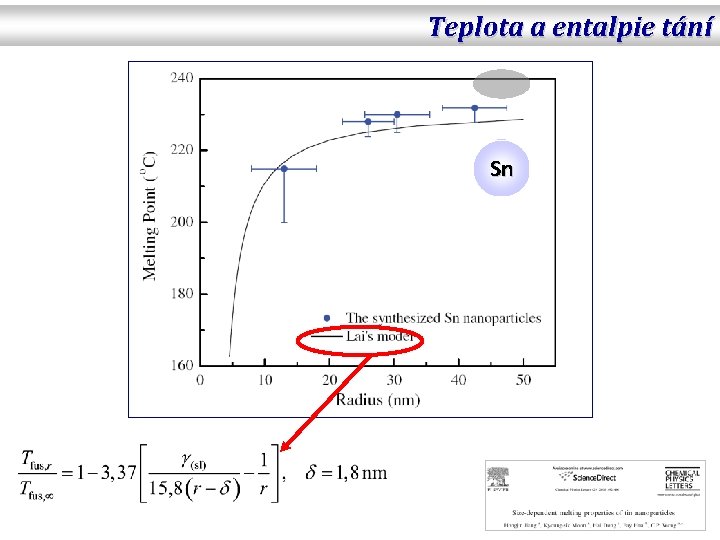
Teplota a entalpie tání DSC TA Instrum. 2970, 10 mg, 5 °C/min, N 2(gas) Sn d = 85 10 nm Sn d = 26 10 nm

Teplota a entalpie tání Sn

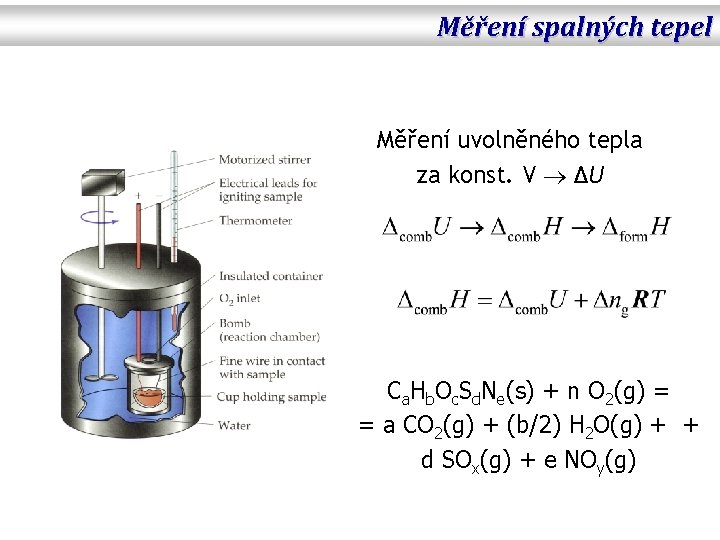
Měření spalných tepel Měření uvolněného tepla za konst. V ΔU Ca. Hb. Oc. Sd. Ne(s) + n O 2(g) = = a CO 2(g) + (b/2) H 2 O(g) + + d SOx(g) + e NOy(g)

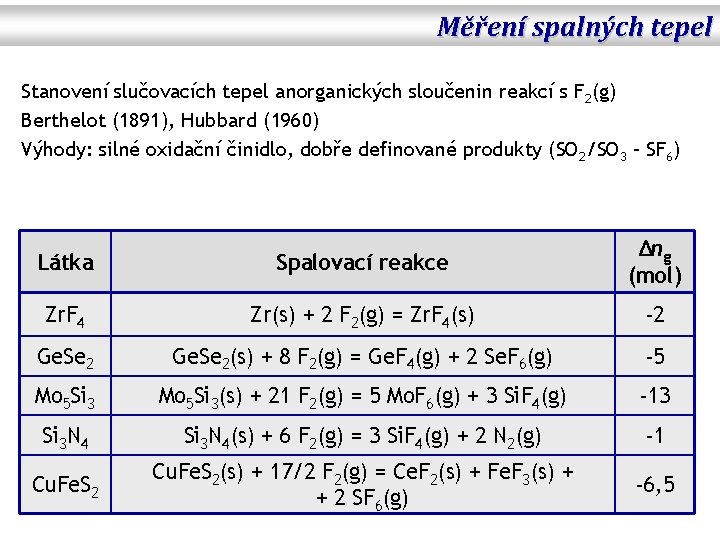
Měření spalných tepel Stanovení slučovacích tepel anorganických sloučenin reakcí s F 2(g) Berthelot (1891), Hubbard (1960) Výhody: silné oxidační činidlo, dobře definované produkty (SO 2/SO 3 – SF 6) Látka Spalovací reakce Δng (mol) Zr. F 4 Zr(s) + 2 F 2(g) = Zr. F 4(s) -2 Ge. Se 2(s) + 8 F 2(g) = Ge. F 4(g) + 2 Se. F 6(g) -5 Mo 5 Si 3(s) + 21 F 2(g) = 5 Mo. F 6(g) + 3 Si. F 4(g) -13 Si 3 N 4(s) + 6 F 2(g) = 3 Si. F 4(g) + 2 N 2(g) -1 Cu. Fe. S 2(s) + 17/2 F 2(g) = Ce. F 2(s) + Fe. F 3(s) + + 2 SF 6(g) -6, 5

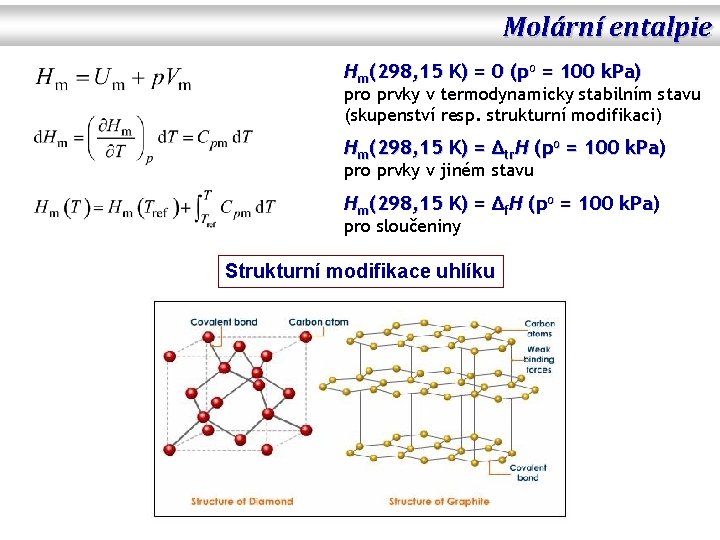
Molární entalpie Hm(298, 15 K) = 0 (po = 100 k. Pa) pro prvky v termodynamicky stabilním stavu (skupenství resp. strukturní modifikaci) Hm(298, 15 K) = Δtr. H (po = 100 k. Pa) pro prvky v jiném stavu Hm(298, 15 K) = Δf. H (po = 100 k. Pa) pro sloučeniny Strukturní modifikace uhlíku

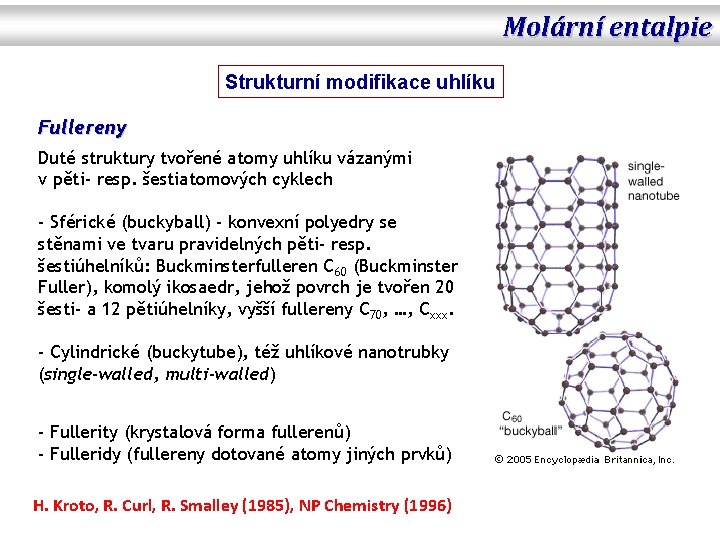
Molární entalpie Strukturní modifikace uhlíku Fullereny Duté struktury tvořené atomy uhlíku vázanými v pěti- resp. šestiatomových cyklech - Sférické (buckyball) - konvexní polyedry se stěnami ve tvaru pravidelných pěti- resp. šestiúhelníků: Buckminsterfulleren C 60 (Buckminster Fuller), komolý ikosaedr, jehož povrch je tvořen 20 šesti- a 12 pětiúhelníky, vyšší fullereny C 70, …, Cxxx. - Cylindrické (buckytube), též uhlíkové nanotrubky (single-walled, multi-walled) - Fullerity (krystalová forma fullerenů) - Fulleridy (fullereny dotované atomy jiných prvků) H. Kroto, R. Curl, R. Smalley (1985), NP Chemistry (1996)

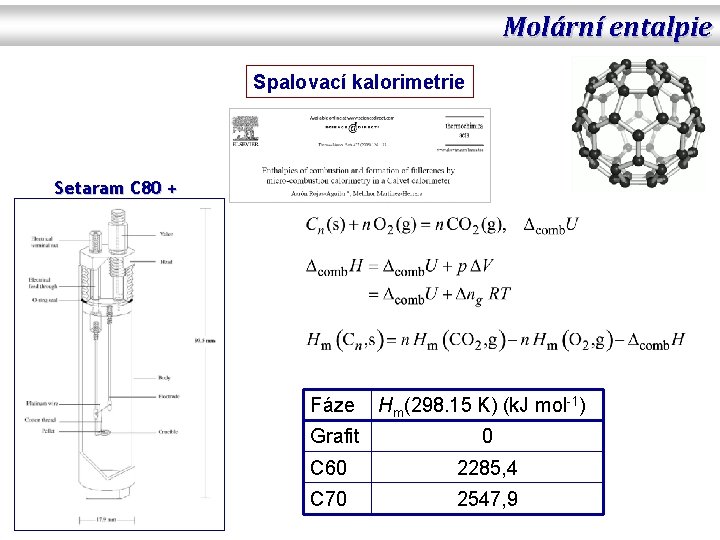
Molární entalpie Spalovací kalorimetrie Setaram C 80 + Fáze Hm(298. 15 K) (k. J mol-1) Grafit 0 C 60 2285, 4 C 70 2547, 9

Molární entalpie Stabilita různých foremuhlíku Fáze Grafit Hm(298. 15 K) (k. J at-1) 0 Diamant 2, 5 C 60 38, 1 C 70 36, 4

Měření rozpouštěcích tepel • Měří se tepelný efekt spojený s rozpuštěním studované látky ve vhodném rozpouštědle • Aplikací Hessova zákona se stanoví požadovaná termochemická veličina • Lze získat hodnoty Δtr. H, Δf. H, Δmix. H

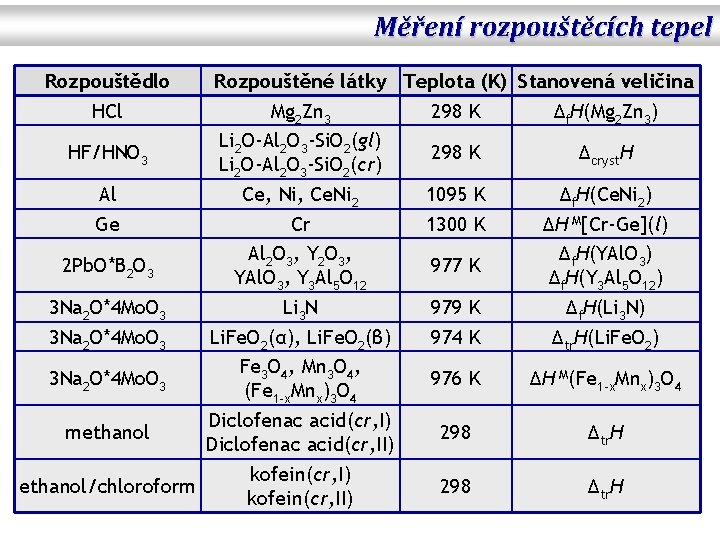
Měření rozpouštěcích tepel Rozpouštědlo HCl Rozpouštěné látky Teplota (K) Stanovená veličina Mg 2 Zn 3 298 K Δf. H(Mg 2 Zn 3) Li 2 O-Al 2 O 3 -Si. O 2(gl) HF/HNO 3 298 K Δcryst. H Li 2 O-Al 2 O 3 -Si. O 2(cr) Al Ce, Ni, Ce. Ni 2 1095 K Δf. H(Ce. Ni 2) Ge Cr 1300 K ΔH M[Cr-Ge](l) Al 2 O 3, Y 2 O 3, Δf. H(YAl. O 3) 2 Pb. O*B 2 O 3 977 K YAl. O 3, Y 3 Al 5 O 12 Δf. H(Y 3 Al 5 O 12) 3 Na 2 O*4 Mo. O 3 Li 3 N 979 K Δf. H(Li 3 N) 3 Na 2 O*4 Mo. O 3 Li. Fe. O 2(α), Li. Fe. O 2(β) 974 K Δtr. H(Li. Fe. O 2) Fe 3 O 4, Mn 3 O 4, 3 Na 2 O*4 Mo. O 3 976 K ΔH M(Fe 1–x. Mnx)3 O 4 Diclofenac acid(cr, I) methanol 298 Δtr. H Diclofenac acid(cr, II) kofein(cr, I) ethanol/chloroform 298 Δtr. H kofein(cr, II)

Povrchová energie Rozpouštěcí kalorimetrie Y 2 O 3 Kubická (patm) a monoklinická (HP) modifikace Rozpouštěcí kalorimetrie - Vzorky (cub) a (mon) o různém měrném povrchu - Rozpouštědlo 3 Na 2 O· 4 Mo. O 3 - Teplota 700 °C

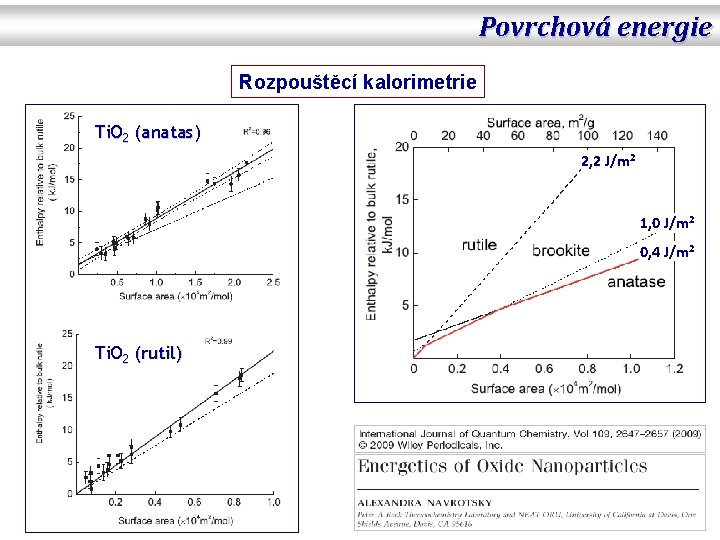
Povrchová energie Rozpouštěcí kalorimetrie Ti. O 2 (anatas) 2, 2 J/m 2 1, 0 J/m 2 0, 4 J/m 2 Ti. O 2 (rutil)

Povrchová energie Rozpouštěcí kalorimetrie –korekce adsorbované H 2 O • Vzorky oxidů o různém měrném povrchu (BET). • Stanovení množství adsorbované vody před měřením vážením (TG/FTIR). • Stanovení Hds v ox. taveninách 3 Na 2 O· 4 Mo. O 3 nebo 2 Pb. O·B 2 O 3 ( 700 °C). • Stanovení Hads. • Určení specifické povrchové entalpie hsurf γsurf z termochemického cyklu.

Povrchová energie Rozpouštěcí kalorimetrie A. Navrotsky et al. Science 2010; 330: 199 -201

Adsorpční teplo

Adsorpční teplo

Adsorpční teplo

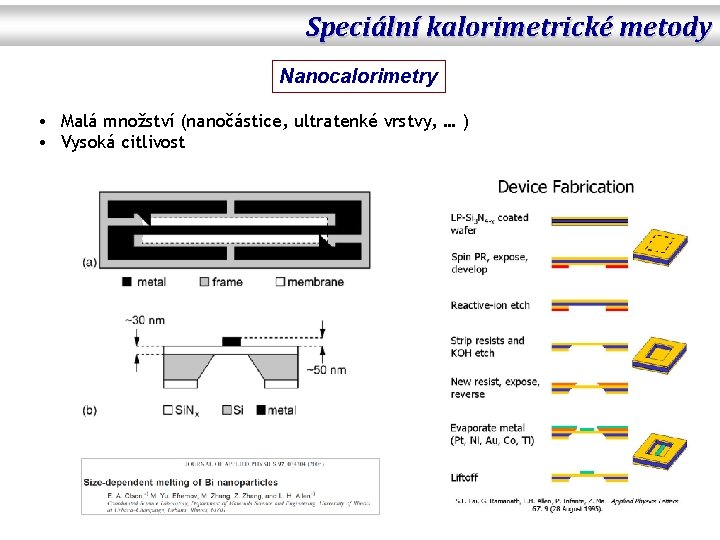
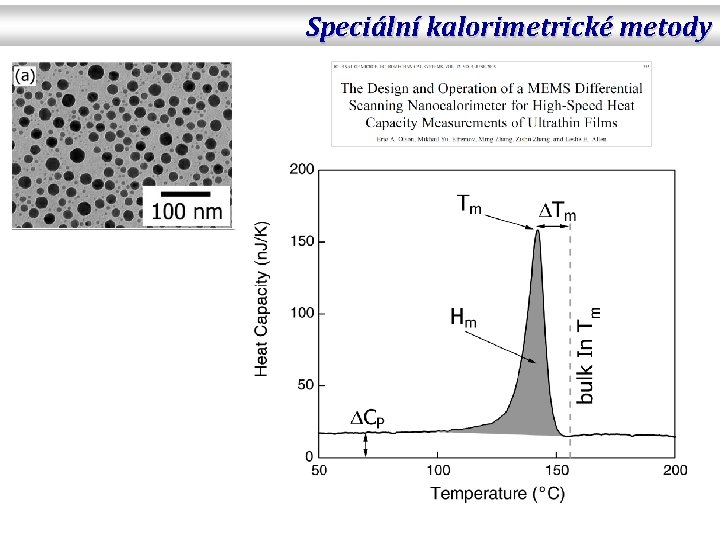
Speciální kalorimetrické metody Nanocalorimetry • Malá množství (nanočástice, ultratenké vrstvy, … ) • Vysoká citlivost

Speciální kalorimetrické metody

Závěr Kalorimetrie je velice účinný a užitečný nástroj při studiu nanomateriálů Další informace: http: //www. vscht. cz/ipl/materialy. html