MARKERS GENETICO MOLECOLARI nelle patologie oncoematologiche Nellambito delle

MARKERS GENETICO MOLECOLARI nelle patologie onco-ematologiche Nell’ambito delle patologie onco-ematologiche un marcatore genetico-molecolare è un’alterazione del genoma che causa l‘insorgenza del tumore e/o influenza il suo sviluppo (traslocazioni, delezioni cromosomiche o monosomie, mutazioni -> acquisite a livello somatico!) A essere interessati sono soprattutto proto-oncogeni, geni oncosoppressori, e geni per le catene pesanti delle immunoglobuline (linfociti B) o per il recettore TCR (linfociti T) Questi geni acquisiscono quindi proprietà carcinogenetiche

PATOGENESI MOLECOLARE DI LEUCEMIE E LINFOMI Gli eventi molecolari che generano queste patologie sono: 1) TRASLOCAZIONE BILANCIATA -> 1) aumento dell’espressione di una proteina “critica” per giustapposizione di un proto-oncogene o in generale di un gene master* vicino al gene delle immunoglobuline o del recettore TCR che contengono potenti enhancer cellulo-specifici; 2) fusione di sequenze di due geni diversi che portano all’espressione di oncoproteine chimeriche; 2) delezioni cromosomiche e monosomie (geni oncosoppressori); 3) mutazioni puntiformi (più rare rispetto ai tumori solidi). * = gene che controlla l’attività trascrizionale di altri geni funzionalmente importanti nello sviluppo delle cellule del sangue
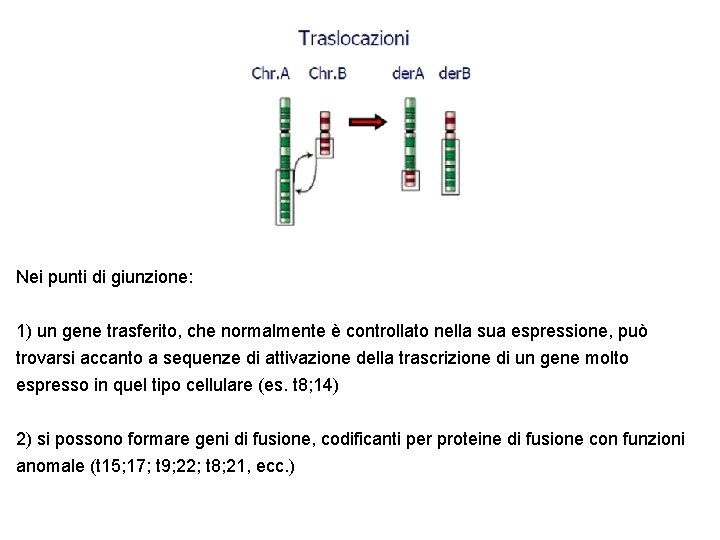
Nei punti di giunzione: 1) un gene trasferito, che normalmente è controllato nella sua espressione, può trovarsi accanto a sequenze di attivazione della trascrizione di un gene molto espresso in quel tipo cellulare (es. t 8; 14) 2) si possono formare geni di fusione, codificanti per proteine di fusione con funzioni anomale (t 15; 17; t 9; 22; t 8; 21, ecc. )
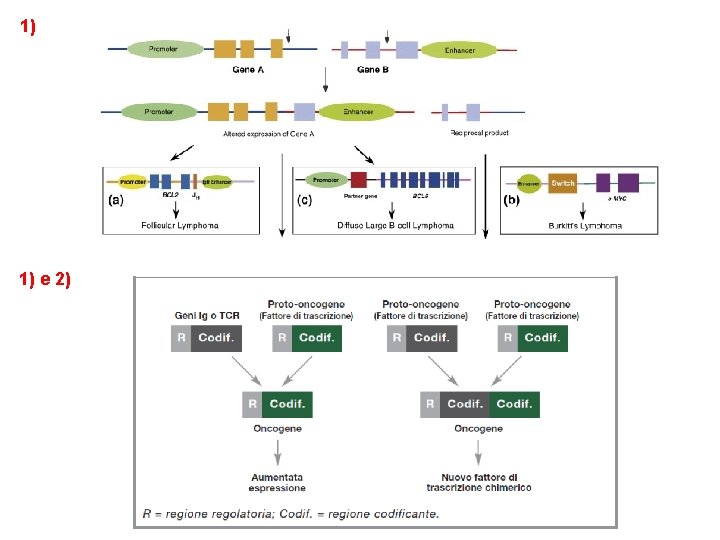
1) 1) e 2)
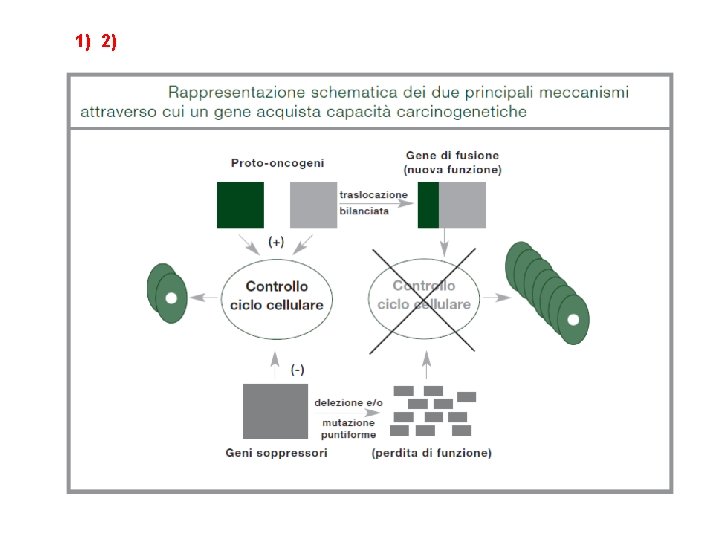
1) 2)

Alcune traslocazioni sono specifiche di una determinata leucemia o linfoma, e non si riscontrano nei soggetti sani (es. t(15; 17) della leucemia promielocitica acuta) Altre traslocazioni sono molto frequenti in particolari patologie (come la t(14; 18) nel linfoma follicolare) ma sono presenti anche in altri linfomi e nei soggetti sani sebbene in numero di copie molto basso DELEZIONI CROMOSOMICHE E MONOSOMIE Alcun tipi di delezioni del 5 q Delezione del cromosoma 17 o del 13 Monosomia 7 e delezione 7 q Perdita di geni oncosoppressori

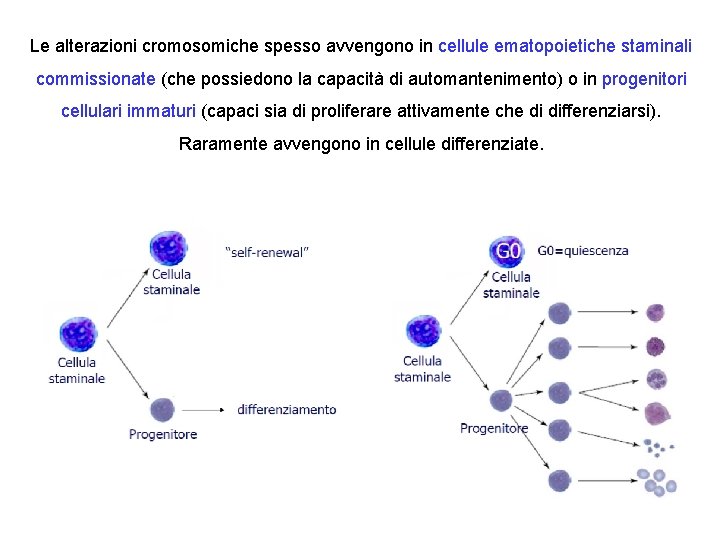
Le alterazioni cromosomiche spesso avvengono in cellule ematopoietiche staminali commissionate (che possiedono la capacità di automantenimento) o in progenitori cellulari immaturi (capaci sia di proliferare attivamente che di differenziarsi). Raramente avvengono in cellule differenziate.
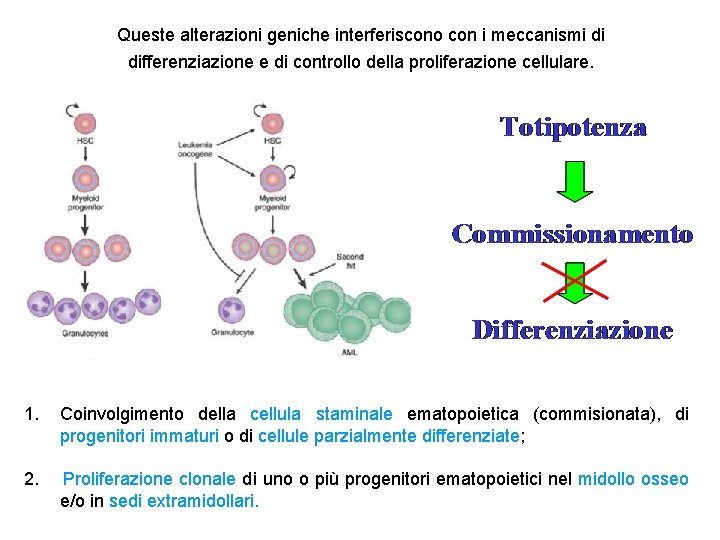
Queste alterazioni geniche interferiscono con i meccanismi di differenziazione e di controllo della proliferazione cellulare. 1. Coinvolgimento della cellula staminale ematopoietica (commisionata), di progenitori immaturi o di cellule parzialmente differenziate; 2. Proliferazione clonale di uno o più progenitori ematopoietici nel midollo osseo e/o in sedi extramidollari.
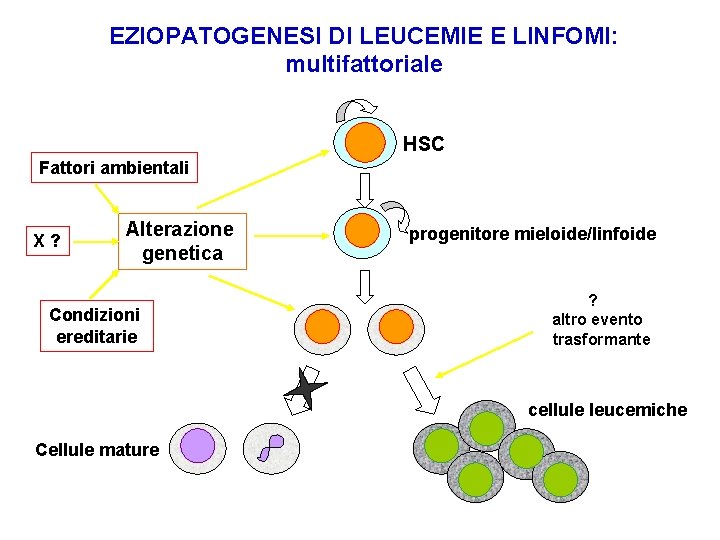
EZIOPATOGENESI DI LEUCEMIE E LINFOMI: multifattoriale HSC Fattori ambientali X? Alterazione genetica Condizioni ereditarie progenitore mieloide/linfoide ? altro evento trasformante cellule leucemiche Cellule mature
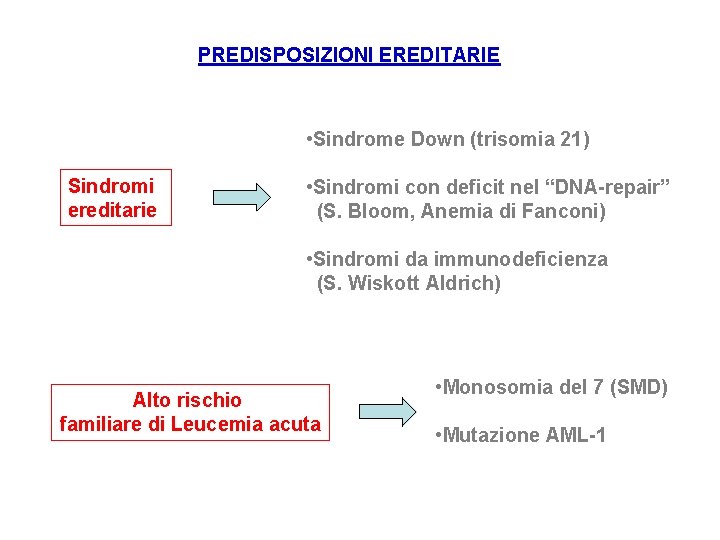
PREDISPOSIZIONI EREDITARIE • Sindrome Down (trisomia 21) Sindromi ereditarie • Sindromi con deficit nel “DNA-repair” (S. Bloom, Anemia di Fanconi) • Sindromi da immunodeficienza (S. Wiskott Aldrich) Alto rischio familiare di Leucemia acuta • Monosomia del 7 (SMD) • Mutazione AML-1
FATTORI AMBIENTALI Agenti fisici Agenti chimici Agenti virali • Radiazionizzanti • Sorgenti elettromagnetiche • Benzene (sigarette, industrie inquinamento atmosferico) • Altri composti aromatici • Ossido di etilene (x prodotti petrolchimici, sterilizzante) • Fenossi-erbicidi • Uretano, nitrosamine (sigarette) • Chemioterapia (es. alchilanti) • HTLV-1 (retrovirus oncogeni) • EBV

METOLOGIE DIAGNOSTICHE NELLE PATOLOGIE ONCO-EMATOLOGICHE Una diagnosi precisa richiede un approccio multiparametrico!

Leucemie e Linfomi possono essere diagnosticati e differenziati sulla base di quattro tipi di analisi: 1. Sintomi clinici 2. Analisi morfologia cellulare e istologia 4. Analisi molecolari e genetiche 3. Immunofenotipizzazione


Sensibilità dei vari metodi diagnostici u Analisi morfologica e istologica u Immunoistochimica u Citofluorimetria u Citogenetica u Analisi molecolari (FISH, PCR e RT-PCR, q. RT-PCR, Southern blot, microarray) meno sensibile più sensibile


Analisi molecolare Le tecniche molecolari sono utilizzate per: – La ricerca di specifiche traslocazioni cromosomiche sono alla base della maggior parte dei tumori del sangue (Southern Blot, PCR, RT-PCR, FISH*) – L’analisi di popolazioni monoclonali linfocitarie utilizzando come bersagli molecolari i geni delle immunoglobuline e/o i geni del recettore delle cellule T (TCR) (Southern Blot, PCR). • *=fluorescence in situ hybridization.


Diagnosi molecolare delle linfoproliferazioni maligne: ricerca di una popolazione monoclonale I tumori linfoidi (linfomi e leucemie linfoidi) sono un gruppo eterogeneo di patologie che si originano dalla trasformazione neoplastica di linfociti B o T a vari gradi di maturazione METODI DIAGNOSTICI UTILIZZATI: -Analisi isto-morfologica e cito-morfologica; -Analisi immunoistochimica; -Analisi citofluorimetrica; -Test molecolari. Un test molecolare è utile per confermare o migliorare una diagnosi. Per i tumori linfoidi consiste nella ricerca di una popolazione monoclonale indice di proliferazione maligna Vengono analizzati i geni delle immunoglobuline dei linfociti B e i geni del recettore TCR dei linfociti T che subiscono riarrangiamenti durante la maturazione cellulare
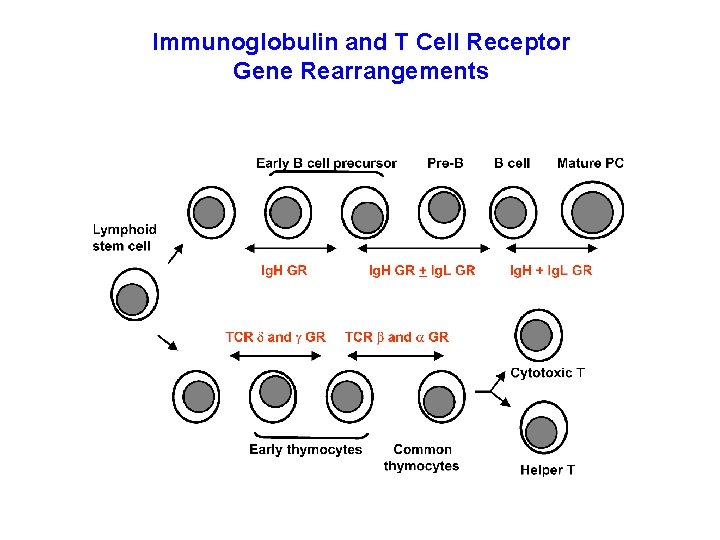
Immunoglobulin and T Cell Receptor Gene Rearrangements
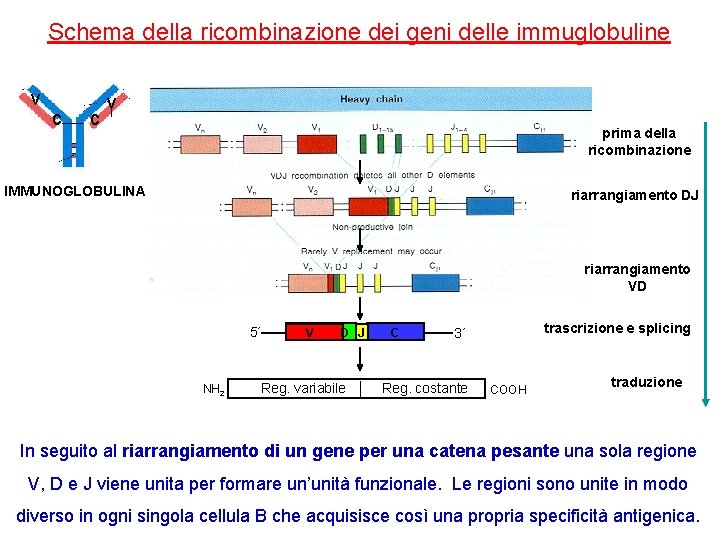
Schema della ricombinazione dei geni delle immuglobuline v c c v prima della ricombinazione IMMUNOGLOBULINA riarrangiamento DJ riarrangiamento VD 5´ NH 2 V V D J Reg. variabile C trascrizione e splicing 3´ Reg. costante COOH traduzione In seguito al riarrangiamento di un gene per una catena pesante una sola regione V, D e J viene unita per formare un’unità funzionale. Le regioni sono unite in modo diverso in ogni singola cellula B che acquisisce così una propria specificità antigenica.
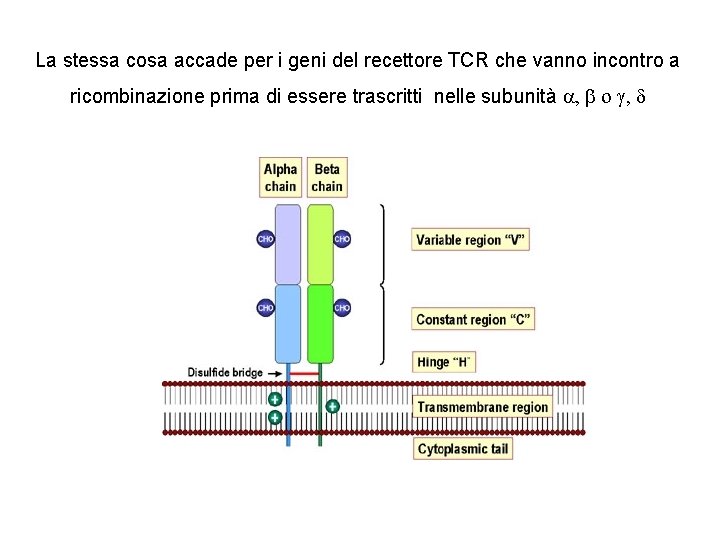
La stessa cosa accade per i geni del recettore TCR che vanno incontro a ricombinazione prima di essere trascritti nelle subunità a, b o g, d
QUINDI: Condizione normale: Il riarrangiamento è casuale e la popolazione linfocitaria è policlonale Condizione patologica: Il riarrangiamento è identico in una parte della popolazione linfocitaria (clone), segno che si è originata da una stessa cellula (tumorale) I geni delle immunoglobuline e del recettore TCR durante lo sviluppo dei linfociti riarrangiano in maniera diversa in ogni singola cellula. Quando ci sono diverse cellule i cui geni presentano lo stesso riarrangiamento si identifica una popolazione linfocitaria monoclonale. Ciò è indice di crescita tumorale.
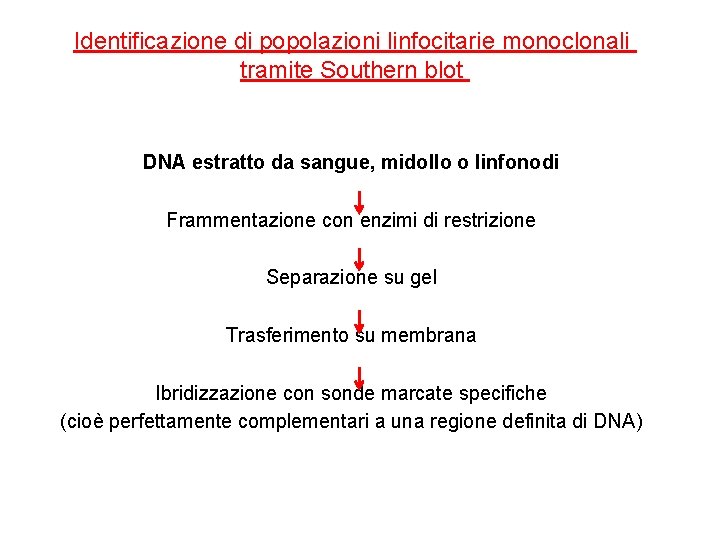
Identificazione di popolazioni linfocitarie monoclonali tramite Southern blot DNA estratto da sangue, midollo o linfonodi Frammentazione con enzimi di restrizione Separazione su gel Trasferimento su membrana Ibridizzazione con sonde marcate specifiche (cioè perfettamente complementari a una regione definita di DNA)

Analisi Southern blot per la determinazione del riarrangiamento dei geni delle Ig • Metodologia: analisi con Southern-blot dei segmenti di DNA che codificano per le regioni variabili delle immunoglobuline con sonde che riconoscono regioni conservate presenti in tutti i geni riarrangiati (segmenti J) • Può rilevare una popolazione clonale che rappresenti 5 -10% della popolazione totale di cellule • L’analisi può essere applicata anche allo studio dei linfomi dei linfociti T in cui i geni del recettore delle cellule T subiscono un processo di riarrangiamento somatico simile ai geni delle immunoglobuline.
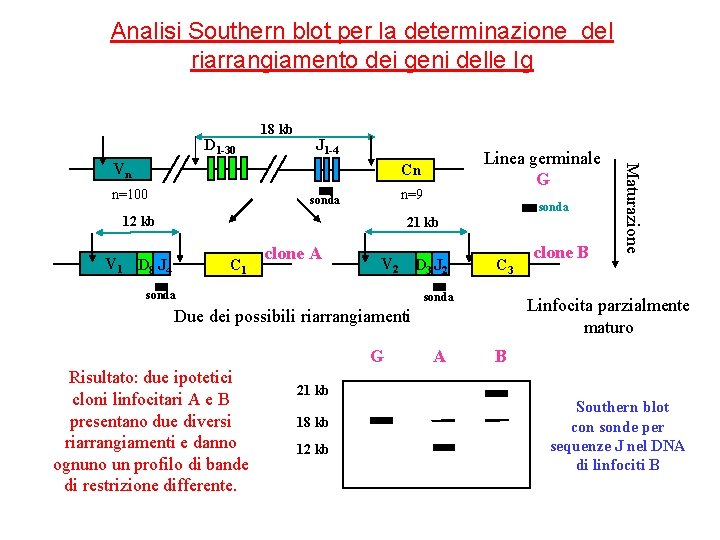
Analisi Southern blot per la determinazione del riarrangiamento dei geni delle Ig D 1 -30 18 kb J 1 -4 Linea germinale G Cn n=100 n=9 sonda 12 kb = sonda 21 kb V 1 D 8 J 4 C 1 clone A V 2 sonda D 3 J 2 C 3 sonda Linfocita parzialmente maturo Due dei possibili riarrangiamenti G Risultato: due ipotetici cloni linfocitari A e B presentano due diversi riarrangiamenti e danno ognuno un profilo di bande di restrizione differente. A clone B Maturazione Vn 5´ B 21 kb 18 kb 12 kb Southern blot con sonde per sequenze J nel DNA di linfociti B
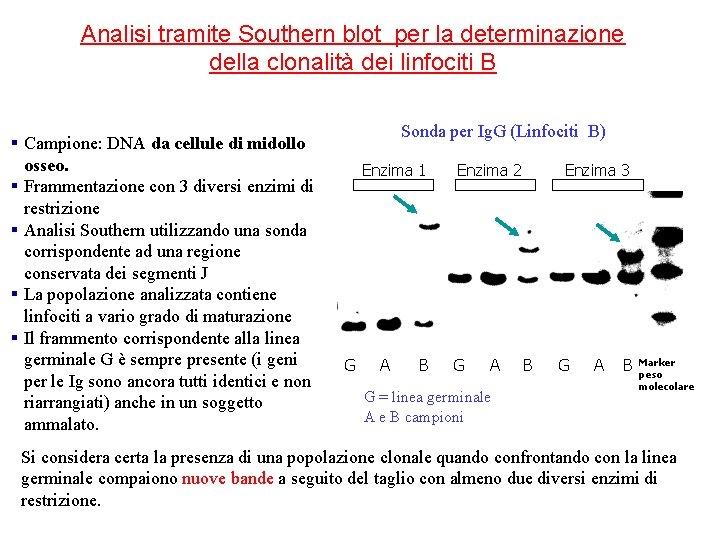
Analisi tramite Southern blot per la determinazione della clonalità dei linfociti B § Campione: DNA da cellule di midollo osseo. § Frammentazione con 3 diversi enzimi di restrizione § Analisi Southern utilizzando una sonda corrispondente ad una regione conservata dei segmenti J § La popolazione analizzata contiene linfociti a vario grado di maturazione § Il frammento corrispondente alla linea germinale G è sempre presente (i geni per le Ig sono ancora tutti identici e non riarrangiati) anche in un soggetto ammalato. Sonda per Ig. G (Linfociti B) Enzima 1 G A B Enzima 2 G A G = linea germinale A e B campioni Enzima 3 B G A B Marker peso molecolare Si considera certa la presenza di una popolazione clonale quando confrontando con la linea germinale compaiono nuove bande a seguito del taglio con almeno due diversi enzimi di restrizione.
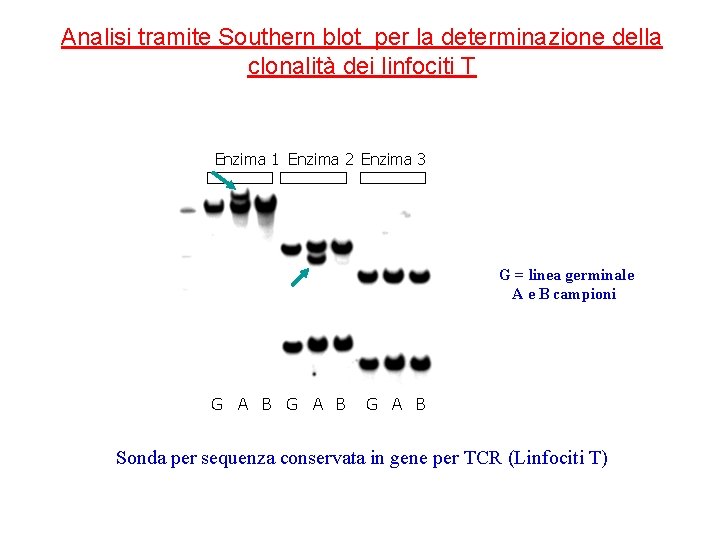
Analisi tramite Southern blot per la determinazione della clonalità dei linfociti T Enzima 1 Enzima 2 Enzima 3 G = linea germinale A e B campioni G A B Sonda per sequenza conservata in gene per TCR (Linfociti T)

Utilizzo della PCR per la valutazione della clonalità cellulare § La PCR è un metodo alternativo per valutare la presenza di una popolazione clonale di cellule B o T § Analogamente al Southern blot permette di analizzare i segmenti di DNA che codificano per le regioni variabili delle immunoglobuline e del recettore delle cellule T Si utilizzano inneschi specifici per corte regioni conservate presenti in tutti i diversi segmenti V e J. Può rilevare una popolazione clonale che rappresenti lo 0, 1% della popolazione.
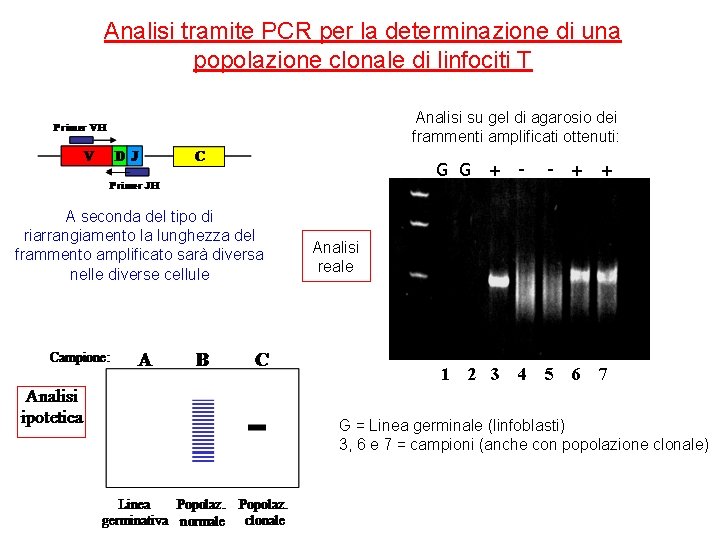
Analisi tramite PCR per la determinazione di una popolazione clonale di linfociti T Analisi su gel di agarosio dei frammenti amplificati ottenuti: A seconda del tipo di riarrangiamento la lunghezza del frammento amplificato sarà diversa nelle diverse cellule G G + - - + + 1 5 Analisi reale 2 3 4 6 7 G = Linea germinale (linfoblasti) 3, 6 e 7 = campioni (anche con popolazione clonale)
mg mg
Perché un linfocita normale diventa neoplastico? Intervengono alterazioni geniche, soprattutto traslocazioni cromosomiche: -vengono attivati o iperespressi geni codificanti per fattori implicati nel controllo dello sviluppo e fattori di trascrizione che influenzano importanti pathway di segnale; -vengono inattivati geni chiave per la differenziazione cellulare o l’apoptosi. Trasformazione neoplastica di un solo linfocita T/B (alterazione genica) Il linfocita vive più a lungo, non si differenzia e prolifera velocemente (no apoptosi) Un elevato numero di linfociti originati dallo stesso precursore si accumula nel sangue o in organi linfatici (popolazione monoclonale)
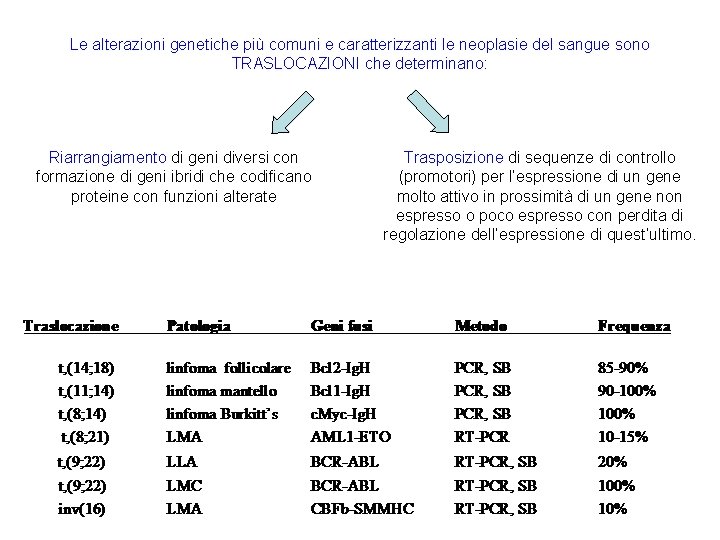
Le alterazioni genetiche più comuni e caratterizzanti le neoplasie del sangue sono TRASLOCAZIONI che determinano: Riarrangiamento di geni diversi con formazione di geni ibridi che codificano proteine con funzioni alterate Trasposizione di sequenze di controllo (promotori) per l’espressione di un gene molto attivo in prossimità di un gene non espresso o poco espresso con perdita di regolazione dell’espressione di quest’ultimo.

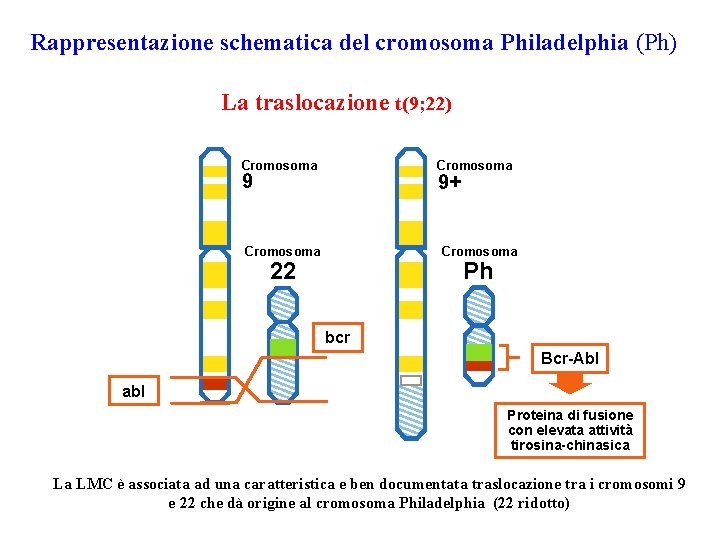
Rappresentazione schematica del cromosoma Philadelphia (Ph) La traslocazione t(9; 22) Cromosoma 9 9+ Cromosoma 22 Ph bcr Bcr-Abl abl Proteina di fusione con elevata attività tirosina-chinasica La LMC è associata ad una caratteristica e ben documentata traslocazione tra i cromosomi 9 e 22 che dà origine al cromosoma Philadelphia (22 ridotto)

La traslocazione coinvolge il breakpoint cluster region gene (BCR) sul cromosoma 22 e il protooncogene di Abelson (ABL) sul cromosoma 9. I punti di rottura sul cromosoma 22 possono essere diversi: -nella major breakpoint cluster region di BCR (M-bcr) -> BCR-ABL avrà un PM di 210 k. Da; (90% delle LMC) -nella minor breakpoint cluster region di BCR (m-bcr) -> BCR-ABL avrà un PM di 190 k. Da; (70% delle leucemie linfoblastiche acute adulti e 90% bimbi) -nella micro breakpoint cluster region di BCR (m-bcr) -> BCR-ABL avrà un PM di 230 k. Da; (leucemia neutrofila cronica).




TEST PER LA DIAGNOSI MOLECOLARE DI ALTERAZIONI GENOMICHE RILEVANTI - PCR, RT-PCR e real-time PCR - Southern blot - Ibridazione “in situ” = FISH (cariotipo) - Citofluorimetria (immunofenotipo)
- Slides: 41