KONSEP DASAR ILMU KIMIA ORGANIK MUNAWAR RAHARJA S



















- Slides: 25

KONSEP DASAR ILMU KIMIA ORGANIK MUNAWAR RAHARJA, S. Si POLITEKNIK KESEHATAN BANJARMASIN JURUSAN KESEHATAN LINGKUNGAN BANJARBARU

Kompetensi Dasar: l Pada Akhir Perkuliahan Mhs memahami konsep dasar Ilmu Kimia Organik. dan hub. nya dengan upaya kesehatan

Pendahuluan n Sampai tahun 1928 KIMIA ORGANIK ialah ilmu yang mempelajari senyawa yang dihasilkan oleh makhluk hidup (manusia, hewan, tumbuhan, dan mikroorganisme). n Tahun 1928, Friedrich Wohler dan Kolbe dapat membuat senyawa organik dari senyawa anorganik. n Sekarang KIMIA ORGANIK adalah ilmu yang mempelajari tentang susunan atom carbon dan ikatannya yang sangat banyak macam dan jumlahnya. n Senyawa organik tersusun dari unsur : C, H, O, N, S, P dan halida. Sumber senyawa organik : tumbuhan, hewan, mikroorganisme dan hasil tambang. n

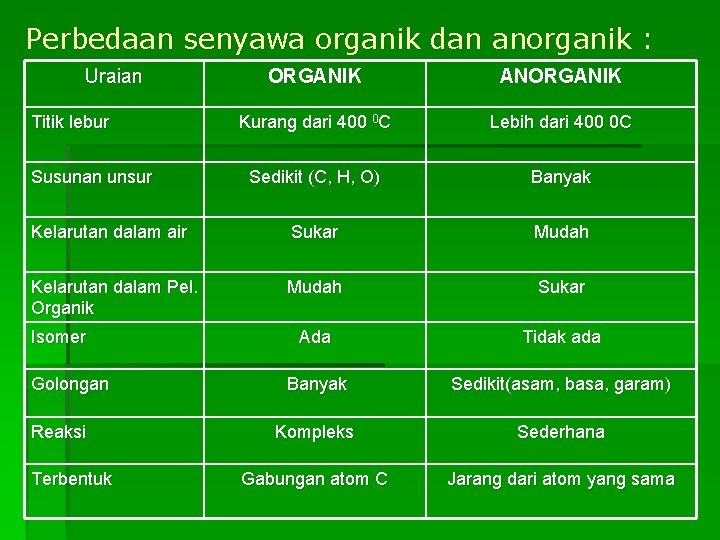
Perbedaan senyawa organik dan anorganik : Uraian ORGANIK ANORGANIK Kurang dari 400 0 C Lebih dari 400 0 C Sedikit (C, H, O) Banyak Kelarutan dalam air Sukar Mudah Kelarutan dalam Pel. Organik Mudah Sukar Ada Tidak ada Banyak Sedikit(asam, basa, garam) Kompleks Sederhana Gabungan atom C Jarang dari atom yang sama Titik lebur Susunan unsur Isomer Golongan Reaksi Terbentuk

Kegunaan Senyawa Organik Ø Ø Bahan Pangan (pengawet, karbohidrat, protein dll) Bahan Sandang (tekstil, zat warna, dll) Bahan bakar (minyak tanah, solar, dll) Bahan industri (plastik/PVC, bahan pembuat cat, tinta, obat-obatan, sebagai pelarut)

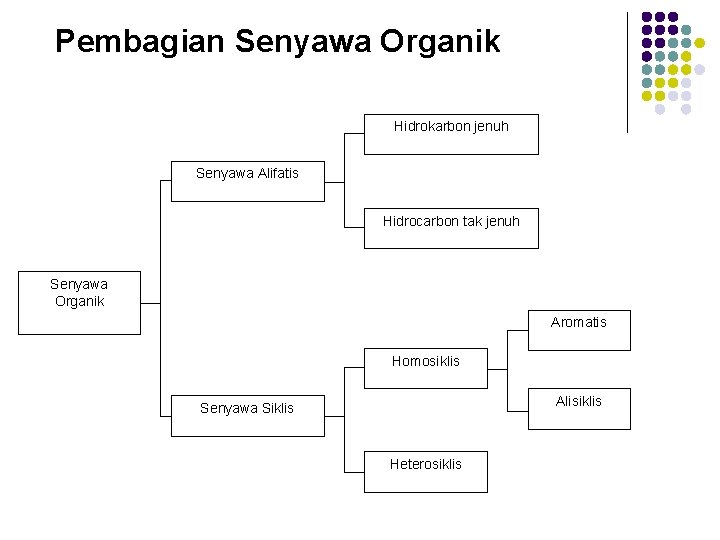
Pembagian Senyawa Organik Hidrokarbon jenuh Senyawa Alifatis Hidrocarbon tak jenuh Senyawa Organik Aromatis Homosiklis Alisiklis Senyawa Siklis Heterosiklis

SENYAWA ALIFATIS l l Terdiri atas rantai carbon ikatan terbuka/rantai carbon lurus. Disebut Hidrokarbon : mengandung unsur C dan H Terdiri dari : 1. Hidrokabon jenuh 2. Hidrokarbon tak jenuh Alkana (Cn. H 2 n+2) Alkena (Cn. H 2 n) Alkuna (Cn. H 2 n-2)

ALKANA l l l Struktur ALKANA : Cn. H 2 n+2 Hidrokarbon jenuh Disebut juga golongan parafin C 1 – C 4 : pada t dan p nomal adalah gas C 4 – C 17 : pada t dan p normal adalah cair > C 18 : pada t dan p normal adalah padat Titik didih makin tinggi : terhadap penambahan unsur C Jumlah atom C sama : yang bercabang mempunyai TD rendah Kelarutan : mudah larut dalam pelarut non polar BJ naik dengan penambahan jumlah unsur C Sumber utama gas alam dan petrolium

l PEMBUATAN ALKANA : 1. Hidrogenasi senyawa Alkena 2. Reduksi Alkil Halida 3. Reduksi metal dan asam l PENGGUNAAN ALKANA : l l l Metana : zat bakar, sintesis, dan carbon black (tinta, cat, semir, ban) Propana, Butana, Isobutana : zat bakar LPG (Liquified Petrolium Gases) Pentana, Heksana, Heptana : sebagai pelarut pada sintesis zat

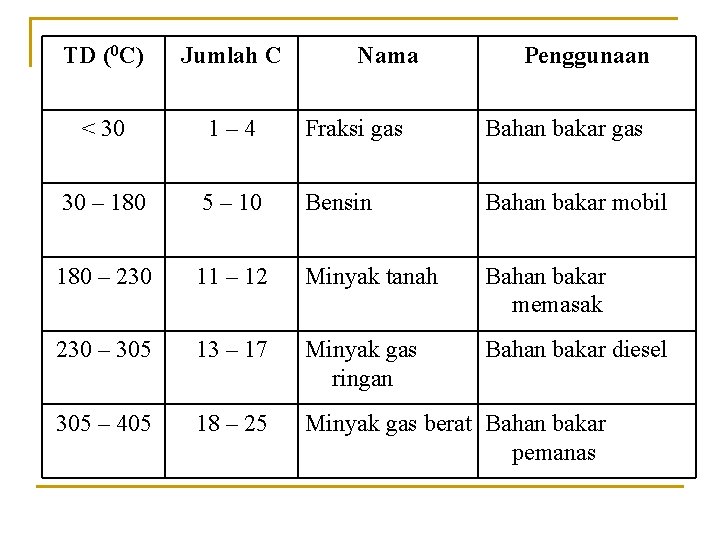
TD (0 C) Jumlah C Nama Penggunaan < 30 1– 4 Fraksi gas Bahan bakar gas 30 – 180 5 – 10 Bensin Bahan bakar mobil 180 – 230 11 – 12 Minyak tanah Bahan bakar memasak 230 – 305 13 – 17 Minyak gas ringan Bahan bakar diesel 305 – 405 18 – 25 Minyak gas berat Bahan bakar pemanas

ALKENA n n n STRUKTUR ALKENA : Cn. H 2 n Hidrokarbon tak jenuh ikatan rangkap dua Alkena = olefin (pembentuk minyak) Sifat fisiologis lebih aktif (sebagai obat tidur) : 2 -metil-2 -butena Sifat sama dengan Alkana, tapi lebih reaktif

n PEMBUATAN ALKENA : n n Dehidrohalogenasi alkil halida Dehidrasi alkohol Dehalogenasi dihalida Reduksi alkuna

Contoh : ETENA = ETILENA = CH 2 l Sifat-sifat : gas tak berwarna, dapat dibakar, bau yang khas, eksplosif dalam udara (pada konsentrasi 3 – 34%) l Terdapat dalam gas batu bara biasa pada proses “cracking” l Pembuatan : pengawahidratan etanaol PENGGUNAAN ETENA : § § § Dapat digunakan sebagai obat bius (dicampur dengan O 2) Untuk memasakkan buah-buahan Sintesis zat lain (gas alam, minyak bumi, etanol)

ALKUNA o o STRUKTUR ALKUNA : Cn. H 2 n-2 CH (etuna/asetilen) Hidrokarbon tak jenuh mempunyai ikatan rangkap tiga Sifat-sifatnya menyerupai alkena, tetapi lebih reaktif o o o ETUNA = ASETILEN CH Pembuatan : Ca. C 2 + H 2 O C 2 H 2 + Ca(OH)2 Sifat-sifat : Suatu senyawaan endoterm, maka mudah meledak Suatu gas, tak berwarna, baunya khas

Penggunaan etuna : o Pada pengelasan : dibakar dengan O 2 memberi suhu yang tinggi ( 30000 C), dipakai untuk mengelas besi dan baja o Untuk penerangan o Untuk sintesis senyawa lain PEMBUATAN ALKUNA o Dehidrohalogenasi alkil halida o Reaksi metal asetilida dengan alkil halida primer

SENYAWA AROMATIK l Permulaan abad ke-19 ditemukan senyawa-senyawa organik yang mempunyai bau (aroma) yang karakteristik yang berasal dari tumbuh-tumbuhan (damar benzoin, cumarin, asam sinamat dll) l BENZEN = C 6 H 6 ¡ Senyawa aromatis yang paling sederhana ¡ Berasal dari batu bara dan minyak bumi ¡ Sifat fisika : cairan, td. 800 C, tak berwarna, tak larut dalam air, larut dalam kebanyakan pelarut organik, mudah terbakar dengan nyala yang berjelaga dan berwarna (karena kadar C tinggi) ¡ Penggunaan Benzen : Dahulu sebagai bahan bakar motor Pelarut untuk banyak zat

ALKIL HALIDA l Senyawa alkil halida merupakan senyawa hidrokarbon baik jenuh maupun tak jenuh yang satu unsur H-nya atau lebih digantikan oleh unsur halogen (X = Br, Cl, I) l Struktur Alkil Halida : R-X (X = Br, Cl, I) l PENGGUNAAN ALKIL HALIDA : ¡ Kloroform (CHCl 3) : pelarut untuk lemak, obat bius (dibubuhi etanol, disimpan dalam botol coklat, diisi sampai penuh). ¡ Tetraklorometana = karbontetraklorida (CCl 4) : pelarut untuk lemak, alat pemadam kebakaran (pyrene, TD rendah 770 C, uapnya berat. ¡ Freon (Freon 12 = CCl 2 F 2, Freon 22 = CHCl 2 F) : pendingin lemari es, alat “air conditioner”, sebagai propellant (penyebar) kosmetik, insektisida, dsb.

ALKOHOL • Struktur Alkohol : R – OH • Alkohol : tersusun dari unsur C, H, dan O • PENGGUNAAN ALKOHOL : – Metanol : pelarut, antifreeze radiator mobil, sintesis formaldehid, metilamina, metilklorida, metilsalisilat, dll. – Etanol : minuman beralkohol, larutan 70 % sebagai antiseptik, sebagai pengawet, dan sintesis eter, koloroform, dll.

FENOL • Fenol : mengandung gugus benzen dan hidroksi • Mempunyai sifat asam • Mudah dioksidasi • Mempunyai sifat antiseptik • Penggunaan sebagai antiseptikum dan sintesis

ETER • Eter : isomer atau turunan dari alkohol (unsur H pada OH diganti oleh alkil atau aril) • Eter : mengandung unsur C, H, dan O • Struktur eter : R – O – R • PENGGUNAAN ETER : • Dietil eter : sebagai obat bius umum, pelarut dari minyak, dsb. • Eter-eter tak jenuh : pada opersi singkat : ilmu kedokteran gigi dan ilmu kebidanan.

ALDEHID • Aldehid adalah suatu senyawa yang mengandung gugus karbonil (C = O) yang terikat pada sebuah atau dua buah unsur hidrogen. • FORMALDEHID = METANAL = H – CHO Sifat-sifat : satu-satunya aldehid yang berbentuk gas pada suhu kamar, tak berwarna, baunya tajam, larutannya dalam H 2 O dari 40 % disebut formalin. Penggunaan : sebagai desinfektans, mengeraskan protein (mengawetkan contoh-contoh biologik), membuat damar buatan.

ASAM KARBOKSILAT n Mengandung gugus COOH yang terikat pada gugus alkil (R – COOH) maupun gugus aril (Ar – COOH). ASAM FORMAT = HCOOH n Sifat fisika : cairan, tak berwarna, merusak kulit, berbau tajam, laut dalam H 2 O dengan sempurna. n Penggunaan : untuk koagulasi lateks, penyamakkan kulit, industri tekstil dan fungisida. ASAM ASETAT = CH 3 – COOH n Sifat : cair TL 170 C, TD 1180 C, larut dalam H 2 O dengan sempurna. n Penggunaan : sintesis anhidrat asam asetat, ester, garam, zat warna, zat wangi, bahan farmasi, plastik, serat buatan, selulosa dan sebagai penambah makanan.

TATA NAMA ALKANA, ALKIL HALIDA DAN ALKOHOL MENURUT IUPAC l Penanaman untuk senyawa organik yang biasa bisa disebut dengan penanaam biasa atau penamaan trivial. Setelah beberapa lama, penamaan yang kita gunakan itu disebut dengan penamaan berdasarkan IUPAC (Internasional Union of Pure and Applied Chemistry)

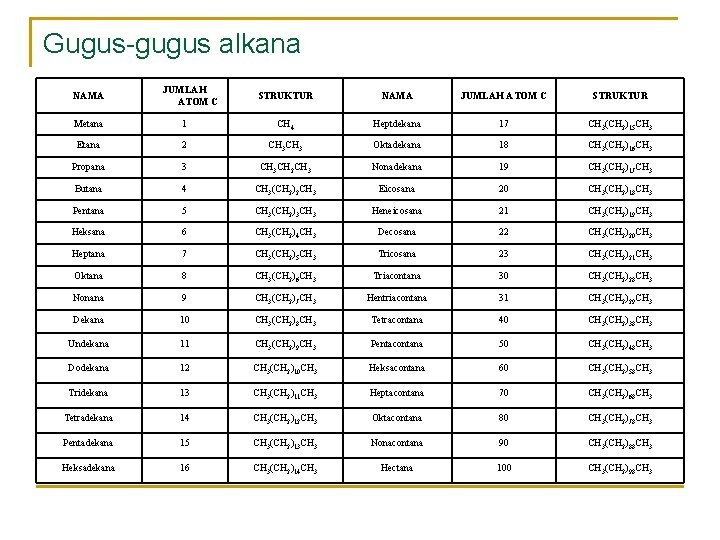
Gugus-gugus alkana NAMA JUMLAH ATOM C STRUKTUR Metana 1 CH 4 Heptdekana 17 CH 3(CH 2)15 CH 3 Etana 2 CH 3 Oktadekana 18 CH 3(CH 2)16 CH 3 Propana 3 CH 3 CH 2 CH 3 Nonadekana 19 CH 3(CH 2)17 CH 3 Butana 4 CH 3(CH 2)2 CH 3 Eicosana 20 CH 3(CH 2)18 CH 3 Pentana 5 CH 3(CH 2)3 CH 3 Heneicosana 21 CH 3(CH 2)19 CH 3 Heksana 6 CH 3(CH 2)4 CH 3 Decosana 22 CH 3(CH 2)20 CH 3 Heptana 7 CH 3(CH 2)5 CH 3 Tricosana 23 CH 3(CH 2)21 CH 3 Oktana 8 CH 3(CH 2)6 CH 3 Triacontana 30 CH 3(CH 2)28 CH 3 Nonana 9 CH 3(CH 2)7 CH 3 Hentriacontana 31 CH 3(CH 2)29 CH 3 Dekana 10 CH 3(CH 2)8 CH 3 Tetracontana 40 CH 3(CH 2)38 CH 3 Undekana 11 CH 3(CH 2)9 CH 3 Pentacontana 50 CH 3(CH 2)48 CH 3 Dodekana 12 CH 3(CH 2)10 CH 3 Heksacontana 60 CH 3(CH 2)58 CH 3 Tridekana 13 CH 3(CH 2)11 CH 3 Heptacontana 70 CH 3(CH 2)68 CH 3 Tetradekana 14 CH 3(CH 2)12 CH 3 Oktacontana 80 CH 3(CH 2)78 CH 3 Pentadekana 15 CH 3(CH 2)13 CH 3 Nonacontana 90 CH 3(CH 2)88 CH 3 Heksadekana 16 CH 3(CH 2)14 CH 3 Hectana 100 CH 3(CH 2)98 CH 3

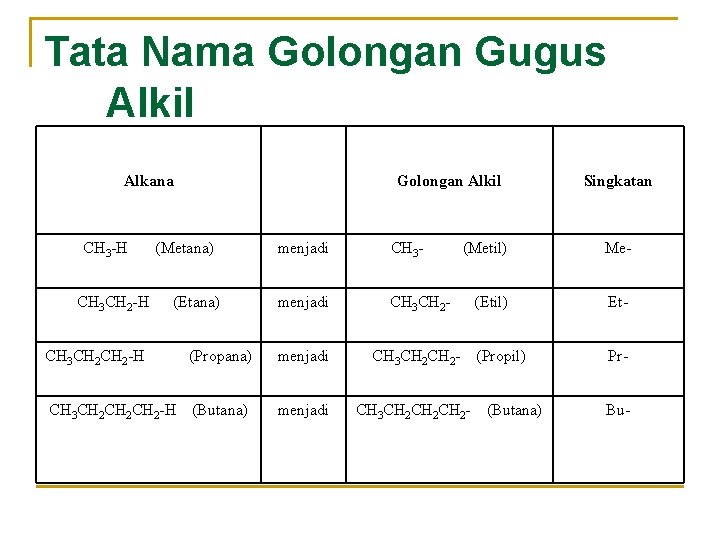
Tata Nama Golongan Gugus Alkil Alkana CH 3 -H CH 3 CH 2 -H Golongan Alkil (Metana) (Etana) menjadi CH 3 - menjadi CH 3 CH 2 - Singkatan (Metil) Me- (Etil) Et- (Propil) Pr- CH 3 CH 2 -H (Propana) menjadi CH 3 CH 2 - CH 3 CH 2 CH 2 -H (Butana) menjadi CH 3 CH 2 CH 2 - (Butana) Bu-