KIMIA ORGANIK Ashfar Kurnia Perkembangan Tahun 1850 Kimia

KIMIA ORGANIK Ashfar Kurnia

Perkembangan Tahun 1850 Kimia dari senyawa yang datang dari banda hidup Tahun 1900 kimia senyawa karbon

Kimia organik dalam kehidupan sehari
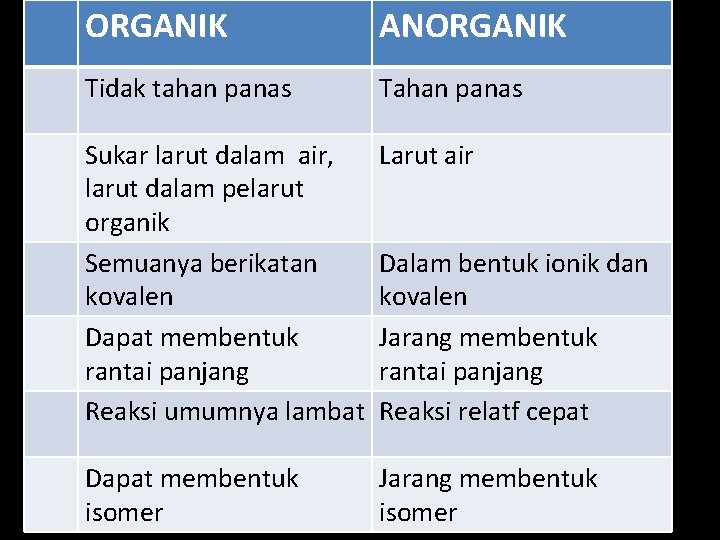
ORGANIK ANORGANIK Tidak tahan panas Tahan panas Sukar larut dalam air, larut dalam pelarut organik Semuanya berikatan kovalen Dapat membentuk rantai panjang Reaksi umumnya lambat Larut air Dapat membentuk isomer Jarang membentuk isomer Dalam bentuk ionik dan kovalen Jarang membentuk rantai panjang Reaksi relatf cepat
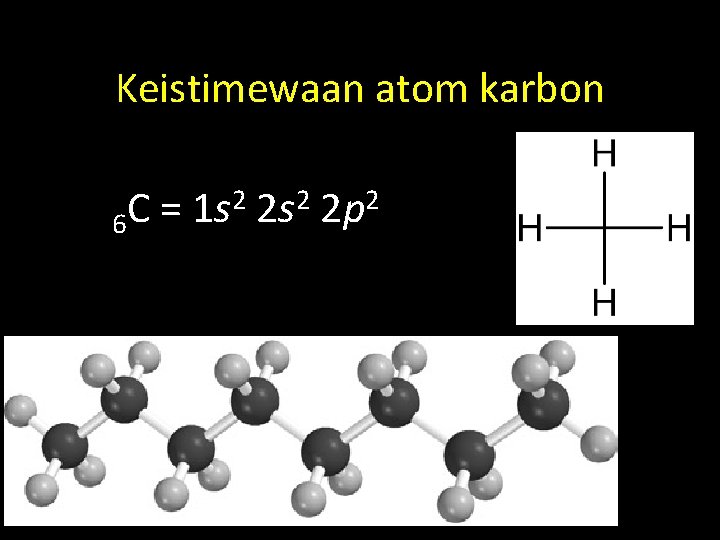
Keistimewaan atom karbon 2 2 s 2 2 p 2 C = 1 s 6
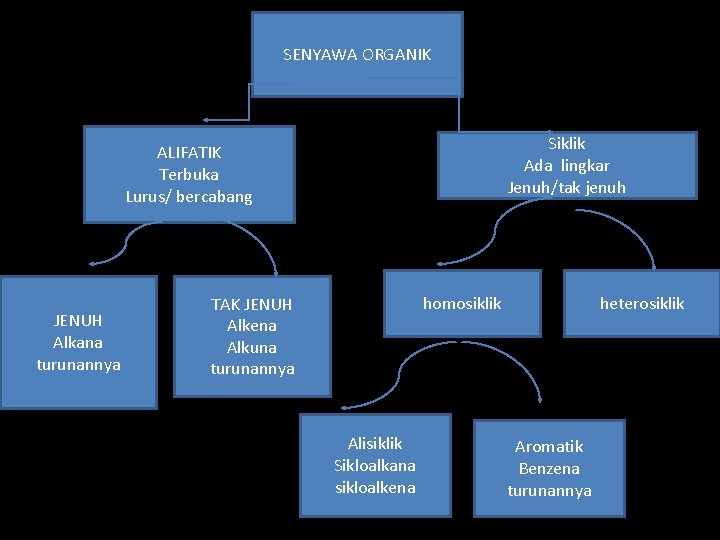
SENYAWA ORGANIK Siklik Ada lingkar Jenuh/tak jenuh ALIFATIK Terbuka Lurus/ bercabang JENUH Alkana turunannya homosiklik TAK JENUH Alkena Alkuna turunannya Alisiklik Sikloalkana sikloalkena heterosiklik Aromatik Benzena turunannya
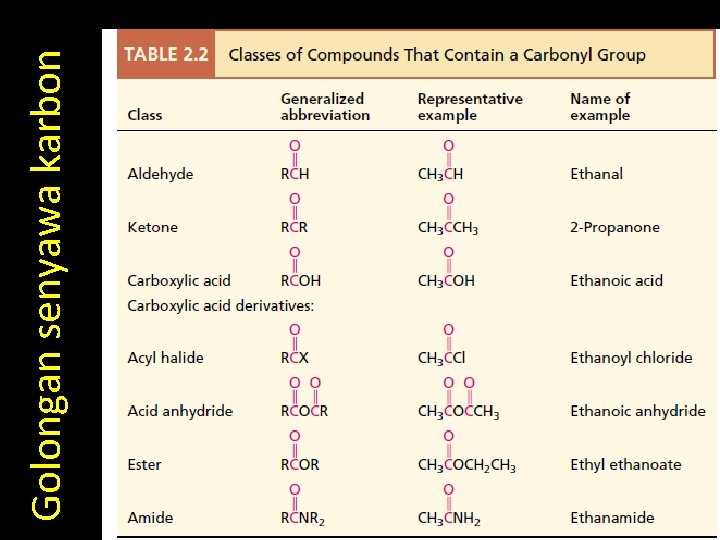
Golongan senyawa karbon

Golongan Kimia Organik • • Hidrokarbon jenuh Hidrokarbon tidak jenuh Alkohol Eter Aldehid Keton Asam karboksilat Ester • • Alkil halida Alkil amina Benzena Turunan benzena Karbohidrat Asam amino & protein Lipid

ALKANA

ALKANA (Cn. H 2 n+2) Hidrokarbon jenuh (“jenuh dengan hidrogen”), merupakan ikatan-ikatan tunggal n NAMA RUMUS 1 2 3 4 Metana Etana Propana Butana CH 4 C 2 H 6 C 3 H 8 C 4 H 10 5 Pentana C 5 H 12 6 Heksana C 6 H 14 7 Heptana C 7 H 16 8 Oktana C 8 H 18 9 Nonana C 9 H 20 10 Dekana C 10 H 22 11 Undekana 12 Dodekana C 11 H 24 C 12 H 26

Isomer Alkana Isomer senyawa yang mempunyai rumus molekul yang sama tetapi struktur yang berbeda. Isomer alkana dimulai butana CH 3 – CH 2 – CH 3 n butana CH 3 – CH 3 Metil propana (iso butana) CH 3
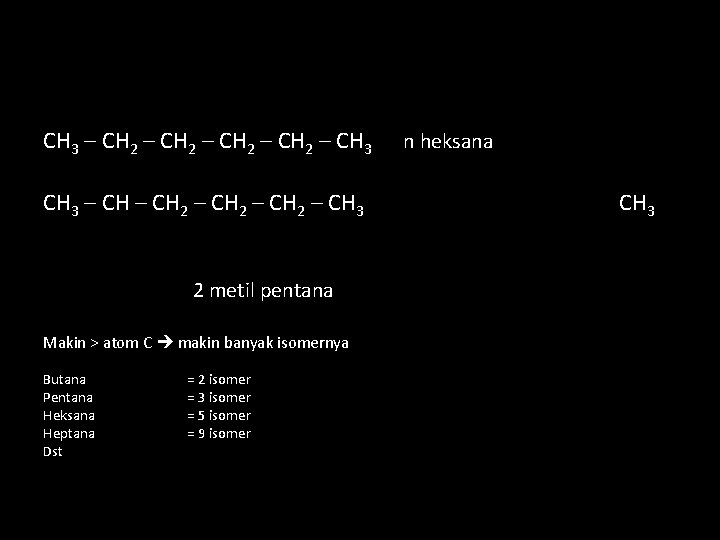
CH 3 – CH 2 – CH 2 – CH 3 2 metil pentana Makin > atom C makin banyak isomernya Butana Pentana Heksana Heptana Dst = 2 isomer = 3 isomer = 5 isomer = 9 isomer n heksana CH 3

TATA NAMA ALKANA IUPAC (International Union of Pure ang Applied Chemistry) Struktur senyawa organik dapat digunakan untuk menurunkan namanya dan sebaliknya, bahwa suatu struktur yang unik dapat digambarkan untuk tiap nama. Banyak karbon I 2 3 4 5 6 7 8 9 IO Struktur Nama CH 4 CH 3 CH 2 CH 3(CH 2 h. CH 3(CH 2)4 CH 3(CHz)s. CH 3(CH 2)6 CH 3 CHi. CH 2 h. CH 3(CH 2)s. CH 3 metana propana butana pentana heksana heptana oktana nonana dekana

Rantai Samping • Bila gugus fungsional dilekatkan pada suatu rantai alkana rantai lurus induk • Gugus-gugus ditandai dalam nama senyawa oleh awalan dan akhiran pada nama induknya.

Rantai samping (side chain) atau cabang suatu gugus alkil sebagai cabang dari suatu rantai induk dinamai menurut induk alkananya & berakhiran -il CH 2 – CH 2 – CH 3 ?
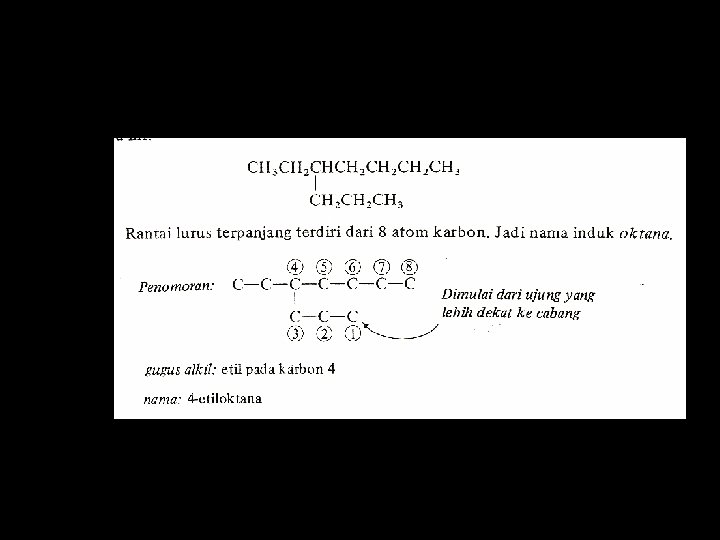

Rantai Samping Bercabang • Awalan iso- (dari kata isometrik) menyatakan cabang metil pada ujung rantai samping alkil

Cabang Ganda Jika 2 cabang atau > terikat pada suatu rantai induk d+ lebih banyak awalan pada nama induk. Awalan diurutkan secara alfabet, dengan nomor masing-masing yang menyatakan posisi lekatnya. Jika 2 substituen atau > pada suatu induk itu sama (misalnya 2 gugus metil) penamaannya digabung dimetil 2 gugus metil trimetil 3 gugus metil


Substituen Awalan Lain • Gugus fungsional diberi nomor (serendah mungkin) dan gugus identik didahului oleh di- atau tri-

Sifat – Sifat Fisika • • • Senyawa- senyawa rendah ( C 1 – C 4) T & P normal cair Senyawa- senyawa sedang ( C 5 – C 17) T & P normal padat Senyawa- senyawa tinggi ( C 18 atau lebih) T & P normal gas Titik didih (t. d) > C > ( + 20˚ - 30˚/ 1 atom C) Bila jumlah atom C sama senyawa yg mmiliki rantai cabang t. d < lurus, > cabang t. d < • Berat jenis > C >

Sumber Alkana • Alam Sumber utama daripada alkana adalah gas alam dan petroleum. Dengan cara penyulingan/destilasi. Gas metana sering terjadi di rawa-rawa pembusukan tanaman, adanya bakteri dalam proses anaerob

ALKENA

Alkena sebuah kelompok hidrokarbon yang mengandung ikatan karbon-karbon rangkap (C=C). • Rumus umum: Cn. H 2 n • Suku alkena yang paling kecil terdiri dari dua atom C etena. Nama alkena sesuai dengan nama alkana dengan mengganti akhiran – ana menjadi -ena.

Tata nama alkena 1. 2. 3. 4. IUPAC Tentukan rantai induk, rantai karbon terpanjang dari ujung satu ke ujung yang lain yang melewati ikatan rangkap, berilah nama alkena sesuai jumlah atom C pada rantai induk. Penomoran dimulai dari ujung rantai induk yang terdekat dengan rangkap. Jika terdapat cabang berilah nama cabang dengan alkil sesuai jumlah atom C cabang tersebut. Jika terdapat lebih dari satu cabang, aturan penamaan sesuai dengan aturan pada tatanama alkana. Urutan penamaan: nomor cabang-nama cabang-nomor rangkap-rantai induk
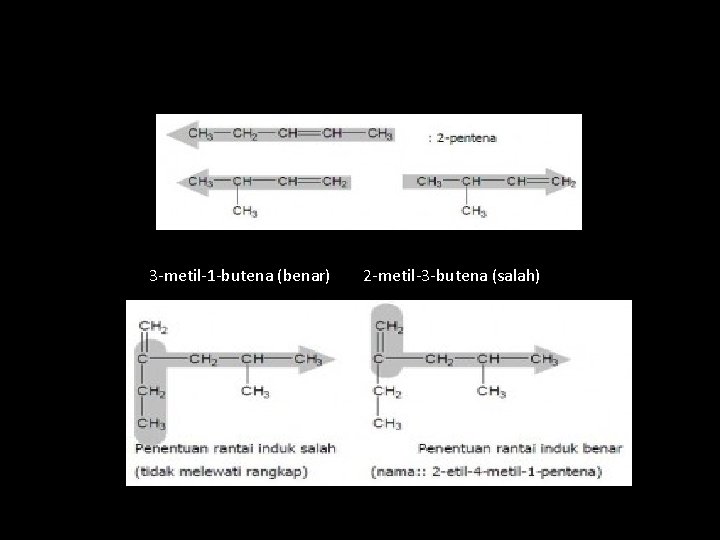
3 -metil-1 -butena (benar) 2 -metil-3 -butena (salah)
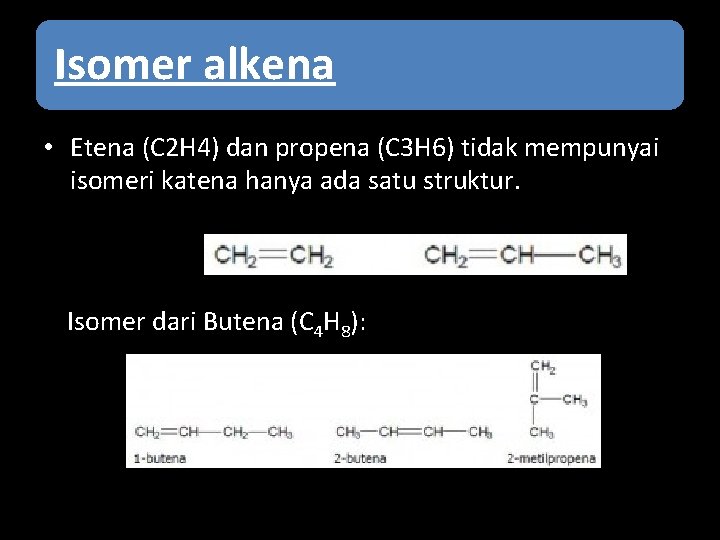
Isomer alkena • Etena (C 2 H 4) dan propena (C 3 H 6) tidak mempunyai isomeri katena hanya ada satu struktur. Isomer dari Butena (C 4 H 8):

Sifat Fisik 1. Pada suhu kamar, tiga suku yang pertama adalah gas, suku-suku berikutnya adalah cair dan suku-suku tinggi berbentuk padat. 2. Dapat terbakar dengan nyala yang berjelaga karena kadar karbon alkena lebih tinggi daripada alkana yang jumlah atom karbonnya sama. 3. Alkena hampir tidak dapat larut dalam air, tapi larut dalam pelarut-pelarut orgaik Nama alkena Mr Titik leleh Titik didih (0 C) Kerapatan (g/Cm 3) Fase pada 250 C molekul C 2 H 4 28 (o. C) -169 -104 0, 568 Gas Propena C 3 H 6 42 -185 -48 0, 614 Gas 1 -Butena C 4 H 8 56 -185 -6 0, 630 Gas 1 -Pentena C 5 H 10 70 -165 30 0, 643 Cair 1 -Heksena C 6 H 12 84 -140 63 0, 675 Cair 1 -Heptena C 7 H 14 98 -120 94 0, 698 Cair 1 -Oktena C 8 H 16 112 -102 122 0, 716 Cair 1 -Nonesa C 9 H 18 126 -81 147 0, 731 Cair 1 -Dekena C 10 H 20 140 -66 171 0, 743 Cair Etena Rumus

Sifat Kimia Adanya ikatan rangkap dua antara dua buah atom karbon gugus fungsional dari alkena menentukan adanya reaksi-reaksi yang khusus bagi alkena, yaitu adisi, polimerisasi dan pembakaran 1. Adisi pengubahan ikatan rangkap (tak jenuh) menjadi ikatan tunggal (jenuh) dengan cara menangkap atom/gugus lain. a. Reaksi alkena dengan halogen (halogenisasi)
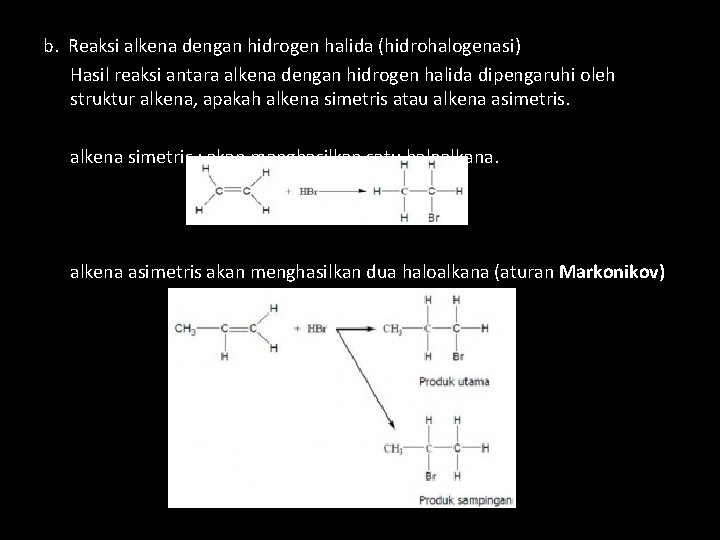
b. Reaksi alkena dengan hidrogen halida (hidrohalogenasi) Hasil reaksi antara alkena dengan hidrogen halida dipengaruhi oleh struktur alkena, apakah alkena simetris atau alkena asimetris. alkena simetris : akan menghasilkan satu haloalkana. alkena asimetris akan menghasilkan dua haloalkana (aturan Markonikov)

c. Reaksi alkena dengan hidrogen (hidrogenasi) 1. Reaksi ini akan menghasilkan alkana. 2. Alkena dapat mengalami polimerisasi. penggabungan molekul-molekul sejenis menjadi molekul -molekul raksasa sehingga rantai karbon sangat panjang. Molekul yang bergabung disebut monomer, sedangkan molekul raksasa yang terbentuk disebut polimer.
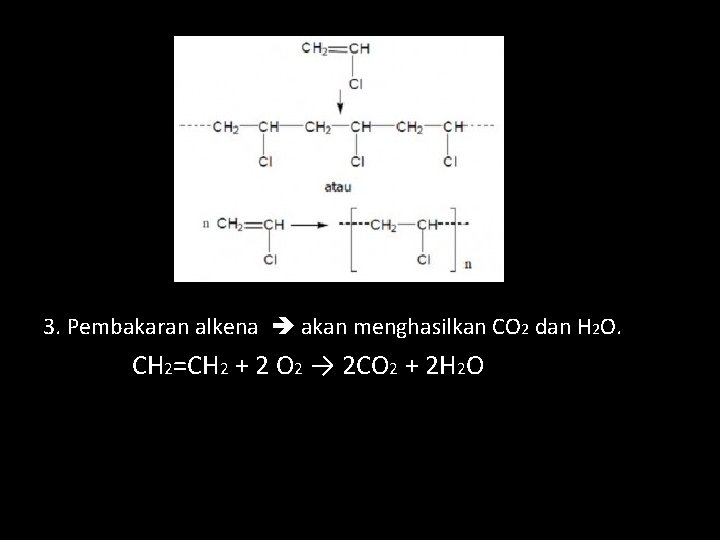
3. Pembakaran alkena akan menghasilkan CO 2 dan H 2 O. CH 2=CH 2 + 2 O 2 → 2 CO 2 + 2 H 2 O

Pembuatan • Dehidrasi Alkohol

ALKUNA

ALKUNA : Cn. H 2 n-2 • 1 Ikatan C-C rangkap 3 • Alkuna tersederhana asetilena, CH≡CH Tatanama : 1. Trivial turunan dari asetilena mengganti 1 atau 2 atom H dengan gugus alkil. CH 3 − C ≡ C − CH 2 − CH 3 dimetil asetilena etil metil asetilena

2. IUPAC - Alkuna berantai lurus diberi nama menurut alkana induknya dengan mengubah akhiran -ana -una - Beri nomor atom C yang mengemban ikatan rangkap 3 dengan nomor terendah, kecuali terdapat gugus fungsi dengan prioritas lebih tinggi Contoh : HC ≡ C – CH 3 | CH 3 3 – metil – 1 - butuna
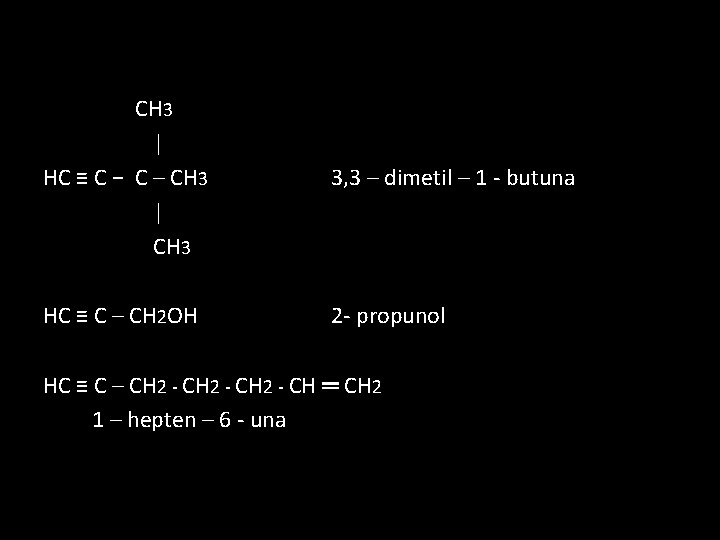
CH 3 | HC ≡ C − C – CH 3 | CH 3 3, 3 – dimetil – 1 - butuna HC ≡ C – CH 2 OH 2 - propunol HC ≡ C – CH 2 - CH ═ CH 2 1 – hepten – 6 - una
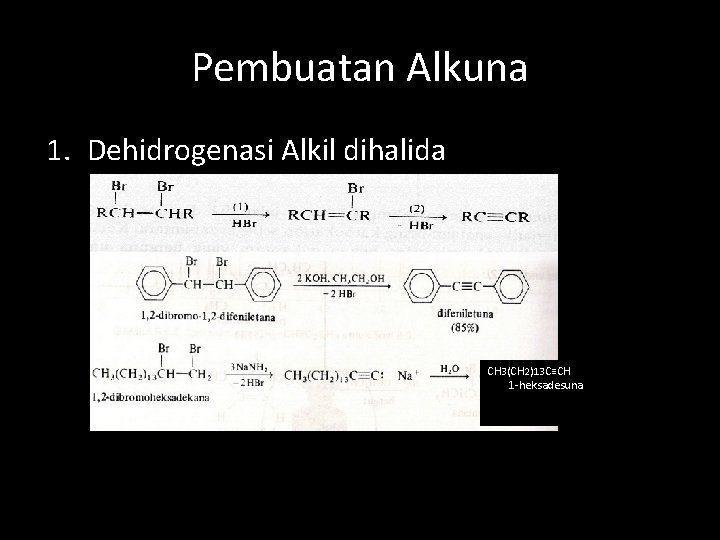
Pembuatan Alkuna 1. Dehidrogenasi Alkil dihalida CH 3(CH 2)13 C≡CH 1 -heksadesuna

2. Reaksi Grignard 3. Pemanjangan asetilida
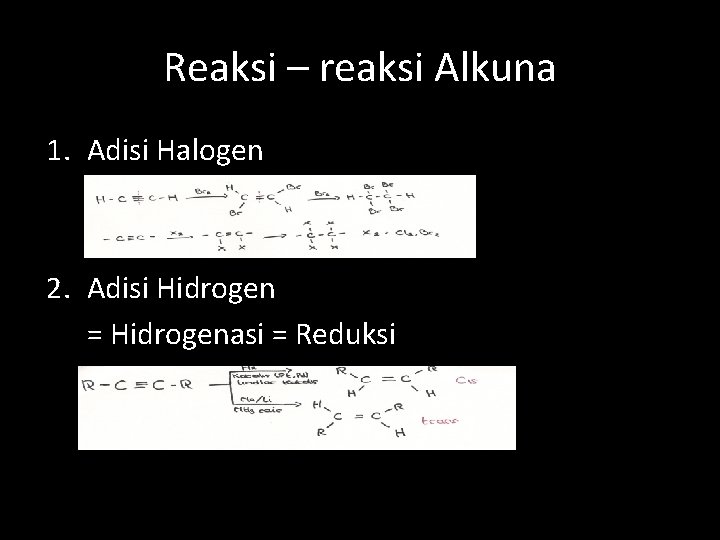
Reaksi – reaksi Alkuna 1. Adisi Halogen 2. Adisi Hidrogen = Hidrogenasi = Reduksi
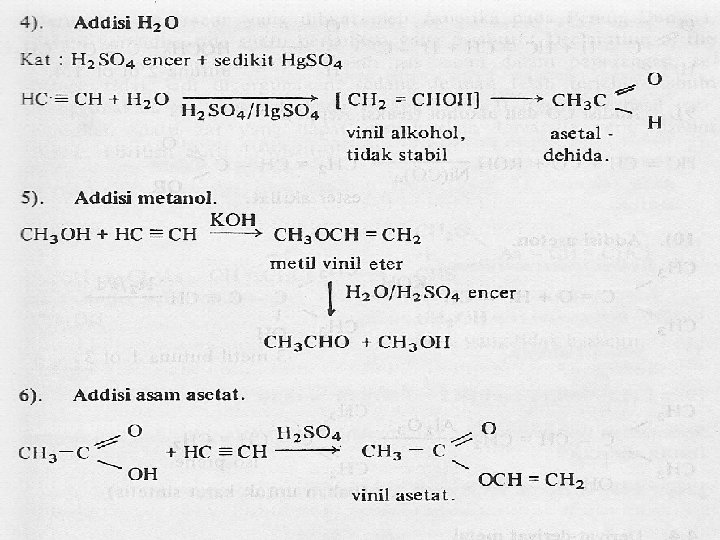

7. Adisi Hidogen Halida

Tugas 1. Jelaskan apa yang dimaksud dengan, dan kecenderungan dalam sistem periodik. 1. 2. 3. 4. Jari jari atom Keelektronegatifan Afinitas ionisasi 2. Sebutkan macam-macam ikatan kimia, cotohnya masing-masing 3. Sebutkan macam-macam reaksi kimia, contohnya masing-masing
- Slides: 44