TERMOKIMIA PENGERTIAN Termokimia adalah cabang dari ilmu kimia

TERMOKIMIA PENGERTIAN Termokimia adalah cabang dari ilmu kimia yang mempelajari hubungan antara reaksi dengan panas.

1. SISTEM : Sesuatu yang menjadi pusat perhatian kita dalam hal ini adalah seluruh proses kimia yang terjadi. 2. LINGKUNGAN : Sesuatu diluar sistem. 3. KALOR REAKSI : Besarnya kalor yang menyertai reaksi yaitu bentuk energi yang mengalir dari sistem ke lingkungan atau sebaliknya karena ada perbedaan suhu. 4. ENTALPI : Jumlah total semua bentuk energi.

ENTALPHI(H) : Jumlah total semua bentuk energi. Perubahan entalphi (ΔH)terjadi bila sistem melepas (eksoterm) atau menyerap kalor (endoterm). Dalam reaksi : A + B ------- AB ( reaktan/pereaksi ) ( produk ) maka : ΔH reaksi = Hp - Hr

REAKSI EKSOTERM 1. Reaksi yang membebaskan kalor 2. Kalor berpindah dari sistem ke lingkungan ΔH ΔH = Hp kecil = - - Hr - besar

REAKSI ENDOTERM Reaksi yang memerlukan kalor Penulisan persamaan reaksinya sbb: ΔH ΔH = Hp - Hr besar kecil = +

JENIS PERUBAHAN ENTALPI 1. Perubahan entalpi pembentukan (ΔHf) 2. Perubahan entalpi penguraian ( ∆Hd ) 3. Perubahan entanpi pembakaran ( ∆Hc) 4. Perubahan entalpi netralisasi ( ∆Hn ) Yang jelas senyawa yang dibentuk, diuraikan dibakar dan reaksi asam basa harus 1 mol

1. Perubahan entalpi pembentukan (ΔHf) adalah perubahan entalpi pembentukan 1 mol senyawa dari unsurnya. [ΔHf beberapa unsur telah ditabelkan. ] Misal : ΔHf ∆Hf ∆Hf CH 3 OH (l) Fe(OH)3 (s) KMn. O 4 (s) CHCl 3 (s) = - 200, 6 kj /mol = - 823 kj / mol = - 837, 2 Kj/mol = - 103, 14 kj/mol Penulisan persamaannya sebagai berikut :

Persamaan termokimianya C(s) +2 H 2(g)+1/2 O 2 CH 3 OH , ΔHf=-200 kj Fe(s)+3/2 O 2(g)+3/2 H 2(g) Fe(OH)3(s) ΔHf=-823 kj K(s) + Mn(s) + 2 O 2(g) KMn. O 4 C(s) +1/2 H 2(g) + 3/2 Cl 2(g) CHCl 3 (s) ∆Hf = - 103, 14 Kj ∆Hf = - 837, 2 kj

Tulis persamaan pembentukan 2 mol air dengan membebaskan 136, 6 kkal Persamaan termokimia : 2 H 2(g) + 02 2 H 2 O , ΔH = 136, 6 kkal ΔH pembentukan : ……………. . . . .
![2. Perubahan entalpi penguraian [ ∆Hd ] Adalah perubahan entalpi pada penguraian 1 mol 2. Perubahan entalpi penguraian [ ∆Hd ] Adalah perubahan entalpi pada penguraian 1 mol](http://slidetodoc.com/presentation_image_h/eb947b13a3bf24da2edfb2919a56c7a6/image-10.jpg)
2. Perubahan entalpi penguraian [ ∆Hd ] Adalah perubahan entalpi pada penguraian 1 mol senyawa menjadi unsurnya. [merupakan kebalikan dari perubahan entalpi pembentukan ] Misal : ∆Hf CO 2 = - 393, 5 kj/mol ∆Hd CO 2 = +393, 5 kj/mol Persamaan termonya : CO 2(g) C(s) +O 2(g) ∆Hd=393, 5 kj
![3. Perubahan entalpi pembakaran[ ∆Hc] Adalah perubahan entalpi pada pembakaran 1 mol zat. Misal 3. Perubahan entalpi pembakaran[ ∆Hc] Adalah perubahan entalpi pada pembakaran 1 mol zat. Misal](http://slidetodoc.com/presentation_image_h/eb947b13a3bf24da2edfb2919a56c7a6/image-11.jpg)
3. Perubahan entalpi pembakaran[ ∆Hc] Adalah perubahan entalpi pada pembakaran 1 mol zat. Misal : * ∆H pembakaran CH 4 = 112 kkal/mol Persamaan termonya. . . . * Perhatikan persamaan termokimia berikut : 2 H 2(g) + O 2 2 H 2 O ∆H = - 571 kj Tentukan ∆Hc =. . . . .
![4. Perubahan entalpi netralisasi[ ∆Hn] Adalah perubahan entalpi pada penetralan 1 mol asam oleh 4. Perubahan entalpi netralisasi[ ∆Hn] Adalah perubahan entalpi pada penetralan 1 mol asam oleh](http://slidetodoc.com/presentation_image_h/eb947b13a3bf24da2edfb2919a56c7a6/image-12.jpg)
4. Perubahan entalpi netralisasi[ ∆Hn] Adalah perubahan entalpi pada penetralan 1 mol asam oleh basa atau 1 mol basa oleh asam. Misal : * ∆H netralisasi H 2 SO 4 oleh Na. OH = 200 kj/mol Persamaan termonya. . . . H 2 SO 4 + 2 Na. OH Na 2 SO 4 + 2 H 2 O ∆Hn H 2 SO 4 = - 200 kj/mol

LATIHAN SOAL Buatlah persamaan termokimia dari : 1. Penguraian Ca CO 3 2. Pembakaran C 3 H 6 3. Pembakaran C 5 H 10 4. Netralisasi Mg(OH)2 oleh HNO 3 5. Netralisasi H 3 PO 4 oleh KOH

∆H REAKSI DAPAT DIHITUNG DENGAN BEBERAPA CARA PERUBAHAN ENTALPH (∆H) /KALOR REAKSI : Perubahan jumlah total semua bentuk energi pada suatu reaksi kimia. 1. DENGAN ALAT KALORIMETER 2. DENGAN HUKUM HESS 3. DENGAN MENGGUNAKAN DATA ∆Hf ZAT 4. DENGAN DATA ENERGI IKAT.

KALORIMETER Pengukuran perubahan kalor dengan menggunakan alat kalorimeter. q larutan = m. c. ∆t Keterangan : q = kalor (joule) m = massa air atau larutan dalam kalorimeter (gram) c = kalor jenis (J/g. K) ∆t = kenaikan suhu ( K ) CATATAN : q reaksi = - q larutan ∆H = q reaksi ∆H = - q larutan

CONTOH SOAL : Jika 100 ml larutan Na. OH 1 M direaksikan dengan 100 ml HCl 1 M dalamsebuah bejana, ternyata suhu larutan naik dari 290 C menjadi 37, 50 C. Jika larutan dianggap sama dengan air, kalor jenis 4, 2 J/g. K, massa jenis air 1 g/ml. Tentukan ∆H ! Pembahasan : Q lart = m. c. ∆t = (100+100) gx 4, 2 J/g. Kx(37, 5 - 29)K = 7149 joule ∆H = -q larutan ∆H= -7149 joule

HUKUM HESS Bunyi HUKUM HESS : “Kalor reaksi dari suatu reaksi tidak bergantung apakah reaksi tersebut berlangsung satu tahap atau beberapa tahap” KEPENTINGAN : Hukum Hess sangat penting dalam perhitungan kalor reaksi yang tidak dapat ditentukan secara eksperimen. Contoh reaksi : 1. Reaksi langsung A B ΔH 1 = x Kkal 2. Secara tidak langsung ΔH 2 = b Kkal a) lewat C A C C B ΔH 3 = c Kkal
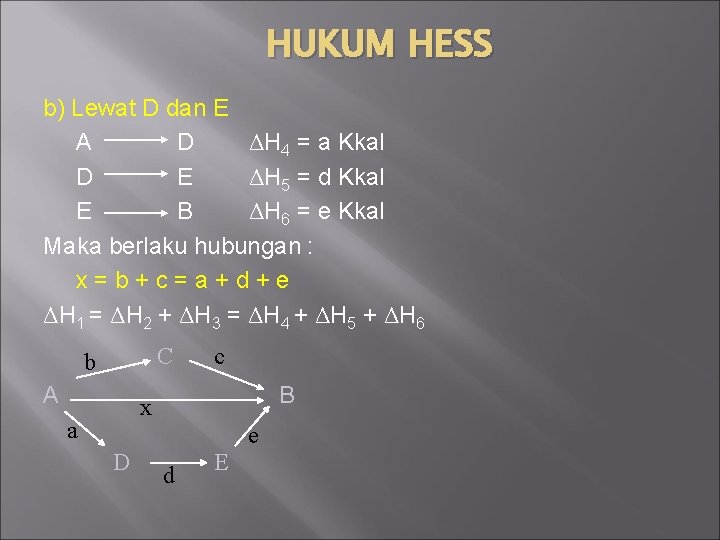
HUKUM HESS b) Lewat D dan E A D ΔH 4 = a Kkal D E ΔH 5 = d Kkal E B ΔH 6 = e Kkal Maka berlaku hubungan : x=b+c=a+d+e ΔH 1 = ΔH 2 + ΔH 3 = ΔH 4 + ΔH 5 + ΔH 6 C b A c B x a D d E e

HUKUM HESS Contoh soal : 1. Diketahui : 2 H 2(g) + O 2(g) 2 H 2 O(cair) ΔH = -136 Kkal H 2(g) + O 2(g) H 2 O 2(cair) ΔH = -44, 8 Kkal Hitung ΔH untuk reaksi : 2 H 2 O 2(cair) 2 H 2 O(cair) + O 2 Jawab : 2 H 2 + O 2 2 H 2 O (cair) ΔH = -136 Kkal 2 H 2 O 2 2 H 2 + 2 O 2 ΔH = +89, 6 Kkal + 2 H 2 O 2 (cair) 2 H 2 O(cair) + O 2 ΔH = -46, 4 Kkal

HUKUM HESS 2. Diketahui : I. C + O 2 II. H 2 + ½ O 2 III. 2 C + 3 H 2 CO 2 H 2 O C 2 H 6 ΔH = - 94 Kkal ΔH = - 68 Kkal ΔH = - 20 Kkal Ditanyakan : berapa x pada reaksi : C 2 H 6 + 7/2 O 2 2 CO 2 + 3 H 2 O ΔH = x Kkal Jawab : I. 2 C + 2 O 2 2 CO 2 ΔH = -188 Kkal II. 3 H 2+ 3/2 O 2 3 H 2 O ΔH = - 204 Kkal III. C 2 H 6 2 C + 3 H 2 ΔH = 20 Kkal C 2 H 6 + 7/2 O 2 2 CO 2 + 3 H 2 O ΔH = - 372 Kkal, maka x = -372 Kkal. + ΔH = -372 Kkal

3. Menentukan ∆H menggunakan entalpi pembentukan ( ∆H 0 f) Untuk reaksi : m. A + n. B p. C + q. D ∆H=…?

Contoh


LATIHAN SOAL : 1. Diketahui ∆Hf sebagai berikut : ∆Hf C 2 H 2(g) = + 52 kj/mol ∆Hf CO 2 = - 394 kj/mol ∆Hf H 2 O = -286 kj/mol a. hitunglah perubahan entalpi pembakaran etena (C 2 H 2 )! b. hitunglah perubahan entalpi untuk 26 gram etena!

Latihan soal : 2. Diket ∆H pembentukan standar: ∆ Hf CH 3 OH= -238, 6 kj/mol ∆ Hf CO 2 = -4905 kj/mol ∆ Hf H 20 = -250 kj/mol tentukan entalpi pembakaran 22, 4 L metanol dalam keadaan STP 3. Diket entalpi pebentukan standar NH 3 (∆ Hf NH 3 = 46, 1 kj/mol). Tentukan entalpi pembentukan standar 0. 34 gr NH 3

Jawaban 2. Reaksi Pembakaran metanol : CH 3 OH + 3/2 O 2 ---> CO 2 + 2 H 2 O ∆ H = (delta Hf CO 2 + delta Hf H 2 O) - (delta Hf CH 3 OH + delta Hf O 2) ∆ H = (-4905 kj/mol + 2 x (-250 kj/mol)) - (-238, 6 kj/mol + 3/2 x 0) ∆ H = (-4905 kj/mol + -500 kj/mol) - (-238, 6 kj/mol + 0) ∆ H = (-5405 kj/mol) - (-238, 6 kj/mol) ∆ H = (-5405 kj/mol + 238, 6 kj/mol) ∆ H = -5166, 4 kj/mol 3. 1/2 N 2 + 3/2 H 2 ---> NH 3 ∆ H f= 46, 1 kj/mol NH 3 = 0, 34/17 mol NH 3 = 0, 02 ∆Hf 1 mol NH 3 = 46, 1 kj/mol maka ∆ Hf 0, 02 mol NH 3 = 46, 1 kj/mol x 0, 02 = 0, 922 k. J entalpi pembentukan standar 0. 34 gr NH 3 (atau 0, 02 mol) = 0, 922 k. J

4. Menentukan ∆H dengan mengunakan data Energi Ikatan energi ikat adalah energi yg diperlukan untuk memutuskan ikatan 1 molekul gas menjadi atom-atom gas. ∆H = jumlah energi ikatan yang putus – jumlah energi ikatan hasil yang terbentuk ∆H = jumlah energi ikatan ruas kiri – jumlah energi ikatan ruas kanan
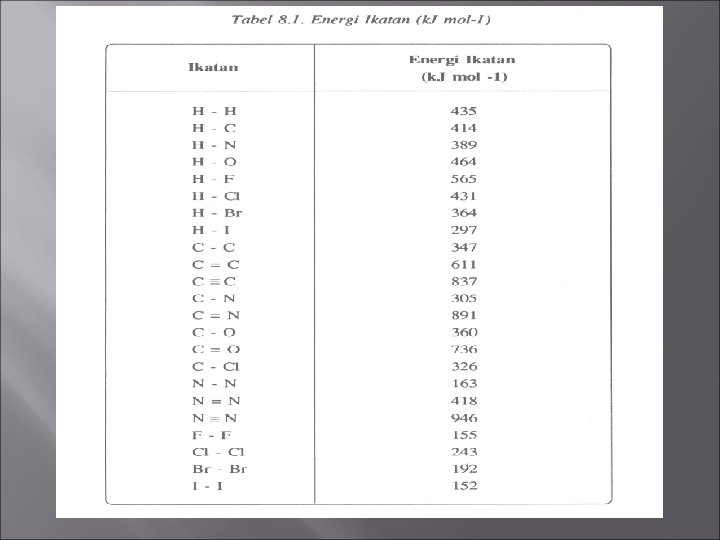

CONTOH

Contoh Soal: Jika diketahui energi ikatan N-N = 946 k. J/mol dan H – H = 436 k. J/mol, dan reaksi: 2 NH 3 (g) ------>. N 2 (g) + 3 H 2 (g) H = +92 k. J maka energi ikatan rata-rata N – H adalah … a. 1173, 0 k. J d. 195, 5 k. J b. 586, 5 k. J e. 159, 5 k. J c. 391, 0 k. J Jawab: C 2 H–N–H ------> N-N + 3 H–H H = + 92 k. J | H H = EI (kiri) - EI (kanan) +92 = (6. N – H) – (N N + 3. H – H) +92 = (6. N – H) – (946 + 3 x 436) N – H = = 391 k. J
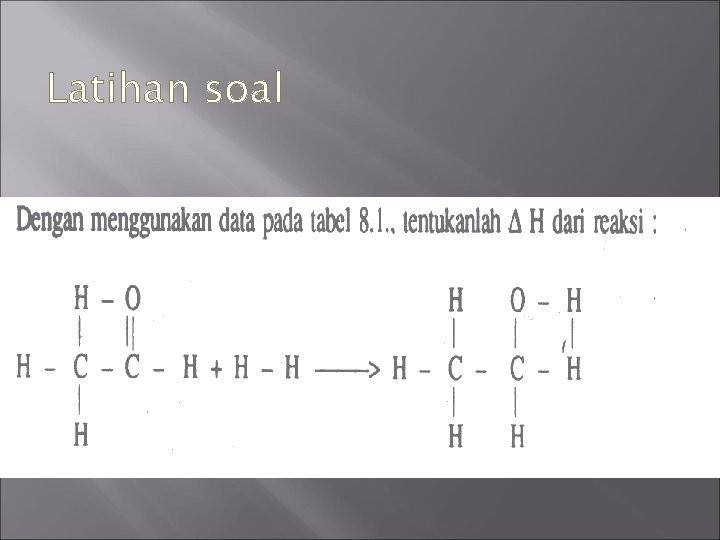
Latihan soal


Contoh Soal Persamaan Termokimia 1. Reaksi 1 mol gas metana dengan 2 mol gas oksigen membebaskan kalor sebesar 802, 3 k. J pada temperatur 298 K dan tekanan 1 atm. Tentukan persamaan termokimianya! 2. Rekasi karbon dan gas hidrogen membentuk 1 mol C 2 H 2 pada temperatur 25° dan tekanan 1 atm membutuhkan kalor 226, 7 k. J/mol. Tentukan persamaan termokimianya! 33

Contoh Soal Dalam kalorimeter terdapat zat yang bereaksi secara eksotermik dan ternyata 0, 5 kg air yang mengelilinginya sebagai pelarut mengalami kenaikan temperatur sebesar 3˚C. Kalor jenis air = 4, 2 J/gram ˚C. Berapa kalor reaksi zat yang bereaksi itu? 34

Menentukan Harga Perubahan Entalpi 2. Menentukan harga perubahan entalpi dengan menggunakan hukum Hess. Hukum Hess “ perubahan entalpi reaksi hanya tergantung keadaan awal dan keadaan akhir sistem yang tidak tergantung pada jalannya reaksi. Kegunaan hukum Hess ialah untuk menghitung ∆H yang sukar diperoleh melalui percobaan. 35

Contoh Soal Ada 2 cara untuk memperoleh gas CO 2 yaitu : 1. Cara langsung. C(s) + O 2(g) CO 2(g) ∆H = -393, 5 k. J 2. Cara tidak langsung. C + ½O 2 CO ∆H = -110, 5 k. J CO + ½O 2 CO 2 ∆H = -283, 0 k. J + C + O 2 CO 2 ∆H = -393, 5 k. J 36

Gambar 3. Reaksi Pembentukan Gas CO 2 ∆H 3 = -393, 5 k. J C + O 2 CO 2 ∆H 1 = -110, 5 k. J ∆H 2 = -283, 5 k. J CO + ½O 2 37
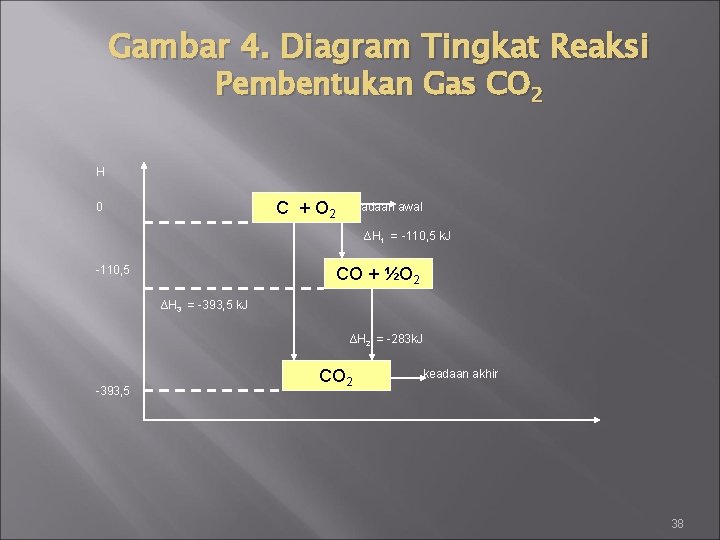
Gambar 4. Diagram Tingkat Reaksi Pembentukan Gas CO 2 H C + O 2 0 keadaan awal ∆H 1 = -110, 5 k. J CO + ½O 2 -110, 5 ∆H 3 = -393, 5 k. J ∆H 2 = -283 k. J -393, 5 CO 2 keadaan akhir 38

Menentukan Harga Perubahan Entalpi 3. Menetukan harga perubahan entalpi dengan menggunakan entalpi pembentukan. a PQ + b RS c PS + d QR reaktan produk ∆H = (c. ∆H˚f PS + d. ∆H˚f QR) – (a. ∆H˚f PQ + b. ∆H˚f RS) ∆H = ∑ ∆H˚f (produk) - ∑ ∆H˚f (produk) 39

Soal 1 Tentukan entalpi pembakaran gas etana, jika diketahui : ∆H˚f C 2 H 6 (g) = - 84, 7 k. J/mol-1 ∆H˚f CO 2 (g) = -393, 5 k. J/mol-1 ∆H˚f H 2 O (l) = -285, 8 k. J/mol-1 40

Soal 2 Tulislah persamaan termokimianya : a. Entalpi pembakaran C 2 H 5 OH(l) = -1. 234, 7 k. J/mol-1 b. Entalpi pembentukan NH 4 Cl = -317, 1 k. J/mol-1 41

Soal 3 Pada penguraian 1 mol gas amonia diperlukan kalor sebesar 46, 2 k. J/mol-1 a. Tulis persamaan termokimianya. b. Berapa harga ∆H pembentukan gas amonia? c. Pembentukan amonia tergolong reaksi eksoterm atau endoterm? d. Buatlah diagram tingkat energi untuk penguraian gas amonia. 42

Soal 4 Diketahui : ∆H˚f CO 2 (g) = -393, 5 k. J/mol-1 ∆H˚f H 2 O (l) = -285, 8 k. J/mol-1 ∆H˚f C 3 H 8 (g) = -103, 8 k. J/mol-1 Tentukan perubahan entalpi pembakaran C 3 H 8 (g) membentuk gas CO 2 dan air! Tentukan jumlah kalor yang dibebaskan pada pembakaran sempurna 4, 4 gram C 3 H 8 (g) 43

Soal 5 Diketahui reaksi-reaksi sebagai berikut : C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O ∆H= -2. 820 k. J/mol-1 C 2 H 5 OH + 3 O 2 2 CO 2 + 3 H 2 O ∆H= -1. 380 k. J/mol-1 Hitunglah perubahan entalpi untuk reaksi fermentasi glukosa C 6 H 12 O 6 ------- 2 Cfermen 2 H 5 OH + 2 CO 2 44

Tabel 1. Daftar ΔHºf Pembentukan Standar Senyawa 45

Energi Ikatan Energi ikatan adalah energi yang diperlukan untuk memutuskan ikatan kimia dalam 1 mol senyawa berwujud gas menjadi atom-atom gas pada keadaan standar. Energi ikatan diberi simbol D dan dinyatakan dalam satuan k. J/mol. 46

Contoh Soal 1 Tentukan energi ikatan dari : 1. Reaksi penguraian Cl 2(g). 2. Reaksi penguraian HBr(g). Catatan : Atom adalah partikel terkecil materi yang tidak dapat dibagi. Unsur adalah bentuk materi yang tidak dapat disederhanakan lagi dengan reaksi kimia. 47

Energi Ikatan Rata-rata Untuk molekul yang terdiri dari tiga atau lebih atom maka digunakan istilah energi ikatan rata-rata. Cara menghitung energi ikatan rata yaitu dengan menggunakan entalpi pembentukan standar dan entalpi atomisasi standar. 48

Contoh Soal 2 Diketahui data-data sbb : ΔH˚f CH 4(g) = -78, 8 k. J/mol ΔH˚f atom C(g) = +718, 4 k. J/mol ΔH˚f atom H(g) = 217, 9 k. J/mol Hitunglah energi ikatan C-H dalam molekul metana. 49

ΔH Reaksi Berdasarkan Energi Ikatan Reaksi kimia terjadi karena ada pemutusan ikatan dan pembentukan ikatan. Ikatanikatan pada reaktan akan putus dan terjadi ikatan baru pada produk. Oleh karena itu, perubahan entalpi dapat dicari dari selisih ΔH pemutusan ikatan dan ΔH pembentukan ikatan. ΔH = ΔH pemutusan ikatan – ΔH pembentukan ikatan 50

Contoh Soal 3 Dengan menggunakan tabel energi ikatan, hitunglah energi yang dibebaskan pada pembakaran 1 mol gas etana (C 2 H 6)! Catatan : Pada pemutusan ikatan diperlukan energi (ΔH = +). Pada pembentukan ikatan dilepaskan energi (ΔH = -) 51
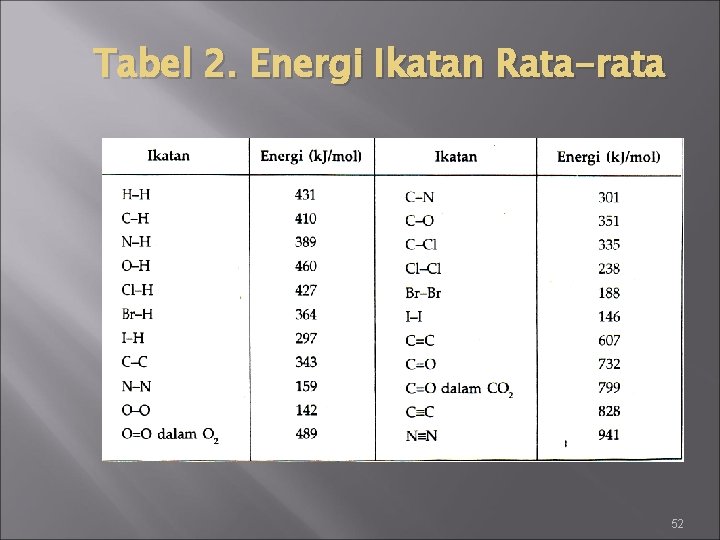
Tabel 2. Energi Ikatan Rata-rata 52

- Slides: 53