Termokimia adalah cabang Ilmu kimia yang mempelajari hubungan

Termokimia adalah : cabang Ilmu kimia yang mempelajari hubungan antara reaksi kimia dengan energi panas/kalor yang menyertainya

Sistim dan lingkungan �Setiap Proses kimia (reaksi kimia ) selalu disertai dengan perubahan energi �Energi yang menyertai reaksi kimia dipertukarkan antara sistim dan lingkungannya. �Sistim : segala sesuatu yang menjadi pusat perhatian kita �Lingkungan : semua yang ada diluar sistim. �Contoh : untuk mengamati kelarutan garam Na. Cl dalam air, maka kristan Na. Cl dimasukkan kedalam bejana yang berisi air �Dalam hal ini yang menjadi sistim adalah Kristal Na. Cl dan air, sedangkan lingkungan adalah bejana dan udara sekitarnya.
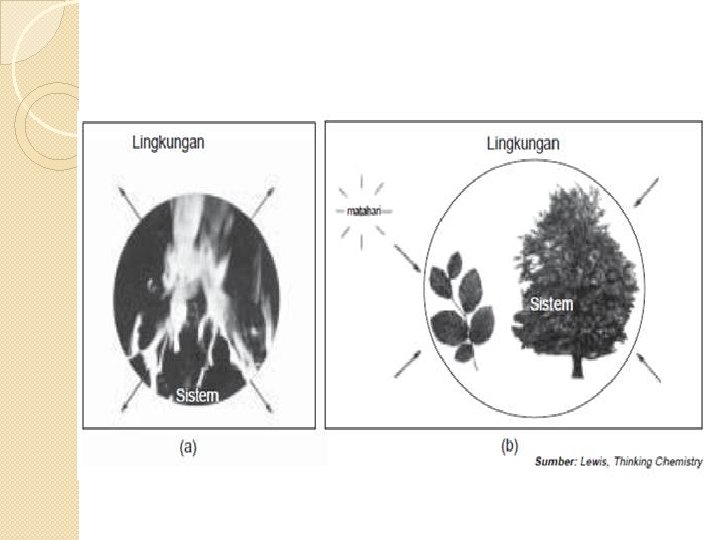

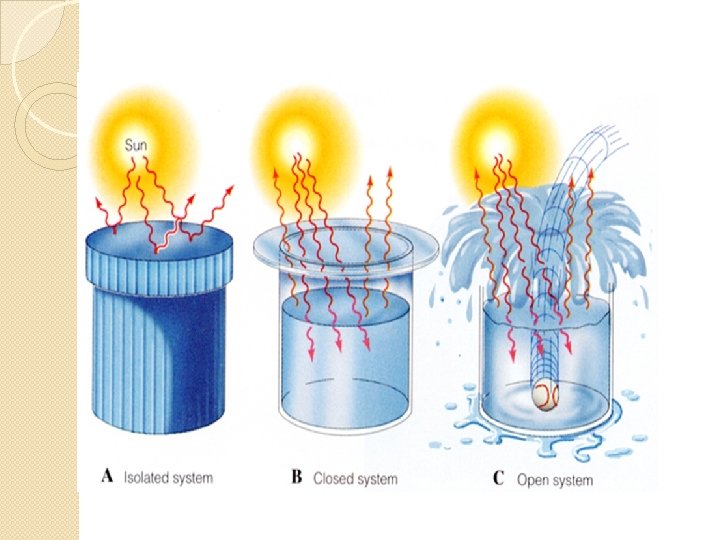
Sistim dapat dibedakan atas 3 : 1. Sistem terbuka : sistem dimana baik materi maupun energi dapat dipertukarkan dengan lingkungan. Misalnya teh panas dlm gelas akan melepaskan panas ke lingkungannya sehingga menjadi dingin. 2. Sistem tertutup : sistem dimana hanya dapat mengalami pertukaran energi dengan lingkungannya, sedangkan materi tidak dapat dipertukarkan. Misalnya teh panas dalam botol tertutup dapat melepas panas ke lingkungannya sehingga menjadi dingin, tapi volume air tetap. 1. Sistem terisolasi : sistem dimana baik materi maupun energi (panas) tidak dapat dipertukarkan ke lingkungan. Misalnya teh panas dalam termos, energi panas yang dikandung teh berpindah ke lingkungan dengan sangat lambat.

Proses yang terjadi dalam sistim dapat dibedakan atas 2 yaitu : 1. Proses Isotermal : terjadi perpindahan kalor antara sistim dan lingkungannya atau sebaliknya, sehingga suhu sistim tetap selama proses berlangsung 2. Proses adiabatik : antara sistim dan lingkungan tidak terjadi perpindahan kalor selama proses berlangsung

Azas kekekalan Energi • • Energi adalah kemampuan untuk melakukan kerja Setiap sistim memiliki energi. Beberapa bentuk energi antara lain : Energi kalor, energi kimia, energi listrik, energi cahaya, energi bunyi, energi mekanik dll. Suatu bentuk energi dapat berubah menjadi bentuk energi lain

• • • Energi Listrik Energi panas : pada setrika listrik Energi mekanik Energi Listrik : pada generator Listrik Energi Kimia Energi Listrik : pada accu (baterai basah ) Energi Listrik Energi Kimia : pada proses penyepuhan Dll



Perubahan energi dalam sistim terjadi karena sistim menerima atau melepaskan sejumlah kalor (q) dan menerima atau melakukan kerja (w), maka perubahan itu dinyatakan sebagai berikut : E = q + w Jika q negatif ( ) : sistim melepaskan kalor q positif ( ) : sistim menerima kalor w negatif ( ): sistim melakukan kerja w positif ( ) : sistim menerima kerja

Persamaan di atas merupakan pernyataan matematik dari Hukum Pertama Termodinamika yang berbunyi : Perubahan energi dalam (E) suatu sistim adalah jumlah panas (q) yang diserap atau dilepas dengan kerja (w) yang dilakukan atau di terima oleh sistim itu • Hukum ini sesuai dengan Hukum Kekekalan Energi yang berbunyi : Energi tidak dapat diciptakan dan tidak dapat dimusnahkan. • jika suatu energi hilang akan timbul energi dalam bentuk lain yang jumlahnya sama. •

• • • Jika selama proses berlangsung tidak terjadi perpindahan kalor dari sistim ke lingkungan atau sebaliknya (proses adiabatik) maka perubahan energi dalam sistim sama dengan jumlah kerja yang dilakukan atau diterima oleh sistim itu E = w Jika selama proses berlangsung tidak ada kerja yang dilakukan atau diterima (w=0), maka perubahan energi dalam sistim sama dengan jumlah panas yang di serap atau dilepas oleh sistim itu E = q Jika selama proses tidak terjadi perpindahan panas dan tidak ada kerja yang dilakukan, maka perubahan energi dalam sisitim sama dengan nol E = 0

Entalpi reaksi

• • • Q adalah selisih dari dua besaran (U + PV) yang merupakan fungsi keadaan. Fungsi keadaan yang baru ini disebut Entalpi dan diberi lambang H dari Heat Conten (Ingg) atau Enthalen (ger) = kandungan panas jadi H = U + PV Entalpi (H) adalah jumlah total bentuk energi yang dikandung oleh suatu sistim /zat Entalpi mutlak suatu sistim tidak dapat ditentukan, yang dapat ditentukan adalah perubahan entalpinya (∆H). perubahan entalpi sisitim adalah selisish antara entalpi hasil reaksi (akhir) dengan entalpi pereaksi (awal) ∆H = H 2 – H 1

umumnya proses kimia berlangsung pada tekanan tetap sehingga : Q = (U 2 – PV 2 ) – (U 1 – PV 1) maka Q = H 2 – H 1 atau ∆H = Qp Qp = kalor reaksi pada tekanan tetap • Jadi perubahan entalpi suatu sistim sama dengan kalor yang diserap atau dilepaskan oleh sistim pada tekanan tetap. • Jika suatu sistim membebaskan sebanyak Q joule kalor, maka entalpi sistim akan berkurang sebesar Q joule dan jika sistim menerima sebanyak Q joule kalor maka entalpi sistim akam bertambah sebesar Q joule Jadi : ►jika reaksi membebaskan kalor maka ∆H = -Qp ►jika reaksi menyerap kalor maka ∆H = +Qp •

Persamaan Termokimia adalah : Persamaan reaksi yang disertai dengan perubahan entalpinya (∆H) • Harga ∆H yang tertera dalam persamaan termokimia berhubungan erat dengan koefisien reaksi dan fase zat-zat yang terlibat dalam reaksi tersebut. Contoh : • Pembentukan 1 mol gas ammoniak dari gas Nitrogen dan gas Hidrogen pada suhu 25 o. C dan tekanan 1 atm dibebaskan kalor sebesar 46, 19 k. J • Pernyataan ini dapat dituliskan dalam bentuk persamaan termokimia sebagai berikut :

Reaksi Eksoterm adalah reaksi yang membebaskan kalor. Pembebasan kalor ditandai dengan naiknya suhu lingkungan Pembebasan kalor mengakibatkan kandungan energi (entalpi) sistim berkurang dari keadaan semula ( H 2 H 1 ), sehingga perubahan entalpi (∆H) sistim harganya negatif ( ) ∆H = H 2 – H 1 0
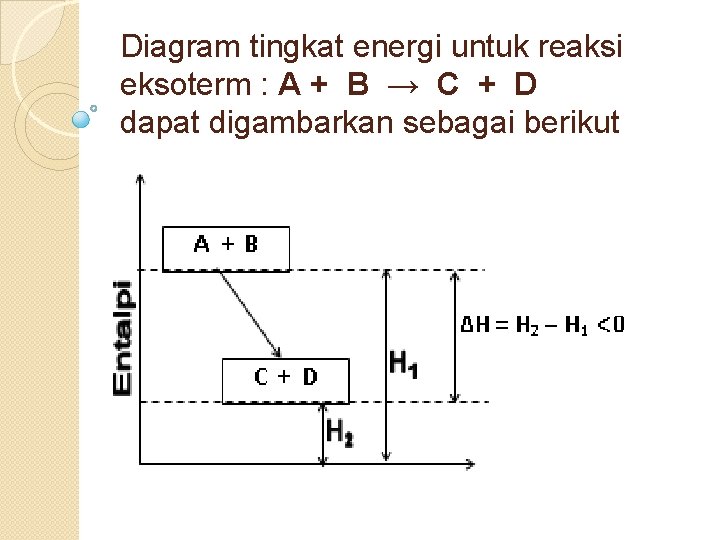
Diagram tingkat energi untuk reaksi eksoterm : A + B → C + D dapat digambarkan sebagai berikut

: contoh reaksi eksoterm 1. C 2 H 6(g) + 3½O 2(g) → 2 CO 2(g) + 3 H 2 O(g) + 212, 8 kkal atau C 2 H 6(g) + 3½O 2(g) → 2 CO 2(g) + 3 H 2 O(g) ∆H = - 212, 8 kkal 2. Ca. O(s) + H 2 O(l) → Ca(OH)2(s) + 39, 06 kkal atau Ca. O(s) + H 2 O(l) → Ca(OH)2(s) ∆H = - 39, 06 kkal

Reaksi endoterm adalah reaksi yang memerlukan/menyerap kalor Penyerapan kalor ditandai dengan turunnya suhu lingkungan Penyerapan kalor akan mengakibatkan kandungan kalor (entalpi) sistim lebih tinggi dari entalpi semula ( H 2 H 1), sehingga harga perubahan entalpi sistim adalah Positif ( ) ∆H = H 2 – H 1 0
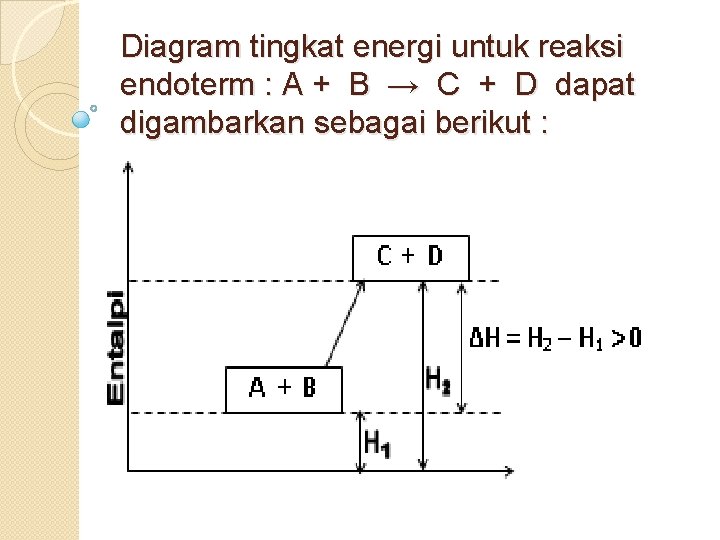
Diagram tingkat energi untuk reaksi endoterm : A + B → C + D dapat digambarkan sebagai berikut :

Contoh reaksi endoterm 1. Ba(OH)2(s)+2 NH 4 Cl(s) → Ba. Cl 2(s)+2 NH 3 (g)+2 H 2 O(l) -12, 68 kkal atau Ba(OH)2(s)+2 NH 4 Cl(s)→Ba. Cl 2(s)+2 NH 3(g)+2 H 2 O(l)∆H=+2, 68 kkal 2. 2 Na. HCO 3 → Na 2 CO 3 + CO 2 + H 2 O - 128, 4 k. J atau 2 Na. HCO 3 → Na 2 CO 3 + CO 2 + H 2 O ∆H = +128, 4 k. J

• • adalah : Perubahan entalpi yang menyertai suatu reaksi kimia pada suhu dan tekanan tertentu. Perubahan entalpi reaksi sangat tergantung pada suhu dan tekanan, oleh karena itu perlu ditetapkan suatu keadaan yang tetap sebagai standar. Berdasarkan kesepakatan, suhu 250 C (298 K) dan tekanan 1 atm (76 cm. Hg) ditetapkan sebagai keadaan sandar, karena pada suhu 250 C dan tekanan 1 atm umumnya zat memiliki bentuk yang paling stabil. Jadi perubahan entalpi suatu reaksi yang diukur pada suhu 250 C dan tekanan 1 atm disebut Perubahan Entalpi Standar yang diberi

Jenis-jenis perubahan entalpi standar 1. Entalpi Pembentukan Standar/ Standard Enthalpy Of Formation ( ∆Hf. O ) adalah Perubahan entalpi pada pembentukan 1 mol suatu zat / senyawa dari unsur-unsurnya pada keadaan standar ( suhu 25 o. C, tekanan 1 atm) misalnya pada pembentukan 1 mol gas CO 2 dari gas karbon dan gas oksigen pada suhu 25 o. C dan tekanan 1 atm dibebaskan kalor sebesar 94, 1 kkal. Jadi ∆Hf. O CO 2 = -94, 1 kkal C(s) + O 2(g) → CO 2(g) ∆HO = -94, 1 kkal

2. Entalpi Penguraian Standar/Standard Enthalpy of Decomposition (∆Hd. O ) Adalah : Perubahan entalpi pada penguraian 1 mol senyawa menjadi unsur-unsurnya pada keadaan standar ( suhu 25 o. C, dan tekanan 1 atm) Misalnya : Untuk menguraikan 1 mol gas CO menjadi gas

Hukum Lavoisier-Laplace "Jumlah kalor yang dilepaskan pada pembentukan 1 mol zat dari unsur-unsurya = jumlah kalor yang diperlukan untuk menguraikan zat tersebut menjadi unsur-unsur pembentuknya. " Artinya : Apabila reaksi dibalik maka tanda kalor yang terbentuk juga dibalik dari positif menjadi negatif atau sebaliknya Jadi : ∆Hfo = ∆Hdo Contoh: N 2(g) + 3 H 2(g) � 2 NH 3(g) ; � H = - 112 k. J 2 NH 3(g) � N 2(g) + 3 H 2(g) ; � H = + 112 k. J

3. Entalpi Pembakaran Standar/Standard Enthalpy of Combustion (∆HCO ) Adalah Perubahan entalpi pada pembakaran 1 mol unsur atau senyawa pada keadaan standar (suhu 25 o. C, dan tekanan 1 atm) Misalnya : Pada pembakaran 1 mol alkohol (C 2 H 5 OH) dibebaskan kalor sebesar 227 kkal Maka ∆HCO C 2 H 5 OH = 227 kkal/mol C 2 H 5 OH(l) + 3 O 2 → 2 CO 2 + 3 H 2 O ∆Ho = -128, 4 k. J

4. Entalpi Penetralan Standar/Standard Enthalpy of Netralisation (∆Hno) Adalah Perubahan entalpi pada penetralan asam atau basa yang menghasilkan 1 mol air pada keadaan standar (suhu 25 o. C, dan tekanan 1 atm) Misalnya : • Pada penetralan asam klorida oleh basa Na. OH yang menghasilkan 1 mol air dibebaskan kalor sebesar 13, 7 kkal • Maka ∆Hno Na. OH atau HCl = -13, 7 kkal/mol • Na. OH(aq) + HCl(aq) → Na. Cl(aq) + H 2 O(l) ∆Ho = -13, 7 kkal

5. Entalpi Pelarutan Standar/Standard Enthalpy of Solubility ( ∆HSo )

6. Entalpi Penguapan Standar/Standard Enthlpy of Vaporation (∆Hvapo) Adalah : Perubahan entalpi pada penguapan 1 mol zat cair menjadi gas sesuai titik didihnya pada keadaan standar (suhu 25 o. C, dan tekanan 1 atm) Misalnya Untuk menguapkan 1 mol air yang berwujud cair diperlukan kalor sebesar 44 k. J Maka ∆Hvapo H 2 O = +44 k. J/mol H 2 O(l) → H 2 O(g) ∆Ho = +44 k. J

7. Entalpi Pengatoman Standar/ Standard Enthalpy of Atomisation (∆Hato) adalah : Perubahan entalpi pada pembentukan 1 mol atom-atom unsur dalam fase gas pada keadaan standar (suhu 25 o. C, dan tekanan 1 atm) misalnya : Pada pembentukan 1 mol atom Karbon dalam fase gas pada keadaan standar diperlukan kalor sebesar 718, 4 k. J maka ∆Hato = + 718 k. J/mol C (s) → C (g) ∆Ho = + 718 k. J

8. Entalpi Peleburan Standar/ Standard Enthalpy of Fusion(∆Hfuso) Adalah : Perubahan entalpi pada peleburan 1 mol zat padat menjadi zat cair sesuai titik leburnya pada keadaan standar (suhu 25 o. C, dan tekanan 1 atm) Misalnya : Untuk melebur 1 mol air berwujud padat (es) menjadi cair diperlukan kalor sebesar 6, 01 k. J Maka ∆Hfuso H 2 O = +6, 01 k. J/mol H 2 O(s) → H 2 O(l) ∆Ho = +6, 01 k. J

Bersambung……. . ! �Sampai jumpa pada pelajaran berikutnya.
- Slides: 34