KONSEP DASAR IKATAN KIMIA 10292020 Kimia Dasar EvaZulfahYasser









- Slides: 11

KONSEP DASAR IKATAN KIMIA 10/29/2020 Kimia Dasar (Eva/Zulfah/Yasser) 1

Tujuan § Mempelajari ikatan kimia, struktur Lewis, dan aturan oktet. § Mempelajari ikatan kovalen dan kekuatannya. § Dapat menggambar struktur Lewis. § Mengetahui pengecualian dalam aturan oktet. 10/29/2020 Kimia Dasar (Eva/Zulfah/Yasser) 2

Soal-soal § Mengapa ketika garam dapur dilarutkan § § § dalam air dingin mudah larut, sedangkan gula sukar larut? Mengapa intan jauh lebih keras daripada grafit? Sebutkan macam-macam ikatan kimia, dan sebutkan sifat-sifatnya. Apakah perbedaan antara ikatan van der Waals dengan ikatan London. 10/29/2020 Kimia Dasar (Eva/Zulfah/Yasser) 3

§ Ikatan kimia: gaya yang menahan atom atau ion dalam senyawa § Ikatan kimia : 1. ikatan ion 2. ikatan kovalen 3. ikatan logam § Ikatan ion: gaya elektrostatik antara 2 ion yang berlawanan muatan. Logam cenderung melepas elektron dan membentuk kation, sementara nonlogam cenderung menerima elektron dan membentuk anion. § Ikatan kovalen: ikatan antara 2 atau lebih dengan konsep membagi elektron untuk dipakai bersama. 10/29/2020 Kimia Dasar (Eva/Zulfah/Yasser) 4

§ Ikatan logam: ikatan antar logam dimana § § § elektron valensi atom logam bebas untuk bergerak dalam struktur padatan logam. Struktur Lewis: simbol dimana elektron valensi dari atom atau ion digambarkan sebagai titik , dengan masing-masing titik mewakili satu elektron. Atom cenderung untuk melepas, menambah, atau berbagi elektron untuk mencapai konfigurasi elektron gas mulia. Aturan oktet: atom cenderung untuk melepas, menambah, atau berbagi elektron sampai atom tersebut memiliki 8 elektron valensi. 10/29/2020 Kimia Dasar (Eva/Zulfah/Yasser) 5

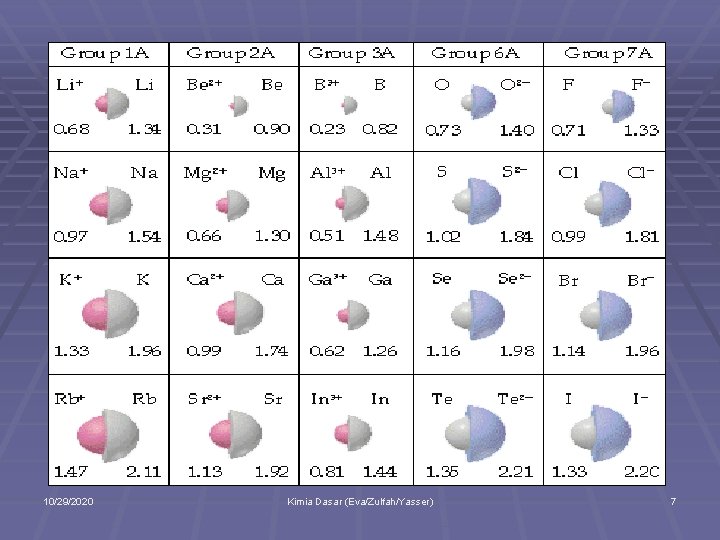
Ukuran Ion § Ketika atom kehilangan elektron, kation yang § § § terbentuk memiliki ukuran yang lebih kecil daripada atom netralnya. Mengapa? Ketika atom mendapat elektron, anion yang terbentuk memiliki ukuran yang lebih besar daripada atom netralnya. Mengapa? Isoelektron: atom, ion, atau molekul yang memiliki jumlah elektron yang sama. Pada deretan atom isoelektronik, seperti Li+, Be 2+, B 3+, jari-jarinya berkurang dari kiri ke kanan. Mengapa? 10/29/2020 Kimia Dasar (Eva/Zulfah/Yasser) 6

10/29/2020 Kimia Dasar (Eva/Zulfah/Yasser) 7

Perkecualian Terhadap Aturan Oktet Tipe- tipe perkecualian: c Molekul dengan jumlah elektron yang ganjil, contoh: NO Distribusikan elektron terlebih dahulu pada atom yang paling elektronegatif Oksigen memiliki struktur oktet lengkap, sementara nitrogen tidak 10/29/2020 Kimia Dasar (Eva/Zulfah/Yasser) 8

c. Molekul dimana sebuah atomnya memiliki elektron kurang dari sebuah oktet, contoh: BF 3, BF 3 -NH 3 c. Molekul dimana sebuah atomnya memiliki elektron lebih dari sebuah oktet, contoh: SF 6 10/29/2020 Kimia Dasar (Eva/Zulfah/Yasser) 9

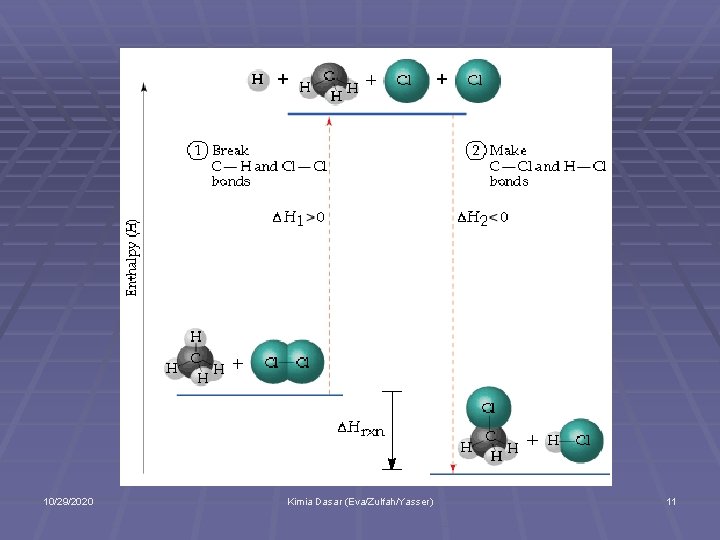
Kekuatan Ikatan Kovalen § Kekuatan ikatan diindikasikan dengan banyaknya energi yang diperlukan untuk memutuskan ikatan tersebut. § Entalpi ikatan: energi yang diperlukan untuk memutuskan 1 mol ikatan. § Makin panjang ikatan kovalen, makin kecil energi ikatannya. Mengapa? 10/29/2020 Kimia Dasar (Eva/Zulfah/Yasser) 10

10/29/2020 Kimia Dasar (Eva/Zulfah/Yasser) 11