Hemiski Reakcii Hemiskite reakcii se procesi vo koi




































- Slides: 46

Hemiski Reakcii Hemiskite reakcii se procesi vo koi nastanuvaat hemiski promeni na elementite ili soedinenijata {to se u~esnici vo toj proces. -Deka vo eden sistem se odviva hemiska reakcija najlesno }e prepoznaeme ako vo tekot na procesot se izdvojuva gas, se promenuva bojata na rastvorot ili se dobiva cvrst talog-toa se vizuelni hemiski promeni -Vo hemiskite reakcii imame supstanci {to se prisutni na po~etokot na hemiskata reakcija i tie se narekuvaat REAKTANTI, i supstanci {to se dobivaat na krajot od hemiskata reakcija, tie se narekuvaat PRODUKTI

Hemiski Reakcii • Supstanci {to reagiraat na po~etokot na reakcijata-reaktanti • Supstanci {to se dobivaat pri hemiskata reakcija-produkti • Reaktantite pretrpuvaat hemiski promeni i pritoa se dobivaat produkti-toa e hemiska reakcija saharoza To. C---> jaglerod + voda reaktant produkti reaktant produkt

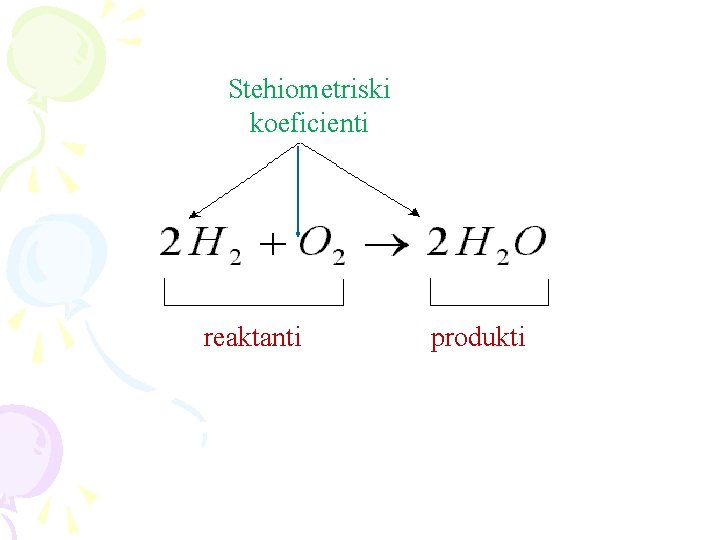
Da zapomnime: Hemiskite reakcii se opi{uvaat preku hemiski ravenki. Od levata strana na hemiskata ravenka se pi{uvaat hemiskite formuli ili simboli za reaktantite, a od desnata strana se pi{uvaat hemiskite formuli za produktite. Kaj hemiskite ravenki, brojot na soodvetnite atomi od levata i desnata strana na ravenkata mora da bide identi~en. Matemati~ki ka`uvame deka hemiskite ravenki mora da bidat izedna~eni. Za taa cel, pred hemiskite formuli i simboli na reaktantite i produktite se stavaat soodvetni stehiometriski koeficienti. Stehiometriskite koeficienti ni ka`uvaat kolku molovi od dadenata supstanca u~estvuvaat vo hemiskata reakcija. Primer: reakcija na dobivawe na voda od vodorod i kislorod. 2 H 2 + O 2 = 2 H 2 O Hemiskata ravenka ni ka`uva deka vo ovaa reakcija 2 mola vodorod reagiraat so 1 mol kislorod i pritoa se dobivaat 2 mola na voda.

Stehiometriski koeficienti reaktanti produkti

Vidovi na hemiski reakcii • Reakcii na kombinirawe ili sinteza • Reakcii na razgraduvawe • Reakcii so precipitacija (formirawe talog) (toa se reakcii na istisnuvawe) • Reakcii na neutralizacija – kiselini – bazi Reakcii na formirawe na kompleksni soedinenija • Oksido-redukciski reakcii

Reakcii na sinteza -formirawe na novo soedinenie od poednostavni soedinenija ili elementi Primer: 2 H 2 + O 2 = 2 H 2 O Reakcii na razgraduvawe (dekompozicija) -razgraduvawe na edno slo`eno soedinenie na sostavnite komponenti od koi toa soedinenie e izgradeno Primer: NH 4 Cl (zagrevawe) = NH 3 + HCl

Reakcii na precipitacija (ili reakcii na jonska izmena) -naj~esto se prosledeni so formirawe na talog -se reakcii koga od dve soedinenija (naj~esto od jonski tip) {to se vo rastvor se dobiva novo soedinenie koe {to e vo vid na te{ko rastvorliv talog (precipitacija), ili nov tip na jonsko soedinenie (jonska izmena) 1. Primer za reakcija na precipitacija: Ag. NO 3 + Na. Cl = Ag. Cl + Na. NO 3 Bel talog 2. Primer za reakcija na jonska izmena

Reakcii na neutralizacija: Se reakcii pome|u kiselini i bazi pri koi kako produkti se dobivaat sol i voda • Kiselini -se – Supstanci {to davaat H+ joni koga se rastvoreni vo voda Bazi -se Supstanci {to davaat OH- joni koga se rastvoreni vo voda

kiselina + baza ---> “sol” + voda H 2 SO 4 + 2 KOH ---> K 2 SO 4 + 2 H 2 O Zabele{ka: Koga se nao|aat rastvoreni vo voda, najgolem del od kiselinite bazite i solite ne opstojuvaat kako molekuli, tuku tie se disocirani na joni. Onie kiselini bazi i soli {to vo voden ratsvor se potpolno disocirani na joni se nare~eni JAKI kiselini i jaki bazi. HCl (voda) ---> H+ + Cl. Na. OH (voda) ---> Na+ + OHK 2 SO 4 (voda) ---> 2 K+ + SO 42 - Procesot na razlo`uvawe na edno soedinenie na joni vo prisustvo na voda se vika disocija

Najgolem del od kiselinite, bazite i solite se Elektroliti, a toa zna~i • Nivnite vodeni rastvori sproveduvaat elektri~na energija poradi prisustvoto na joni • Jak elektrolit-celosno joniziran vo rastvorite • Slab elektrolit -delumno joniziran vo rastvorite • Ne-elektroliti -nejonski rastvori, postojat kako rastvoreni molekuli vo voda, primer Alkohol vo voda

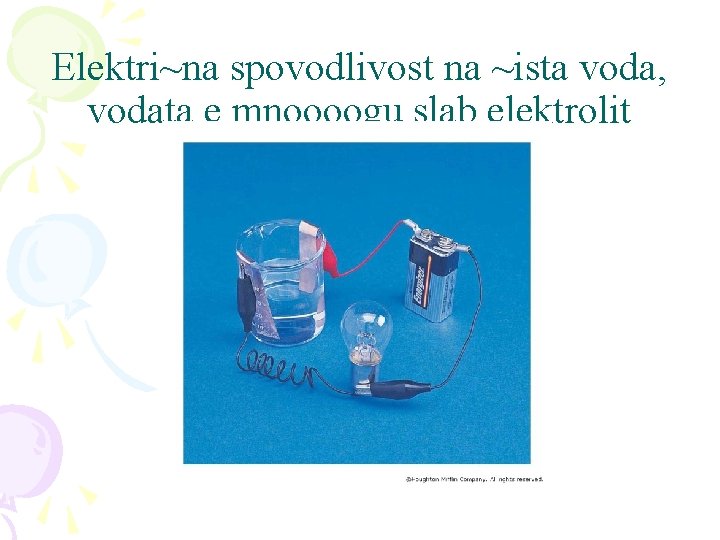
Elektri~na spovodlivost na ~ista voda, vodata e mnoooogu slab elektrolit

Jak Elektrolit-HCl

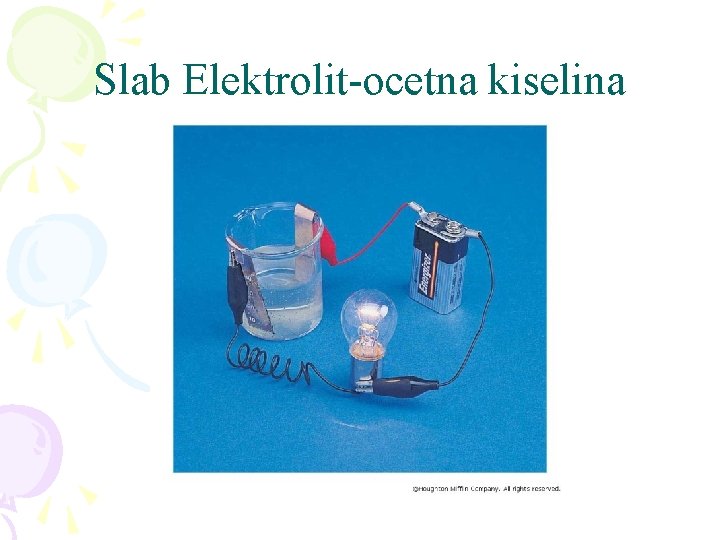
Slab Elektrolit-ocetna kiselina

Reakcii na formirawe na kompleksni soedinenija Kompleksnite soedinenija (naj~esto se oboeni)se poseben tip na hemiski supstancii koi poka`uvaat isklu~itelno golema stabilnost i te{ko disociraat vo vodeni rastvori Primer: 6 KCN + Fe. Cl 3 ---> K 3[Fe(CN)6] + 3 KCl kalium heksacijanoferat (III)

Oksido-redukciski reakcii ili REDOKS Reakcii

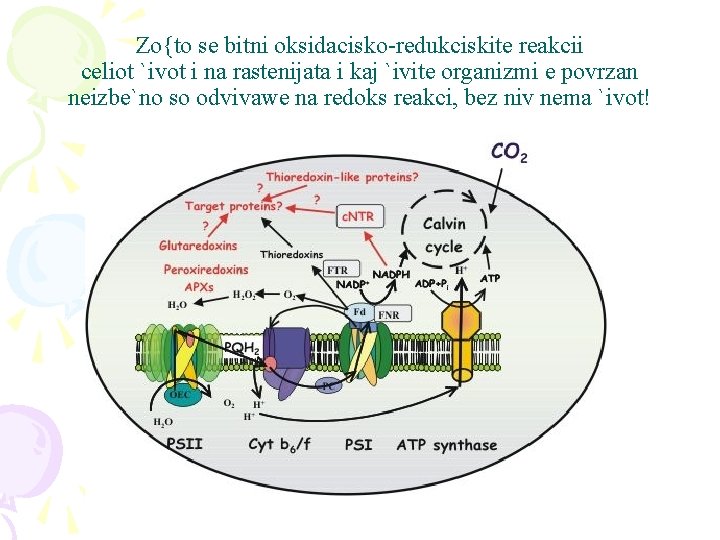
Zo{to se bitni oksido redukciskite reakcii? Eve samo nekoi od pozna~ajnite redoks procesi za da imame podobra pretstava -Di{eweto -Procesite na korozija -Goreweto na gorivata -Reakciite vo `ivite organizmi pri sintezata na ATP i sintezata na kislorod vo rastenijata -Dejstvoto na lekovite vrz raznite mikroorganizmi pri raznite bolesti -Dejstvoto na pesticidite vrz {tetnicite -. . .

[to se toa oksido-redukciski reakcii? Za razlika od jonskite reakcii, ili reakciite na neutralizacija, kaj koi ne doa|a do promena na valentnosta na u~esnicite vo hemiskite reakcii, kaj oksidoredukciskite reakcii doa|a do promena na valentnosta na najmalku dva atomi od u~esnicite vo hemiskata reakcija. -Primer • 2 Fe 3+ + Sn 2+ -> 2 Fe 2+ + Sn 4+ -Vo ovaa reakcija `elezo (iii) + kalaj (ii) reagiraat razmenuvaat elektroni pritao se dobivaat kako produkti `elezo (ii) + kalaj (iv). Vkupniot polne` od levata i desnata strana mora da bide ednakov (vo slu~ajov toj e 8+). -Zna~i kaj oksido-redukciskite reakcii doa|a do RAZMENA (primawe i oddavawe) na elektroni pome|u reaktanite vo taa hemiska reakcija

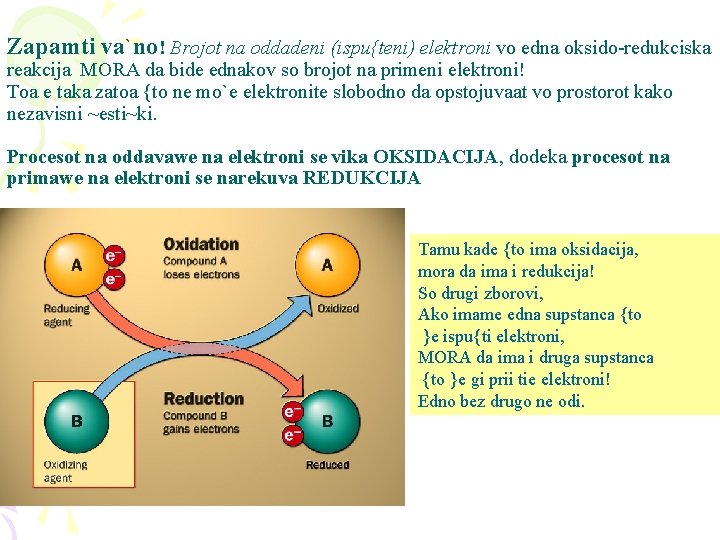
Zapamti va`no! Brojot na oddadeni (ispu{teni) elektroni vo edna oksido-redukciska reakcija MORA da bide ednakov so brojot na primeni elektroni! Toa e taka zatoa {to ne mo`e elektronite slobodno da opstojuvaat vo prostorot kako nezavisni ~esti~ki. Procesot na oddavawe na elektroni se vika OKSIDACIJA, dodeka procesot na primawe na elektroni se narekuva REDUKCIJA Tamu kade {to ima oksidacija, mora da ima i redukcija! So drugi zborovi, Ako imame edna supstanca {to }e ispu{ti elektroni, MORA da ima i druga supstanca {to }e gi prii tie elektroni! Edno bez drugo ne odi.

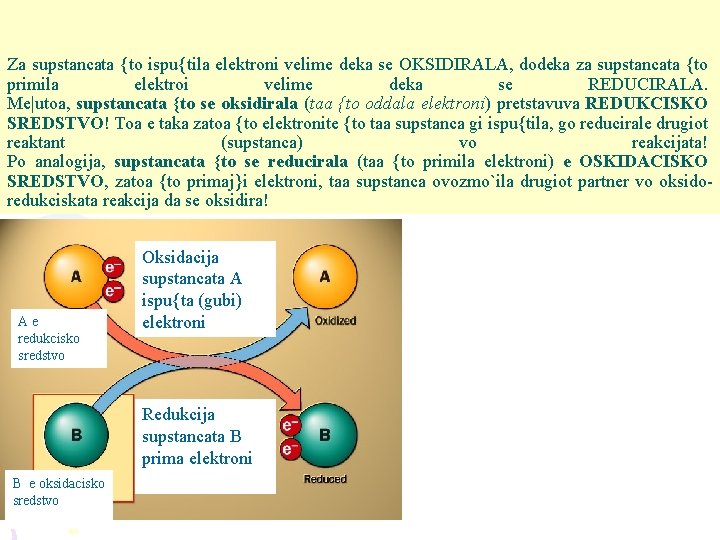
Za supstancata {to ispu{tila elektroni velime deka se OKSIDIRALA, dodeka za supstancata {to primila elektroi velime deka se REDUCIRALA. Me|utoa, supstancata {to se oksidirala (taa {to oddala elektroni) pretstavuva REDUKCISKO SREDSTVO! Toa e taka zatoa {to elektronite {to taa supstanca gi ispu{tila, go reducirale drugiot reaktant (supstanca) vo reakcijata! Po analogija, supstancata {to se reducirala (taa {to primila elektroni) e OSKIDACISKO SREDSTVO, zatoa {to primaj}i elektroni, taa supstanca ovozmo`ila drugiot partner vo oksidoredukciskata reakcija da se oksidira! Ae redukcisko sredstvo Oksidacija supstancata A ispu{ta (gubi) elektroni Redukcija supstancata B prima elektroni B e oksidacisko sredstvo

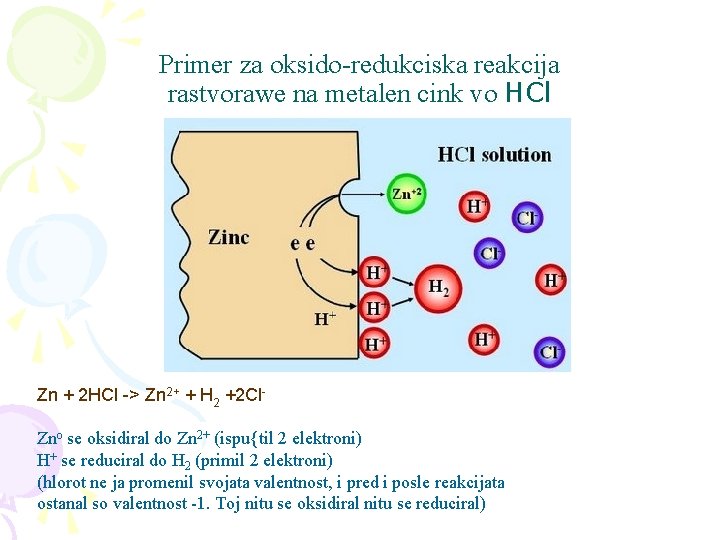
Primer za oksido-redukciska reakcija rastvorawe na metalen cink vo HCl Zn + 2 HCl -> Zn 2+ + H 2 +2 Cl. Zno se oksidiral do Zn 2+ (ispu{til 2 elektroni) H+ se reduciral do H 2 (primil 2 elektroni) (hlorot ne ja promenil svojata valentnost, i pred i posle reakcijata ostanal so valentnost -1. Toj nitu se oksidiral nitu se reduciral)

Drug primer za oksido-redukciska reakcijacinkova plo~ka potopena vo rastvor na bakarni joni

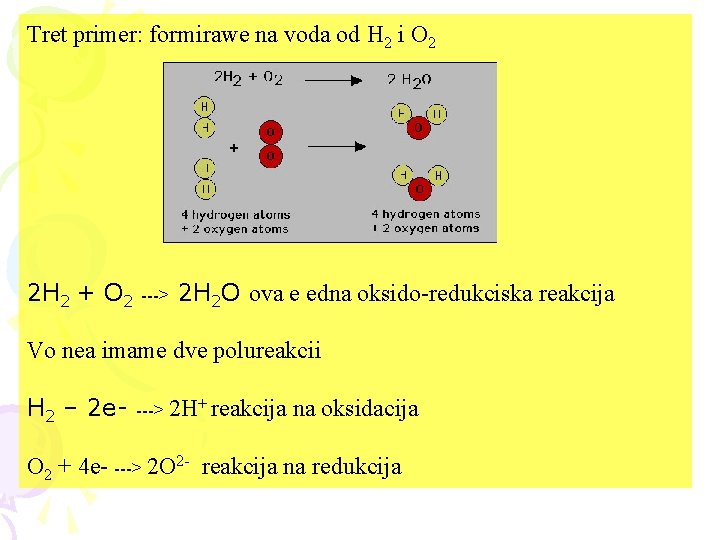
Tret primer: formirawe na voda od H 2 i O 2 2 H 2 + O 2 ---> 2 H 2 O ova e edna oksido-redukciska reakcija Vo nea imame dve polureakcii H 2 – 2 e- ---> 2 H+ reakcija na oksidacija O 2 + 4 e- ---> 2 O 2 - reakcija na redukcija

Izramnuvawe na oksido-redukciskite ravenki -Pravila 1. Valentnosta na sekoj element vo slobodna (atomarna ) sostojba e NULA 2. Koga e vo soedinenija, kislorodot ima (naj~esto) valentnost -2 3. Koga e svrzan vo soedinenija, vodorot ima (naj~esto( valentnost +1 4. Halogenite elementi koga se svrzani imaat valentnost od -1; 5. Koga se svrzani vo soedinenija, alkalnite metali (Na, K, Cs, imaat valentnost +1, a zemnoalkalnite (Mg, Ca, Sr +2) 6. Pri izramnuvawe na redoks reakciite, najprvo gi pi{uvame valentnite broevi na site reaktanti i produkti, i potoa gledame koi reaktantite si gi promenile svoite valentnosti. Potoa pravime ednostavna matemati~ka operacija so cel da vidime kolkav e brojot na ispu{teni i primeni elektroni. Toa }e ne dovede do situacija kako polesno matemati~ki da ja izramnime ravenkata.

Primer za izramnuvawe na redoks reakcii -Redoks reakcija od najednostaven vid-reagirawe na metalen natrium so gasovit hlor, oksidoredukcisko izramnuvawe • 2 Nao + Cl 2 o = 2 Na+1 Cl-1 • Nao -1 e => Na+1 • Cl 2 o +2 e => 2 Cl-1 2 2 1 Najmal zaedni~ki sodr`atel za 2 i za 1 e 2

Primeri za redoks reakcii-da se izedna~at • Cu. S + HNO 3 -> Cu SO 4 + NO + H 2 O • Fe + Cu. Cl 2 -> Fe. Cl 2 + Cu • H 2 + O 2 -> H 2 O

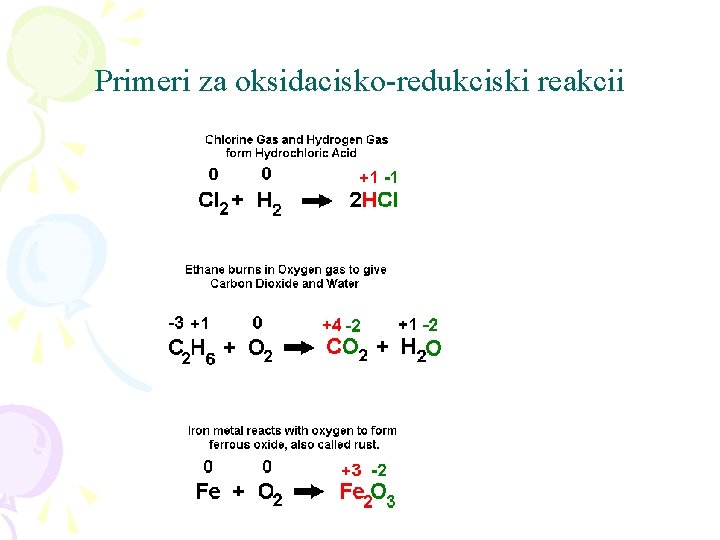
Primeri za oksidacisko-redukciski reakcii

Zo{to se bitni oksidacisko-redukciskite reakcii celiot `ivot i na rastenijata i kaj `ivite organizmi e povrzan neizbe`no so odvivawe na redoks reakci, bez niv nema `ivot!


Identify the oxidizing agent in the reaction: 2 Al(s) + 6 H+ ==> 2 Al 3+(aq) + 3 H 2(g) Al, H+, Al 3+, H 2 Identify the oxidizing agent in the reaction:

Oxidation States Rules for Assigning Oxidation States 1. zero for uncombined element 2. charge on monatomic ion 3. F is always -1; other halogens -1 except when combined with more electronegative halogen or oxygen

Oxidation States Rules for Assigning Oxidation States 4. H is +1 except in metal hydrides, where H is -1 5. O is -2 except when combined with F (then +1 or +2) or in peroxides, -1. 6. sum of oxidation states equals charge on ion or molecule

Oxidation State What is the oxidation state of S in H 2 SO 4? • H => +1 • O => -2 • neutral compound, thus sum equals zero • 4 O => 4*-2 = -8 • 2 H => 2*+1 = +2 • 0 = +2 + (x) + (-8) x = +6

Oxidation State What is the oxidation state of Cl in HCl. O 4? • H => +1 • O => -2 • neutral compound, thus sum equals zero • 4 O => 4*-2 = -8 • H => 1*+1 = +1 • 0 = +1 + (y) + (-8) y = +7

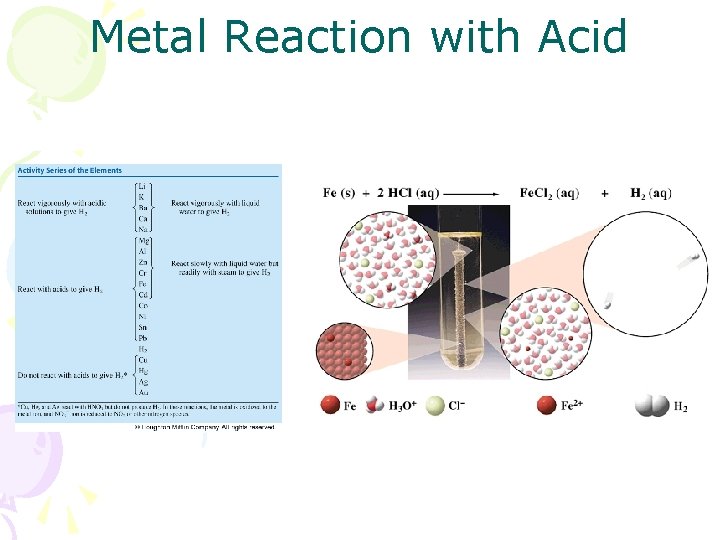
Activity Series of Metals • Highest metal in series is the most reactive • A reactive metal will react with ions of less reactive metal to produce ions of reactive metal and atoms of the less reactive metal

Metal Reaction with Acid

Single Displacement

2 Cu(s) + O 2 (g) ---> 2 Cu. O(s) The oxidation number of copper in the product is Cu(0), Cu(II) In the reaction, copper metal is reduced, oxidized, unchanged in oxidation state

Molarity The number of moles of solute per liter of solution. molarity => M moles of solute M = ---------liter of units => molar = solution moles/liter = M

EXAMPLE: Lye, which is sodium hydroxide, can be neutralized by sulfuric acid. How many milliliters of 0. 200 M H 2 SO 4 are needed to react completely with 25. 0 m. L of 0. 400 M Na. OH? 2 Na. OH(aq) + H 2 SO 4(aq) -----> Na 2 SO 4(aq) + 2 H 2 O

EXAMPLE: Lye, which is sodium hydroxide, can be neutralized by sulfuric acid. How many milliliters of 0. 200 M H 2 SO 4 are needed to react completely with 25. 0 m. L of 0. 400 M Na. OH? 2 Na. OH(aq) + H 2 SO 4(aq) -----> Na 2 SO 4(aq) + 2 H 2 O (25. 0 m. L Na. OH) #m. L H 2 SO 4 = -----------

EXAMPLE: Lye, which is sodium hydroxide, can be neutralized by sulfuric acid. How many milliliters of 0. 200 M H 2 SO 4 are needed to react completely with 25. 0 m. L of 0. 400 M Na. OH? 2 Na. OH(aq) + H 2 SO 4(aq) -----> Na 2 SO 4(aq) + 2 H 2 O (25. 0 m. L Na. OH) (0. 400 mol Na. OH) #m. L --- H 2 SO 4 = ---------------------(1 L Na. OH)

EXAMPLE: Lye, which is sodium hydroxide, can be neutralized by sulfuric acid. How many milliliters of 0. 200 M H 2 SO 4 are needed to react completely with 25. 0 m. L of 0. 400 M Na. OH? 2 Na. OH(aq) + H 2 SO 4(aq) -----> Na 2 SO 4(aq) + 2 H 2 O (25. 0 m. L Na. OH) (0. 400 mol Na. OH)(1 L) #m. L H 2 SO 4 = ---------------------------(1 L Na. OH) (1000 m. L)

EXAMPLE: Lye, which is sodium hydroxide, can be neutralized by sulfuric acid. How many milliliters of 0. 200 M H 2 SO 4 are needed to react completely with 25. 0 m. L of 0. 400 M Na. OH? 2 Na. OH(aq) + H 2 SO 4(aq) -----> Na 2 SO 4(aq) + 2 H 2 O (25. 0) (0. 400 mol Na. OH)(1) (1 mol H 2 SO 4) #m. L H 2 SO 4 = --------------------------(1) (1000) (2 mol Na. OH)

EXAMPLE: Lye, which is sodium hydroxide, can be neutralized by sulfuric acid. How many milliliters of 0. 200 M H 2 SO 4 are needed to react completely with 25. 0 m. L of 0. 400 M Na. OH? 2 Na. OH(aq) + H 2 SO 4(aq) -----> Na 2 SO 4(aq) + 2 H 2 O (25. 0)(0. 400)(1 mol H 2 SO 4)(1000 m. L H 2 SO 4) #m. L H 2 SO 4 = ---------------------------(1) (1000) (2) (0. 200 mol H 2 SO 4)

EXAMPLE: Lye, which is sodium hydroxide, can be neutralized by sulfuric acid. How many milliliters of 0. 200 M H 2 SO 4 are needed to react completely with 25. 0 m. L of 0. 400 M Na. OH? 2 Na. OH(aq) + H 2 SO 4(aq) -----> Na 2 SO 4(aq) + 2 H 2 O (25. 0)(0. 400)(1)(1000 m. L H 2 SO 4) #m. L H 2 SO 4 = ---------------------(1) (1000) (2) (0. 200)

EXAMPLE: Lye, which is sodium hydroxide, can be neutralized by sulfuric acid. How many milliliters of 0. 200 M H 2 SO 4 are needed to react completely with 25. 0 m. L of 0. 400 M Na. OH? 2 Na. OH(aq) + H 2 SO 4(aq) -----> Na 2 SO 4(aq) + 2 H 2 O (25. 0)(0. 400)(1)(1000 m. L H 2 SO 4) #m. L H 2 SO 4 = ---------------------(1) (1000) (2) (0. 200) = 25. 0 m. L H 2 SO 4