Gli atomi e le molecole IN NATURA ESISTONO
















- Slides: 26


Gli atomi e le molecole • IN NATURA ESISTONO 92 PARTICELLE ELEMENTARI, DETTE ATOMI , CHE COSTITUISCONO L’UNITÀ STRUTTURALE PIÙ PICCOLA DELLA MATERIA. • GLI ATOMI SONO COSTITUITI DA UN NUCLEO, NEL QUALE SI TROVANO I PROTONI (PARTICELLE CARICHE POSITIVAMENTE) E I NEUTRONI ( CHE SONO NEUTRI, CIOÈ SENZA CARICA), ATTORNO AL QUALE IN VARIE POSIZIONI ORBITANO GLI ELETTRONI (PARTICELLE MOLTO PIÙ PICCOLE DELLE PRECEDENTI E CARICHE NEGATIVAMENTE). DATO CHE IL NUMERO DELLE CARICHE NEGATIVE È UGUALE A QUELLO DELLE CARICHE POSITIVE, GLI ATOMI RISULTANO ELETTRICAMENTE NEUTRI.

Gli atomi e le molecole • LA MATERIA SI FORMA CON LA STESSA LOGICA CHE PRESIEDE AL GIOCO DELLE COSTRUZIONI DOVE, A PARTIRE DA ALCUNE TIPOLOGIE LIMITATE DI MATTONCINI E CON UN PO’ DI FANTASIA, È POSSIBILE CREARE MOLTISSIMI OGGETTI. • ALLO STESSO MODO COMBINANDOSI FRA LORO, GLI ATOMI DANNO LUOGO ALLE MOLECOLE DI TUTTE LE SOSTANZE PRESENTI IN NATURA. IL LAVORO NECESSARIO PER SEPARARE DUE MOLECOLE PUÒ ESSERE MAGGIORE O MINORE A SECONDA DELL’ENERGIA, DETTA ENERGIA DI LEGAME, CHE LE TIENE INSIEME. L’ENERGIA DI LEGAME ESPRIME IL LAVORO CHE UNA FORZA DEVE COMPIERE PER SOTTRARRE UNA MOLECOLA ALL’ATTRAZIONE DELLA MOLECOLA VICINA.


L'ATOMO NELLA FILOSOFIA GRECA V SECOLO A. C. I FILOSOFI GRECI LEUCIPPO, DEMOCRITO ED EPICURO RIBADISCONO CHE IL NASCERE NON É CHE UN "AGGREGARSI DI COSE CHE SONO", E IL MORIRE UN "DISGREGARSI”. ATTRIBUENDO ALLE PARTICELLE ULTIME DELLA MATERIA TERMINE ATOMO (DAL GRECO ÀTOMOS: NON-DIVISIBILE) NON PERCETTIBILE CON I SENSI, MA SOLO CON L'INTELLIGENZA. L'ATOMO VIENE PENSATO COME "PIENO“, SI SUPPONE NECESSARIAMENTE IL VUOTO, SENZA VUOTO GLI ATOMI NON POTREBBERO DIFFERENZIARSI E NEMMENO MUOVERSI. LE TRASFORMAZIONI DELLE SOSTANZE VENGONO SPIEGATE IPOTIZZANDO MOVIMENTO. CHE GLI ATOMI SONO IN CONTINUO

L'ATOMO NEL MEDIOEVO E RINASCIMENTO DOMINATA DALLE IDEE DI ARISTOTELE, LA MATERIA COMPOSTA IN PROPORZIONI VARIABILI DA E’ QUATTRO ELEMENTI FONDAMENTALI E DI QUATTRO QUALITA’. ELEMENTI QUALITA’ TERRA SECCA-FREDDA ARIA UMIDA-CALDA ACQUA FREDDA–UMIDA FUOCO CALDO-SECCO SEGUE UN LUNGO PERIODO, CHE SI ESTENDE FINO AL XVI SECOLO, E DURANTE IL QUALE, IN APPLICAZIONE DELLA TEORIA DI ARISTOTELE PIÚ O MENO RIMANEGGIATA, CONTINUA LA VANA RICERCA DELLA "PIETRA FILOSOFALE" ; É IL PERIODO DELL'ALCHIMIA.

L’ATOMO DAL 1600 AL 1850 SI PRESUME ESISTENZA DI PIU’ ELEMENTI IL CHIMICO ANTOINE LAVOISIER INDIVIDUA UN NUMERO ABBASTANZA NUTRITO DI ELEMENTI. JOHN DALTON, INSEGNANTE ELEMENTARE, NEL TEMPO SCIENZE LIBERO NATURALI SI DEDICAVA RITENEVA CHE ALLE GLI ATOMI FOSSERO DOTATI DI GANCI CHE LI TENEVANO UNITI, ATTRIBUIVA A CIASCUN ATOMO OLTRE CHE UNA RAPPRESENTAZIONE SIMBOLICA ANCHE UN PESO. NEL 1850 PUBBLICO’ UNA TABELLA CHE IN SEGUITO VENNE ESTESA E MIGLIORATA.

L'ATOMO DAL 1850 AL 1900 NEL 1897 IL FRANCESE JOHN JOSEPH THOMSON ERA RIUSCITO AD IDENTIFICARE L’ELETTRONE ED ESPOSE IL PRIMO MODELLO ATOMICO: IPOTIZZO’ CHE L’ATOMO AVESSE UNA STRUTTURA OMOGENEA, CON LA MASSA E LA CARICA POSITIVA DISTRIBUITE UNIFORMEMENTE IN TUTTO L’ATOMO ED INSERITI ALL’INTERNO GLI ELETTRONI.

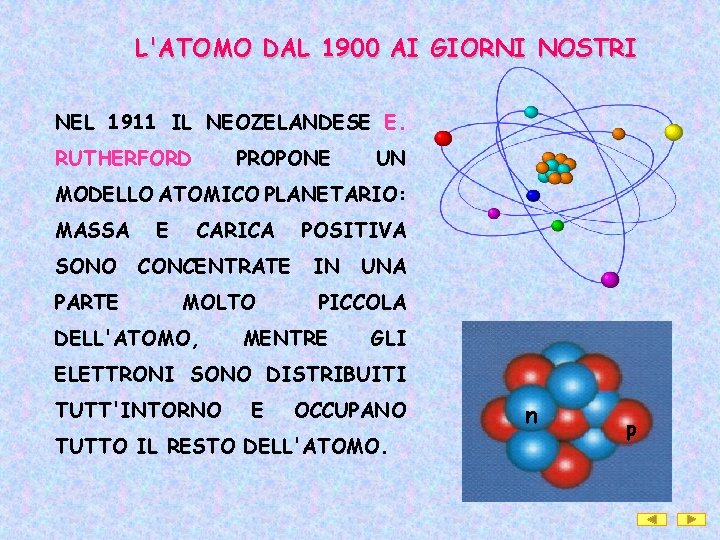
L'ATOMO DAL 1900 AI GIORNI NOSTRI NEL 1911 IL NEOZELANDESE E. RUTHERFORD PROPONE UN MODELLO ATOMICO PLANETARIO: MASSA E CARICA SONO CONCENTRATE PARTE MOLTO DELL'ATOMO, POSITIVA IN UNA PICCOLA MENTRE GLI ELETTRONI SONO DISTRIBUITI TUTT'INTORNO E OCCUPANO TUTTO IL RESTO DELL'ATOMO. n p

NEL 1913 IL DANESE N. BOHR ESPONE UN NUOVO MODELLO ATOMICO, SECONDO IL QUALE GLI ELETTRONI POSSONO MUOVERSI, SENZA IRRAGIARE, SU ORBITE CIRCOLARI STAZIONARIE. IL SUO MODELLO É SUCCESSIVAMENTE PERFEZIONATO DAL TEDESCO A. SOMMERFELD, CHE IPOTIZZÓ LA FORMA ELITTICA DELLE ORBITE PERMESSE.

DURANTE GLI ANNI ‘ 20 GRAZIE AL CONTRIBUTO DI L. V. DE BROGLIE, N. BOHR, W. PAULI, W. HEISEMBERG, E. SCHROEDINGER LA STRUTTURA DELL'ATOMO VIENE INTERPRETATA SECONDO IL MODELLO, TUTT'OGGI ACCETTATO COSTITUITA DA: PROTONI (DOTATI DI CARICA POSITIVA), NEUTRONI (ELETTRICAMENTE NEUTRI) ED ELETTRONI (DOTATI DI CARICA NEGATIVA). L. V. DE BROGLIE W. HEISEMBERG E. SCHROEDINGER N. BOHR W. PAULI

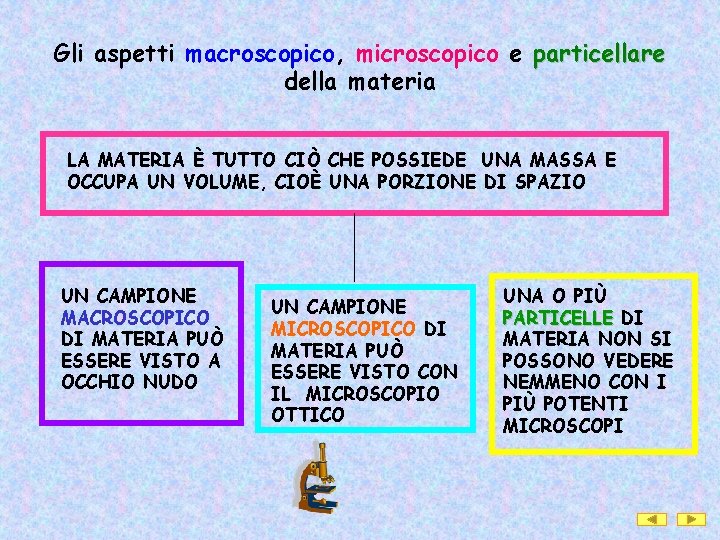
Gli aspetti macroscopico, microscopico e particellare della materia LA MATERIA È TUTTO CIÒ CHE POSSIEDE UNA MASSA E OCCUPA UN VOLUME, CIOÈ UNA PORZIONE DI SPAZIO UN CAMPIONE MACROSCOPICO DI MATERIA PUÒ ESSERE VISTO A OCCHIO NUDO UN CAMPIONE MICROSCOPICO DI MATERIA PUÒ ESSERE VISTO CON IL MICROSCOPIO OTTICO UNA O PIÙ PARTICELLE DI MATERIA NON SI POSSONO VEDERE NEMMENO CON I PIÙ POTENTI MICROSCOPI

Gli stati della materia • A LIVELLO MACROSCOPICO LE SOSTANZE POSSONO ASSUMERE TRE STATI : SOLIDO, LIQUIDO E AERIFORME. 1. LO STATO SOLIDO HA UNA FORMA È UN VOLUME PROPRIO (UN LINGOTTO D’ORO NON MODIFICA LE SUE CARATTERISTICHE GEOMETRICHE). 2. LO STATO LIQUIDO HA UN VOLUME PROPRIO MA NON FORMA PROPRIA (L’OLIO ASSUME LA FORMA DEL RECIPIENTE CHE LO CONTIENE, PUR OCCUPANDO SEMPRE UN UGUALE VOLUME). 3. LO STATO AERIFORME NON HA NÉ FORMA NÉ VOLUME PROPRI (TENDE A ESPANDERSI, OCCUPANDO TUTTO LO SPAZIO DEL CONTENITORE, QUALUNQUE FORMA E VOLUME ESSO ABBIA).

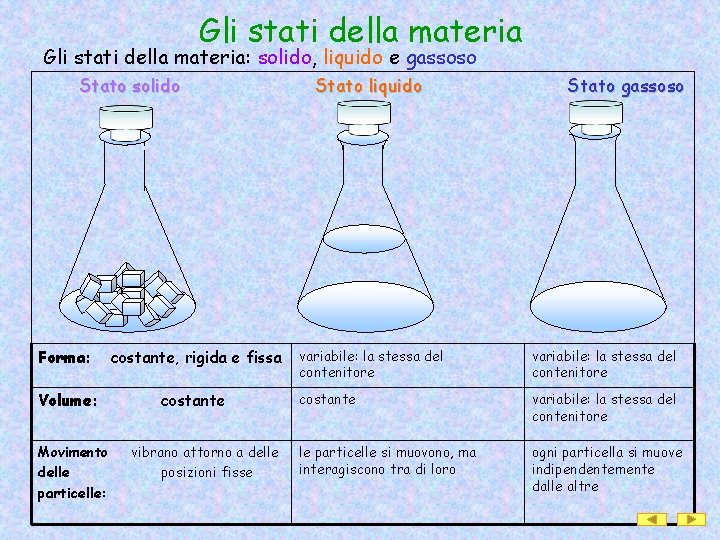
Gli stati della materia: solido, liquido e gassoso Stato solido Forma: costante, rigida e fissa Volume: costante Movimento delle particelle: vibrano attorno a delle posizioni fisse Stato liquido Stato gassoso variabile: la stessa del contenitore costante variabile: la stessa del contenitore le particelle si muovono, ma interagiscono tra di loro ogni particella si muove indipendentemente dalle altre

Gli stati della materia Il reticolo cristallino è la struttura, che cambia a seconda del tipo di solido, determinata dal modo con il quale gli atomi o le molecole prendono posizione gli uni accanto agli altri.

CAMBIAMENTI DI STATO • IL PASSAGGIO DA UNO STATO DELLA MATERIA ALL’ALTRO PRENDE IL NOME DI CAMBIAMENTO DI STATO. • QUALUNQUE SOSTANZA PUÒ PASSARE DA UNO STATO DI AGGREGAZIONE A UN ALTRO. LA CONDIZIONE PERCHÉ CIÒ AVVENGA È FORNIRLE O SOTTRARLE ENERGIA.

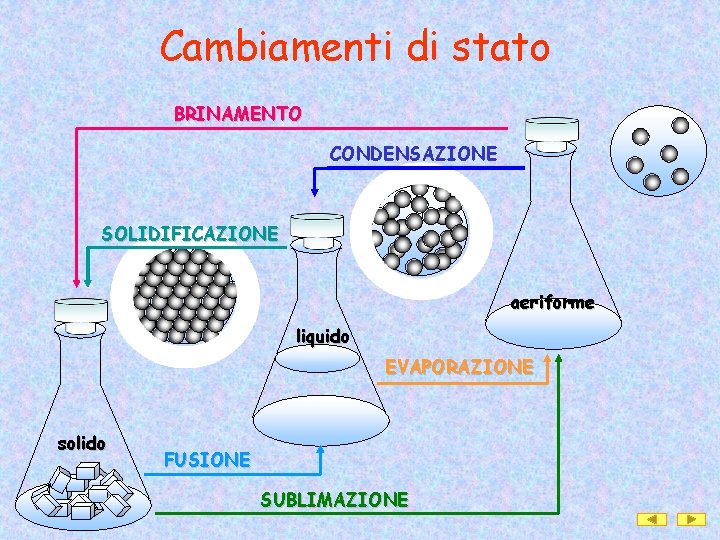
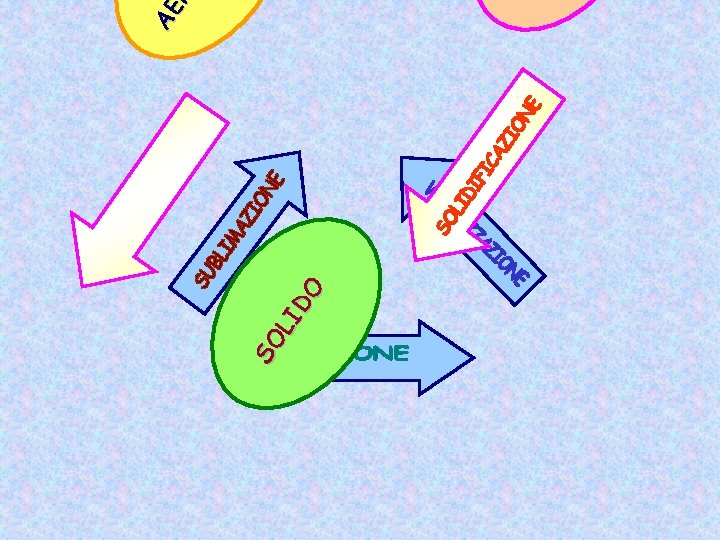
Cambiamenti di stato BRINAMENTO CONDENSAZIONE SOLIDIFICAZIONE aeriforme liquido EVAPORAZIONE solido FUSIONE SUBLIMAZIONE

SO LI DO AE

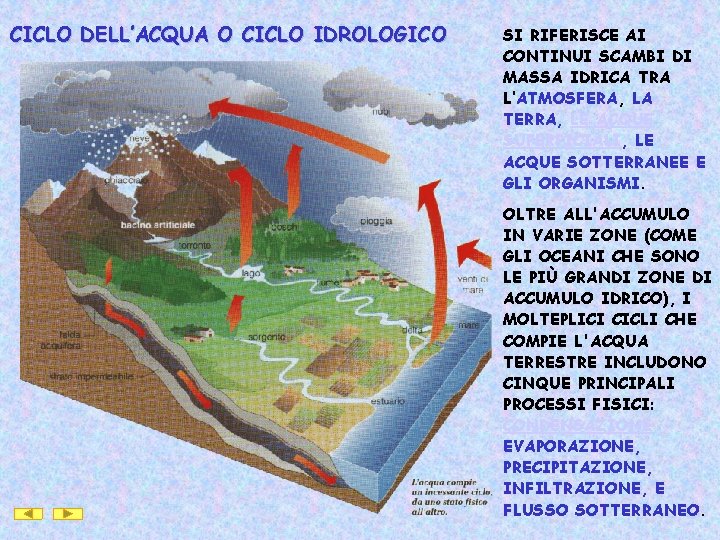
CICLO DELL’ACQUA O CICLO IDROLOGICO SI RIFERISCE AI CONTINUI SCAMBI DI MASSA IDRICA TRA L‘ATMOSFERA, LA TERRA, LE ACQUE SUPERFICIALI, LE ACQUE SOTTERRANEE E GLI ORGANISMI. OLTRE ALL'ACCUMULO IN VARIE ZONE (COME GLI OCEANI CHE SONO LE PIÙ GRANDI ZONE DI ACCUMULO IDRICO), I MOLTEPLICI CICLI CHE COMPIE L'ACQUA TERRESTRE INCLUDONO CINQUE PRINCIPALI PROCESSI FISICI: CONDENSAZIONE EVAPORAZIONE, PRECIPITAZIONE, INFILTRAZIONE, E FLUSSO SOTTERRANEO.

FUSIONE E SOLIDIFICAZIONE • SE FORNIAMO CALORE CON REGOLARITÀ A UN SOLIDO, OSSERVIAMO CHE INIZIALMENTE LA SUA TEMPERATURA AUMENTA. POI, PERÒ, COMINCIA UNA FASE DURANTE LA QUALE LA TEMPERATURA SI MANTIENE INVARIATA E, CONTEMPORANEAMENTE, SI VERIFICA IL PROCESSO DI FUSIONE • LA FUSIONE È IL PASSAGGIO DI UNA SOSTANZA DALLO STATO SOLIDO A QUELLO LIQUIDO CHE AVVIENE A TEMPERATURA COSTANTE. • LA TEMPERATURA COSTANTE ALLA QUALE SI VERIFICA LA FUSIONE. VIENE INDICATA COME TEMPERATURA DI

FUSIONE E SOLIDIFICAZIONE CHE COSA ACCADE STATO SOLIDO PUNTO DI VISTA MICRO-SCOPICO PUNTO DI VISTA MACROSCOPICO STATO LIQUIDO A CAUSA DEL CALORE FORNITO AUMENTA L’ENERGIA CINETICA MEDIA DELLE MOLECOLE A CAUSA DEL CALORE FORNITO SI INDEBOLISCONO I LEGAMI MOLECOLARI A CAUSA DEL CALORE FORNITO AUMENTA L’ENERGIA CINETICA MEDIA DELLE MOLECOLE LA TEMPERATURA RESTA COSTANTE LA TEMPERATURA AUMENTA

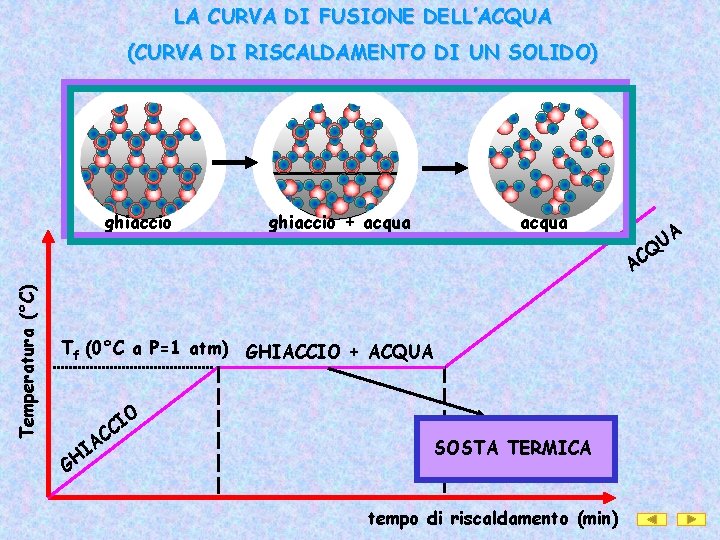
LA CURVA DI FUSIONE DELL’ACQUA (CURVA DI RISCALDAMENTO DI UN SOLIDO) ghiaccio acqua ghiaccio + acqua Temperatura (°C) Q C A UA Tf (0°C a P=1 atm) GHIACCIO + ACQUA I H G I C AC O SOSTA TERMICA tempo di riscaldamento (min)

FUSIONE LA QUANTITÀ DI CALORE NECESSARIA PER TRASFORMARE L’UNITÀ DI MASSA DI UNA SOSTANZA DALLO STATO SOLIDO A QUELLO LIQUIDO, UNA VOLTA CHE SI TROVA ALLA TEMPERATURA DI FUSIONE (COST. ), SI CHIAMA CALORE LATENTE DI FUSIONE ( Cf). DEFINIAMO IL CALORE LATENTE DI FUSIONE COME IL RAPPORTO FRA CALORE ASSORBITO Q DALLA SOSTANZA E LA SUA MASSA m: m A PARTIRE DALLA FORMULA SI DETERMINA L’UNITÀ DI MISURA: MISURA

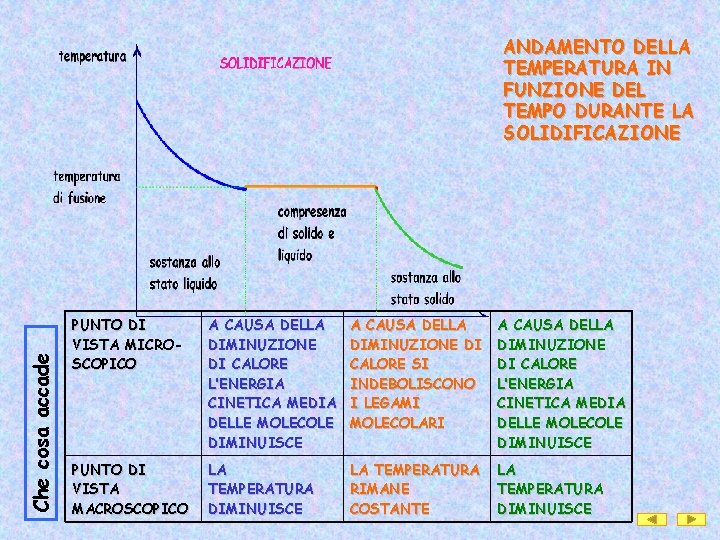
Che cosa accade ANDAMENTO DELLA TEMPERATURA IN FUNZIONE DEL TEMPO DURANTE LA SOLIDIFICAZIONE PUNTO DI VISTA MICROSCOPICO A CAUSA DELLA DIMINUZIONE DI CALORE L’ENERGIA CINETICA MEDIA DELLE MOLECOLE DIMINUISCE A CAUSA DELLA DIMINUZIONE DI CALORE SI INDEBOLISCONO I LEGAMI MOLECOLARI A CAUSA DELLA DIMINUZIONE DI CALORE L’ENERGIA CINETICA MEDIA DELLE MOLECOLE DIMINUISCE PUNTO DI VISTA MACROSCOPICO LA TEMPERATURA DIMINUISCE LA TEMPERATURA RIMANE COSTANTE LA TEMPERATURA DIMINUISCE

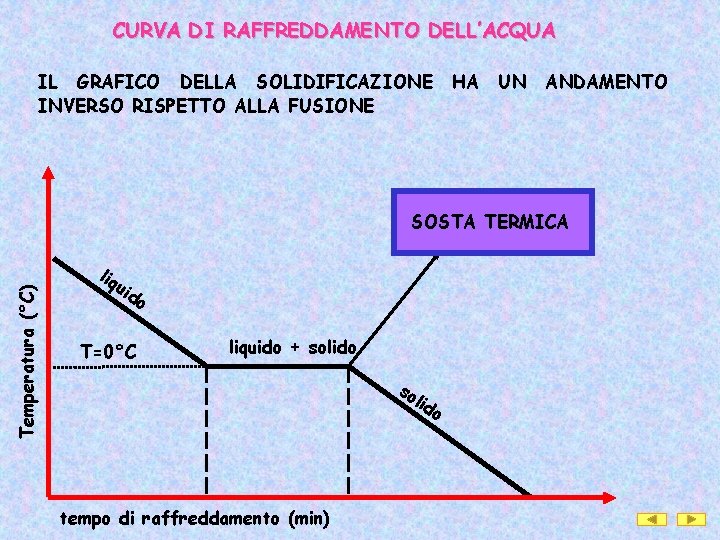
CURVA DI RAFFREDDAMENTO DELL’ACQUA IL GRAFICO DELLA SOLIDIFICAZIONE INVERSO RISPETTO ALLA FUSIONE HA UN ANDAMENTO Temperatura (°C) SOSTA TERMICA liq uid o T=0°C liquido + solido so li do tempo di raffreddamento (min)

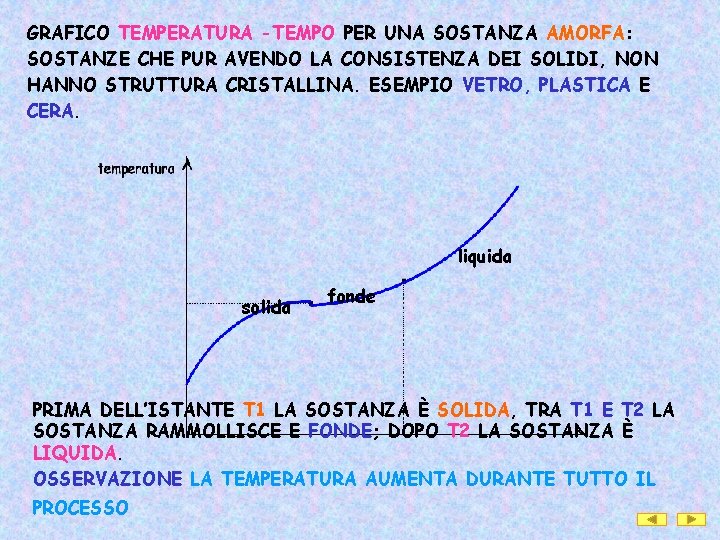
GRAFICO TEMPERATURA -TEMPO PER UNA SOSTANZA AMORFA: SOSTANZE CHE PUR AVENDO LA CONSISTENZA DEI SOLIDI, NON HANNO STRUTTURA CRISTALLINA. ESEMPIO VETRO, PLASTICA E CERA. liquida solida fonde PRIMA DELL’ISTANTE T 1 LA SOSTANZA È SOLIDA, TRA T 1 E T 2 LA SOSTANZA RAMMOLLISCE E FONDE; DOPO T 2 LA SOSTANZA È LIQUIDA. OSSERVAZIONE LA TEMPERATURA AUMENTA DURANTE TUTTO IL PROCESSO