OXIZI DEFINIIE Oxizii sunt compui binari ai oxigenului
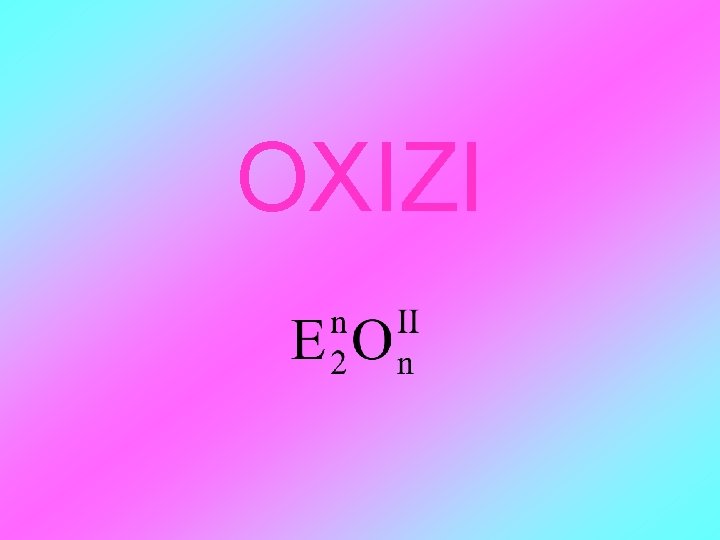
OXIZI

DEFINIŢIE Oxizii sunt compuşi binari ai oxigenului cu alte elemente, metale sau nemetale. CO 2 Mg. O

CLASIFICARE După caracterul chimic al elementului cu care se combină oxigenul, oxizii se clasifică în: • Oxizi ai nemetalelor (oxizi acizi), care, de obicei, în reacţie cu apa formează acizi. SO 3 + H 2 O → H 2 SO 4 • Oxizi ai metalelor (oxizi bazici), care, de obicei, în reacţie cu apa formează baze. Ca. O + H 2 O → Ca(OH)2

DENUMIRE La denumirea oxizilor acizi se ţine cont de faptul că majoritatea nemetalelor pot forma doi sau mai mulţi oxizi. Din acest motiv, în denumirea acestora se indică numărul de atomi de oxigen din moleculă prin prefixe de multiplicitate adăugate cuvântului oxid, urmat de denumirea nemetalului: Nr. O 1 Prefix mono- 2 3 di- tri- 4 5 6 7 tetra- penta- hexa- hepta-
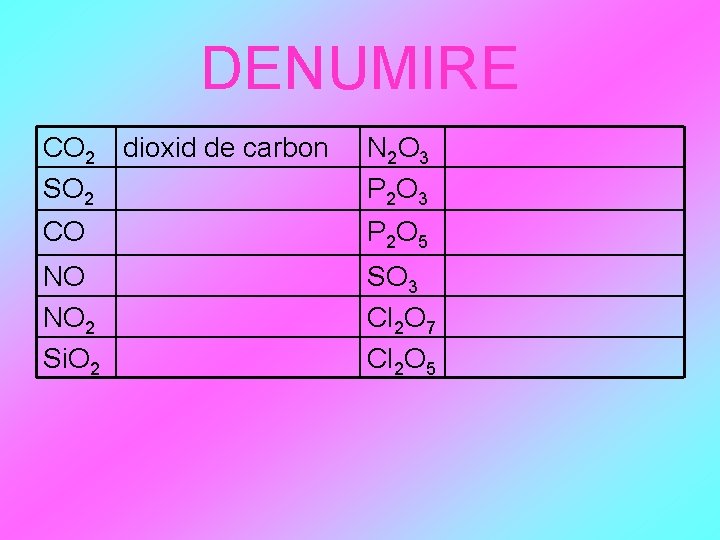
DENUMIRE CO 2 dioxid de carbon SO 2 N 2 O 3 P 2 O 3 CO P 2 O 5 NO NO 2 Si. O 2 SO 3 Cl 2 O 7 Cl 2 O 5

DENUMIRE Pentru denumirea oxizilor bazici se utilizează cuvintele “oxid de “ la care se adaugă denumirea metalului. Dacă metalul poate avea mai multe valenţe, se indică în paranteză valenţa metalului.
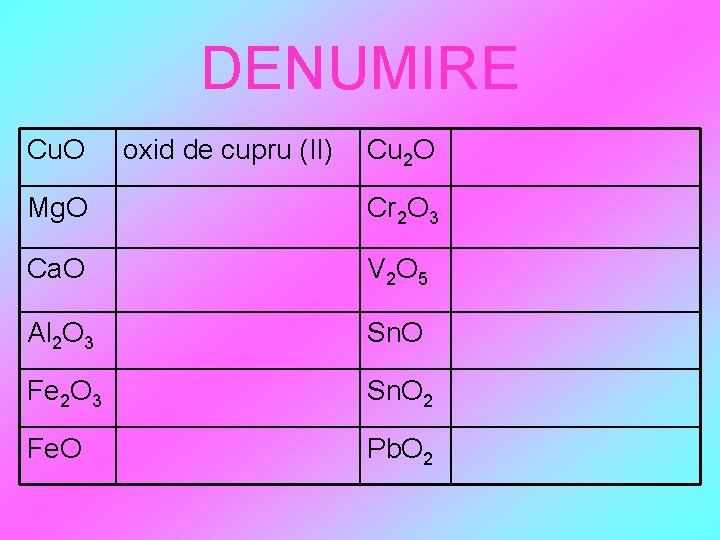
DENUMIRE Cu. O oxid de cupru (II) Cu 2 O Mg. O Cr 2 O 3 Ca. O V 2 O 5 Al 2 O 3 Sn. O Fe 2 O 3 Sn. O 2 Fe. O Pb. O 2

METODE DE OBŢINERE 1. Combinarea oxigenului cu metalele: K + O 2 → Mg + O 2 → Al + O 2 → Fe + O 2 → Cu + O 2 → Au + O 2 → 2. Combinarea oxigenului cu nemetalele: C + O 2 → S + O 2 → P 4 + O 2 → H 2 + O 2 → 3. Descompunerea termică a carbonaţilor: Ca. CO 3 → Cu. CO 3 →

PROPRIETĂŢI FIZICE • Stare de agregare: solizi sau gazoşi; • Culoare: incolori sau coloraţi. Fe. O Cu. O Mg. O Al 2 O 3 -alumina CO 2 Al 2 O 3 -rubin SO 2 Al 2 O 3 -safir NO 2 Si. O 2 Al 2 O 3 -safir Hg. O Al 2 O 3 -safir

PROPRIETĂŢI CHIMICE 1. Reacţia cu apa: 2. Oxizii nemetalelor: SO 2 + H 2 O → CO 2 + H 2 O → • Oxizii metalelor: Ca. O + H 2 O → Na 2 O + H 2 O →

PROPRIETĂŢI CHIMICE 2. Reacţia oxizilor acizi cu bazele: SO 2 + Mg(OH)2 → CO 2 + Na. OH → 3. Reacţia oxizilor bazici cu acizii: Ca. O + H 2 SO 4 → Cu. O + HCl →

UTILIZĂRI • • Materii prime: Al 2 O 3, Fe. O; Construcţii: Ca. O (var nestins), Si. O 2 (nisip); Obţinerea acizilor: SO 2, SO 3, CO 2, P 2 O 3; Catalizatori: Mn. O 2, V 2 O 5, Al 2 O 3; Pigmenţi (coloranţi): Pb 3 O 4, Fe 2 O 3, Cr 2 O 3; Obţinerea sticlei: Si. O 2(cuarţ); Pietre semipreţioase.
- Slides: 12