LA TAVOLA PERIODICA TAVOLA PERIODICA In natura esistono




- Slides: 7

LA TAVOLA PERIODICA

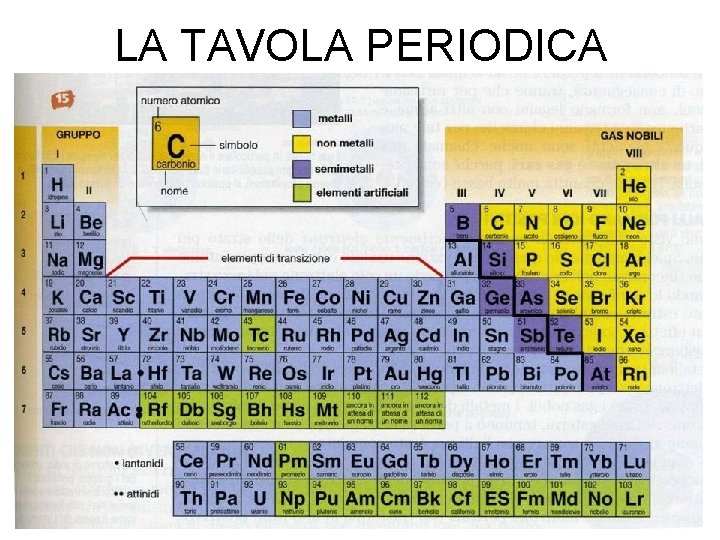
TAVOLA PERIODICA • In natura esistono 92 elementi naturali e una decina di elementi artificiali • Per meglio visualizzare le loro proprietà sono stati sistemati in una TAVOLA PERIODICA. • nella tavola periodica si evidenziano delle colonne verticali (gruppi) e delle colonne orizzontali (periodi) • Gli elementi che si trovano nello stesso gruppo hanno lo stesso numero di elettroni sull’ultimo livello e hanno le stesse proprietà chimiche. • Ogni elementi si distingue dal successivo per il numero di protoni nel nucleo.

TAVOLA PERIODICA • È stata disegnata in modo da far risaltare le somiglianze fra elementi dello stesso gruppo. • Es. tutti gli elementi del gruppo I hanno 1 elettrone sull’ultimo livello e si comportano quindi nello stesso modo nella formazione dei composti. Spesso si hanno somiglianze fra elementi di gruppi diversi ma sempre isoelettronici (es. elementi del gruppo IIIA e IIIB)

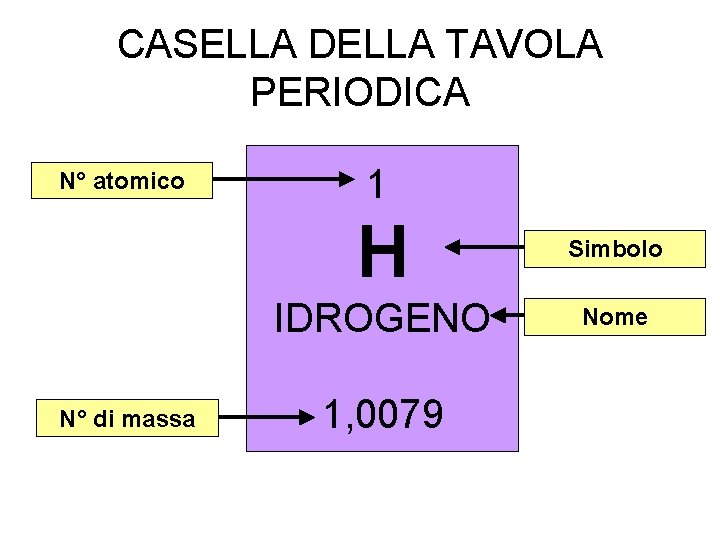
CASELLA DELLA TAVOLA PERIODICA N° atomico N° di massa 1 H Simbolo IDROGENO Nome 1, 0079

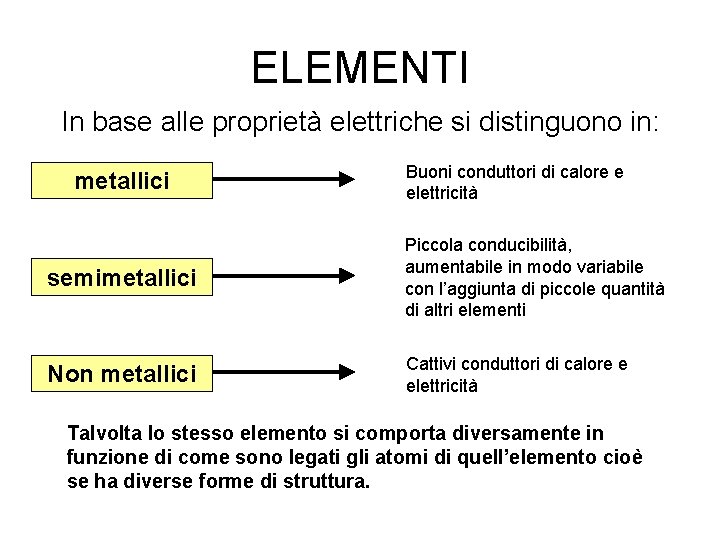
ELEMENTI In base alle proprietà elettriche si distinguono in: metallici Buoni conduttori di calore e elettricità semimetallici Piccola conducibilità, aumentabile in modo variabile con l’aggiunta di piccole quantità di altri elementi Non metallici Cattivi conduttori di calore e elettricità Talvolta lo stesso elemento si comporta diversamente in funzione di come sono legati gli atomi di quell’elemento cioè se ha diverse forme di struttura.

PERIODI • In senso orizzontale si ha che andando verso destra aumenta l’elettronegatività degli elementi, cioè la tendenza ad attirare gli elettroni di legame. • Inoltre aumenta il carattere non metallico

GAS NOBILI • Gli elementi dell’VIII gruppo hanno 8 elettroni(o 2 per He) sull’ultimo livello. • Sono quindi stabili, cioè non hanno la tendenza a formare legami. • Esistono pertanto come molecole monoatomiche • Tutti gli altri elementi per poter esistere devono formare molecole bi- o pluriatomiche













