EL ENLACE QUMICO Los tomos se unen Profesora













- Slides: 26

EL ENLACE QUÍMICO “Los átomos se unen” Profesora: Marianet Zerené

Objetivo clase v. Identificar en que consiste el enlace químico y relacionarlo con la configuración electrónica.

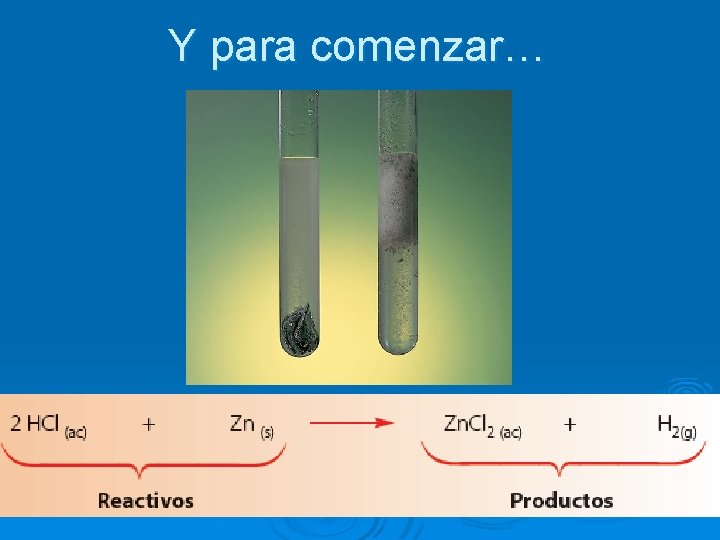
Y para comenzar…

Preguntas….

Una primera aproximación para interpretar el enlace Ø A principios del siglo XX, el científico Lewis, observando la poca reactividad de los gases nobles (estructura de 8 electrones en su último nivel), sugirió que los átomos al enlazarse “tienden” a adquirir una distribución de electrones de valencia igual a la del gas noble más próximo REGLA DEL OCTETO

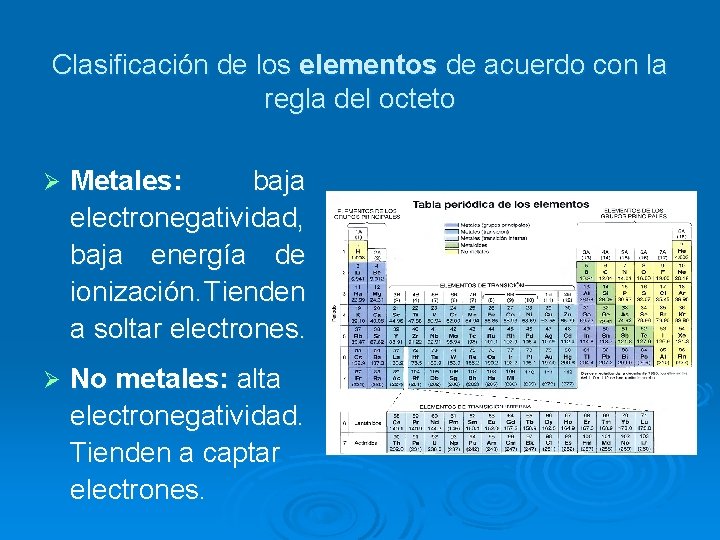
Clasificación de los elementos de acuerdo con la regla del octeto Ø Metales: baja electronegatividad, baja energía de ionización. Tienden a soltar electrones. Ø No metales: alta electronegatividad. Tienden a captar electrones.

¿Qué es el enlace químico? Es la fuerza que mantiene unidos a los átomos dentro de la molécula de una sustancia estable.

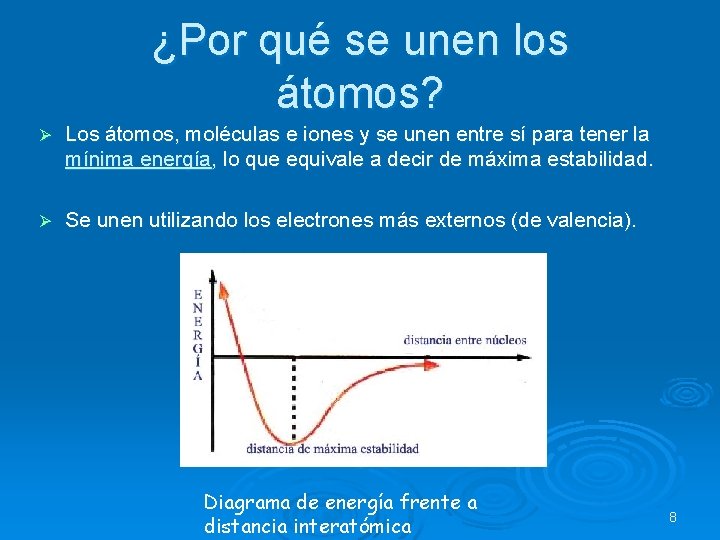
¿Por qué se unen los átomos? Ø Los átomos, moléculas e iones y se unen entre sí para tener la mínima energía, lo que equivale a decir de máxima estabilidad. Ø Se unen utilizando los electrones más externos (de valencia). Diagrama de energía frente a distancia interatómica 8


Electronegatividad (EN): Ø Es la capacidad que tiene un átomo para ganar electrones de otro átomo. v

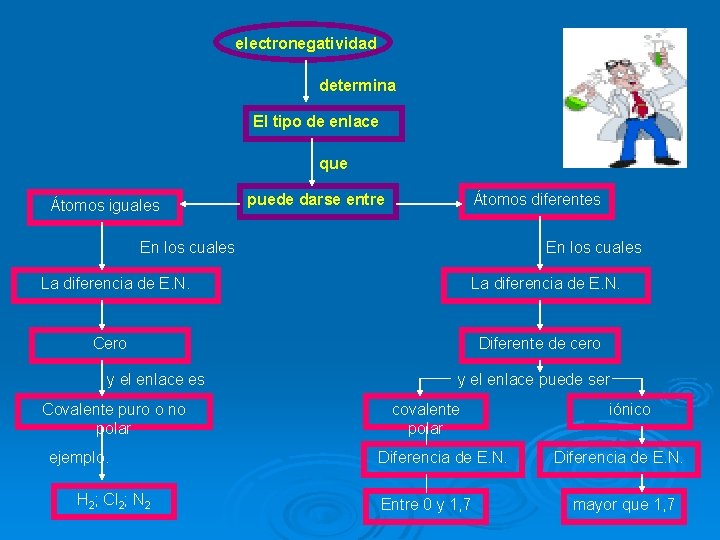
electronegatividad determina El tipo de enlace que Átomos iguales puede darse entre Átomos diferentes En los cuales La diferencia de E. N. Cero y el enlace es Covalente puro o no polar ejemplo. H 2; Cl 2; N 2 Diferente de cero y el enlace puede ser covalente polar Diferencia de E. N. Entre 0 y 1, 7 iónico Diferencia de E. N. mayor que 1, 7

ESTRUCTURAS O SIMBOLOS DE LEWIS OBJETIVO: X Conocer y aplicar las estructuras de Lewis. Relacionar los simbolos de Lewis con el enlace químico.

v Los gases nobles presentan gran estabilidad química, y existen como moléculas mono-atómicas. e- de Valencia v Su configuración electrónica es muy estable y contiene 8 He). e- en la capa de valencia (excepto el v La idea de enlace covalente fue sugerida en 1916 por G. N. Lewis: G. N. Lewis Los átomos pueden adquirir estructura de gas noble compartiendo electrones para formar un enlace de pares de electrones. He Ne Ar Kr Xe Rn 2 8 8 8

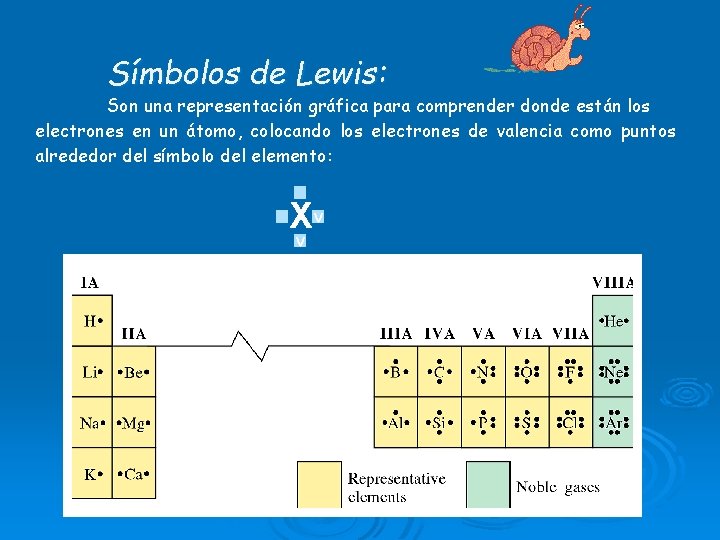
Símbolos de Lewis: Son una representación gráfica para comprender donde están los electrones en un átomo, colocando los electrones de valencia como puntos alrededor del símbolo del elemento: Xv v

Regla del octeto: Los átomos se unen compartiendo electrones hasta conseguir completar la última capa con 8 e- (4 pares de e-) es decir conseguir la configuración de gas noble: s 2 p 6 Tipos de pares de electrones: 1 - Pares de e- compartidos entre dos átomos (representado con una línea entre los átomos unidos) · enlaces sencillos · enlaces dobles · enlaces triples 2 - Pares de e- no compartidos (ó par solitario)

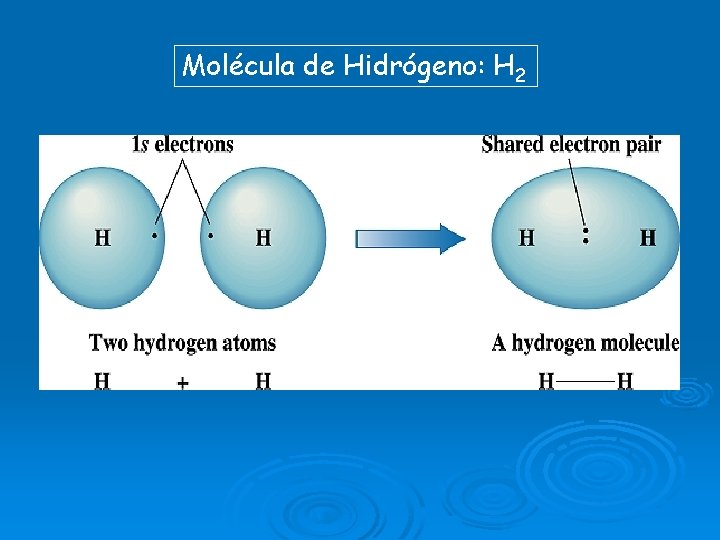
Molécula de Hidrógeno: H 2

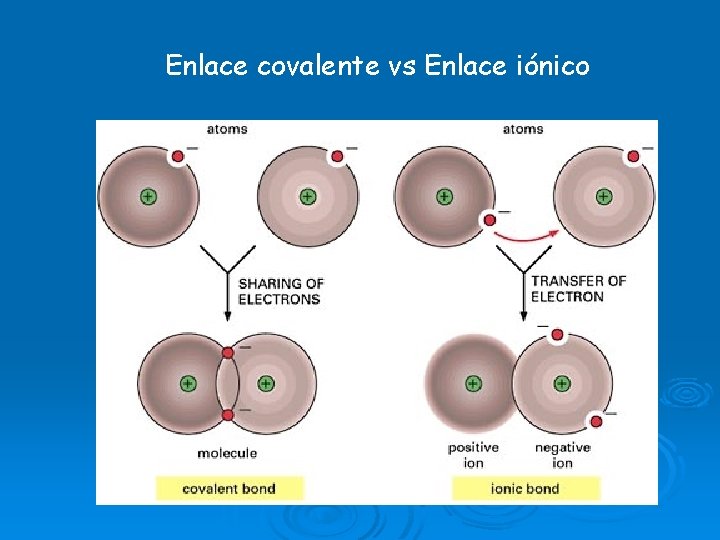
Enlace covalente vs Enlace iónico

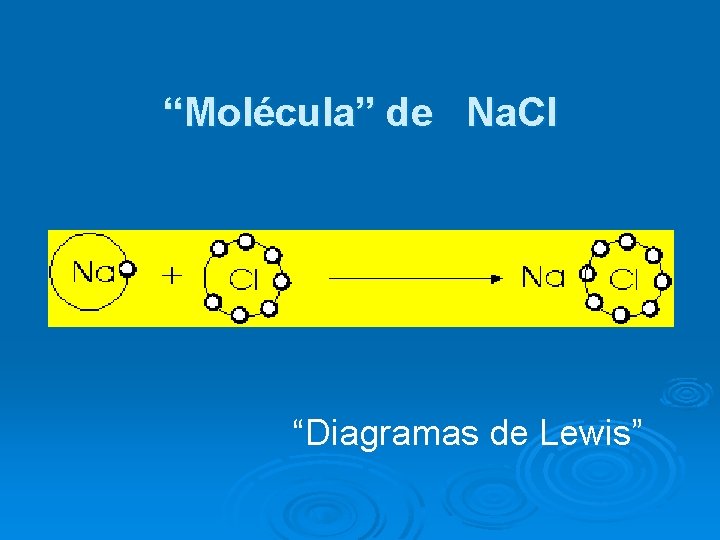
“Molécula” de Na. Cl “Diagramas de Lewis”

“Molécula” de Mg. F 2

¿Como se dibujan las estructuras de Lewis? PASO 1: Se suman los e- de valencia de los átomos presentes en la molécula. Ejemplo 1: CH 4 C: 1 s 22 s 2 p 2 4 e. H: 1 s 1 1 e- x 4= 4 e- 8 e- PASO 2: Se dibuja una estructura esquemática con los símbolos atómicos unidos mediante enlaces sencillos.

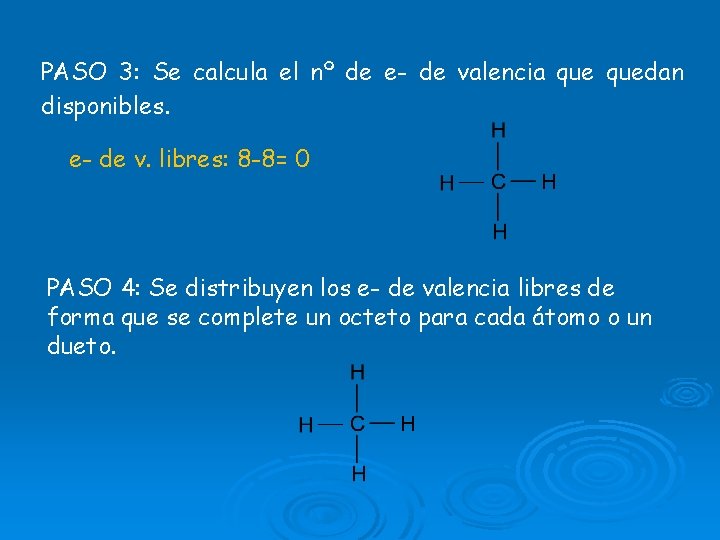
PASO 3: Se calcula el nº de e- de valencia quedan disponibles. e- de v. libres: 8 -8= 0 PASO 4: Se distribuyen los e- de valencia libres de forma que se complete un octeto para cada átomo o un dueto.

¿Como se dibujan las estructuras de Lewis? PASO 1: Se suman los e- de valencia de los átomos presentes en la molécula. Ejemplo 4: SO 2 S: 3 s 2 p 4 6 e. O: 2 s 2 p 4 6 e-x 2 = 12 18 e- PASO 2: Se dibuja una estructura esquemática con los símbolos atómicos unidos mediante enlaces sencillos.

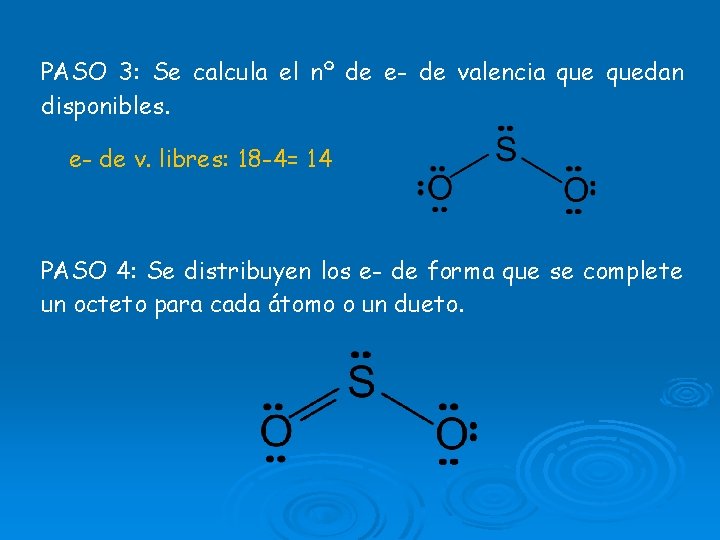
PASO 3: Se calcula el nº de e- de valencia quedan disponibles. e- de v. libres: 18 -4= 14 PASO 4: Se distribuyen los e- de forma que se complete un octeto para cada átomo o un dueto.

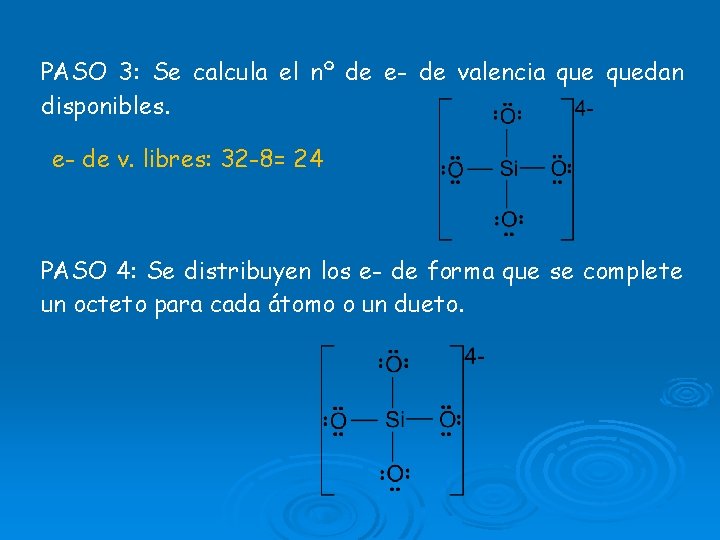
¿Como se dibujan las estructuras de Lewis? PASO 1: Se suman los e- de valencia de los átomos presentes en la molécula. Ejemplo 3: Si. O 4 -4 Si: 3 s 2 p 2 4 e. O: 2 s 2 p 4 6 e-x 4 = 24 + 4 cargas neg. 32 e- PASO 2: Se dibuja una estructura esquemática con los símbolos atómicos unidos mediante enlaces sencillos.

PASO 3: Se calcula el nº de e- de valencia quedan disponibles. e- de v. libres: 32 -8= 24 PASO 4: Se distribuyen los e- de forma que se complete un octeto para cada átomo o un dueto.

A trabajar… 1. - Desarrolla en tu cuaderno las actividades en amarillo del texto que están en la unidad de enlace químico. Serán décimas para la prueba