Dans les minraux silicats 4 O Mn O
![Polymérisation des tétraèdres silicatés neutralisation des charges des oxygènes [Si. O 4]4 - [Si Polymérisation des tétraèdres silicatés neutralisation des charges des oxygènes [Si. O 4]4 - [Si](https://slidetodoc.com/presentation_image_h2/44c2060087d4d79b1506b4348939c084/image-5.jpg)







![Tétraèdres isolés a) Aucun des tétraèdres [Si. O 4]4 - ne partage d’oxygène avec Tétraèdres isolés a) Aucun des tétraèdres [Si. O 4]4 - ne partage d’oxygène avec](https://slidetodoc.com/presentation_image_h2/44c2060087d4d79b1506b4348939c084/image-15.jpg)









![A 2+3 Les différents sites Grenat B 3+2 [Si. O 4]3 A 2+3 Les différents sites Grenat B 3+2 [Si. O 4]3](https://slidetodoc.com/presentation_image_h2/44c2060087d4d79b1506b4348939c084/image-27.jpg)
![Grenat : A 2+3 B 3+2 [Si. O 4]3 Grenat bleu = Si pourpre Grenat : A 2+3 B 3+2 [Si. O 4]3 Grenat bleu = Si pourpre](https://slidetodoc.com/presentation_image_h2/44c2060087d4d79b1506b4348939c084/image-28.jpg)








- Slides: 38

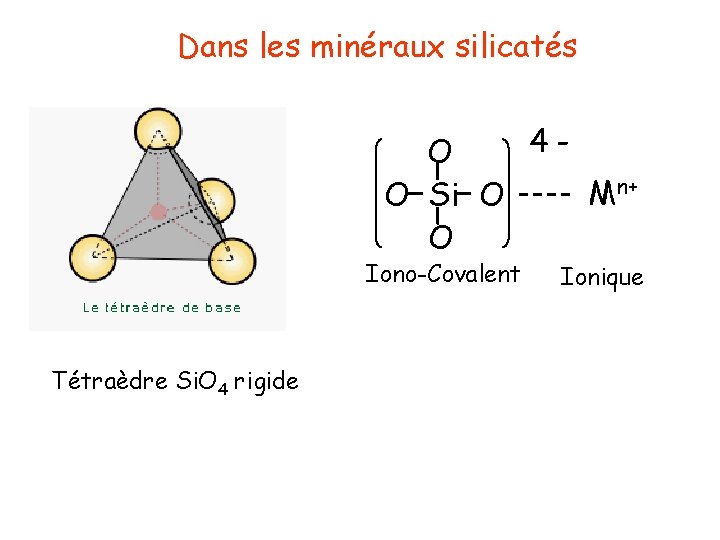
Dans les minéraux silicatés 4 O Mn+ O Si O O Iono-Covalent Tétraèdre Si. O 4 rigide Ionique

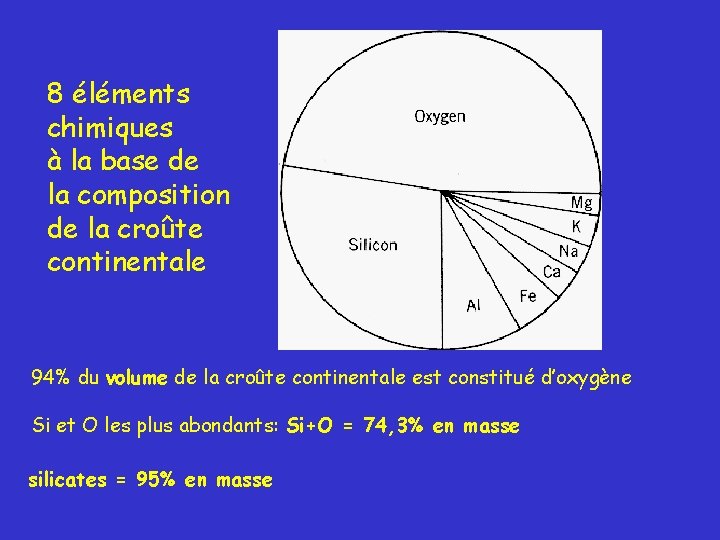
8 éléments chimiques à la base de la composition de la croûte continentale 94% du volume de la croûte continentale est constitué d’oxygène Si et O les plus abondants: Si+O = 74, 3% en masse silicates = 95% en masse

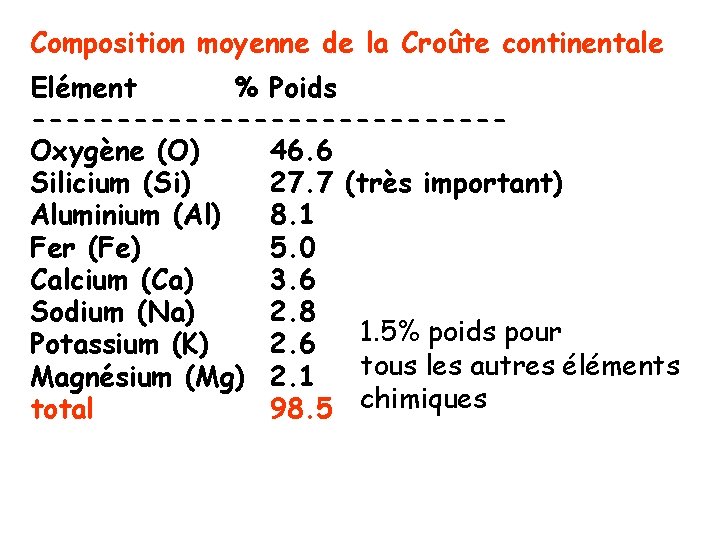
Composition moyenne de la Croûte continentale Elément % Poids --------------Oxygène (O) 46. 6 Silicium (Si) 27. 7 (très important) Aluminium (Al) 8. 1 Fer (Fe) 5. 0 Calcium (Ca) 3. 6 Sodium (Na) 2. 8 1. 5% poids pour Potassium (K) 2. 6 tous les autres éléments Magnésium (Mg) 2. 1 total 98. 5 chimiques

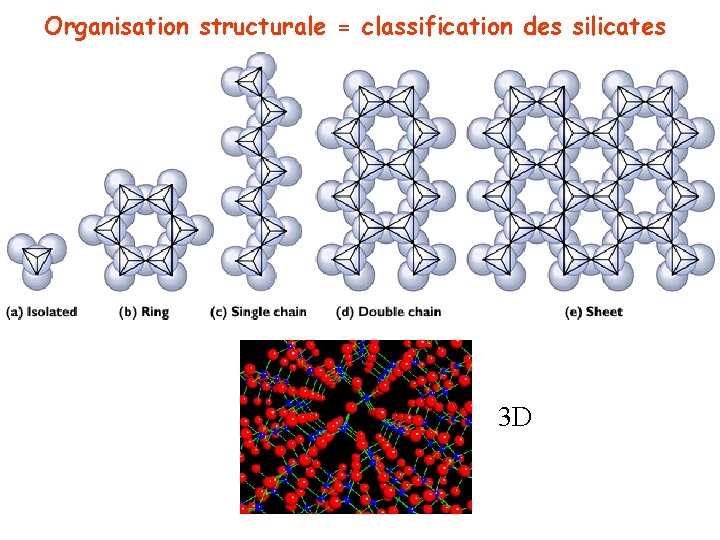
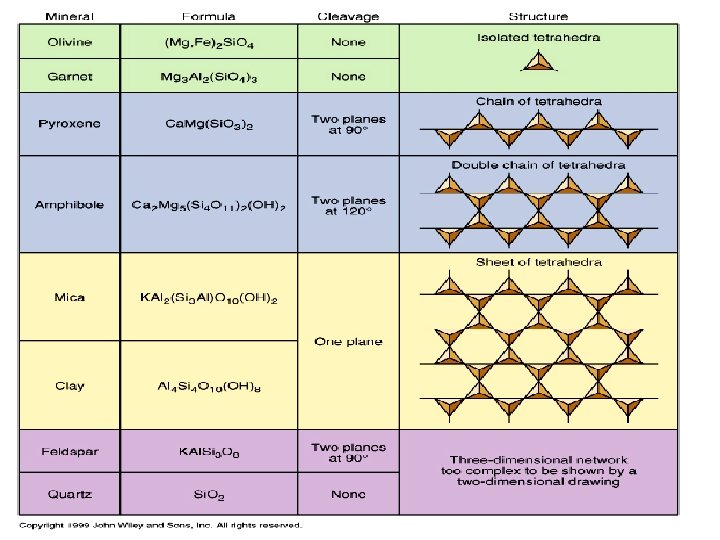
Organisation structurale = classification des silicates 3 D
![Polymérisation des tétraèdres silicatés neutralisation des charges des oxygènes Si O 44 Si Polymérisation des tétraèdres silicatés neutralisation des charges des oxygènes [Si. O 4]4 - [Si](https://slidetodoc.com/presentation_image_h2/44c2060087d4d79b1506b4348939c084/image-5.jpg)
Polymérisation des tétraèdres silicatés neutralisation des charges des oxygènes [Si. O 4]4 - [Si 4 O 11]6 - [Si 2 O 7]6 - [Si 6 O 18]12 - [Si 2 O 6]4 - [Si 2 O 5]2 - [Si. O 2]0

Les principaux minéraux silicatés a) Minéraux silico-alumineux Quartz Feldspath K plagioclases Si. O 2 KAl. Si 3 O 8 orthose Na. Al. Si 3 O 8 - Ca. Al 2 Si 2 O 8 Albite Anorthite Muscovite (mica) KAl 3 Si 3 O 10 (OH) 2

b) Minéraux ferro-magnésiens Biotite (mica) Amphiboles K (Mg, Fe)3 Al. Si 3 O 10(OH) 2 (Mg, Fe. . . )5 Si 8 O 22(OH) 2 (Ca, Na. . . )2 Pyroxènes (Ca, Mg, Fe)2 Si 2 O 6 Olivines (Mg, Fe) 2 Si. O 4 Grenats Na. Al. Si 2 O 6 Mg 3 Al 2(Si. O 4)3 Grande importance des groupements hydroxyles: présence de fluides hydratés (croûte, manteau).


Modes de formation Trois exemples: A) Cristallisation à partir de silicates fondus olivine dans roche volcanique (basalte)

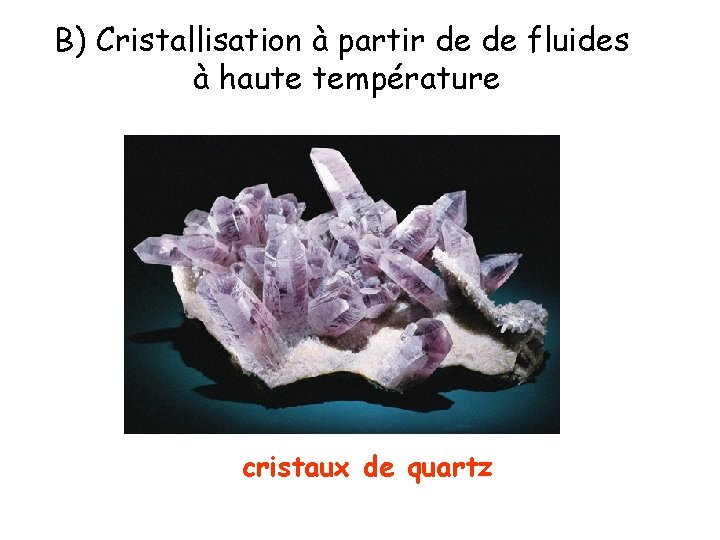
B) Cristallisation à partir de de fluides à haute température cristaux de quartz

C) Transformation en argile d’un feldspath altéré par une solution (pluies, eau circulant) les alcalins sont libérés dans la solution, Réorganisation en carbonates et silice dissoute Al, Si restent pour construire des argiles 2 KAl. Si 3 O 8+2 (H+ + CO 3 ) + H 2 O = Al 2 Si 2 O 5(OH)4 + 2 KCO 3 + 4(Si. O 2)d 2 -

méthodes d’étude Le microscope optique polarisant Lumière naturelle Lumière polarisée

Microscopie électronique à balayage: échelle du mm Précipités de carbonates bactériens atoll de Kiritimati, Pacifique photo au microscope électronique à balayage largeur de l'image: 10 microns

Microscopie électronique en transmission: en dessous du nm 19, 2 A Sections hexagonales de canaux dans un silicate de métamorphisme: les ronds représentent les tétraèdres et non les atomes individuels.
![Tétraèdres isolés a Aucun des tétraèdres Si O 44 ne partage doxygène avec Tétraèdres isolés a) Aucun des tétraèdres [Si. O 4]4 - ne partage d’oxygène avec](https://slidetodoc.com/presentation_image_h2/44c2060087d4d79b1506b4348939c084/image-15.jpg)
Tétraèdres isolés a) Aucun des tétraèdres [Si. O 4]4 - ne partage d’oxygène avec un autre tétraèdre [Si. O 4]4 - : Ils ne partagent pas d’oxygène pontant b) Les oxygènes du tétraèdre sont partagés avec des polyèdres de plus grande taille (octaèdre, cube…) c) Ces minéraux ne présentent pas de plan de clivage

I) Les olivines (Mg, Fe)2 Si. O 4 2 pôles purs: Forstérite (Mg) et fayalite (Fe) Olivines du Pakistan

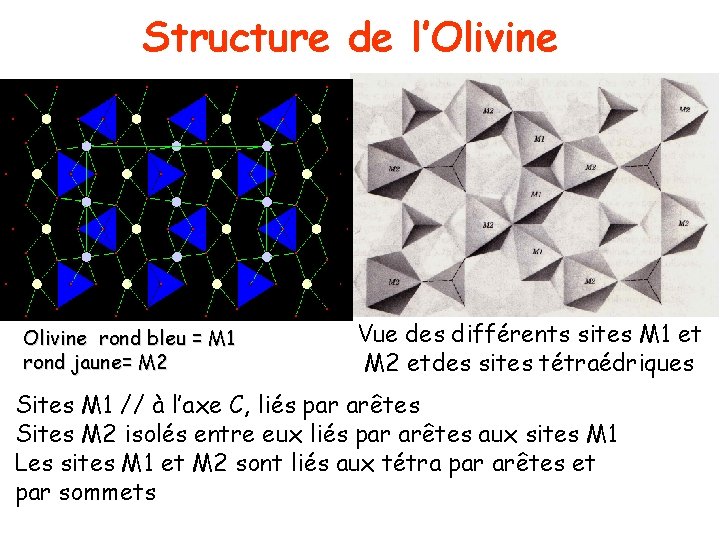
Structure de l’Olivine rond bleu = M 1 rond jaune= M 2 Vue des différents sites M 1 et M 2 etdes sites tétraédriques Sites M 1 // à l’axe C, liés par arêtes Sites M 2 isolés entre eux liés par arêtes aux sites M 1 Les sites M 1 et M 2 sont liés aux tétra par arêtes et par sommets

Les sites occupés par les éléments dans l’olivine @ Sites M 1 et M 2 contiennent Fe 2+, Mg 2+ et Ni 2+ Préférence du site M 1 pour Fe 2+ et Ni 2+ @ Existence de solutions solides complètes pour Fe, Mg et Mn car rayon équivalent @ Pour la monticellite (Ca. Mg. Si. O 4) pas de solution solide complète car Ca (1Å) Ca entre dans les sites M 2 et Mg dans les sites M 1

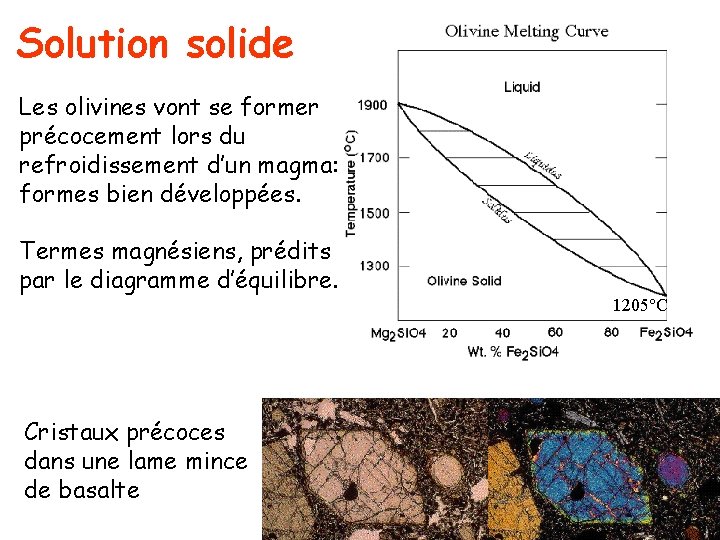
Solution solide Les olivines vont se former précocement lors du refroidissement d’un magma: formes bien développées. Termes magnésiens, prédits par le diagramme d’équilibre. 1205°C Cristaux précoces dans une lame mince de basalte

Observation microscope polarisant Lame mince en lumière polarisée Constituants des roches basiques et ultrabasiques du manteau grains de cette roche (dunite) = olivine

Relation structure et propriétés @ La densité du minéral augmente en fonction de la teneur en fer. @ transition de phase olivine - spinelle à HP, HT Compressibilité des M>tétra M 2 > M 1 A 150 Kbars les deux sites sont à la même taille et donc transition vers la phase spinelle qui ne possède qu’un seul type de site octaédrique = séismes profonds Lorsque T et P augmente encore passage à Mg. Si. O 3 +Mg. O

@ La couleur (de plus en plus foncée) Variation en fonction de la Substitution de Mg 2+ par Fe 2+

Existence naturelle a)Les olivines = premiers produits de cristallisation (magmas riches en fer et Mg et pauvres en silice) b)Les roches les plus riches en olivines sont les dunites et les péridotites (ol, px, gt) = roches du manteau Présentes dans les basaltes (fond des océans) Forstérites = matériau à pt de fusion élevé (1890°C) minéraux réfractaires (ex: briques de four de verrerie) Lors de l’altération olivine = serpentines (amiantes)

II) Les grenats lumière polarisée Isotropes optiquement Minéraux du métamorphisme (Al octaédrique: haute pression), dans les schistes, parfois dans quelques roches ignées en trace, granite et péridotite

Grenat ferrique Fe 3+ (andradite) Les grenats présentent généralement des faces bien développées. Des éléments colorants (ions de transition) se substituent au Mg 2+

Les Familles de Grenats Pyrope : Mg 3 Al 2 Si 3 O 12 Ouvarovite: Ca 3 Cr 2 Si 3 O 12 Almandin: Fe 3 Al 2 Si 3 O 12 Grossulaire: Ca 3 Al 2 Si 3 O 12 Spessartite: Mn 3 Al 2 Si 3 O 12 Andradite: Ca 3 Fe 3+2 Si 3 O 12 “Pyralspites” - B = Al “Ougrandites” - A = Ca A coordinence 8 B coordinence 6 A = gros cations divalents 2+ ou monovalents 1+ B = cations trivalents 3+
![A 23 Les différents sites Grenat B 32 Si O 43 A 2+3 Les différents sites Grenat B 3+2 [Si. O 4]3](https://slidetodoc.com/presentation_image_h2/44c2060087d4d79b1506b4348939c084/image-27.jpg)
A 2+3 Les différents sites Grenat B 3+2 [Si. O 4]3
![Grenat A 23 B 32 Si O 43 Grenat bleu Si pourpre Grenat : A 2+3 B 3+2 [Si. O 4]3 Grenat bleu = Si pourpre](https://slidetodoc.com/presentation_image_h2/44c2060087d4d79b1506b4348939c084/image-28.jpg)
Grenat : A 2+3 B 3+2 [Si. O 4]3 Grenat bleu = Si pourpre = A turquoise = B

Solutions solides complexes Spessartine: Manganèse Grossulaire: Fer Uvarovite: chrome

Gisements 1)Roches métamorphiques Pyralspites dans Schistes Ougrandites dans carbonates 2)Roches ignées Dans péridotites

@ L’altération des grenats donne des serpentines du talc, de la chlorite et de l’épidote. @ Dans les grenats sédimentaires (grossulaire dominant, andradite, ouvarovite) des groupements hydroxyles peuvent se substituer aux tétra Si. O 4 = hydrogrossulaires (8. 5% H 2 O) Lorsque Ti 4+ entre dans les sites B et Na dans les sites A de ces grenats on obtient la mélanite ou grenat noir (assez commun)

Les grenats comme géomatériaux Ils sont principalement utilisés comme: @abrasifs dans les industries du bois, du cuir et du plastique @pour le décapage par sablage @Pour la confection de papier abrasif, @Pour le surfaçage du verre @Pour la filtration.

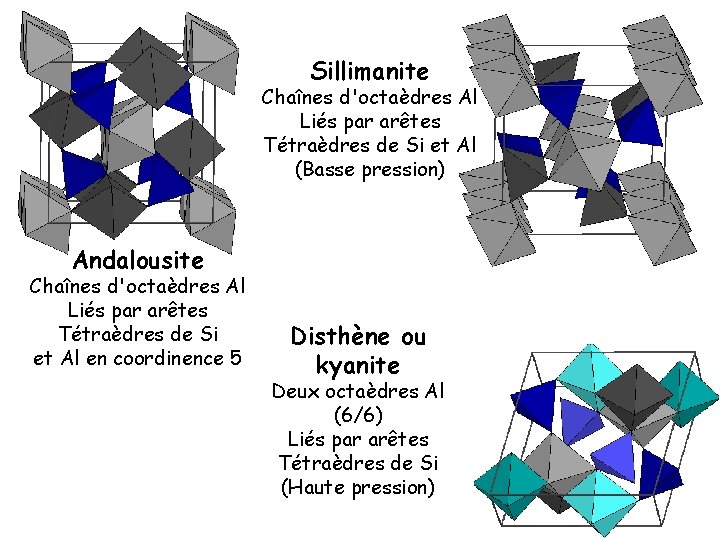
III) Les silicates d’alumine, Al 2 Si. O 5 Le disthène: métamorphisme de haute pression

Adaptation d’une structure minérale à des modifications de P-T = différents polymorphes Intérêt: calage P-T des roches qui contiennent ces phases. Point triple vers 500°C et 4 kbars (12 km env. ) 3, 6 Augmentation de la densité avec P 3, 23 6/6 3, 2 6/5 6/4 Augmentation du nombre de voisins de Al avec P (4, 5, 6)

Sillimanite Chaînes d'octaèdres Al Liés par arêtes Tétraèdres de Si et Al (Basse pression) Andalousite Chaînes d'octaèdres Al Liés par arêtes Tétraèdres de Si et Al en coordinence 5 Disthène ou kyanite Deux octaèdres Al (6/6) Liés par arêtes Tétraèdres de Si (Haute pression)

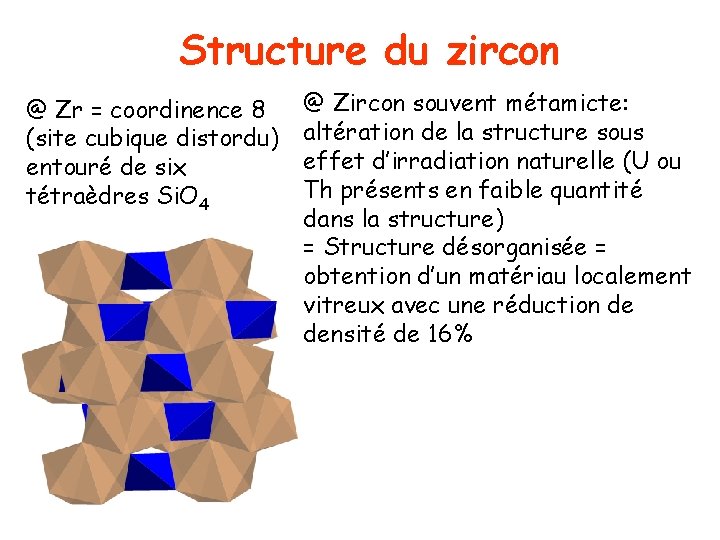
IV) Le zircon Zr. Si. O 4 pouvant contenir du Hf en remplacement de Zr

Structure du zircon @ Zr = coordinence 8 (site cubique distordu) entouré de six tétraèdres Si. O 4 @ Zircon souvent métamicte: altération de la structure sous effet d’irradiation naturelle (U ou Th présents en faible quantité dans la structure) = Structure désorganisée = obtention d’un matériau localement vitreux avec une réduction de densité de 16%

@ Minéral accessoire des roches magmatiques et sédimentaires = peu altérable, datation possible des terrains dans lesquels il a été enfoui Utilisation du zircon @ Utilisation industrielle = source de Zr métal (industrie nucléaire) @ Zr. O 2 matériau réfractaire