Curso de Tcnicas Electroqumicas Fundamentos Ignacio Gonzlez Martnez



























- Slides: 46

Curso de Técnicas Electroquímicas (Fundamentos) Ignacio González Martínez Carlos Eduardo Frontana Vázquez Víctor Manuel Ugalde Saldívar 1

Q. Carlos Eduardo Frontana Vázquez Dr. Víctor Manuel Ugalde Saldívar Universidad Autónoma Metropolitana Unidad Iztapalapa Universidad Nacional Autónoma de México ultrabuho@yahoo. com. mx Universidad Metropolitana Unidad Iztapalapa Electroquímica molecular (Química Orgánica) vmus@xanum. uam. mx vmus@servidor. unam. mx Electroquímica molecular (Química Inorgánica) 2

Calendario de actividades Semana 1 Día Tema Tipo de sesión Martes 26 de julio Fundamentos Explicación y ejemplos Miércoles 27 de julio Cronoamperometría Explicación y ejemplos Jueves 28 de julio Voltamperometría de corriente muestreada Explicación y ejemplos Viernes 29 de julio Cronoamperometría Experimental 3

Calendario de actividades Semana 2 Día Tema Tipo de sesión Lunes 1 de agosto Voltamperometría de barrido lineal Explicación y ejemplos Miércoles 3 de agosto Casos experimentales Explicación y ejemplos Jueves 4 de agosto Voltamperometría de barrido lineal Experimental Viernes 5 de agosto Espectroelectroquímica Explicación y ejemplos 4

Fundamentos de electroquímica • Reacciones en disolución (reacciones redox) • Celda electroquímica • Reacción electroquímica • Potenciometría de corriente nula • Electrodo Normal de Hidrógeno y sistemas de referencia • Potenciostato (instrumentación) • Factores que alteran la velocidad del proceso: • Transferencia de carga (BV) • Transferencia de masa (Nernst-Planck) • Leyes de Fick 5

Retos Tecnológicos XXI Medio Ambiente Contaminación Ambiental Tecnologías “Limpias” -Aire -Agua -Suelo -Transformación -Extracción de productos naturales -Energéticas 6

Retos Tecnológicos XXI Industrial Innovación Tecnologías “Limpias” Disminución de costos 7

Retos Tecnológicos XXI Ciencia Básica Desarrollo de Teorías Relaciones estructura-actividad Mayor implicación en el proceso productivo 8

Fundamentos de electroquímica • Reacciones en disolución (reacciones redox) • Celda electroquímica • Reacción electroquímica • Potenciometría de corriente nula • Electrodo Normal de Hidrógeno y sistemas de referencia • Potenciostato (instrumentación) • Factores que alteran la velocidad del proceso: • Transferencia de carga (BV) • Transferencia de masa (Nernst-Planck) • Leyes de Fick 9

Reacciones “redox” Red 1 + Ox 1 Ox 2 + Red 2 Fe 2+ + Ce 4+ Fe 3+ + Ce 3+ Fe 2+ + Fe 3+ + Ce 4+ Ce 3+ DGrxn = G mezcla final – G mezcla inicial Mezcla final= [j] después del avance de un coeficiente estequiométrico 10

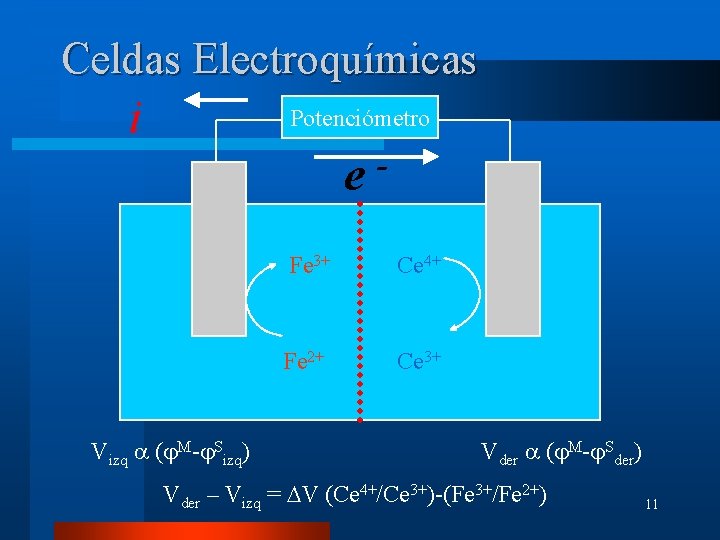
Celdas Electroquímicas i Potenciómetro e Vizq ( M- Sizq) - Fe 3+ Ce 4+ Fe 2+ Ce 3+ Vder ( M- Sder) Vder – Vizq = DV (Ce 4+/Ce 3+)-(Fe 3+/Fe 2+) 11

Reacciones electroquímicas Toda reacción que involucra transferencia de carga A TRAVÉS de la interfase y, por lo tanto, un FLUJO DE CORRIENTE (J), se llama REACCIÓN ELECTROQUÍMICA De transferencia iónica: Ag+ (soln) + e- (metal) Ag (metal) H 3 O+ (soln) + e-(metal) Had + H 2 O 2 Had H 2 (g) A+ (ac) A+ (org) De transferencia electrónica Fe 3+ (soln) + e- (metal) Fe 2+ (soln) 12

Introducción • Electroquímica: Inicio formal a partir de los trabajos de Volta y Galvani (celdas de energía y fenómenos biológicos). • Estudio de estructuras y procesos en la interfase formada por un conductor electrónico y un conductor iónico (o entre dos conductores iónicos) 13

Propiedades de la reacción electroquímica v J, si sólo ocurre una reacción química en el sistema l Sensible al estado de la superficie. l Modifica el término DG por valores zi eo Df l Al variar Df, es posible controlar la velocidad de reacción e incluso revertir su dirección 14

Fundamentos de electroquímica • Reacciones en disolución (reacciones redox) • Celda electroquímica • Reacción electroquímica • Potenciometría de corriente nula • Electrodo Normal de Hidrógeno y sistemas de referencia • Ley de Nernst • Potenciostato (instrumentación) • Factores que alteran la velocidad del proceso: • Transferencia de carga (BV) • Transferencia de masa (Nernst-Planck) • Leyes de Fick 15

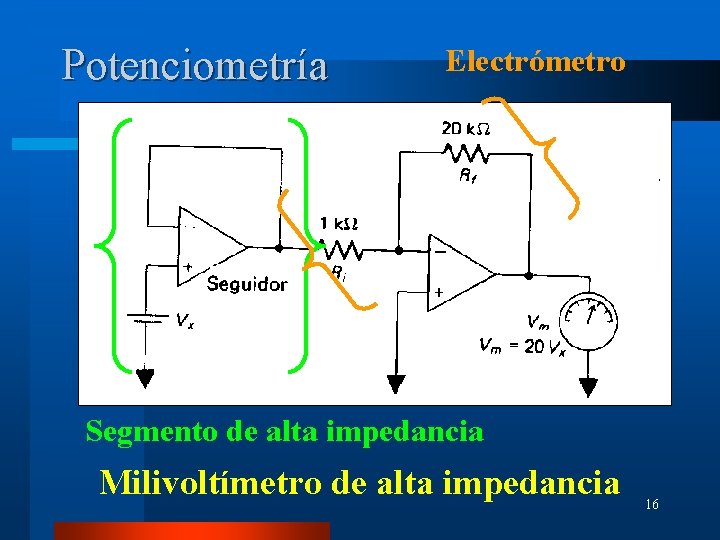
Potenciometría Electrómetro Segmento de alta impedancia Milivoltímetro de alta impedancia 16

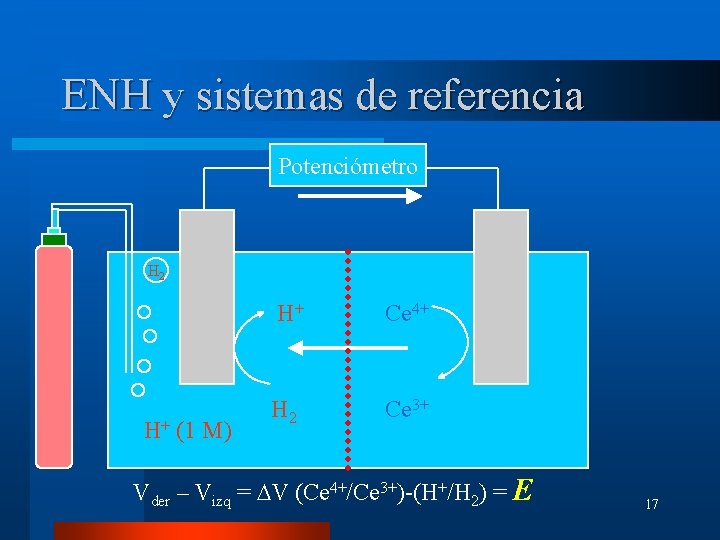
ENH y sistemas de referencia Potenciómetro H 2 H+ (1 M) H+ Ce 4+ H 2 Ce 3+ Vder – Vizq = DV (Ce 4+/Ce 3+)-(H+/H 2) = E 17

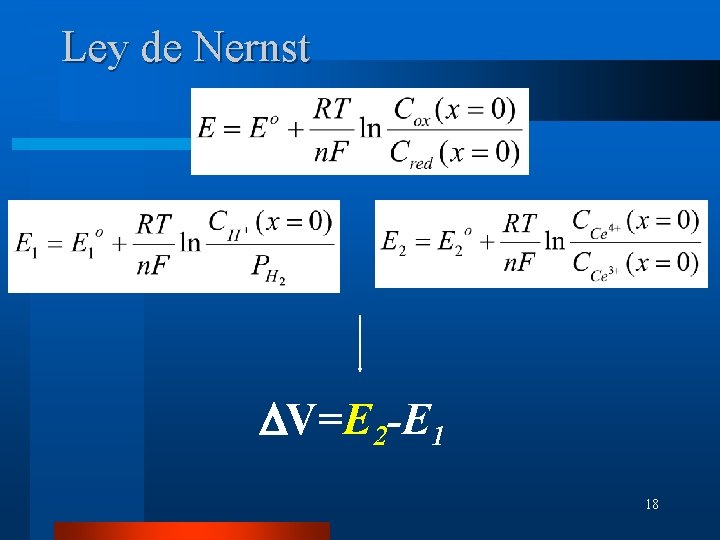
Ley de Nernst DV=E 2 -E 1 18

Condiciones de aplicabilidad de E DV = E 2, sí y sólo sí • Vizq = ENH (Sistema de referencia) • [Ox]x=0=[Ox]* • [Red]x=0=[Red]* (no hay reacción química) • icelda 0 [A] = [A] después de la llamada doble capa(“Energía”) eléctrica E es lax=0 condición termodinámica de mi sistema 19

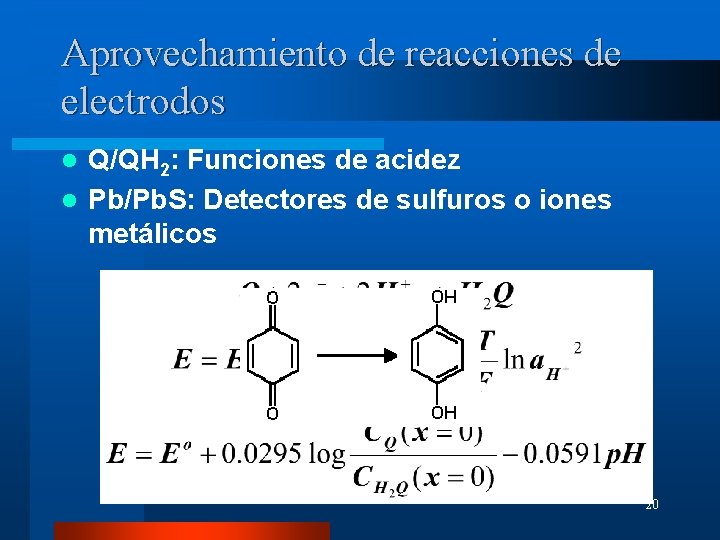
Aprovechamiento de reacciones de electrodos Q/QH 2: Funciones de acidez l Pb/Pb. S: Detectores de sulfuros o iones metálicos l 20

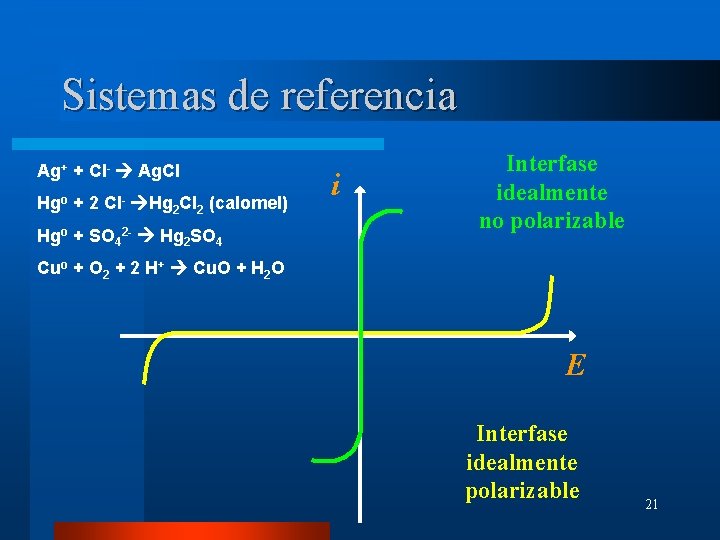
Sistemas de referencia Ag+ + Cl- Ag. Cl Hgo +2 Cl- Hg 2 Cl 2 (calomel) Hgo + SO 42 - Hg 2 SO 4 i Interfase idealmente no polarizable Cuo + O 2 + 2 H+ Cu. O + H 2 O E Interfase idealmente polarizable 21

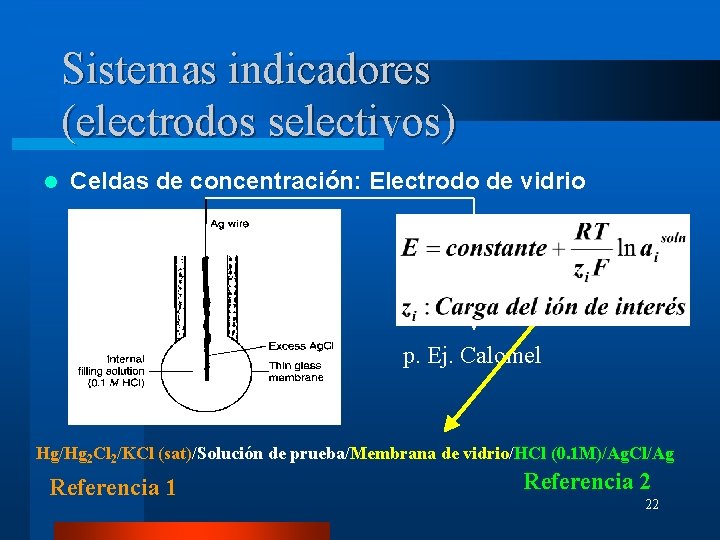
Sistemas indicadores (electrodos selectivos) l Celdas de concentración: Electrodo de vidrio p. Ej. Calomel Hg/Hg 2 Cl 2/KCl (sat)/Solución de prueba/Membrana de vidrio/HCl (0. 1 M)/Ag. Cl/Ag Referencia 1 Referencia 2 22

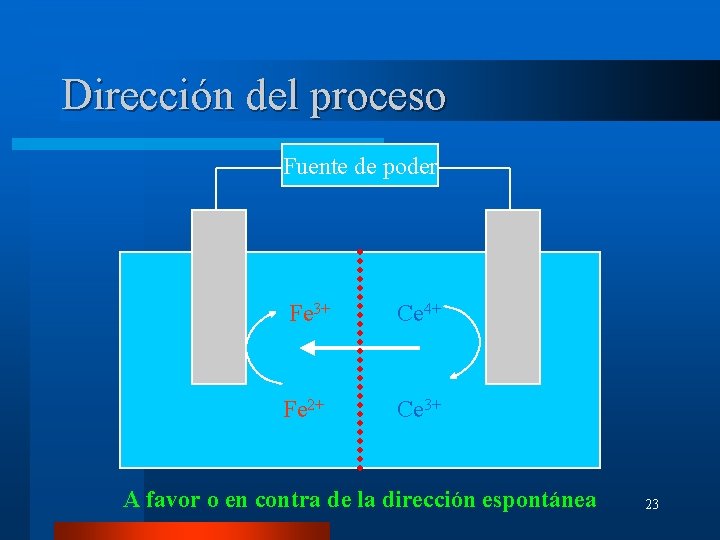
Dirección del proceso Fuente de poder Fe 3+ Ce 4+ Fe 2+ Ce 3+ A favor o en contra de la dirección espontánea 23

Fundamentos de electroquímica • Reacciones en disolución (reacciones redox) • Celda electroquímica • Reacción electroquímica • Potenciometria de corriente nula • Electrodo Normal de Hidrogeno y sistemas de referencia • Ley de Nernst • Potenciostato (instrumentación) • Factores que alteran la velocidad del proceso: • Transferencia de carga (BV) • Transferencia de masa (Nernst-Planck) • Leyes de Fick 24

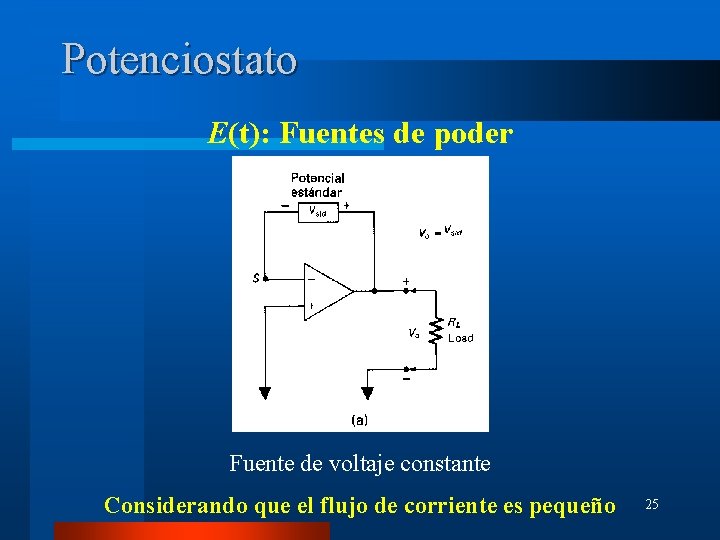
Potenciostato E(t): Fuentes de poder Fuente de voltaje constante Considerando que el flujo de corriente es pequeño 25

Fundamentos de electroquímica • Reacciones en disolución (reacciones redox) • Celda electroquímica • Reacción electroquímica • Potenciometria de corriente nula • Electrodo Normal de Hidrogeno y sistemas de referencia • Potenciostato (instrumentación) • Factores que alteran la velocidad del proceso • Transferencia de carga (BV) • Transferencia de masa (Nernst-Planck) • Leyes de Fick 26

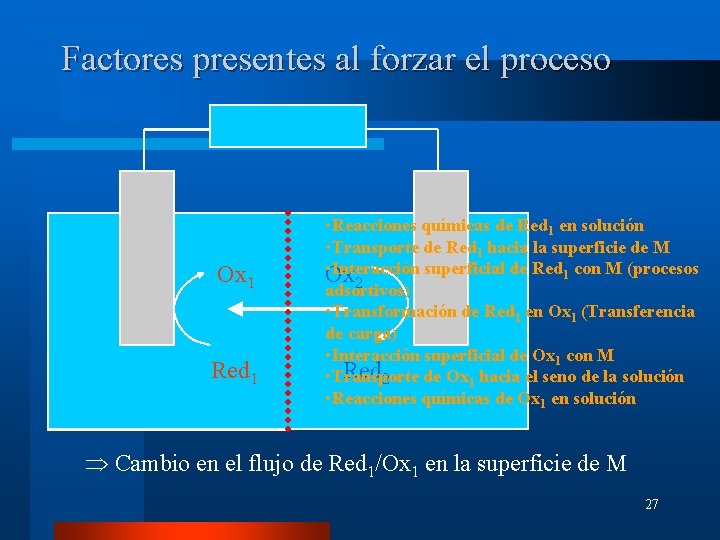
Factores presentes al forzar el proceso Ox 1 Red 1 • Reacciones químicas de Red 1 en solución • Transporte de Red 1 hacia la superficie de M • Interacción superficial de Red 1 con M (procesos Ox 2 adsortivos) • Transformación de Red 1 en Ox 1 (Transferencia de carga) • Interacción superficial de Ox 1 con M Red 2 de Ox 1 hacia el seno de la solución • Transporte • Reacciones químicas de Ox 1 en solución Cambio en el flujo de Red 1/Ox 1 en la superficie de M 27

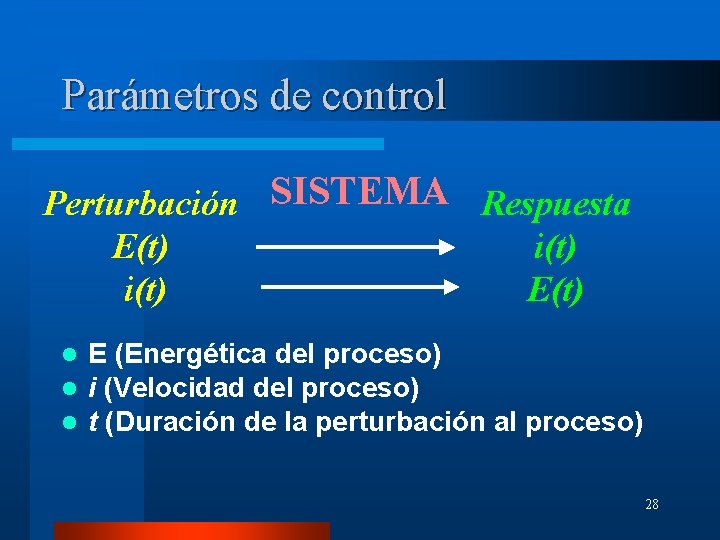
Parámetros de control Perturbación SISTEMA Respuesta E(t) i(t) E(t) l l l E (Energética del proceso) i (Velocidad del proceso) t (Duración de la perturbación al proceso) 28

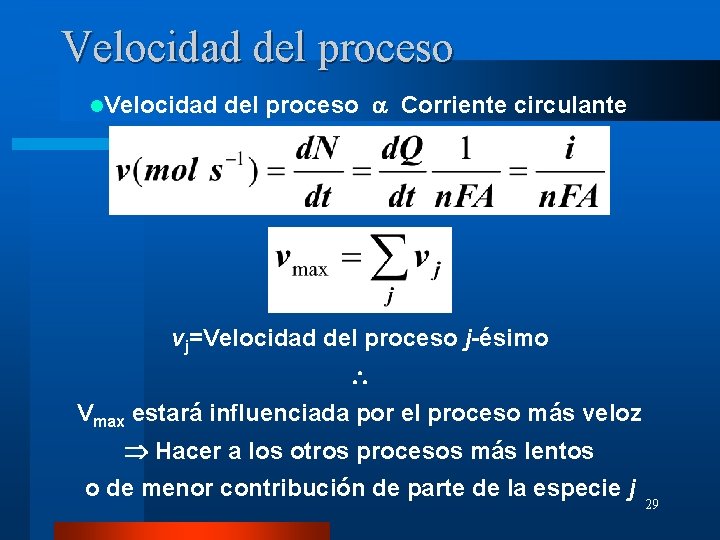
Velocidad del proceso l. Velocidad del proceso Corriente circulante vj=Velocidad del proceso j-ésimo Vmax estará influenciada por el proceso más veloz Hacer a los otros procesos más lentos o de menor contribución de parte de la especie j 29

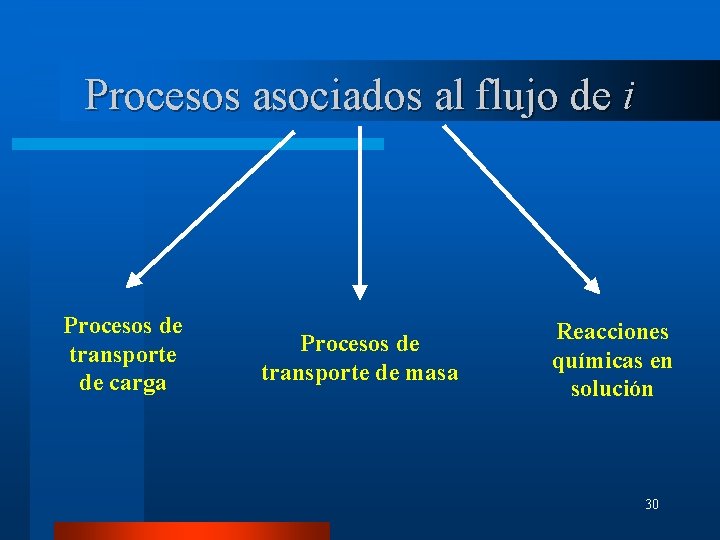
Procesos asociados al flujo de i Procesos de transporte de carga Procesos de transporte de masa Reacciones químicas en solución 30

Selección de condiciones experimentales Vproceso = vtransferencia de carga + vtransporte de masa + vreacciones químicas Transferencia de carga TM y Rxns Q Rápidas Transporte de masa TC y Rxns Q Rápidas Reacciones químicas TC y TM Rápidadas 31

Fundamentos de electroquímica • Reacciones en disolución (reacciones redox) • Celda electroquímica • Reacción electroquímica • Potenciometria de corriente nula • Electrodo Normal de Hidrogeno y sistemas de referencia • Potenciostato (instrumentación) • Factores que alteran la velocidad del proceso • Transferencia de carga (BV) • Transferencia de masa (Nernst-Planck) • Leyes de Fick 32

Transferencia de carga Ecuación de Butler-Volmer ineta = io {exp( a z F h/RT) – exp(- c z F h/RT)} Ecuación de Wagner-Traud icorrosión = ioa {exp( aa F [f*- foa]/RT) -exp(- ac F [f*- foa]/RT) } = - ioc {exp( ca F [f*- foc]/RT) - exp(- cc F [f*- foc]/RT) } 33

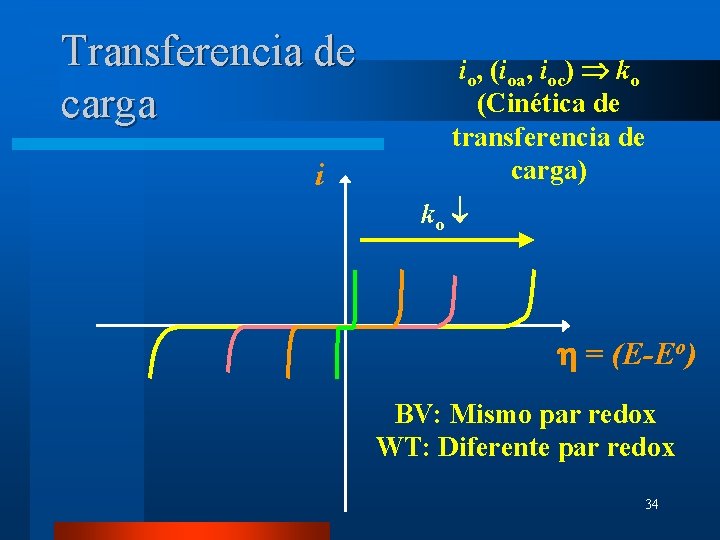
Transferencia de carga i io, (ioa, ioc) ko (Cinética de transferencia de carga) ko h = (E-Eo) BV: Mismo par redox WT: Diferente par redox 34

Cantidad a electrolizar Relaciones Área vs Volumen, Área vs Concentración A/V o A/C bajo Poca electrólisis total (microelectrólisis) A/V o A/C alto Consumo alto de sustancia (macroelectrólisis) Selección del método = f (Eficiencia de transferencia de masa) 35

Fundamentos de electroquímica • Reacciones en disolución (reacciones redox) • Celda electroquímica • Reacción electroquímica • Potenciometria de corriente nula • Electrodo Normal de Hidrogeno y sistemas de referencia • Potenciostato (instrumentación) • Factores que alteran la velocidad del proceso: • Transferencia de carga (BV) • Transferencia de masa (Nernst-Planck) • Leyes de Fick 36

Transporte de masa Difusión Migración Convección Otros factores influirán en J(x) total (Rxns químicas, adsorción, presencia de nuevas fases, etc. ) Ecuación de Nernst-Planck 37

Leyes de Fick Condiciones de distribución espacial de concentración Condiciones de distribución temporal de concentración xk: k-ésima coordenada espacial de distribución 38

Difusión en una sola dimensión = 0 No hay transformación (i=0) 0 Hay transformación (i 0) = 0 Flujo constante (Estado estacionario) 0 Flujo variable (Estado no estacionario, “transient techniques”) 39

Fundamentos de electroquímica • Reacciones en disolución (reacciones redox) • Celda electroquímica • Reacción electroquímica • Potenciometría de corriente nula • Electrodo Normal de Hidrógeno y sistemas de referencia • Potenciostato (instrumentación) • Factores que alteran la velocidad del proceso: • Transferencia de carga (BV) • Transferencia de masa (Nernst-Planck) • Leyes de Fick 40

41

42

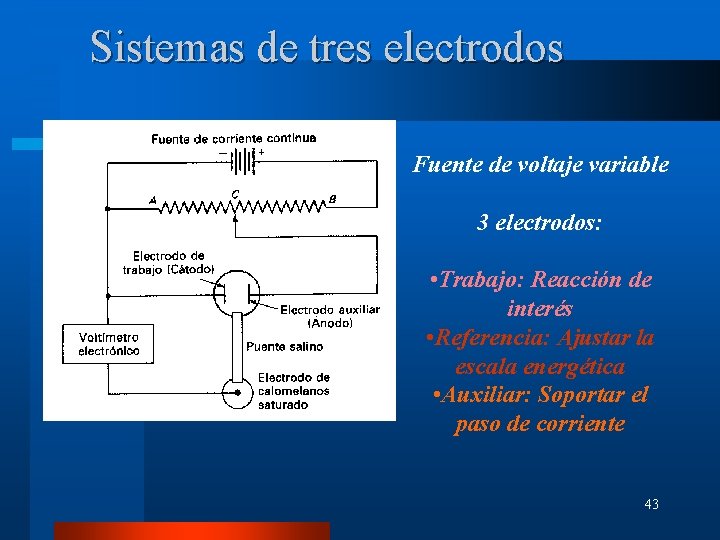
Sistemas de tres electrodos Fuente de voltaje variable 3 electrodos: • Trabajo: Reacción de interés • Referencia: Ajustar la escala energética • Auxiliar: Soportar el paso de corriente 43

Micro y macroelectrólisis Relaciones Área vs Volumen, Área vs Concentración A/V o A/C bajo Poca electrólisis total (microelectrólisis) (cantidad transformada=2%Co*) A/V o A/C alto Consumo alto de sustancia (macroelectrólisis) (transformación total) Selección del método = f (Eficiencia de transferencia de masa) 44

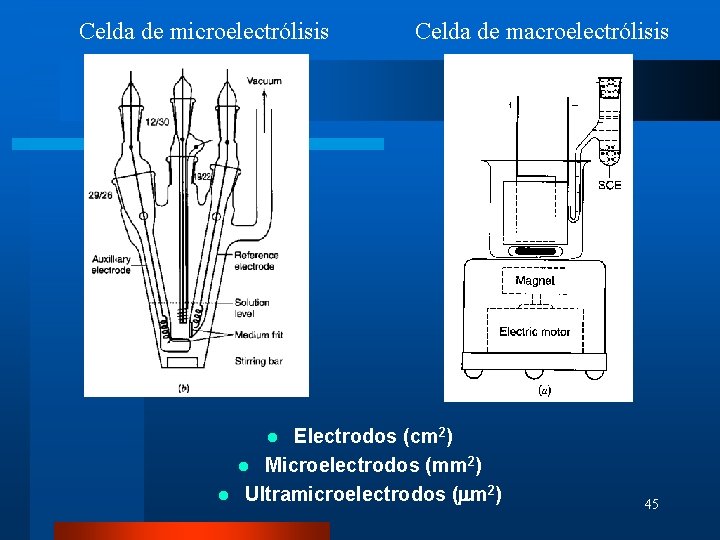
Celda de microelectrólisis Celda de macroelectrólisis Electrodos (cm 2) l Microelectrodos (mm 2) l Ultramicroelectrodos (mm 2) l 45

Condiciones de validez l No hay transferencia de masa l Conducción iónica Fuente de voltaje variable 3 electrodos: • Trabajo: Reacción de interés • Referencia: Ajustar la escala energética • Auxiliar: Soportar el paso de corriente 46