Biotechnolgia gnmanipulcik transzgenikus llnyek Kovcs Tams 2020 Biotechnolgia

Biotechnológia, génmanipulációk, transzgenikus élőlények Kovács Tamás 2020.

Biotechnológia • • • • Rekombináns DNS technológia DNS klónozás Restrikciós endonukleáz Gélelektroforézis Hibridizáció Southern blot Rekombináns DNS ligáz Baktérium transzfromáció Plazmid, vektorok, klónozó vektorok DNS könyvtár- genomika c. DNS könyvtár-m. RNS PCR DNS szekvenálás, humán genom projekt In situ hibridizáció

Klónozás A DNS-klónozás során egy DNSfragmentumot megfelelő gazdasejtben sokszorosítanak, amplifikálnak. klón: (1) Genetikailag azonos sejtek vagy egyedek összessége, amelyek aszexuális osztódással keletkeznek egy közös őstől. (2) Aszexuális úton létrejött egyed, amely azonos "szülőjével". (A "klónozás" alapjelentése valamit végtelen számban előállítani. ) Dolly Tapsilla, Klonilla (magyar vonatkozás) Dolly, 1996. július 5. , Edinburgh
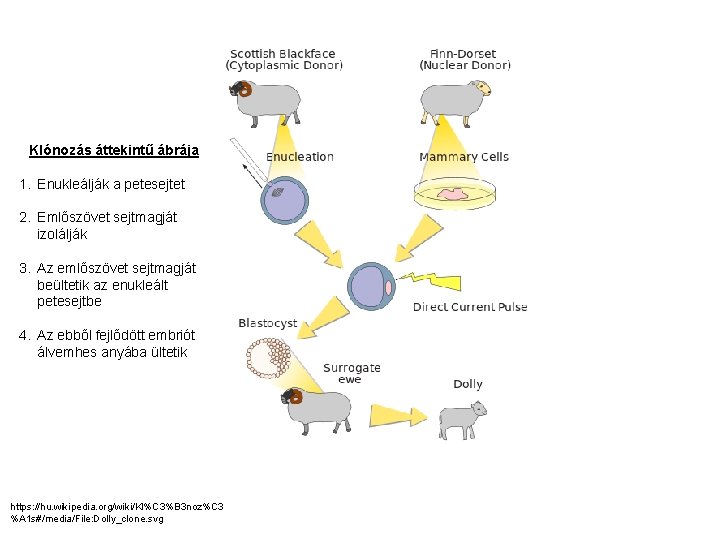
Klónozás áttekintű ábrája 1. Enukleálják a petesejtet 2. Emlőszövet sejtmagját izolálják 3. Az emlőszövet sejtmagját beültetik az enukleált petesejtbe 4. Az ebből fejlődött embriót álvemhes anyába ültetik https: //hu. wikipedia. org/wiki/Kl%C 3%B 3 noz%C 3 %A 1 s#/media/File: Dolly_clone. svg

Gyakorlati felhasználás Apasági vizsgálat Bűnügyi minták feldolgozása Mutációk keresése Örökletes betegségek diagnosztizálása igazságügyi orvostani vizsgálatok diagnosztikai vizsgálatok A különböző vizsgálati anyagokból a DNS felsokszorozása PCR-ral történik, tipizálásuk pedig gélelektroforézissel. Lépései: 1. Mintavétel (haj, szájnyálkahártya törlet, vér) 2. DNS felsokszorozása PCR-ral 3. Tipizálás elektroforézissel/génszekvenálás 4. DNS minták kiértékelése 5. Szakvélemény

Biotechnológia Interdiszciplináris tudományterület. Klasszikus biotechnológia: olyan gyártási eljárást jelent, melyben valamilyen élő szervezet vagy annak alkotórészei végzik a termék előállítását. Pl. sör, bor, tejkészítmények. Az új biotechnológiai eljárásokban az ember által bizonyos célból genetikailag módosított élő szervezetek vesznek részt: - mikroorganizmusok - állatok - növények Területekre osztható: piros: diagnosztikai módszerek fehér: ipari biotechnológia zöld: agrár biotechnológia szürke: környezettechnika, környezetvédelem

Biotechnológia Az új biotechnológiai megközelítés lényege, hogy a kívánt fenotípust új/mutáns/szintetikus/szensze/antiszensze gének bevitelén keresztül új vagy módosított fehérjékkel, az anyagcsere megváltozásával érjük el. A génműködés vizsgálatának lehetőségei: – Gén (vagy termékeinek) bejuttatása megfelelő gazdasejtbe vagy gazdaszervezetbe és az előidézett fenotípus változások tanulmányozása – A sejt vagy szervezet saját, endogén génjének vagy a gén termékeinek megsemmisítése vagy hatástalanítása és a gén normális funkciójának megállapítása az észlelt működéskiesések alapján

Rekombináns DNS technológia • • • DNS szakasz azonosítása, izolálása, jellemzése Beépítés hordozóba (vektor + DNS fragment) Bejuttatás gazdasejtbe Elszaporítás gazdasejtben Tisztítás és vizsgálat Példa: humán gyógyszerkészítmény, amit rekombináns technológiával készítenek, az inzulin. -> Ez az első génsebészeti termék. 1982 Humulin: rekombináns baktériumokkal előállított humán inzulin. Tehát baktériumokban működő emberi gén termelte. Tudománytörténet: 1971 Paul Berg állította elő az első rekombináns DNS-t. Egy rákkeltő majomvírus DNS-ét kapcsolta össze E. coli egyik bakteriofágjának DNS-ével.
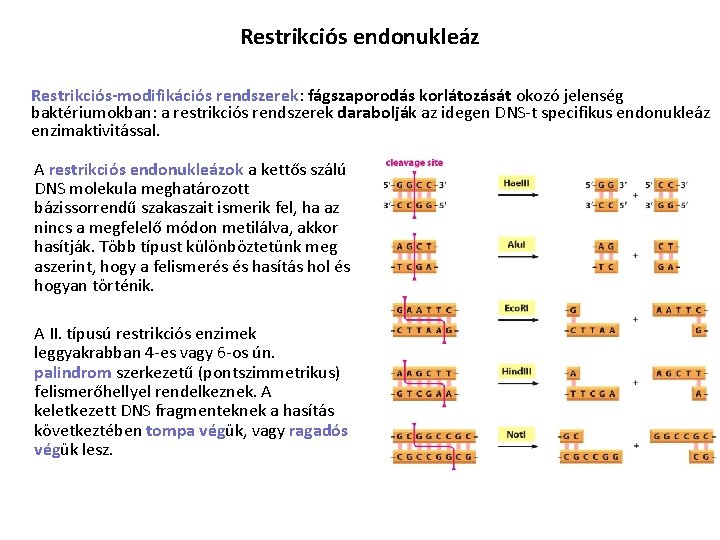
Restrikciós endonukleáz Restrikciós-modifikációs rendszerek: fágszaporodás korlátozását okozó jelenség baktériumokban: a restrikciós rendszerek darabolják az idegen DNS-t specifikus endonukleáz enzimaktivitással. A restrikciós endonukleázok a kettős szálú DNS molekula meghatározott bázissorrendű szakaszait ismerik fel, ha az nincs a megfelelő módon metilálva, akkor hasítják. Több típust különböztetünk meg aszerint, hogy a felismerés és hasítás hol és hogyan történik. A II. típusú restrikciós enzimek leggyakrabban 4 -es vagy 6 -os ún. palindrom szerkezetű (pontszimmetrikus) felismerőhellyel rendelkeznek. A keletkezett DNS fragmenteknek a hasítás következtében tompa végük, vagy ragadós végük lesz.

DNS ligáz Bármilyen eredetű két vagy több DNS-fragment összekapcsolódhat, ha kompatibilis véggel (a szálvégek komplementerek egymással) rendelkezik. Ezáltal a DNS-fragment beépíthető egy vektorba, majd a gazdasejtbe juttatható, ahol róla transzkripció történhet. A beépítéshez azonban egy további enzimre van szükség. Ez a ligáz. A két szomszédos fragment között a DNS cukor foszfát gerinc folytonosságát, a nukleotidok közötti foszfodiészter kötést ligáz enzimek állítják helyre. A DNS-fragment vektorba építésekor is fontos szerepet játszik a fragment és vektor komplementer végeinek összeligálása formájában.
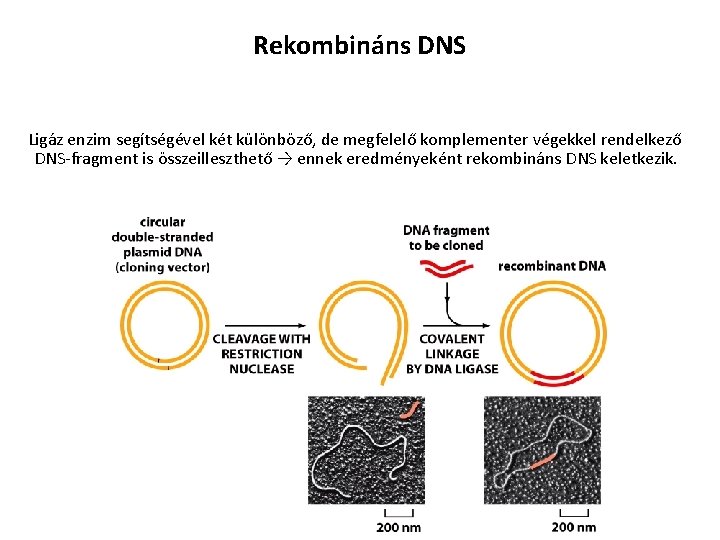
Rekombináns DNS Ligáz enzim segítségével két különböző, de megfelelő komplementer végekkel rendelkező DNS-fragment is összeilleszthető → ennek eredményeként rekombináns DNS keletkezik.

Transzformáció A restrikciós enzimekkel létrehozott, és agaróz-gélen elválasztott DNS-fragmenteket vissza kell juttatni valamilyen sejtbe, hogy azzal együtt el tudjuk szaporítani. Önmagában egy DNS-fragment nem képes replikálódni a sejten belül, ezért olyan hordozó, vektor DNS molekulával kell összekapcsolni, ami képes egy adott rendszerben replikálódni. Ezek a klónozó vektorok lehetnek: – plazmid eredetűek (horizontális géntranszfer) – vírus eredetűek – mesterséges kromoszómák is
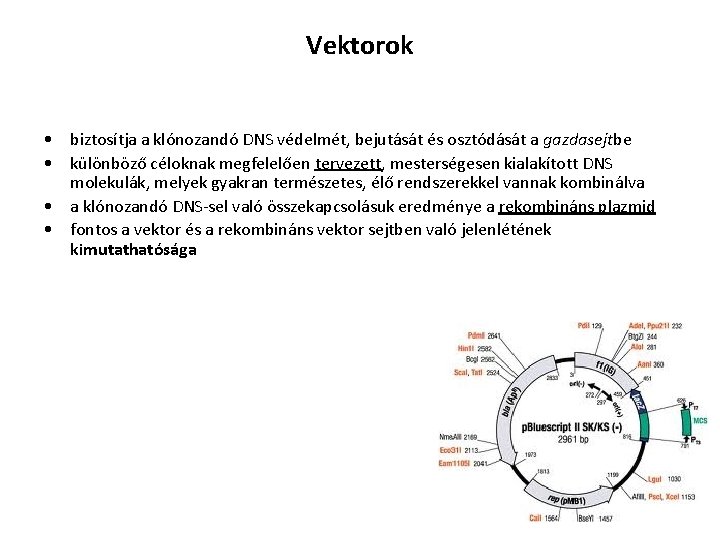
Vektorok • biztosítja a klónozandó DNS védelmét, bejutását és osztódását a gazdasejtbe • különböző céloknak megfelelően tervezett, mesterségesen kialakított DNS molekulák, melyek gyakran természetes, élő rendszerekkel vannak kombinálva • a klónozandó DNS-sel való összekapcsolásuk eredménye a rekombináns plazmid • fontos a vektor és a rekombináns vektor sejtben való jelenlétének kimutathatósága

Vektorok Klónozó – Plazmid – Lambda fág!!! – BAC – YAC • Expressziós – Prokarióta – Eukarióta • Élesztő • Bacillo vírus • Emlős sejt Jellemzői: – replikációs origo a replikációt elindító DNS szekvencia – szelektálható marker, olyan gén, aminek a jelenlétére lehet szelektálni, így a vektort tartalmazó sejtek szelektíven felnöveszthetők, kizárva a vektort nem tartalmazó sejteket (pl. : antibiotikum rezisztencia) – klónozó hely, vagyis egy vagy több olyan restrikciós endonukleáz hasítóhely, amelyből a vektoron csak egy található, hogy az idegen, inszert DNS beépítését segítse
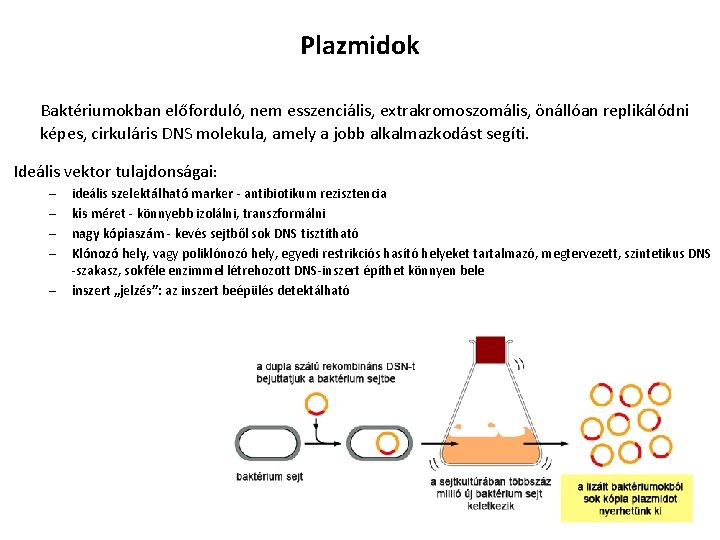
Plazmidok Baktériumokban előforduló, nem esszenciális, extrakromoszomális, önállóan replikálódni képes, cirkuláris DNS molekula, amely a jobb alkalmazkodást segíti. Ideális vektor tulajdonságai: – – – ideális szelektálható marker - antibiotikum rezisztencia kis méret - könnyebb izolálni, transzformálni nagy kópiaszám - kevés sejtből sok DNS tisztítható Klónozó hely, vagy poliklónozó hely, egyedi restrikciós hasító helyeket tartalmazó, megtervezett, szintetikus DNS -szakasz, sokféle enzimmel létrehozott DNS-inszert építhet könnyen bele inszert „jelzés”: az inszert beépülés detektálható

Genomkönyvtárak • a sejt teljes génállománya a megfelelő méretű fragmentekre darabolva vektor molekulákba (pl. lambda fág) építhető • a rekombináns DNS molekulákat fágfehérjékkel becsomagolják és fertőzéssel bejuttatják Escherichia coli baktérium sejtekbe • ha a genomtárból egy meghatározott szekvenciával rendelkező DNS-darabot akarnak kiválasztani, a bakterológiai lemezen létrejött tarfoltok DNS-ét egy filterre viszik át, majd molekuláris hibridizációval választják ki

c. DNS géntár • magasabb rendű eukarióták genomjában nem kódoló (intron) és kódoló (exon) szakaszokat különböztethetünk meg • transzkripció során ezek az intron szakaszok különböző mechanizmusoknak köszönhetően kivágódnak → az érett m. RNS-ben már nincsenek jelen • problémát okoznak a génátviteli kísérletekben: – sokszor nagyméretűek – célsejt nem feltétlenül eukarióta (prokariótákban nincs intron → nem rendelkezik az azt kivágó apparátussal sem) – bejuttatott gén a fehérjeszintézisét nem tudja irányítani • probléma megoldása → c. DNS géntár • lényege: – a vizsgált gén által kódolt (érett) m. RNS-t DNS (c. DNS, complementer DNS) formájába írják át, és ezt a c. DNS-t klónozzák – reverz transzkriptáz enzim (centrális dogma!) • célja általában az, hogy gyakorlati felhasználásra különböző fehérjéket termeltessenek (pl. inzulin, interferon, növekedési faktor……)
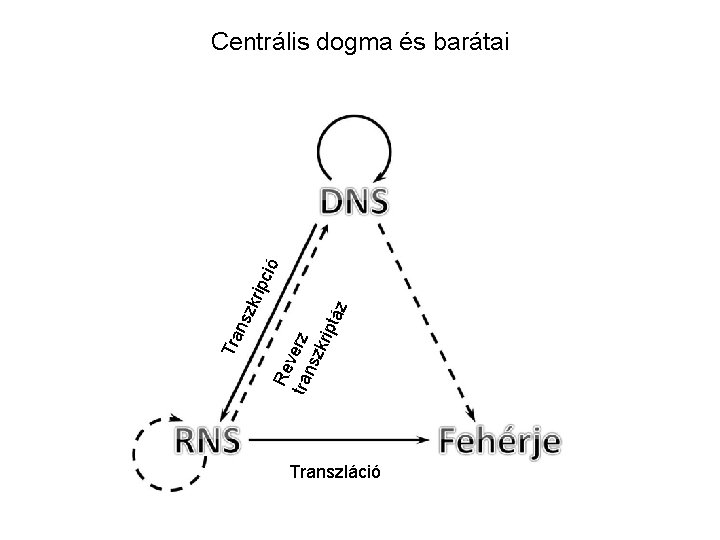
z Re v tra erz nsz krip tá Tra nsz krip ció Centrális dogma és barátai Transzláció

A klónozott gén vizsgálata gélelektroforézis Southern blot Western blot Northern blot PCR http: //semmelweis. hu/igazsagugy/files/2012/06/22_mszlev. pdf
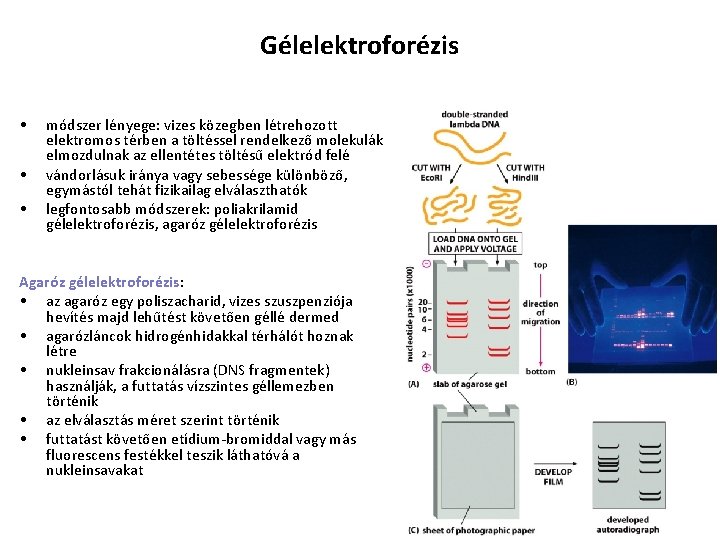
Gélelektroforézis • • • módszer lényege: vizes közegben létrehozott elektromos térben a töltéssel rendelkező molekulák elmozdulnak az ellentétes töltésű elektród felé vándorlásuk iránya vagy sebessége különböző, egymástól tehát fizikailag elválaszthatók legfontosabb módszerek: poliakrilamid gélelektroforézis, agaróz gélelektroforézis Agaróz gélelektroforézis: • az agaróz egy poliszacharid, vizes szuszpenziója hevítés majd lehűtést követően géllé dermed • agarózláncok hidrogénhidakkal térhálót hoznak létre • nukleinsav frakcionálásra (DNS fragmentek) használják, a futtatás vízszintes géllemezben történik • az elválasztás méret szerint történik • futtatást követően etídium-bromiddal vagy más fluorescens festékkel teszik láthatóvá a nukleinsavakat


Hibridizációs technikák - Southern blot • ha denaturált nukleinsavat valamilyen módon jelölt nukleinsavpróba jelenlétében renaturálnak, a jelölt próba bázispárosodni képes a vizsgált mintában jelenlévő, esetleg komplementer láncokkal → detektálható hibrid képződik • vizsgálható, hogy – két nukleinsavlánc (minta és próba) komplementer-e – ha igen, milyen mértékben • számos molekuláris biológiai technika alapját képezi, pl. Southern blot, in situ hibridizáció, FISH, RFLP

Southern blot • célja, hogy nagy molekulasúlyú DNS-ből azonosítson olyan restrikciós fragmentumokat, amelyek valamilyen szempontból érdekes DNS-régiót tartalmaznak • restrikciós endonukleázzal vágott agaróz gélen elválasztott fragmenteket, lúgos közegben denaturációt végeznek és a DNS-t a gélből nitrocellulóz vagy nylon membránra viszik át • radioaktív próbával a hibridizációt a membránon végzik el → a keresett fragmentum az audiogrammon csíkok formájában fog megjelenni
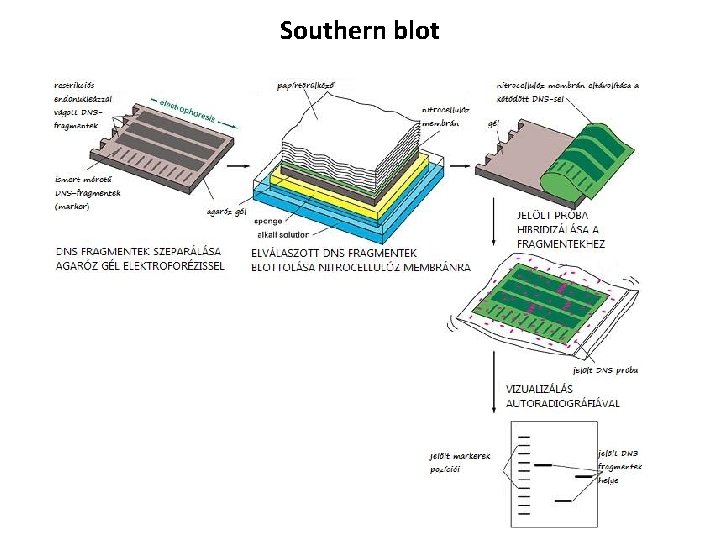
Southern blot


Polymerase chain reaction • a polimeráz láncreakció egy bizonyos DNS szakasz felamplifikálására (megsokszorozására) képes egy DNS mixben • működéséhez szükséges: – szintetizálandó új szál szekvenciáját meghatározó, templát DNS szál – a szintézis kezdetét meghatározó primer: azok az oligonukleotidok, amelynek segítségével meghatározzuk a szintézis kezdetének helyét és irányát – dezoxiribonukleotid-trifoszfát ( d. ATP, d. CTP, d. GTP, d. TTP) • a polimeráz láncreakciónál két oligonukleotid primer által behatárolt DNS szakaszt sokszorozunk meg egy hőstabil DNS polimeráz és számos egymást követő szintézis ciklus segítségével • Lépései: – szálak szétválasztása (denaturálás) – a primerek kötődése (annealing) – az új szálak bioszintézise (extension)

Polymerase chain reaction 1. – – – 2. – – 3. – Denaturálás azt a hőmérsékletet, melynél egy adott kettős szálú DNS fele denaturálódott, egyes szálú állapotban van → olvadási hőmérséklet, jele Tm (melting temperature, ált. 90 -94 C) ez az a hőmérséklet, melynél a potenciális primerkötő helyek felén primer található ezen a hőmérsékleten az enzimatikus reakciók leállnak → hőstabil polimerázra van szükség (pl. Taq polimeráz) Annealing hőmérséklet csökkentése, oligonukleotid primer képes bekötődni a DNS szál komplementer helyére (ált. 36 -72 C) kritikus fázis, reakció specifitása attól függ, hogy a primerek csak a megfelelő célszekvenciához kössenek Extenzió polimeráz optimális hőmérsékletének biztosításakor megszintetizálódik a komplementer DNS szál (ált. 72 C)
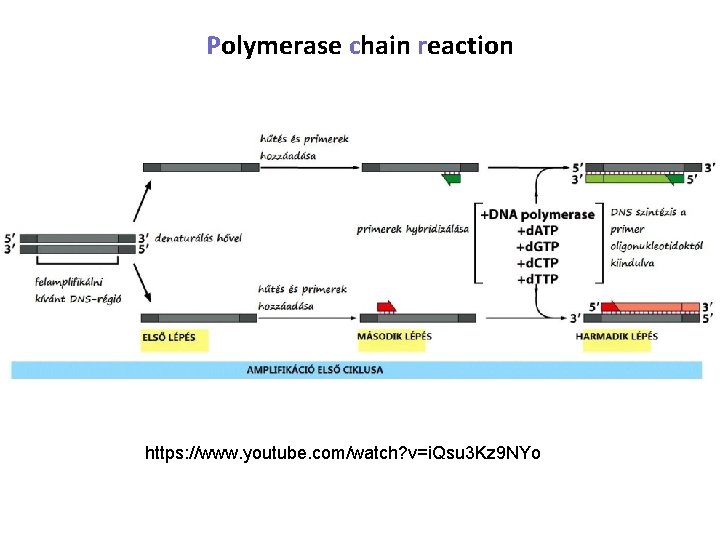
Polymerase chain reaction https: //www. youtube. com/watch? v=i. Qsu 3 Kz 9 NYo
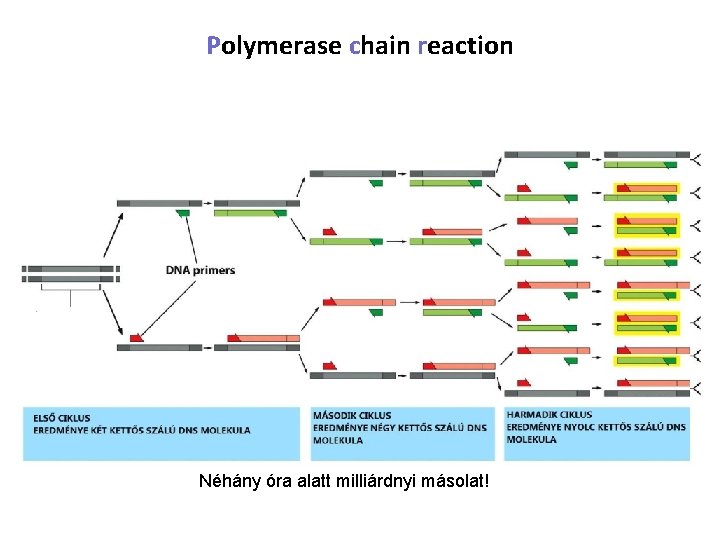
Polymerase chain reaction Néhány óra alatt milliárdnyi másolat!
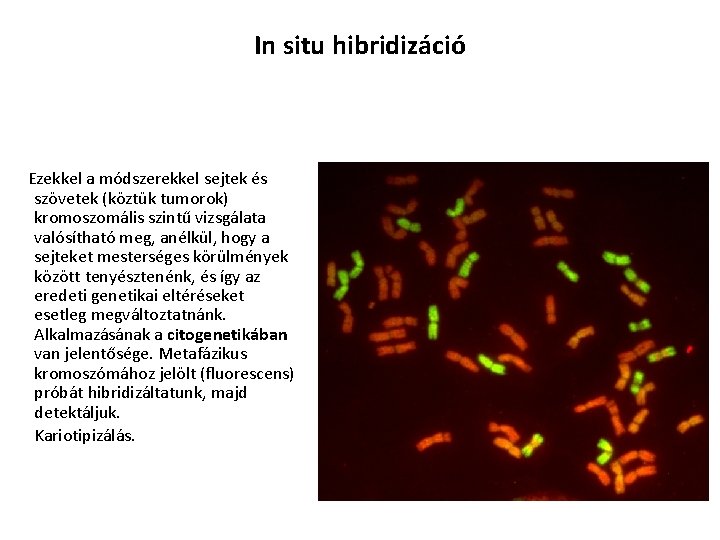
In situ hibridizáció Ezekkel a módszerekkel sejtek és szövetek (köztük tumorok) kromoszomális szintű vizsgálata valósítható meg, anélkül, hogy a sejteket mesterséges körülmények között tenyésztenénk, és így az eredeti genetikai eltéréseket esetleg megváltoztatnánk. Alkalmazásának a citogenetikában van jelentősége. Metafázikus kromoszómához jelölt (fluorescens) próbát hibridizáltatunk, majd detektáljuk. Kariotipizálás.

DNS szekvenálás • DNS-fragmentek elsődleges szerkezetének meghatározása • két módszer: – – Sanger-féle didezoxi, láncterminációs módszer Maxam-Gilbert módszer
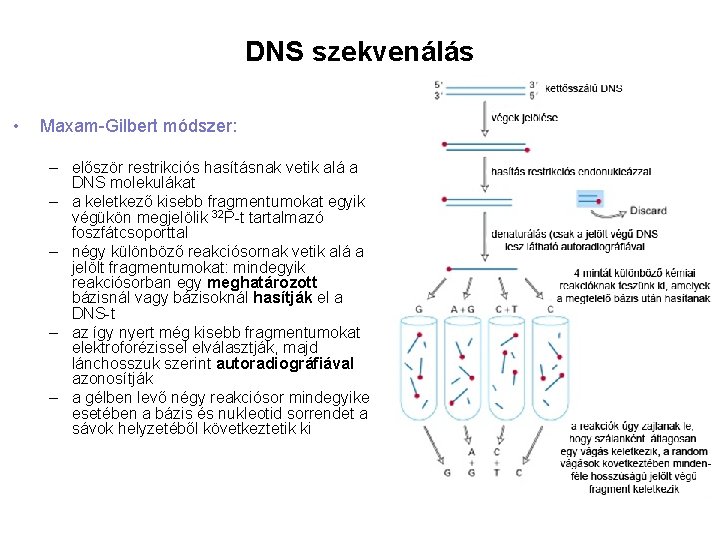
DNS szekvenálás • Maxam-Gilbert módszer: – először restrikciós hasításnak vetik alá a DNS molekulákat – a keletkező kisebb fragmentumokat egyik végükön megjelölik 32 P-t tartalmazó foszfátcsoporttal – négy különböző reakciósornak vetik alá a jelölt fragmentumokat: mindegyik reakciósorban egy meghatározott bázisnál vagy bázisoknál hasítják el a DNS-t – az így nyert még kisebb fragmentumokat elektroforézissel elválasztják, majd lánchosszuk szerint autoradiográfiával azonosítják – a gélben levő négy reakciósor mindegyike esetében a bázis és nukleotid sorrendet a sávok helyzetéből következtetik ki
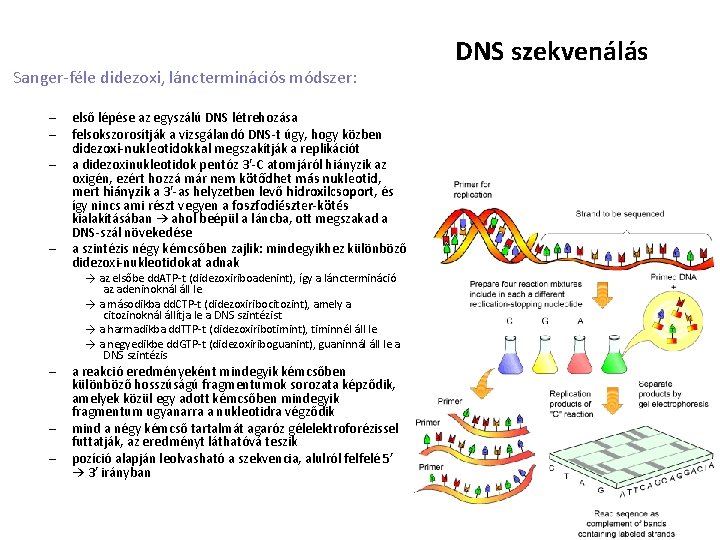
Sanger-féle didezoxi, láncterminációs módszer: – – – – első lépése az egyszálú DNS létrehozása felsokszorosítják a vizsgálandó DNS-t úgy, hogy közben didezoxi-nukleotidokkal megszakítják a replikációt a didezoxinukleotidok pentóz 3′-C atomjáról hiányzik az oxigén, ezért hozzá már nem kötődhet más nukleotid, mert hiányzik a 3′-as helyzetben levő hidroxilcsoport, és így nincs ami részt vegyen a foszfodiészter-kötés kialakításában → ahol beépül a láncba, ott megszakad a DNS-szál növekedése a szintézis négy kémcsőben zajlik: mindegyikhez különböző didezoxi-nukleotidokat adnak → az elsőbe dd. ATP-t (didezoxiriboadenint), így a lánctermináció az adeninoknál áll le → a másodikba dd. CTP-t (didezoxiribocitozint), amely a citozinoknál állítja le a DNS szintézist → a harmadikba dd. TTP-t (didezoxiribotimint), timinnél áll le → a negyedikbe dd. GTP-t (didezoxiriboguanint), guaninnál áll le a DNS szintézis a reakció eredményeként mindegyik kémcsőben különböző hosszúságú fragmentumok sorozata képződik, amelyek közül egy adott kémcsőben mindegyik fragmentum ugyanarra a nukleotidra végződik mind a négy kémcső tartalmát agaróz gélelektroforézissel futtatják, az eredményt láthatóvá teszik pozíció alapján leolvasható a szekvencia, alulról felfelé 5’ → 3’ irányban DNS szekvenálás

Humán Genom Program A képen: • Craig Venter • Bill Clinton • Francis Collins 2001 február: Venter et al. : The sequence of the human genome. Science 291, 1304 -51 International Human Genom sequencing Consortium Initial sequencing and analysis of the human genome. Nature 409, 860 -921

Érdekesség (nem megtanulni!) Humán genomanalízis esetleges társadalmi hatásai • A genetikai betegségek és rendellenességek felismerése sokkal gyorsabb és olcsóbb lesz. • Egyénre szabott génterápia! • A biztosító molekulárisan elemzi a biztosított genomját és abból következtet a várható élettartamra és betegségekre. • Inteligencia és egyéb képességek felmérése a génjeink alapján. (Mi leszel fiam? Nem tudom, majd megnézem a génjeimet. ) • Genetikai predesztináció (arisztokrácia =>genokrácia) ? • A kialakuló humán génsebészet lehetőséget ad az ember genetikai módosítására és természetesen a genetikai betegségek gyógyítására.


Köszönöm a figyelmet!

Az előadás alapjául szolgáltak: • Szabó Klaudia: azonos című előadása • Heszky László & Galli Zsolt: „A genetika alapjai” • Jancsik Veronika: „A sejt molekuláris biológiája”
- Slides: 39