A Segunda Lei da Termodinmica Evitar desperdcios Conservar






















- Slides: 57


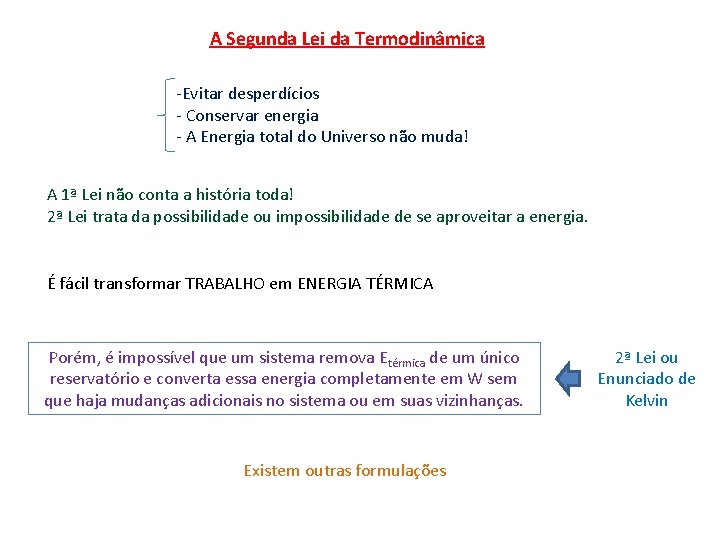
A Segunda Lei da Termodinâmica -Evitar desperdícios - Conservar energia - A Energia total do Universo não muda! A 1ª Lei não conta a história toda! 2ª Lei trata da possibilidade ou impossibilidade de se aproveitar a energia. É fácil transformar TRABALHO em ENERGIA TÉRMICA Porém, é impossível que um sistema remova Etérmica de um único reservatório e converta essa energia completamente em W sem que haja mudanças adicionais no sistema ou em suas vizinhanças. Existem outras formulações 2ª Lei ou Enunciado de Kelvin

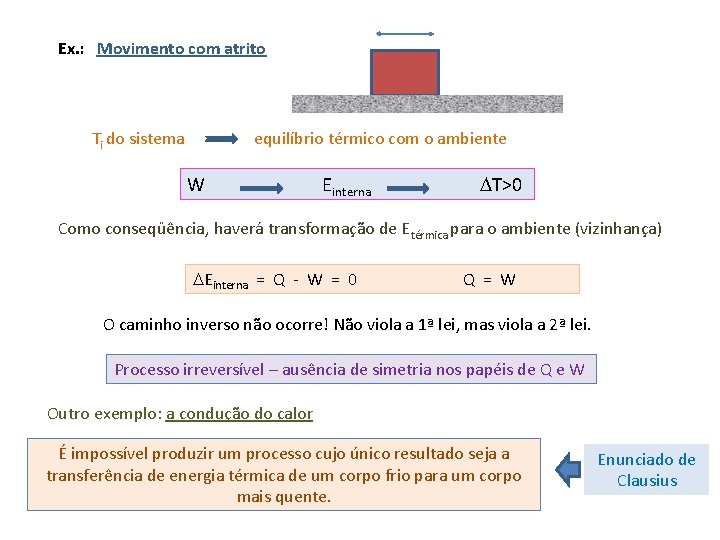
Ex. : Movimento com atrito Ti do sistema equilíbrio térmico com o ambiente W Einterna DT>0 Como conseqüência, haverá transformação de Etérmica para o ambiente (vizinhança) DEinterna = Q - W = 0 Q = W O caminho inverso não ocorre! Não viola a 1ª lei, mas viola a 2ª lei. Processo irreversível – ausência de simetria nos papéis de Q e W Outro exemplo: a condução do calor É impossível produzir um processo cujo único resultado seja a transferência de energia térmica de um corpo frio para um corpo mais quente. Enunciado de Clausius

Máquina térmica – é um dispositivo cíclico com o propósito de converter a maior quantidade possível de calor em trabalho mecânico

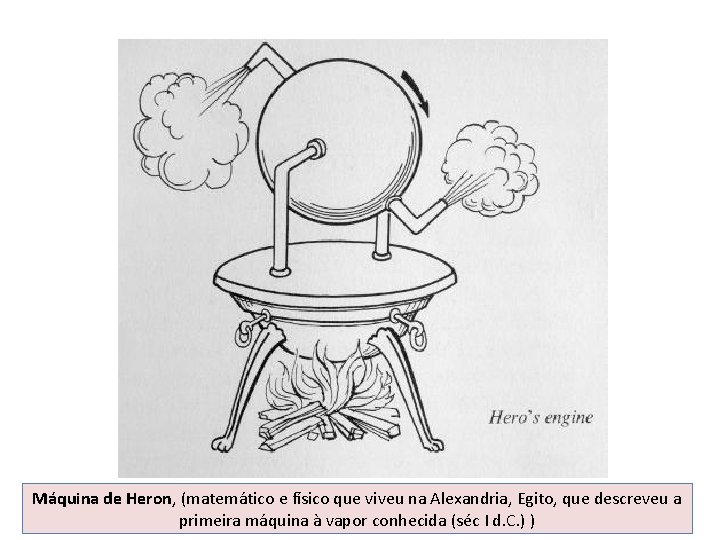
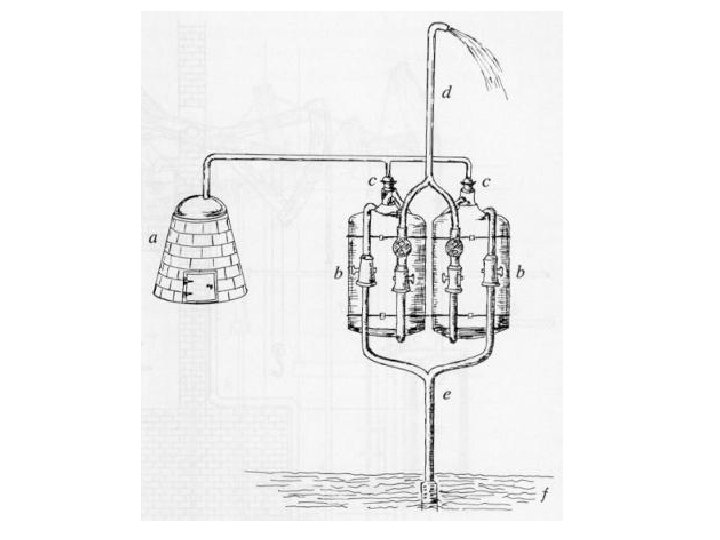
Máquina de Heron, (matemático e físico que viveu na Alexandria, Egito, que descreveu a primeira máquina à vapor conhecida (séc I d. C. ) )

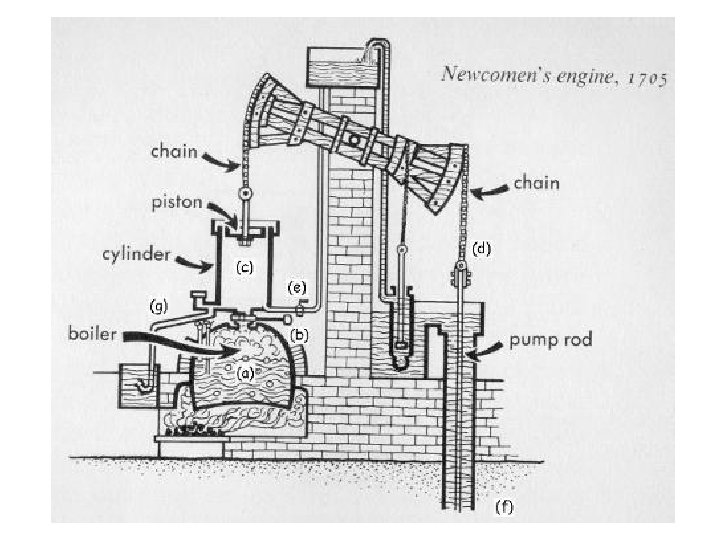
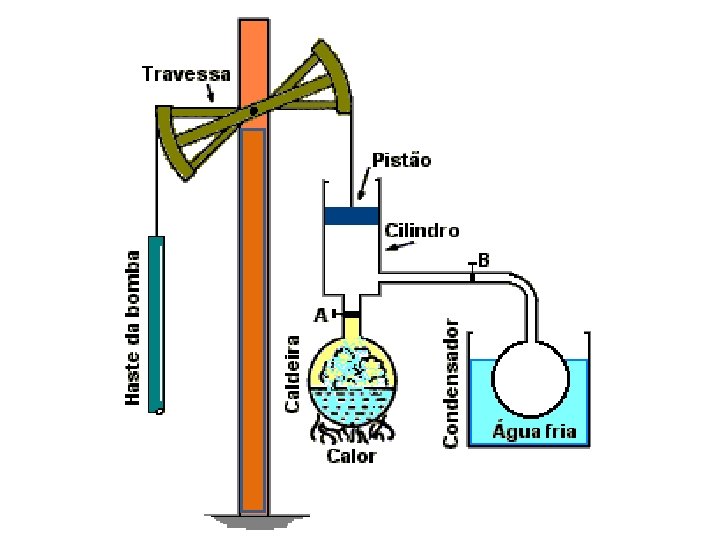
Inventores e aperfeiçoadores de máquinas térmicas Heron → Denis Papin → Thomas Savery → Thomas Newcomen → James Watt

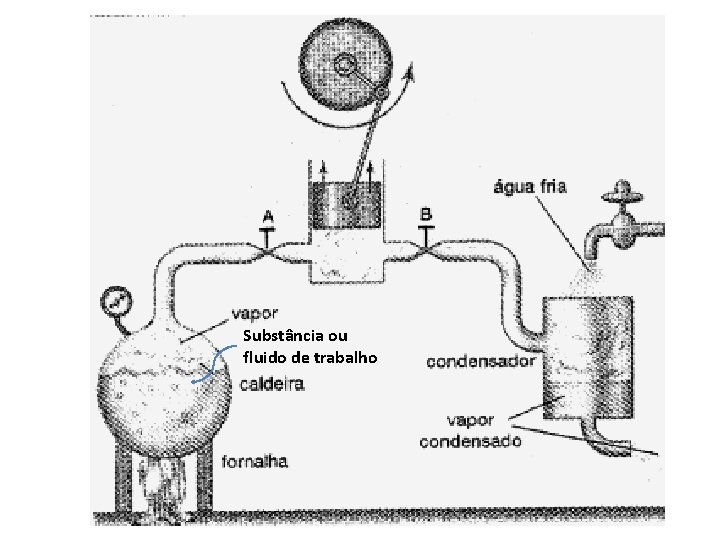
Substância ou fluido de trabalho







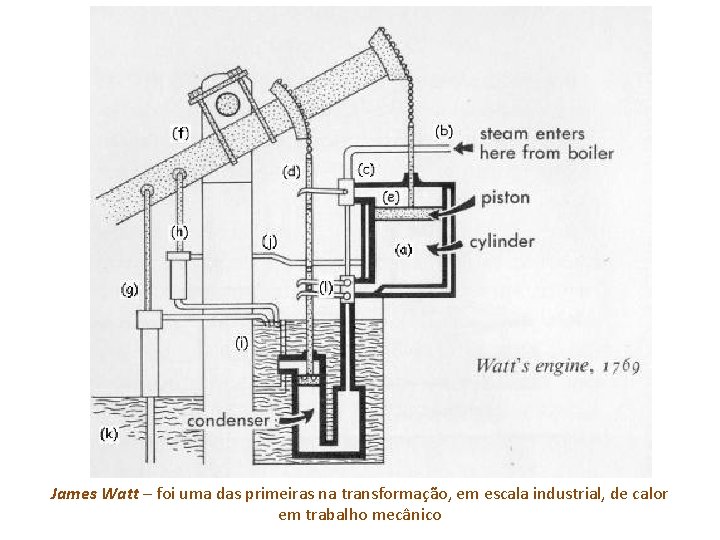
James Watt – foi uma das primeiras na transformação, em escala industrial, de calor em trabalho mecânico

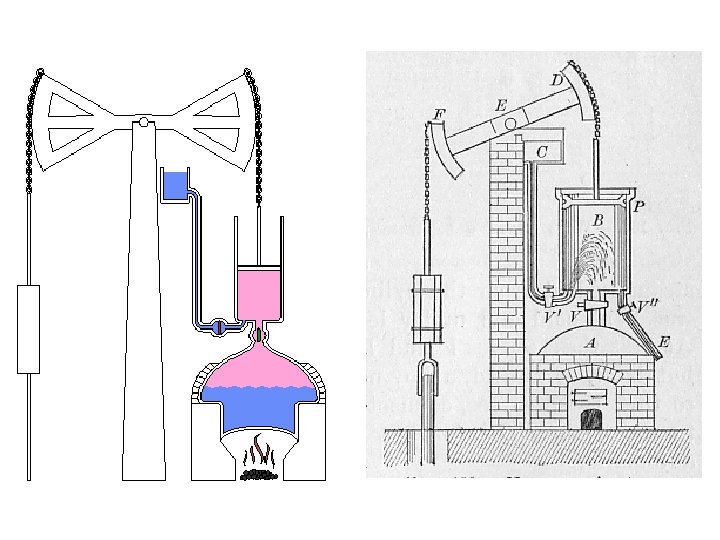
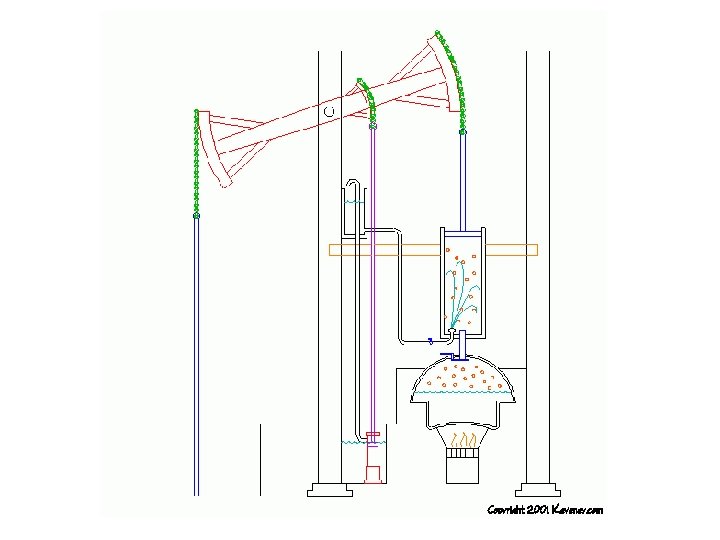
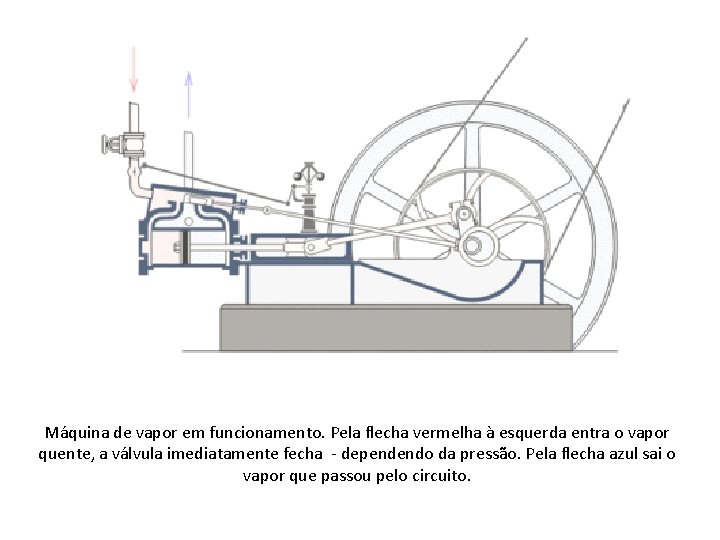
Máquina de vapor em funcionamento. Pela flecha vermelha à esquerda entra o vapor quente, a válvula imediatamente fecha - dependendo da pressão. Pela flecha azul sai o vapor que passou pelo circuito.


Na gravura acima podemos observar uma instalação industrial do século XVIII. As máquinas industriais eram acopladas a eixos que giravam graças a uma máquina térmica a vapor.

As locomotivas a vapor já existiam desde 1808 e, fora dos trilhos, os ônibus a vapor já circulavam comercialmente desde 1825 Motor a gasolina de Daimler

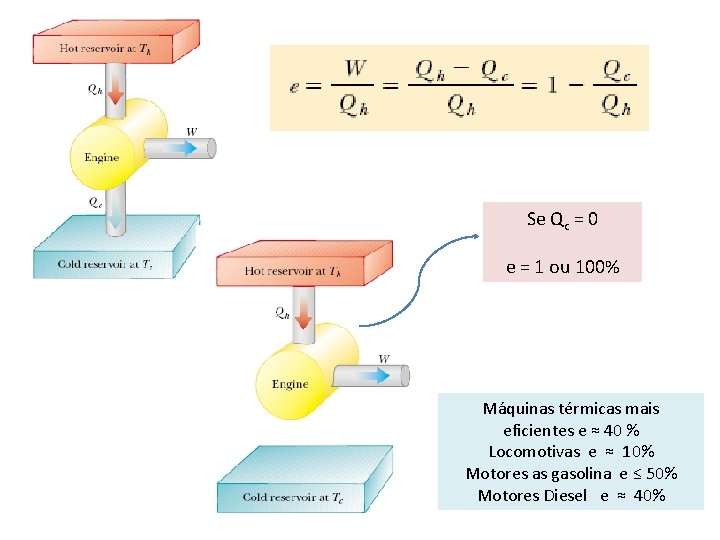
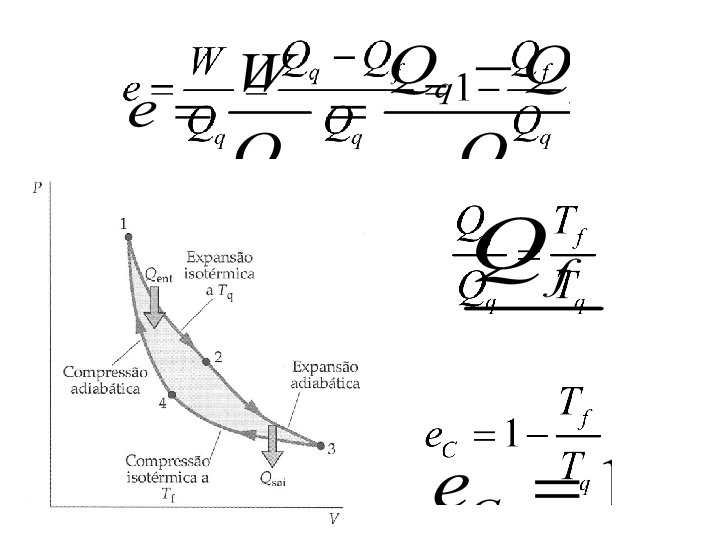
Se Qc = 0 e = 1 ou 100% Máquinas térmicas mais eficientes e ≈ 40 % Locomotivas e ≈ 10% Motores as gasolina e ≤ 50% Motores Diesel e ≈ 40%

Enunciado da segunda lei da termodinâmica relativo à máquina térmica É impossível construir uma máquina térmica, operando em ciclos, que produza o único efeito de extrair calor de um reservatório e realizar uma quantidade equivalente de trabalho A palavra ciclo é importante, pois para um processo que não seja cíclico é possível converter calor completamente em trabalho. Um gás ideal que sofre uma expansão isotérmica é um exemplo disso. Ex 19 -1 Durante cada ciclo uma máquina térmica absorve 200 J de calor de um reservatório quente, realiza trabalho e rejeita 160 J para um reservatório frio. Qual o rendimento da máquina? E X E R C Í C I O Uma máquina térmica tem um rendimento de 35%. a) Qual o trabalho efetuado por ciclo, considerando que a máquina recebe 150 J de energia térmica de um reservatório quente em cada ciclo? b) Que quantidade de energia térmica é descarregada no reservatório frio por ciclos? (a) 52, 5 J (b) 97, 5 J


Motor radial usado em aviões com hélice 22

Motor a vapor 23

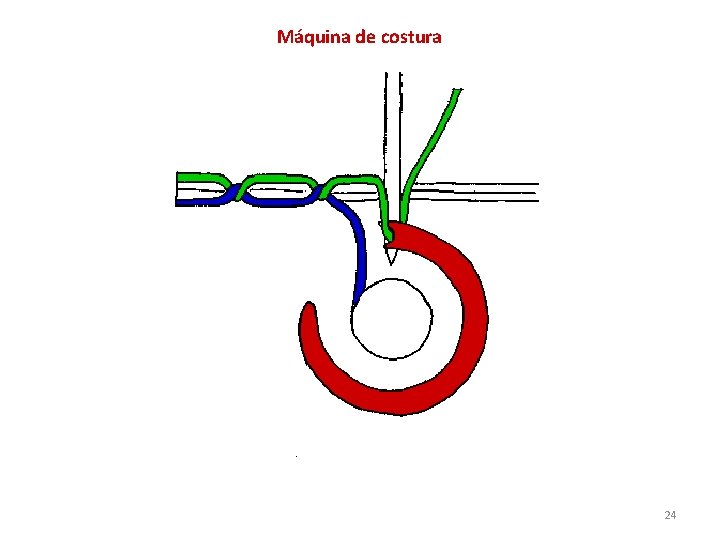
Máquina de costura 24

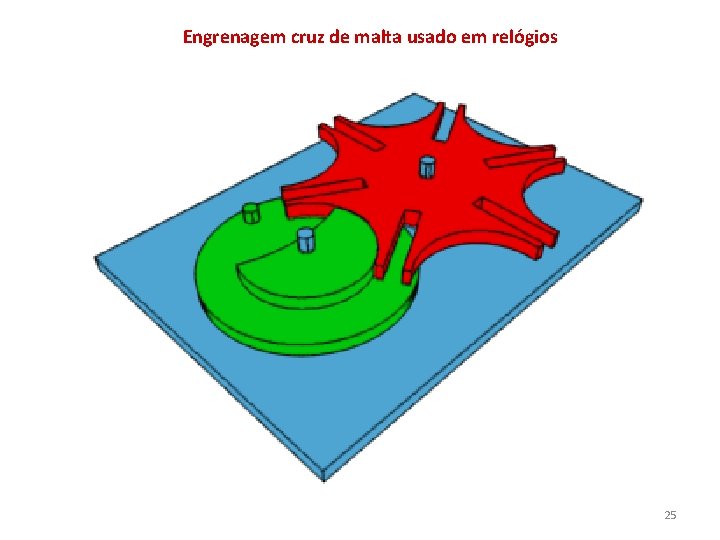
Engrenagem cruz de malta usado em relógios 25

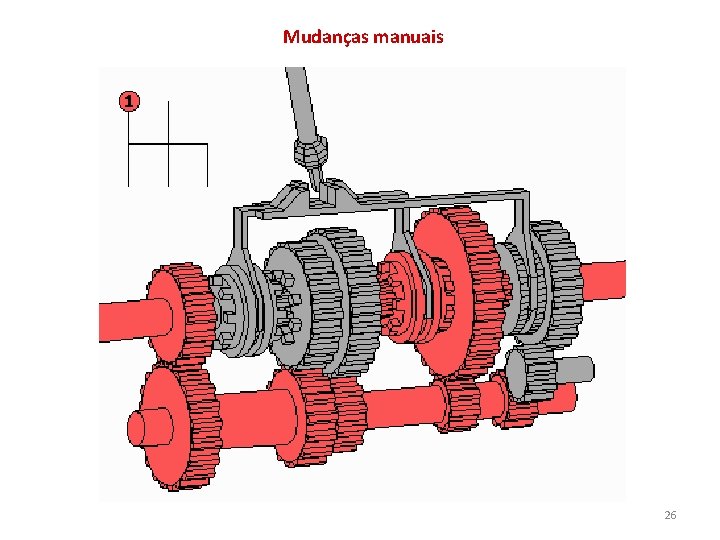
Mudanças manuais 26

Junta homocinética aquela que liga o motor à roda dianteira do carro, permitindo que você ande e vire a roda ao mesmo tempo 27

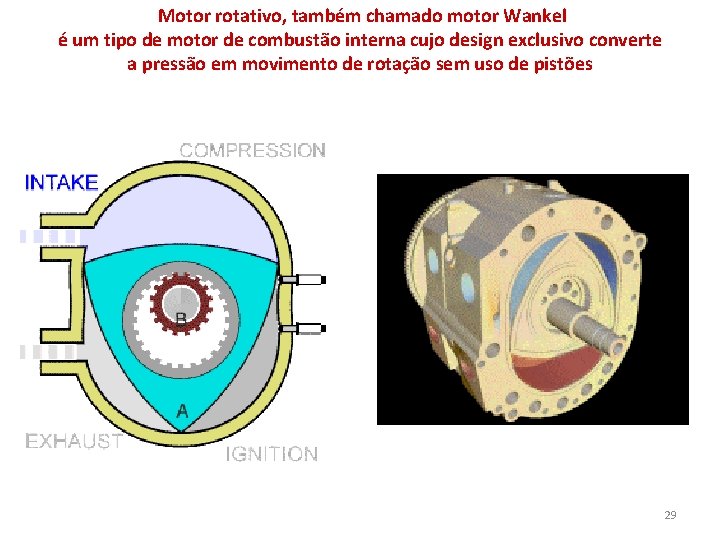
Motor rotativo, também chamado motor Wankel é um tipo de motor de combustão interna cujo design exclusivo converte a pressão em movimento de rotação sem uso de pistões 29

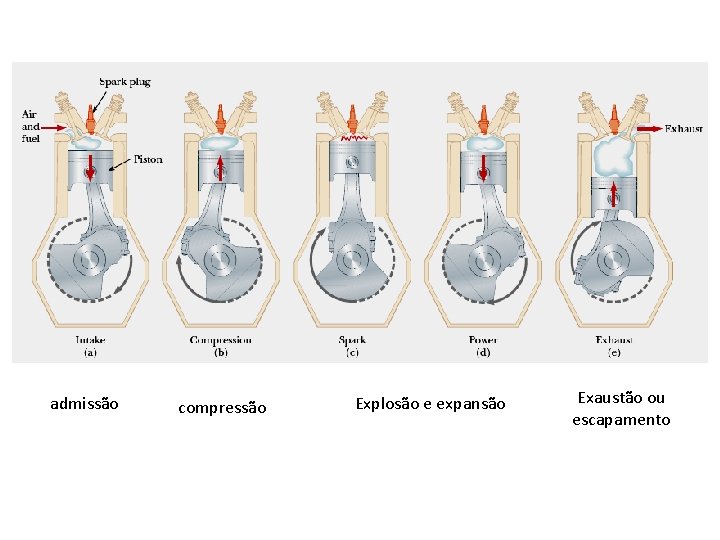
admissão compressão Explosão e expansão Exaustão ou escapamento


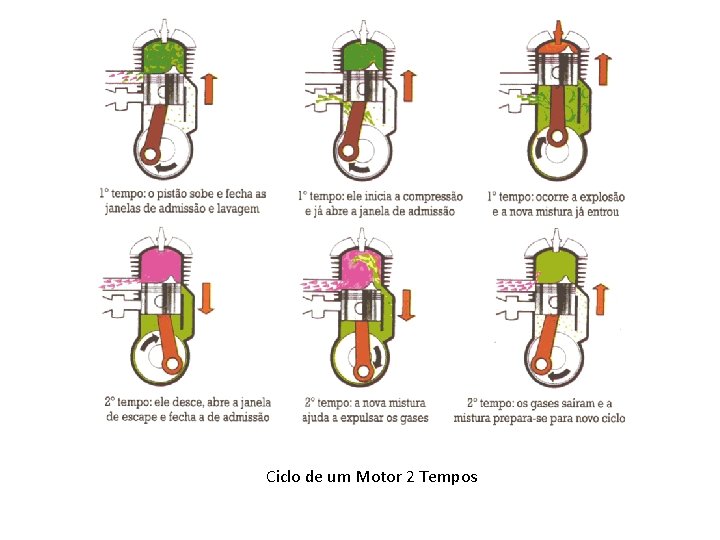
Ciclo de um Motor 2 Tempos


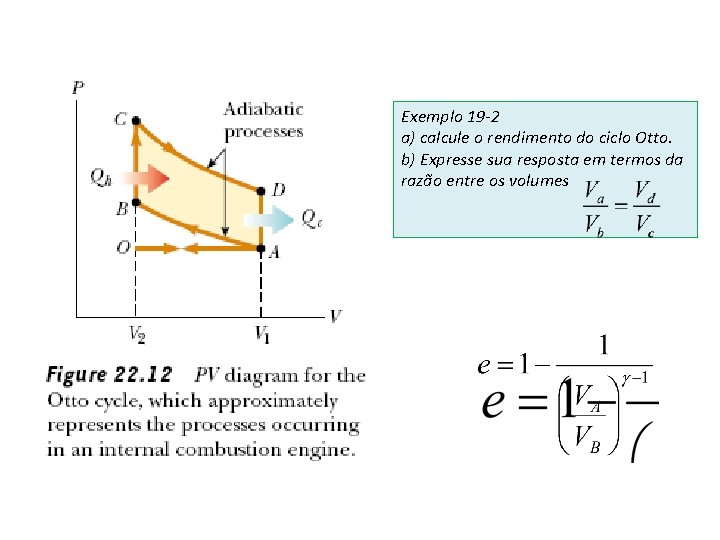
Exemplo 19 -2 a) calcule o rendimento do ciclo Otto. b) Expresse sua resposta em termos da razão entre os volumes


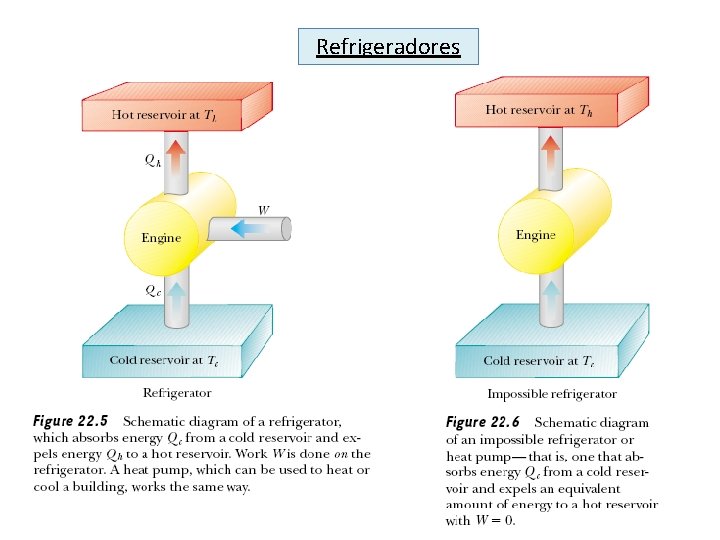
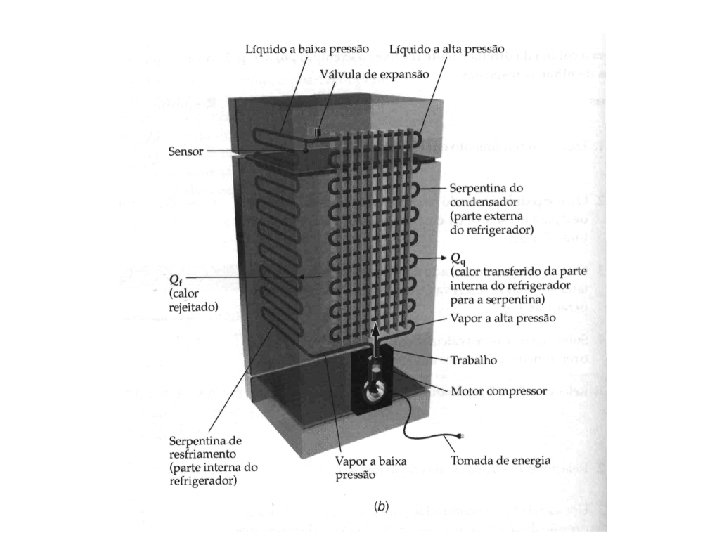
Refrigeradores

Enunciado da segunda lei da termodinâmica relativo ao refrigerador É impossível construir um refrigerador que opere segundo um ciclo e produza o único efeito de extrair calor de um corpo frio e rejeitar a mesma quantidade de calor para um corpo quente COP – coeficiente de desempenho Quanto maior o COP, melhor é o refrigerador! Exemplo 19 -3 Uma hora antes dos convidados começarem a chegar para sua festa você percebe, de repente, que esqueceu de comprar gelo para as bebidas. Assim, você põe às pressas um litro de água a 10 o. C em bandejas de cubo de gelo e as coloca no congelador. Você terá gelo a tempo para seus convidados? O rótulo em seu refrigerador especifica que o equipamento tem um coeficiente de desempenho de 5, 5 e uma potência avaliada em 550 W. Estima-se que somente 10% da potência são utilizados para formar o gelo.

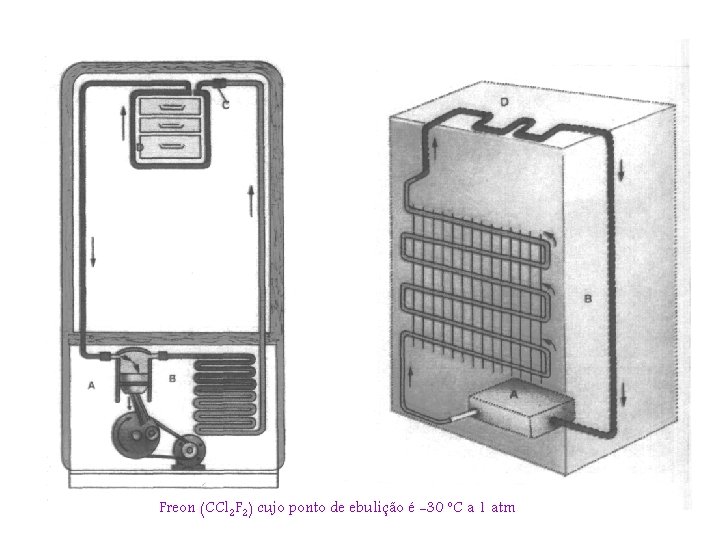
Freon (CCl 2 F 2) cujo ponto de ebulição é -30 o. C a 1 atm


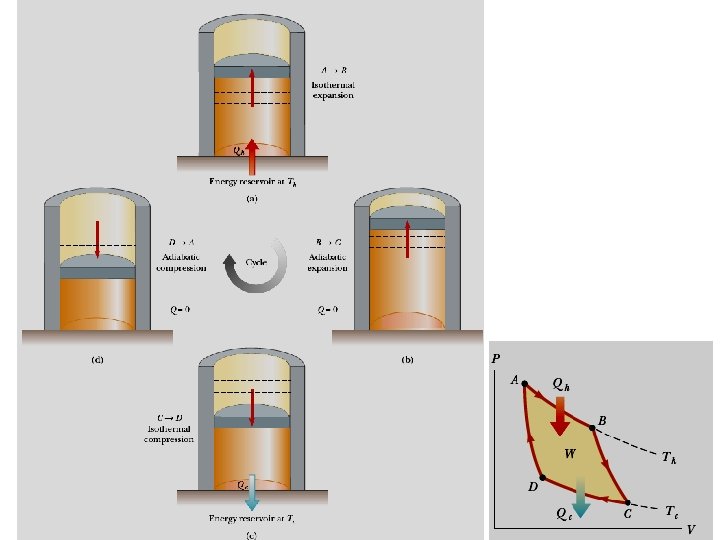
Teorema de Carnot (1824) Publicação de um trabalho: Reflexões sobre o poder motriz do fogo e sobre as máquinas adequadas para desenvolver esse poder. (Sadi Carnot – 1824) Propôs um ciclo ideal, cujo rendimento seria o maior possível Nenhuma máquina térmica, que opere entre dois reservatórios térmicos dados, pode ser mais eficiente do que uma máquina reversível que opere entre os mesmos dois reservatórios




Ex 19 -4 Uma máquina de Carnot opera entre um reservatório quente a 100 o. C (373 K) e um reservatório frio a 0 o. C (273 K). a) Qual o rendimento máximo possível dessa máquina? (e = 26, 8%) b) Se a máquina operar ao revés, como um refrigerador, qual será o coeficiente de desempenho máximo? (COP = 2, 73)

Ex 19 -5 Uma máquina remove 200 J de um reservatório quente a 100 o. C (373 K), realiza 48 J de trabalho e descarrega 152 J para um reservatório frio a 0 o. C (273 K). Que quantidade de trabalho é “perdida” por ciclo devido aos processos irreversíveis presentes na operação desta máquina? Exercício: Uma máquina de Carnot opera entre dois reservatórios de calor, um a 500 K e o outro a 300 K. a) Qual o rendimento desta máquina? (40%) b) Se 200 k. J de calor forem removidos do reservatório quente, que quantidade de trabalho poderia ser realizada? (80 k. J) Exercício: Uma máquina opera entre dois reservatórios de calor, um a 500 K e o outro a 300 K. Considera-se que 500 k. J de calor são removidos do reservatório quente e que são realizados 150 k. J de trabalho durante cada ciclo. Qual o rendimento dessa máquina? (30%)

BOMBAS DE CALOR É uma espécie de refrigerador com objetivo diferente, que é o de aquecer um corpo ou uma região de interesse. A eficiência de uma bomba de calor é representada pelo coeficiente de performance (COP), que é dado pela seguinte fórmula: Onde • é o calor liberado para o reservatório quente. • é o calor extraído do reservatório frio. • é o trabalho realizado no compressor.

Ex 19 -7 Uma bomba de calor ideal é usada para bombear o calor do ar externo, a -5 o. C, para o sistema de calefação de uma casa a 40 o. C. Que quantidade de trabalho é necessária para bombear 1 k. J de calor para o interior da casa?

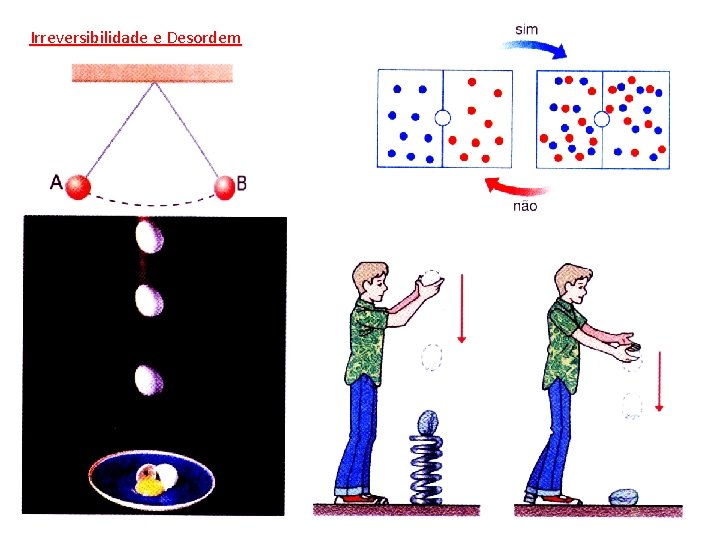
Irreversibilidade e Desordem

Entropia Existe uma função termodinâmica, chamada entropia (S), que é uma medida da desordem de um sistema É uma função do estado do sistema onde d. Qrev é a energia térmica que deve ser transferida para o sistema, num processo reversível, que leva o sistema do estado inicial ao final

Entropia de um gás ideal

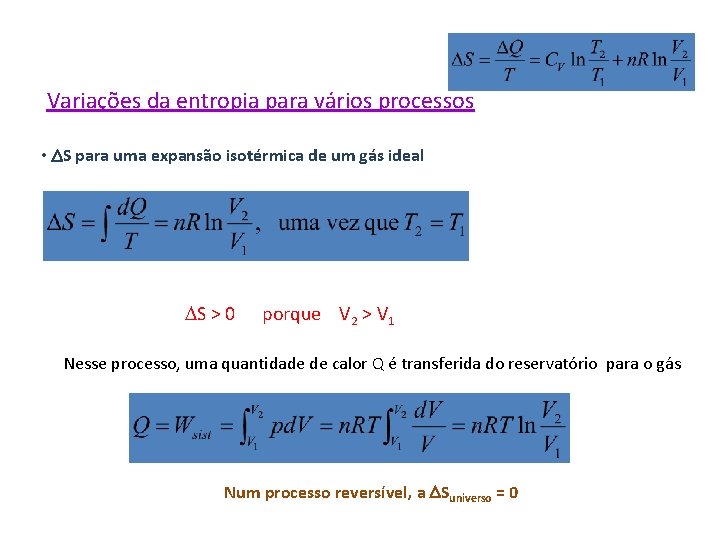
Variações da entropia para vários processos • DS para uma expansão isotérmica de um gás ideal DS > 0 porque V 2 > V 1 Nesse processo, uma quantidade de calor Q é transferida do reservatório para o gás Num processo reversível, a DSuniverso = 0

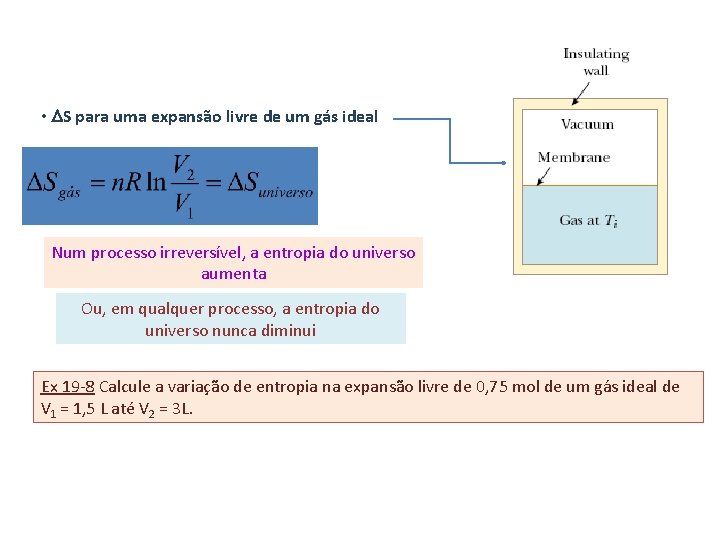
• DS para uma expansão livre de um gás ideal Num processo irreversível, a entropia do universo aumenta Ou, em qualquer processo, a entropia do universo nunca diminui Ex 19 -8 Calcule a variação de entropia na expansão livre de 0, 75 mol de um gás ideal de V 1 = 1, 5 L até V 2 = 3 L.

• DS para processos isobáricos Ex 19 -9 Suponha que 1 kg de água na temperatura T 1 = 30 o. C seja adicionado a 2 kg de água a T 2 = 90 o. C, num calorímetro de capacidade calorífica desprezível, a uma pressão constante de 1 atm. (a) Calcule a variação de entropia do sistema. (b) Calcule a variação de entropia do universo. • DS para uma colisão inelástica Sistema = bloco + chão + atmosfera Não há troca térmica entre o sistema e o exterior. O estado do sistema se altera porque a Eint foi aumentada da quantidade mgh A quantidade de energia que se torna indisponível num processo natural é diretamente proporcional ao aumento total de entropia DS, que acompanha o processo.

• DS na condução de calor de um reservatório para outro Ex 19 -10 - Variação de entropia num ciclo de Carnot Durante cada ciclo, uma máquina de Carnot remove 100 J de energia de um reservatório a 400 K, efetua trabalho e descarrega calor para um reservatório a 300 K. Calcule a variação de entropia de cada reservatório durante cada ciclo e mostre explicitamente que a variação de entropia do universo é nula para este processo reversível.



