ZELTLER VE ZNRLK ZELT VE TRLER zeltiler fiziksel


















































- Slides: 51

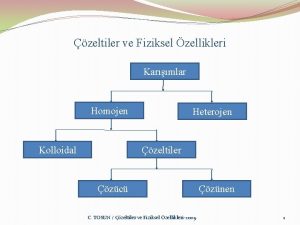
ÇÖZELTİLER VE ÇÖZÜNÜRLÜK

ÇÖZELTİ VE TÜRLERİ Çözeltiler, fiziksel özellikleri her yerinde aynı olan homojen karışımlardır. Bir çözeltide en az iki bileşen vardır. *Çözelti içinde miktarı çok olan bileşene "çözücü", *miktarı az olan bileşene ise "çözünen" denir.

Çözücü ve çözünen; katı, sıvı veya gaz olabilir. Buna göre çeşitli çözeltiler hazırlanabilir. Diğer bir ifadeyle, katı, sıvı ve gaz bir maddenin katı, sıvı ve gaz bir madde içerisinde homojen olarak dağılmasıyla çözeltiler oluşur. Örneğin;

Çözücü Çözünen Örnek Çözelti Sıvı Alkollü su (suda alkolün çözünmesi) Sıvı Katı Tuzlu su (suda tuz çözünmesi) Sıvı çözünmesi) Gaz Amonyaklı su (suda amonyağın Katı Sıvı Amalgam (gümüşte civanın çözünmesi) Katı Pirinç (bakırda çinkonun çözünmesi) Katı Gaz Palladyumda hidrojenin çözünmesi Gaz Azotta oksijenin çözünmesi

ÇÖZÜNME OLGUSU Çözücü ve çözünenin birbiri içinde homojen olarak karışması ile çözünme olayı gerçekleşir. Çözünme, moleküller arasındaki çekim kuvvetine dayanır. Bir çözücünün bir maddeyi çözebilmesi için; çözücü ile çözünen molekülleri arasındaki çekimkuvvetlerinin, çözücü ve çözünenin kendi molekülleri arasındaki çekim kuvvetinden daha büyük olması gerekir.

Örneğin şekerin suda çözünmesi; şeker ile su molekülleri arasındaki çekim kuvvetinin, şeker moleküllerinin kendi arasındaki çekim kuvvetinden daha büyük olmasındandır. Şeker, suda iyonlarına ayrışmadan moleküler halde çözünür.

Genellikle çözünme olayı, çözücü ile çözünenin benzer yapıda olmaları ile gerçekleşir. Bu durum “benzeri çözer” şeklinde ifade edilebilir. Dolayısıyla polar çözücüler polar maddeleri, polar olmayan çözücüler de polar olmayan maddeleri daha iyi çözer. Analitik kimyada genellikle sıvı-sıvı, katı-sıvı ve gaz sıvı çöz. Kullanılır.

ÇÖZÜNÜRLÜK Maddeler değişik ortamlarda farklı miktarlarda çözünür. Bu durumu ifade etmek üzere çözünürlük kavramı kullanılır. Herhangi bir sıcaklıkta, belirli bir hacimdeki çözücü içerisinde, belirli miktar madde çözünür. Ancak verilen belli bir miktar çözücüde çözünen madde miktarı için limit bir değer vardır. Bu limite gelmiş çözeltiye daha fazla çözünen eklenirse, maddenin fazlası çözünmeden kalacaktır. Böyle çözeltilere "doymuş çözeltiler" denir. Doymuş çözeltide çözünen madde miktarına da o maddenin o çözücüdeki "çözünürlüğü" denir.

Çözünürlük genellikle 100 m. L (100 cm 3) veya 100 g çözücüde çözünebilen maddenin gram cinsinden ağırlığı olarak verilir. Örneğin, Na. Cl'ün sudaki çözünürlüğü 20°C da 36 g/100 m. L'dir. Bu ifadeden Na. Cl'ün verilen şartlarda 100 m. L suda 36 g'dan daha fazla çözünmeyeceği anlaşılır.

Doygun hale gelmiş bu çözeltiye daha fazla Na. Cl ilave edildiği takdirde, ilave edilen Na. Cl çözeltide çözünmeden katı halde kalacaktır. Böyle bir çözeltide, katı madde ile o maddenin doygun çözeltisi temas halindedir ve aralarında bir dinamik denge söz konusudur. Bu denge çözünen moleküllerin hızının, çökelen moleküllerin hızına eşit olmasıyla sağlanır. Doymuş bir çözelti için verilen çözünürlük değerinden daha az miktarda madde bulunduran çözeltilere ise "doymamış çözeltiler" denir.

ÇÖZÜNÜRLÜĞE ETKİ EDEN ETMENLER Çözünürlük belirtilirken, sıcaklığın ve çözünmenin yer aldığı ortamın diğer şartlarının tanımlanması gerekir. Çoğunlukla çözeltiler normal atmosfer basıncında hazırlandığından, gazlar dışındaki maddelerin çözünürlükleri basınçtan söz etmeden verilir. Çünkü basınç değişimi, katıların sıvılardaki veya sıvıların sıvılardaki çözünürlüğünü etkilemez, fakat gazların sıvılardaki çözünürlüğünü etkiler ve gazların çözünürlükleri basıncın artması ile artar.

Katı ve sıvıların su içindeki çözünürlükleri genellikle sıcaklık ile artar, gazların çözünürlükleri ise sıcaklıkla azalır. Bu nedenle, çözünürlük ifade edilirken mutlaka hangi sıcaklıkta olduğunu belirtmek gerekir. Ayrıca gazların çözünürlüklerinde, basıncın etkisi büyük olduğundan basıncın da belirtilmesi gerekir. Maddelerin çözünürlüğü, çözücü ve çözünen maddelerin türüne göre değişir. Maddelerin çözünürlüğünü fiziksel ve kimyasal özellikleri etkiler. Bu özellikler polarlık, moleküller arası çekim kuvvetleri gibi özelliklerdir.

Çözünürlük Çarpımı Faz sayısı birden fazla olan dengelere heterojen denge denir. Bazı tuzların sudaki çözünürlükleri çok azdır. Böyle tuzların iyonları ile tuz arasında heterojen denge kurulur. Örneğin Ca. SO 4 suda çok az çözünür. Ca. SO 4(k) (Ca+2 ) (SO 4 -2) buradan Kçç= (Ca+2) (SO 4 -2) = (s)=s 2 yazarız. Kçç : Çözünürlük çarpımıdır.

Örnek : 100 m. L su 25 o. C de Ca. SO 4 ile doyuruluyor. Elde edilen çözeltiden su tamamen uzaklaştırıldığı zaman 0, 248 g Ca. SO 4 elde edildiğine göre; Ca. SO 4 ın 25 o. C deki Kçç=? Bulunuz. ( Ca=40, S=32, O=16)

Çözüm : Ca. SO 4 ın Molaritesini bulalım n/MA 0, 248 g /136 g/mol M = ----------------- 0, 018 M V 0, 1 L (Ca+2 ) = s = 0, 018 M (SO 4)-2 = s = 0, 018 M Ca. SO 4 (Ca+2 ) (SO 4 -2) Kçç= (Ca+2) (SO 4 -2) = (s)=s 2 Kçç = (0, 018) = 3, 2. 10 -4 olur.

Örnek : Pb(OH)2’in belli bir sıcaklıktaki çözünürlük çarpımı 4 x 10 -15’dir. Buna göre Pb(OH)2’in, saf sudaki çözünürlüğünü hesaplayınız

Çözüm : Pb(OH)2’in çözünürlüğü “s” olsun. Pb(OH)2(k) Pb 2+(suda) + 2 OH-(suda) olduğuna göre; [Pb 2+]=s ve [OH-]=2 s olur. Çözünürlük çarpımı ifadesinden Kçç= [Pb 2+][OH-]2 yazılır. Çözünürlükleri yerine yazılırsa; Kçç=(s)(2 s)2 = 4 s 3 = 4 x 10 -15 olduğundan s=1 x 10 -5 bulunur.

Örnek : (Pb. I 2) kurşun iyodürün; a) Çözünürlüğünü b) Her bir iyonun derişimini bulunuz. Kçç = 7, 1. 10 -3

Çökme reaksiyonları Q ve Kçç arasındaki ilişkiye göre sistemin denge hali için yargıda bulunulabilir. Yani; Q = Kçç ise; çözünürlük dengesi kurulmuş demektir. Çözelti doygunluğa ulaşmıştır. Q < Kçç ise; çözelti doymamıştır ve çökme olmaz. Qçç = Kçç oluncaya kadar çözünme devam eder. Q > Kçç ise; iyonların derişimleri çarpımı büyük olduğundan aşırı doygunluk vardır. Q = Kçç oluncaya kadar çökme devam edecektir. Q: İyonların başlangıçtaki konsantrasyonları çarpımıdır.

Örnek Eşit hacimde 2 x 10 -3 M Pb(NO 3)2 ve 2 x 10 -3 M Na. I karıştırılıyor. Pb. I 2 çökeleği oluşur mu? (Kçç=7, 1. 10 -9) Çözüm: Çözeltide Pb+2 ve I- iyonlarının konsantrasyonları yarıya düşer. (2 x 10 -3 M). (V) (Pb+2) = ---------- = 1 x 10 -3 M 2 V (2 x 10 -3 M). (V) (I- ) = --------- = 1 x 10 -3 M 2 V Olarak bulunur. Q= (Pb+2). (I-)2= (1 x 10 -3)(1 x 10 -3 )2 Q= 1 x 10 -9 Q Kçç olduğundan çökme olmaz

Örnek Soru 1) Ca. F 2 ‘ün ; a)Saf sudaki b) 1 x 10 -2 M Ca. Cl 2 içindeki, c) 0, 1 Na. F çözeltisindeki, Çözünürlüklerini bulunuz. (Kçç=3, 4 x 10 -11) 2) Pb. Cl 2’ün 1 M Na. Cl içindeki Çözünürlüğünü bulunuz. (Kçç=1, 7 x 10 -5)

DERİŞİM Belirli bir miktar çözelti veya çözücü içerisinde çözünen madde miktarına DERİŞİM (KONSATRASYON) denir. Çözünen madde miktarı(m) Derişim =----------(C) Çözeltinin Hacmi (V) C = m/V olur. Çözeltideki madde miktarı(m)= C. V Şeklinde hesaplanır.

DERİŞİM VE BİRİMLERİ düşük olan çözeltiler seyreltik çözelti, derişimi yüksek olan çözeltiler ise derişik çözelti olarak bilinir. Ancak bir çözeltide çözünen madde miktarının bilinmesi gerekir. � Derişimi

� Bir çözeltide çözünen madde miktarını nasıl ifade ederiz? � Bir çözeltide çözünen madde miktarı, kütle, hacim, mol terimlerini içeren çeşitli derişim birimleri ile belirtilir. En çok kullanılan derişim birimleri, yüzde derişim, mol kesri, molarite, normalite, molalite, ppm ve ppb'dir. Şimdi bu birimleri görelim.

YÜZDE DERİŞİM



MOL KESRİ


MOLARİTE


Sıvı içinde Sıvı Maddenin Çözünmesiyle Hazırlanan Molar Çözeltiler � Çözünecek sıvı maddenin yoğunluk ve ağırlıkça yüzdesinin bilinmesi gerekir. � Bu bilgiler ambalaj etiketi üzerinde belirtilir.

Örnek 1: Yoğunluğu 1. 18 gr/ml olan ağırlıkça % 35’lik HCl çözeltisinden 2 M, 0. 5 lt’lik HCl çözeltisi nasıl hazırlanır? (MA=36. 5 gr/mol HCl) � Çözüm: � V(ml)=(36. 5 / 1. 18 x 0. 35) x 2 x 0. 5 = 88. 37 ml � orijinal şişedeki asitten alınıp hacmi deiyonize su ile 500 ml’ye tamamlanır.

� Örnek 2: Yoğunluğu 1. 98 gr/m. L olan ve ağırlıkça % 98’lik H 2 SO 4 çözeltisinin molaritesini bulunuz. � (MA=98 gr/mol, H 2 SO 4) Çözüm: 1. 98 gr/ml x 0. 98 (% 98) 1. 9404 gr H 2 SO 4 / ml M=n/V M= (1. 9404/98) / 0. 001 M= 0. 0198 / 0. 001 = 19. 8 M H 2 SO 4

ÇÖZELTİLERİN SEYRELTİLMESİ



MOLALİTE


Normalite (N) Bir litre çözeltide çözünen maddenin eşdeğergram miktarını gösterir. Eyer 1 L çözeltide bir eşdeğer-gram madde çözünmüş ise çözeltinin konsantrasyonu bir Normaldir denir ve derişim (N) ile ifade edilir. Çözünen madde miktarı/Eşd. Ağ Normalite(N) = -------------------Çözeltinin Hacmi(L)

Eşdeğer Ağırlık Çözünen maddenin MA � Eşdeğer Ağ. = --------------Etkime(Tesir) Değerliği Normalite(N) = Molarite x Tesir Değerliği

Eşdeğer ağırlık ise maddenin molekül kütlesinin tesir değerliğine (t) oranıdır. Bir maddenin tesir değerliği reaksiyon esnasında ortama verdiği veya aldığı elektron sayısıdır.

Etkime(Tesir) Değerliği � Asitler için; ortama verdiği H+ sayısı � Bazlar için; yer değiştiren OH- sayısına � Tuzlar için; anyon veya katyonların herhangi birinin toplam yük sayısına eşittir.

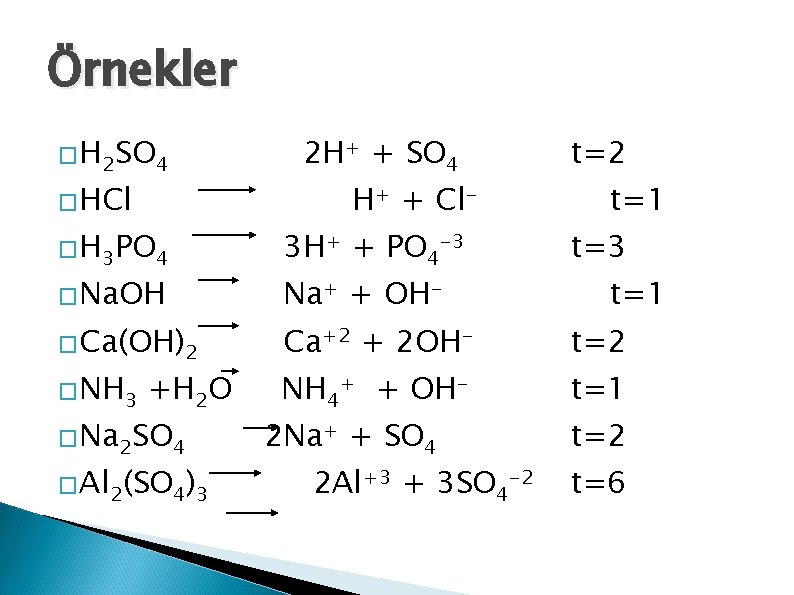
Örnekler �H 2 SO 4 2 H+ + SO 4 t=2 �H 3 PO 4 3 H+ + PO 4 -3 t=3 �Ca(OH)2 Ca+2 + 2 OH- t=2 �HCl �Na. OH �NH 3 +H 2 O �Na 2 SO 4 �Al 2(SO 4)3 H+ + Cl- Na+ + OH- NH 4+ + OH- 2 Na+ + SO 4 2 Al+3 + 3 SO 4 -2 t=1 t=1 t=2 t=6

Örnek 500 m. L 2 N Ca(OH)2 çözeltisi nasıl hazırlanır? (MA= 74 g/mol Çözüm ü N=M x t ve Ca(OH)2’in TD=2 olduğuna göre; 2=M x 2 M=1 mol/L Ca(OH)2 ü M=n/L 1=n/0. 5 n=0. 5 mol Ca(OH)2 ü 0. 5= x / 74 x=37 gr Ca(OH)2 bir miktar deiyonize suda çözüldükten sonra son hacmi 500 ml’e tamamlanır. ü

Örnek 1)100 m. L de 8, 110 gram Fe. Cl 3 ün Normalitesini bulunuz? (Fe: 56 Cl: 35, 5) 2) Litresinde 26, 5 gram Na 2 CO 3 ın; a) Molar deişimini b) Normal derişimini bulunuz. (Na: 23 C: 12 O: 16) 3) 250 m. L 1. 5 N H 2 SO 4 çözeltisi nasıl hazırlanır? (d=1. 85 gr/ml, ağırlıkça % 98’lik ve MA=98 gr/mol)

ppm ve ppb


ÇÖZELTİLERİN BUHAR BASINCI


 Zelt jelentése
Zelt jelentése Bürolarda estetik ve fiziksel koşullar
Bürolarda estetik ve fiziksel koşullar Kalıcı dipollük
Kalıcı dipollük Orta şiddette fiziksel aktivite
Orta şiddette fiziksel aktivite Fiziksel özellik nedir
Fiziksel özellik nedir Ilgi ve yeteneklerimiz fiziksel özelliklerimizdendir
Ilgi ve yeteneklerimiz fiziksel özelliklerimizdendir Allah'ın kulu ve elçisi
Allah'ın kulu ve elçisi Pal değeri nedir
Pal değeri nedir Fiziksel istismar
Fiziksel istismar Molarite nedir
Molarite nedir Fizi pal
Fizi pal Yüksek sıcaklığın neden olduğu rahatsızlıklar
Yüksek sıcaklığın neden olduğu rahatsızlıklar Kabenin fiziksel özellikleri
Kabenin fiziksel özellikleri Kimyasal kirlenme örnekleri
Kimyasal kirlenme örnekleri Donma sonucu oluşan yanıklar
Donma sonucu oluşan yanıklar Mesleki dermatozlar içinde en sık görüleni
Mesleki dermatozlar içinde en sık görüleni Akran zorbalığı şikayet dilekçesi
Akran zorbalığı şikayet dilekçesi 8 sınıf kader ve kazaya örnekler
8 sınıf kader ve kazaya örnekler Srcler
Srcler Duyum ve algı örnekleri
Duyum ve algı örnekleri Fiziksel özellikler
Fiziksel özellikler Zflv ergonomik ayak
Zflv ergonomik ayak Sarı ve mor kartlar
Sarı ve mor kartlar Risk etmenleri
Risk etmenleri Fiziksel değişim örnekleri
Fiziksel değişim örnekleri Fiziksel uygunluk ders notları
Fiziksel uygunluk ders notları Bilgisayarda metin dosyası oluşturmak megep
Bilgisayarda metin dosyası oluşturmak megep