UTVRIVANJE STRUKTURE KOMPLEKSNIH JEDINJENJA Postojanje dva dela kompleksnog



![Utvrđivanje oblika u kome je prisutan sulfat u kompleksu rastvaranjem kompleksa [Co(NH 3)5 Br]SO Utvrđivanje oblika u kome je prisutan sulfat u kompleksu rastvaranjem kompleksa [Co(NH 3)5 Br]SO](https://slidetodoc.com/presentation_image_h2/271214120625277269199dc056dbc540/image-4.jpg)




- Slides: 13

UTVRĐIVANJE STRUKTURE KOMPLEKSNIH JEDINJENJA Postojanje dva dela kompleksnog jedinjenja u kompleksima tipa M [׳ MX 6], [ML 6]X 2 i drugih može se utvrditi jednostavnim analitičkim probama u rastvorima dobijenim selektivnim rastvaranjem kompleksnih jedinjenja u vodi i razblaženim mineralnim kiselinama, i primenom fizičko-hemijskih tehnika i metoda karakterizacije: kvalitativno: - uočavanjem različite boje jedinjenja, - identifikacijom anjona van unutrašnje koordinacione sfere, kvantitativnim određivanjem pojedinačnih komponenti, liganada i jona merenjem provodljivosti rastvora, snimanjem i analizom UV/VIS spektara, snimanjem i analizom IR i Ramanovih spektara, snimanjem i analizom ESR spektara, primenom specifičnih tehnika analize.

Vizuelno određivanje boje kompleksnog jedinjenja Na osnovu prethodnih znanja o kompleksima i iskustva u praktičnom laboratorijskom radu u kvalitativnoj analitičkoj i koordinacionoj hemiji mogu se vizuelnim posmatranjem boje kompleksa uočiti razlike kao posledica razlika u strukturi, jer pojedina kompleksna jedinjenja mogu imati istu bruto molekulsku formulu, a različitu boju. Različitost u bojama javlja se kao posledica različitog načina vezivanja liganada u komplesnom jedinjenju. U tabeli dati su primeri uticaja liganada na boju kompleksnih jedinjenja jona Cu 2+, Ni 2+, Cr 3+ i Fe 2+. Jon metala Cu 2+ Ni 2+ Cr 3+ Fe 2+ Kompleks Boja kompleksa Apsorpcija* [Cu. Cl 4]2 - zeleno-smeđ narandžastom [Cu(H 2 O)6]2+ plav žutom [Cu(NH 3)4]2+ plavo-ljubičast žuto-zelenom [Cu(CN)4]2 - bezbojan ultra-ljubičastom [Ni(H 2 O)6]2+ zelen crvenom [Ni(NH 3)6]2+ ljubičast zelenom [Ni(CN)4]2 - žut plavom [Cr(H 2 O)4 Cl 2]Cl zelen crvenom [Cr(H 2 O)6]Cl 3 svetlo-ljubičast zelenom [Cr(NH 3)6]3+ tamno-ljubičast zelenom [Fe(H 2 O)6]2+ svetlo-zelen infracrvenom [Fe(CN)6]4 - žut plavom

Kvalitativno dokazivanje liganada (jona) u rastvoru Utvrđivanje spoljašnje i unutrašnje sfere kompleksa date molekulske formule Postojanje dva dela koordinacione sfere kompleksa može se pokazati na primeru analize koordinacionog jedinjenja bruto formule Cr. Cl 3∙ 6 H 2 O: rastvaranjem kompleksa [Cr(H 2 O)6]Cl 3 (proba I) i [Cr(H 2 O)3 Cl 3] (proba II) u vodi, a zatim taloženjem hlorida pomoću Ag. NO 3 iz dobijenih rastvora. U prvoj probi se formira talog Ag. Cl, a u drugoj probi nema belog taloga Ag. Cl-a, što pokazuje da se u prvom slučaju Cl- joni nalaze u spoljašnjoj, a u drugom u unutrašnjoj koordinacionoj sferi. Ako se pak rastvaranje ovih dveju proba (kompleksnih jedinjenja) vrši u nekoj kiselini (najčešće razblažena HNO 3), taloženjem hlorida iz rastvora ove dve probe dobijaju se iste količine taloga jer kiselina razara kompleks u potpunosti i oslobađa jone koje taloži -jon.
![Utvrđivanje oblika u kome je prisutan sulfat u kompleksu rastvaranjem kompleksa CoNH 35 BrSO Utvrđivanje oblika u kome je prisutan sulfat u kompleksu rastvaranjem kompleksa [Co(NH 3)5 Br]SO](https://slidetodoc.com/presentation_image_h2/271214120625277269199dc056dbc540/image-4.jpg)
Utvrđivanje oblika u kome je prisutan sulfat u kompleksu rastvaranjem kompleksa [Co(NH 3)5 Br]SO 4 (proba I) i [Co(NH 3)5 SO 4]Br (proba II) u vodi, a zatim taloženjem sulfata pomoću Ba. Cl 2 iz dobijenih rastvora, u prvoj probi dolazi do formiranja taloga Ba. SO 4, dok se u drugoj probi ne formira talog. Ovaj rezultat pokazuje da se SO jon nalazi u različitim koordinacionim sferama ova dva kompleksna jedinjenja, spoljašnjoj (I) i unutrašnjoj (II). Rastvaranjem ova dva kompleksa u kiselini (najčešće razblažena HNO 3) dolazi do razaranja kompleksa u potpunosti i taloženja istih količina sulfata, po dodavanju taložnog reagensa koji sadrži Ba 2+ jone.

Gravimetrijsko taloženje je jedan od načina da se pokaže postojanje dva dela kompleksnog jedinjenja, spoljašnje i unutrašnje koordinacione sfere i odredi kvantitativni odnos između tih delova kompleksne čestice. Na primeru kompleksa [Cr(H 2 O)6]Cl 3 i [Cr(H 2 O)4 Cl 2]Cl∙ 2 H 2 O gravimetrijskim taloženjem hlorida sa Ag+ jonima dobijaju se raličite količine hlorida. Na isti način može se iz kompleksa [Co(NH 3)5 Br]SO 4 istaložiti slobodan SO 42 - anjon u obliku Ba. SO 4, ali ne i iz kompleksa [Co(NH 3)5 SO 4]Br i [Co(NH 3)5 SO 4 Br. Co(NH 3)5]Br 4, zato što se anjon nalazi u unutrašnjoj koordinacionoj sferi kao ligand vezan za centralni atom metala. Razaranjem kompleksa pri rastvaranju u razblaženoj HNO 3 može se istaložiti ista količina sulfata iz rastvora sva tri jedinjenja po odgovarajućem postupku za gravimetrijsko određivanje sulfata u obliku Ba. SO 4.

Merenje molarne provodljivosti Merenjem provodljivosti rastvora kompleksa i poređenjem sa poznatim vrednostima za određeni tip elektrolita utvrđuje se broj čestica na koje disosuje kompleksno jedinjenje. Rastvaranjem kompleksa [Cr(H 2 O)6]Cl 3 i [Cr(H 2 O)4 Cl 2]Cl ∙ 2 H 2 O u vodi i merenjem njihove molarne provodljivosti dobijaju se različite vrednosti zbog različitog broja čestica koje postoje u istoj količini ovih kompleksa. U tabeli 3. 2 dati su primeri disocijacije različitih kompleksa sa odgovarajućim primerom jakog elektrolita koji disosuje na isti broj čestica i ima istu provodljivost. jedinjenje ⇆ disocija Ag. Cl(s) [mol] Provodljivost slična elektrolitu [Co(NH 3)6]Cl 3 ⇆ [Co(NH 3)6]3+ + 3 Cl- 3 Al. Cl 3 [Co(NH 3)5 Cl]Cl 2 ⇆ [Co(NH 3)5 Cl]2 - + 2 Cl- 2 Co. Cl 2 [Co. Cl 2(NH 3)4]Cl ⇆ [Co. Cl 2(NH 3)4]+ + Cl- 1 Na. Cl Svi ovi kompleksi posle zagrevanja rastvora sa razblaženom kiselinom (HNO 3) koja razara komplekse, i dodavanjem Ag+ jona talože istu količinu Ag. Cl(s) jer sadrže istu ukupnu količinu hlorida, ali su joni Cl– vezani u različitim delovima kompleksnih čestica.

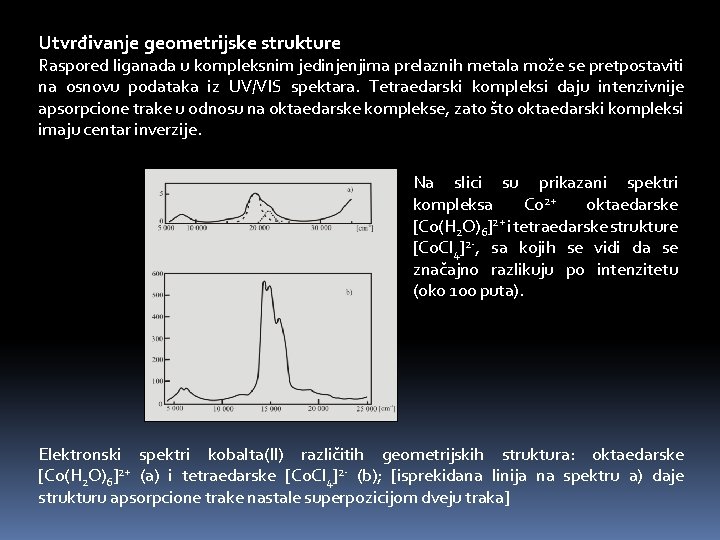
Utvrđivanje geometrijske strukture Raspored liganada u kompleksnim jedinjenjima prelaznih metala može se pretpostaviti na osnovu podataka iz UV/VIS spektara. Tetraedarski kompleksi daju intenzivnije apsorpcione trake u odnosu na oktaedarske komplekse, zato što oktaedarski kompleksi imaju centar inverzije. Na slici su prikazani spektri kompleksa Co 2+ oktaedarske [Co(H 2 O)6]2+ i tetraedarske strukture [Co. Cl 4]2 -, sa kojih se vidi da se značajno razlikuju po intenzitetu (oko 100 puta). Elektronski spektri kobalta(II) različitih geometrijskih struktura: oktaedarske [Co(H 2 O)6]2+ (a) i tetraedarske [Co. Cl 4]2 - (b); [isprekidana linija na spektru a) daje strukturu apsorpcione trake nastale superpozicijom dveju traka]

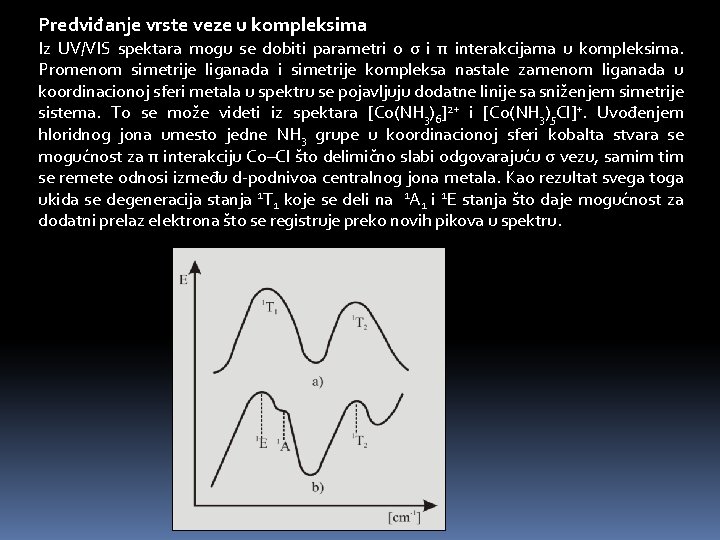
Predviđanje vrste veze u kompleksima Iz UV/VIS spektara mogu se dobiti parametri o σ i π interakcijama u kompleksima. Promenom simetrije liganada i simetrije kompleksa nastale zamenom liganada u koordinacionoj sferi metala u spektru se pojavljuju dodatne linije sa sniženjem simetrije sistema. To se može videti iz spektara [Co(NH 3)6]2+ i [Co(NH 3)5 Cl]+. Uvođenjem hloridnog jona umesto jedne NH 3 grupe u koordinacionoj sferi kobalta stvara se mogućnost za π interakciju Co–Cl što delimično slabi odgovarajuću σ vezu, samim tim se remete odnosi između d-podnivoa centralnog jona metala. Kao rezultat svega toga ukida se degeneracija stanja 1 T 1 koje se deli na 1 A 1 i 1 E stanja što daje mogućnost za dodatni prelaz elektrona što se registruje preko novih pikova u spektru.

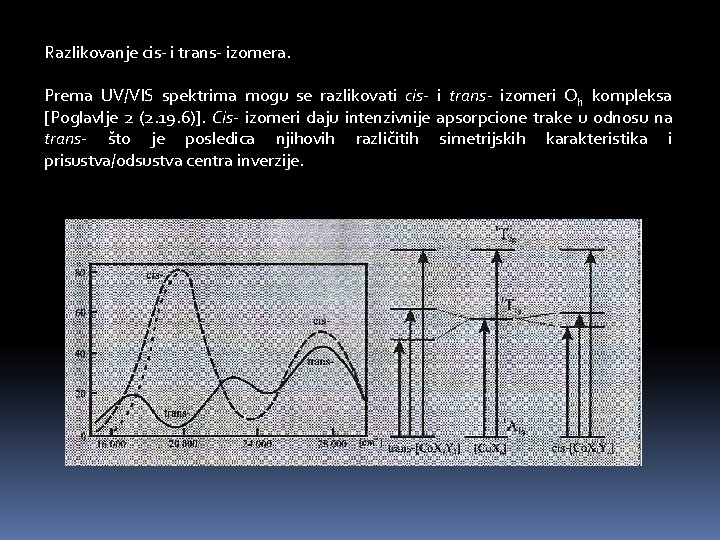
Razlikovanje cis- i trans- izomera. Prema UV/VIS spektrima mogu se razlikovati cis- i trans- izomeri Oh kompleksa [Poglavlje 2 (2. 19. 6)]. Cis- izomeri daju intenzivnije apsorpcione trake u odnosu na trans- što je posledica njihovih različitih simetrijskih karakteristika i prisustva/odsustva centra inverzije.

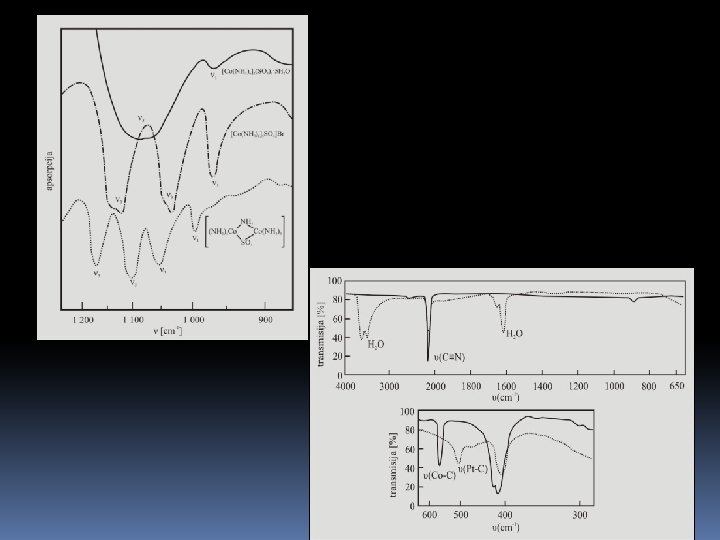
Primena IR spektroskopije Metodom IR spektroskopije dobijaju se značajniji podaci o kompleksnim jedinjenjima i to o: prisustvu vode u kompleksima i načinu vezivanja iste (u koordinacionoj sferi ili van koordinacione sfere) funkcionalnim grupama organskih liganada, načinu vezivanja poliatomskih anjonskih liganada i njihovim simetrijskim karakteristikama, koordinaciji metal-ligand. Na slici koja sledi date su oblasti IR spektara u kojima se javljaju trake za uobičajene anjone neorganskih kiselina i anjonske ligande u kompleksnim jedinjenjima. Relativni položaji apsorpcionih traka u IR spektru za uobičajene anjone neorganskih kiselina koji mogu biti anjonski ligandi ili anjonski deo jedinjenja sa kompleksnim katjonom

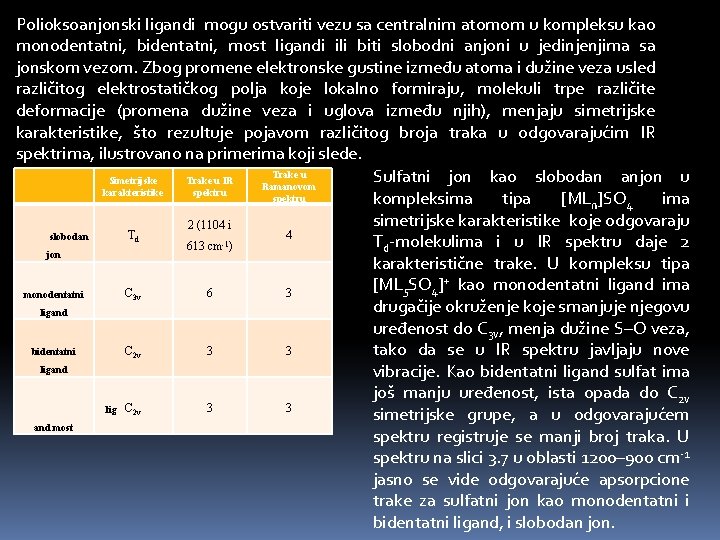
Polioksoanjonski ligandi mogu ostvariti vezu sa centralnim atomom u kompleksu kao monodentatni, bidentatni, most ligandi ili biti slobodni anjoni u jedinjenjima sa jonskom vezom. Zbog promene elektronske gustine između atoma i dužine veza usled različitog elektrostatičkog polja koje lokalno formiraju, molekuli trpe različite deformacije (promena dužine veza i uglova između njih), menjaju simetrijske karakteristike, što rezultuje pojavom različitog broja traka u odgovarajućim IR spektrima, ilustrovano na primerima koji slede. Trake u Sulfatni jon kao slobodan anjon u Simetrijske Trake u IR Ramanovom karakteristike spektru kompleksima tipa [MLn]SO 4 ima simetrijske karakteristike koje odgovaraju 2 (1104 i T 4 slobodan d Td-molekulima i u IR spektru daje 2 613 cm-1) jon karakteristične trake. U kompleksu tipa [ML 5 SO 4]+ kao monodentatni ligand ima C 3 v 6 3 monodentatni drugačije okruženje koje smanjuje njegovu ligand uređenost do C 3 v, menja dužine S–O veza, C 2 v 3 3 tako da se u IR spektru javljaju nove bidentatni ligand vibracije. Kao bidentatni ligand sulfat ima još manju uređenost, ista opada do C 2 v 3 3 lig C 2 v simetrijske grupe, a u odgovarajućem and most spektru registruje se manji broj traka. U spektru na slici 3. 7 u oblasti 1200– 900 cm-1 jasno se vide odgovarajuće apsorpcione trake za sulfatni jon kao monodentatni i bidentatni ligand, i slobodan jon.


Ostale metode analize kompleksnih jedinjenja Za određivanje geometrijske strukture kompleksa, tj. utvrđivanja prostornog rasporeda liganada i njihovih donor atoma oko centralnog atoma metala primenjuje se rentgenska strukturna analiza. Za određivanje elektronske strukture kompleksa, tj. prostorne raspodele elektronske gustine, pored već opisanih i lakše dostupnih , primenjuju se i druge metode i tehnike. Fotoelektronska spektroskopija primenjuje se za određivanje položaja MO energetskih nivoa i njihove popunjenosti valentnim i nevalentnim elektronima konstituenata (metala i liganada), posebno je pogodna za ispitivanje najbliže okoline biometala u kompleksima koji sadrže donor atome kiseonika, azota i sumpora. Nuklearna magnetna rezonanca primenjuje se za dobijanje podataka o načinu koordinacije M–L. γ-rezonantna spektroskopija ima primenu u utvrđivanju strukture bioliganada i drugih liganada sa jonima gvožđa. Termogravimetrija i diferencijalno-termička analiza se takođe mogu primeniti za određivanje oblika prisustva pojedinih atoma i atomskih grupa u kompleksima.