UNIVERSIDAD PERUANA CAYETANO HEREDIA Departamento de Bioqumica Biologa

UNIVERSIDAD PERUANA CAYETANO HEREDIA Departamento de Bioquímica, Biología Molecular & Farmacología Curso Bioquímica 2008 Aminoácidos • • Aminoácidos Estructura y Propiedades Enlace Peptídico Péptidos
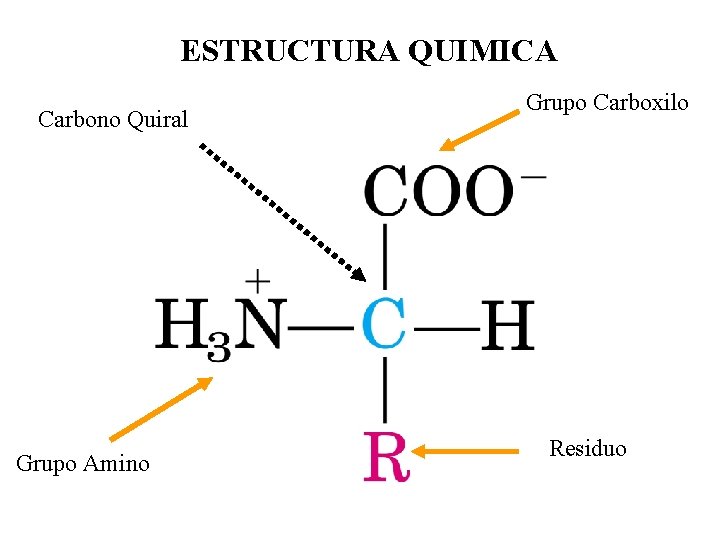
ESTRUCTURA QUIMICA Carbono Quiral Grupo Amino Grupo Carboxilo Residuo
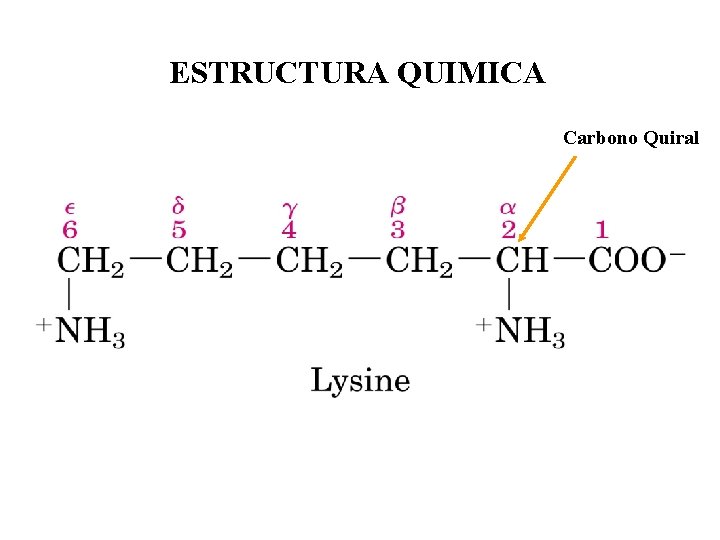
ESTRUCTURA QUIMICA Carbono Quiral
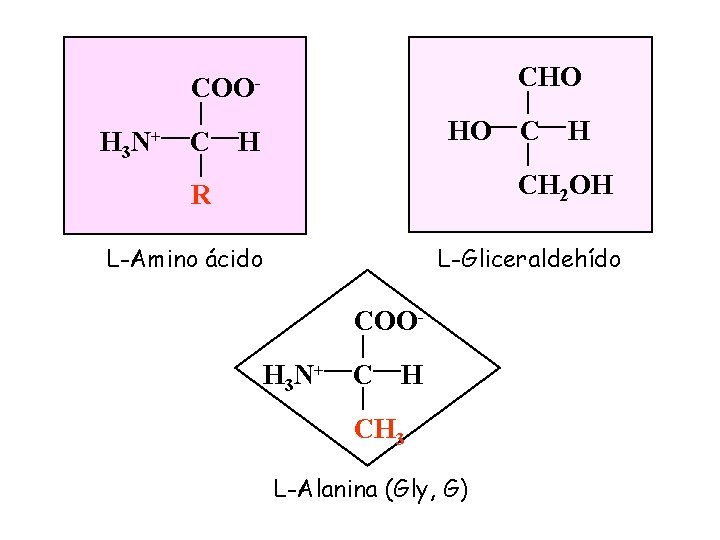
CHO COOH 3 N+ C HO H CH 2 OH R L-Amino ácido L-Gliceraldehído COOH 3 N+ C H CH 3 L-Alanina (Gly, G)
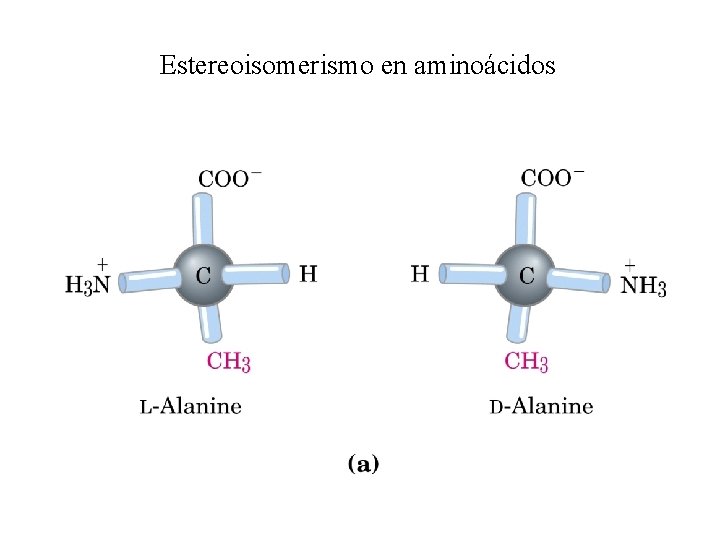
Estereoisomerismo en aminoácidos
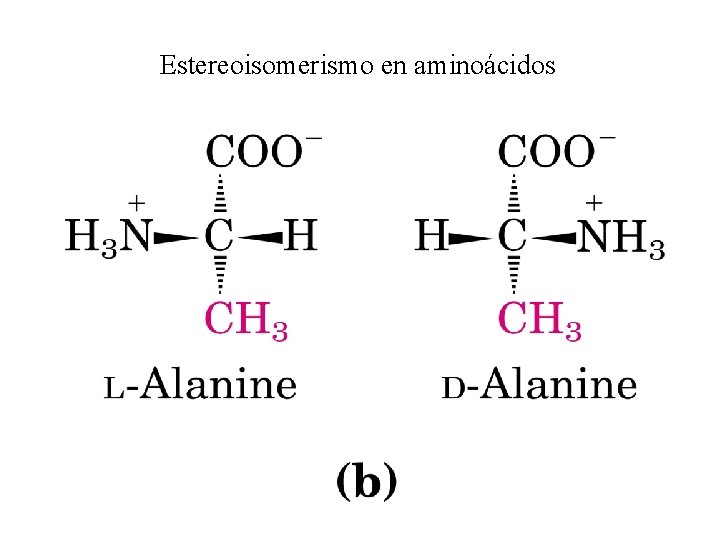
Estereoisomerismo en aminoácidos
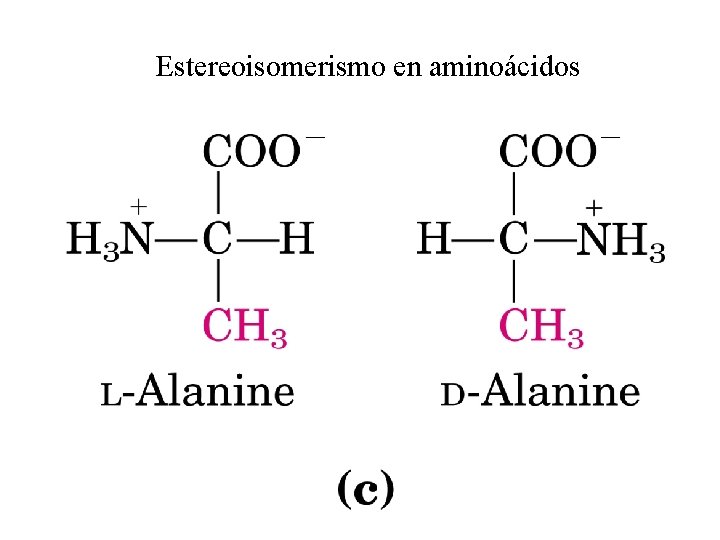
Estereoisomerismo en aminoácidos

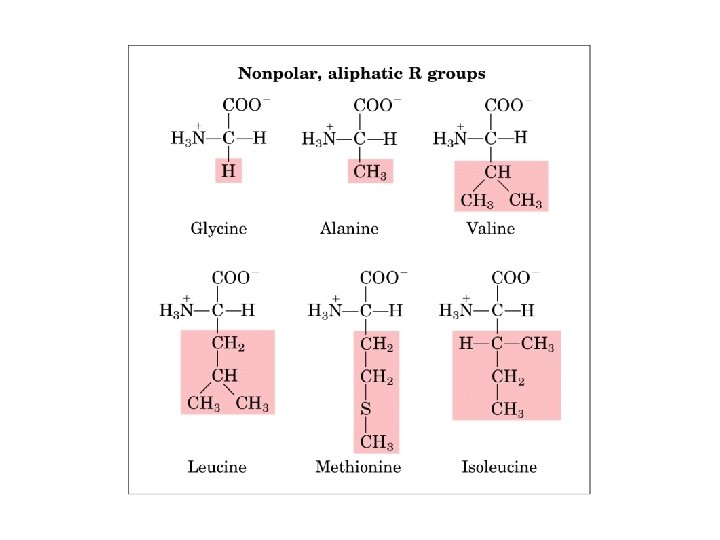
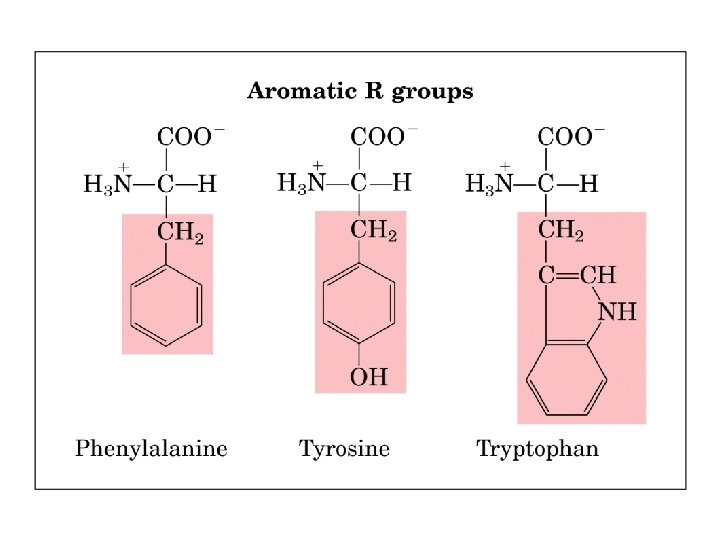
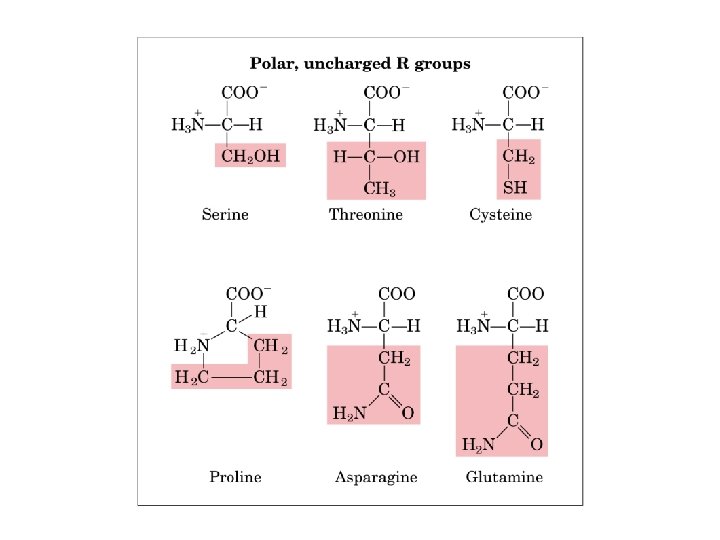
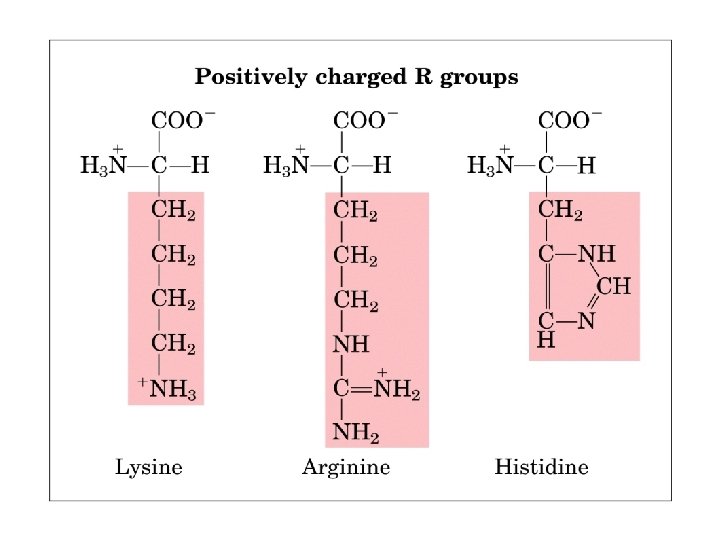
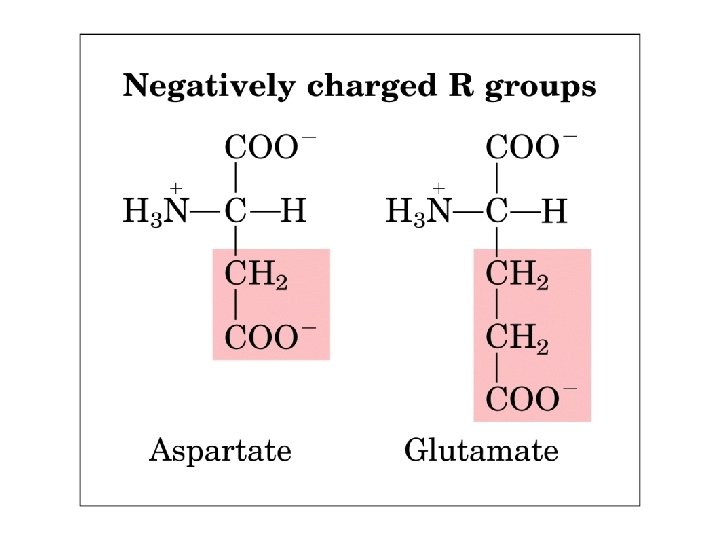
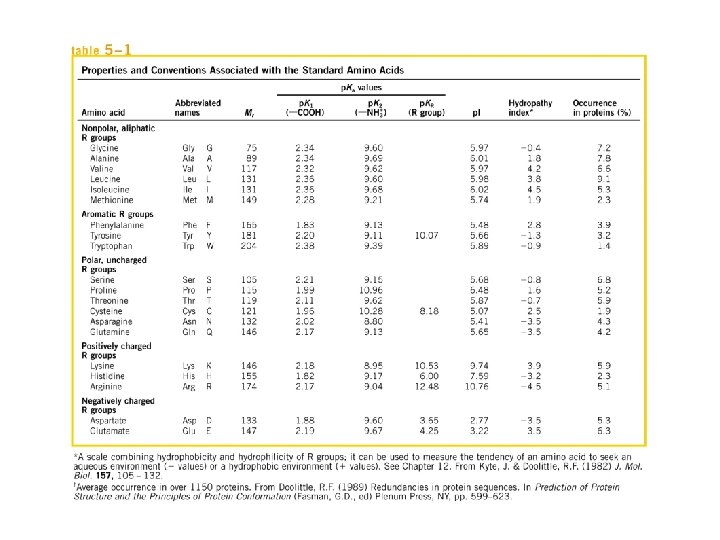
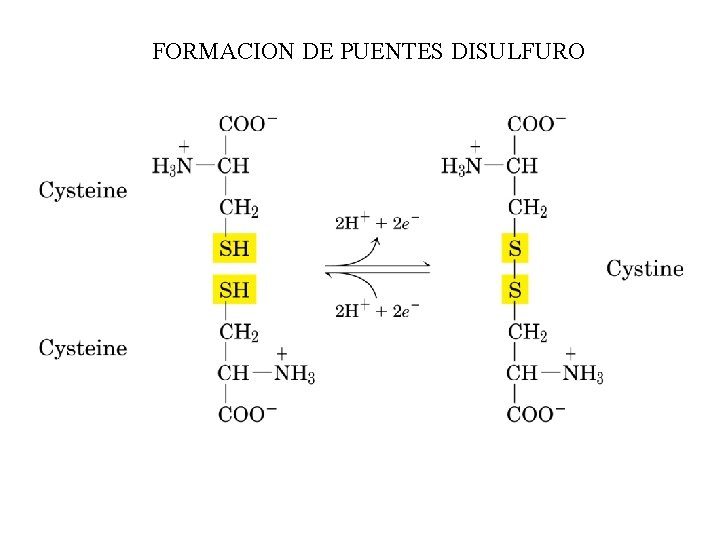
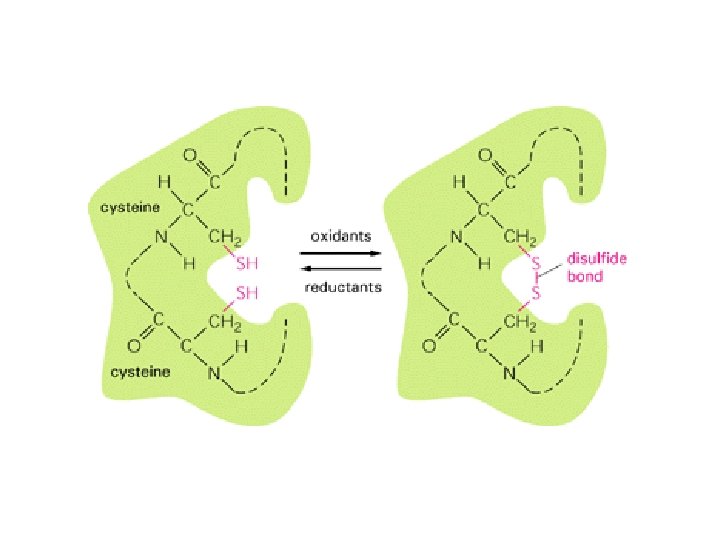
FORMACION DE PUENTES DISULFURO
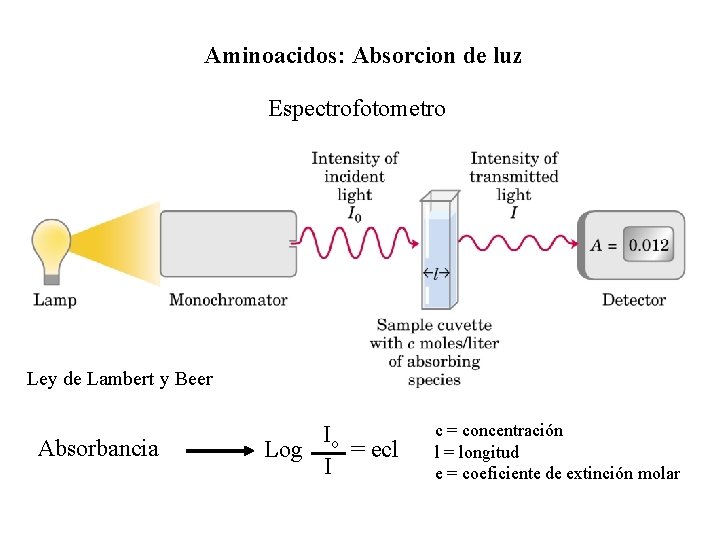
Aminoacidos: Absorcion de luz Espectrofotometro Ley de Lambert y Beer Absorbancia Io Log = ecl I c = concentración l = longitud e = coeficiente de extinción molar
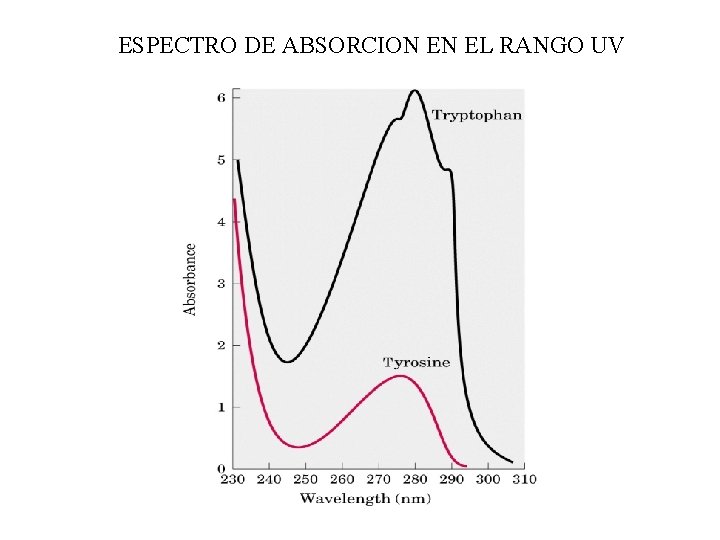
ESPECTRO DE ABSORCION EN EL RANGO UV
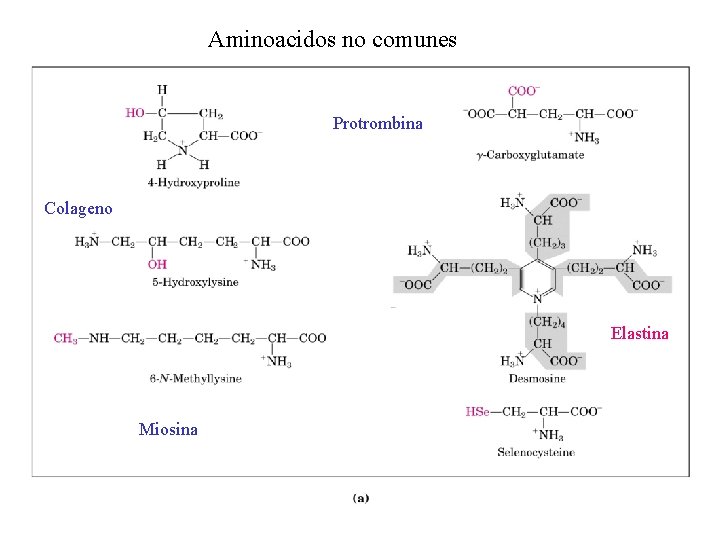
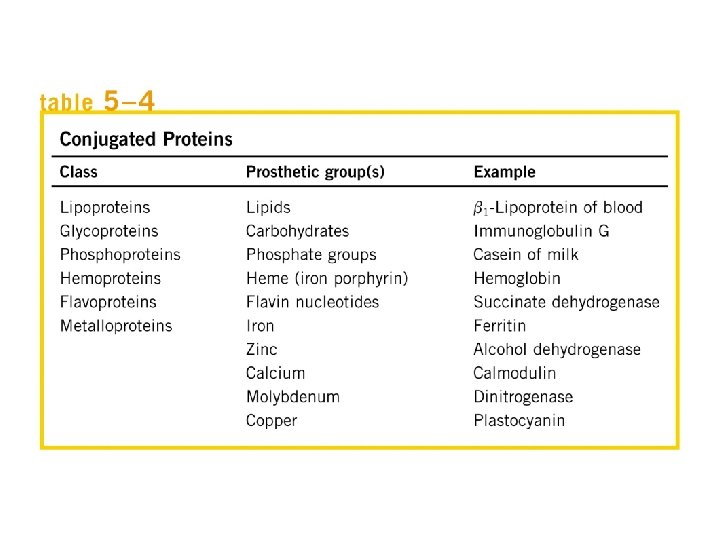
Aminoacidos no comunes Protrombina Colageno Elastina Miosina
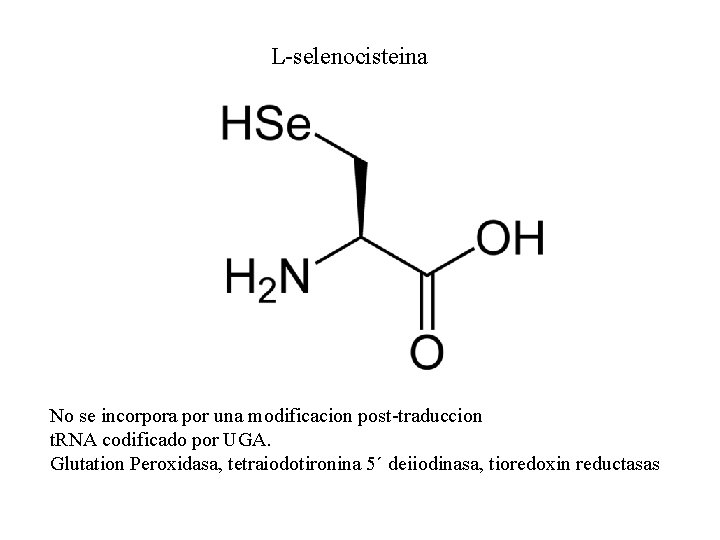
L-selenocisteina No se incorpora por una modificacion post-traduccion t. RNA codificado por UGA. Glutation Peroxidasa, tetraiodotironina 5´ deiiodinasa, tioredoxin reductasas
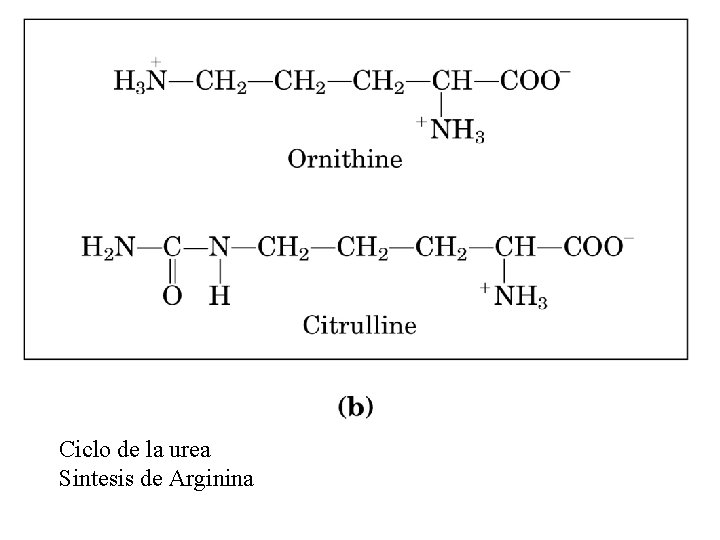
Ciclo de la urea Sintesis de Arginina
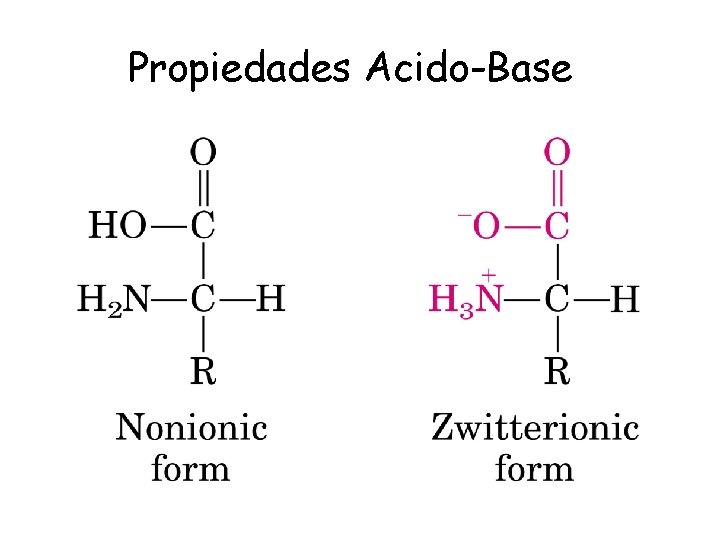
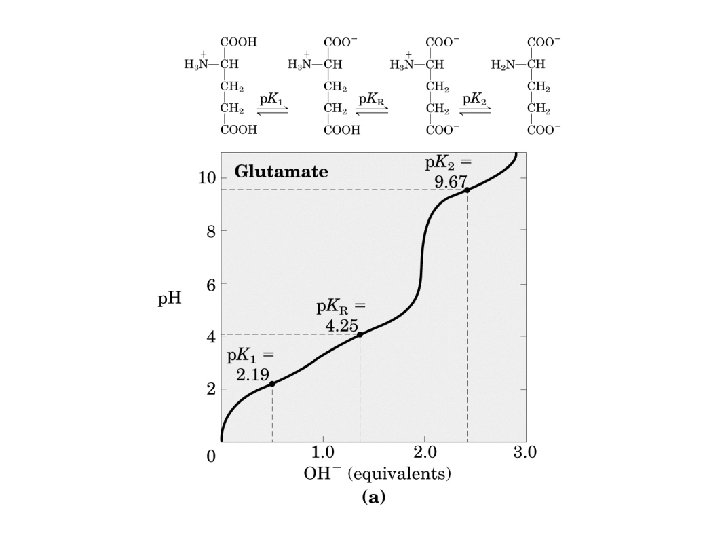
Propiedades Acido-Base
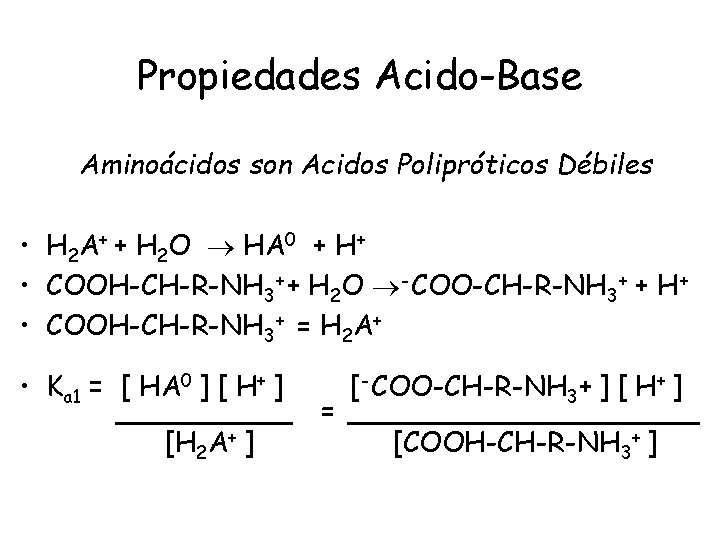
Propiedades Acido-Base Aminoácidos son Acidos Polipróticos Débiles • H 2 A+ + H 2 O HA 0 + H+ • COOH-CH-R-NH 3++ H 2 O -COO-CH-R-NH 3+ + H+ • COOH-CH-R-NH 3+ = H 2 A+ • Ka 1 = [ HA 0 ] [ H+ ] [-COO-CH-R-NH 3+ ] [ H+ ] _____ = __________ [H 2 A+ ] [COOH-CH-R-NH 3+ ]
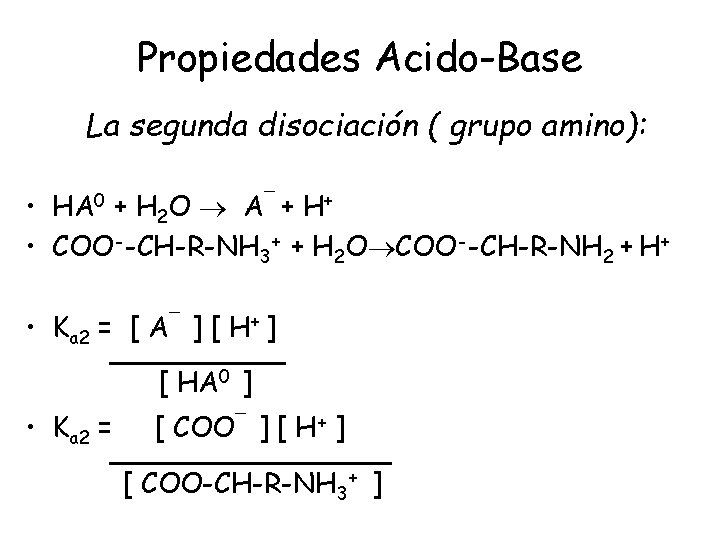
Propiedades Acido-Base La segunda disociación ( grupo amino): • HA 0 + H 2 O A¯ + H+ • COO--CH-R-NH 3+ + H 2 O COO--CH-R-NH 2 + H+ • Ka 2 = [ A¯ ] [ H+ ] _____ [ HA 0 ] • Ka 2 = [ COO¯ ] [ H+ ] ________ [ COO-CH-R-NH 3+ ]
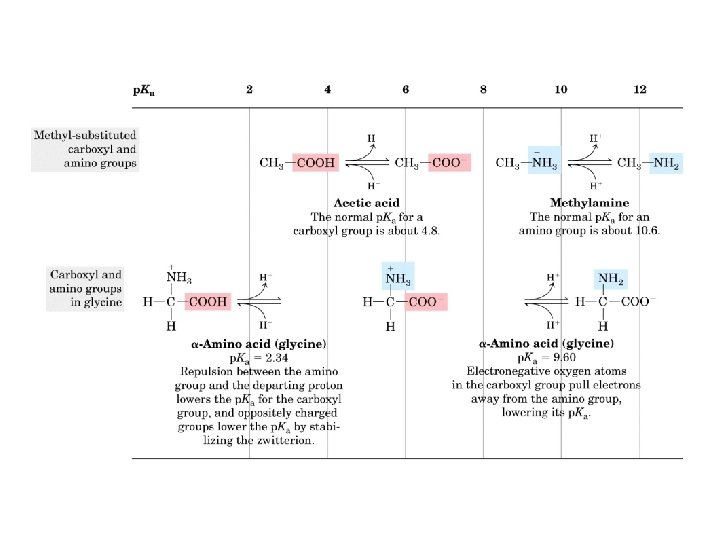
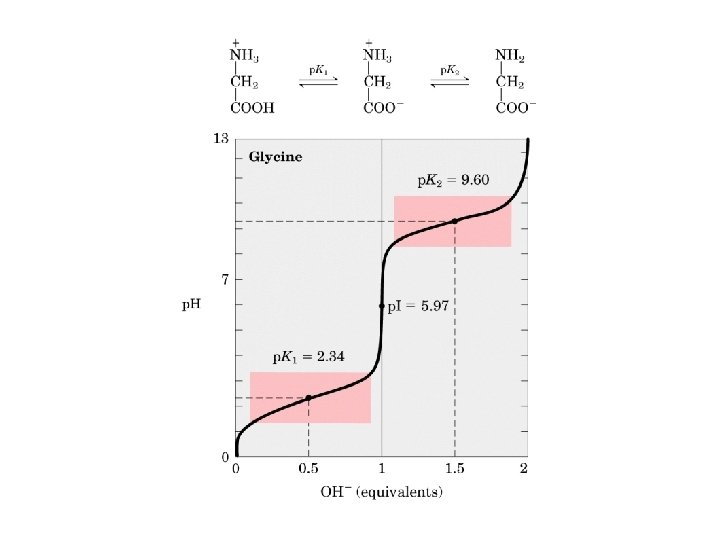


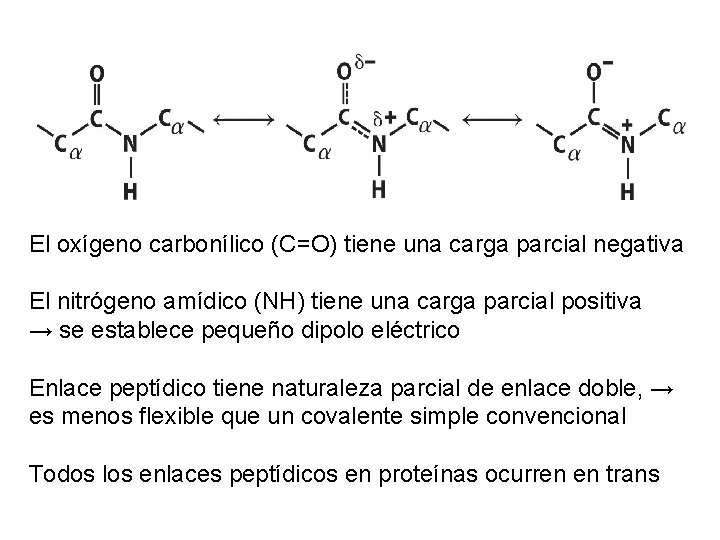
El oxígeno carbonílico (C=O) tiene una carga parcial negativa El nitrógeno amídico (NH) tiene una carga parcial positiva → se establece pequeño dipolo eléctrico Enlace peptídico tiene naturaleza parcial de enlace doble, → es menos flexible que un covalente simple convencional Todos los enlaces peptídicos en proteínas ocurren en trans
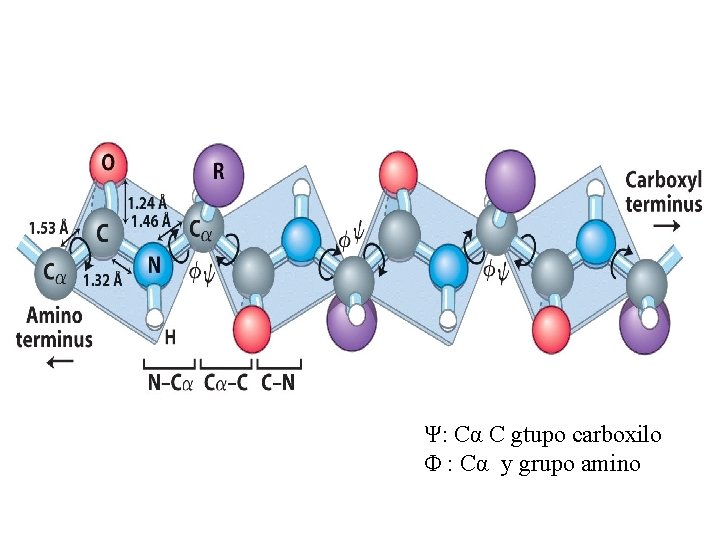
Ψ: Cα C gtupo carboxilo Φ : Cα y grupo amino
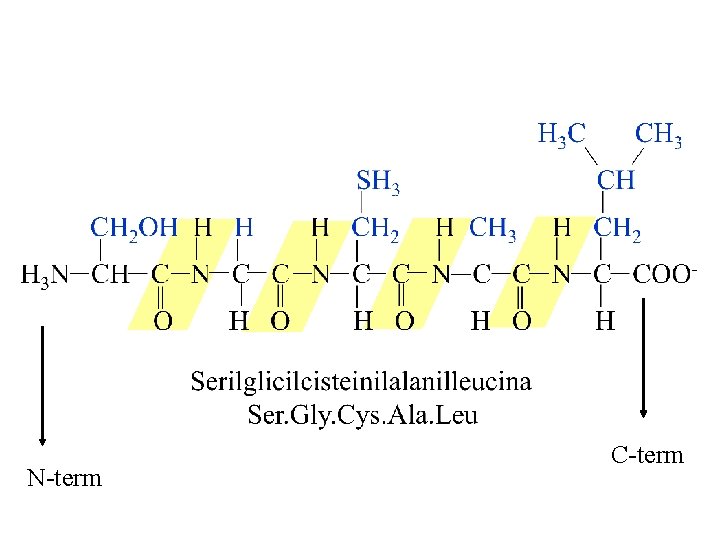
N-term C-term

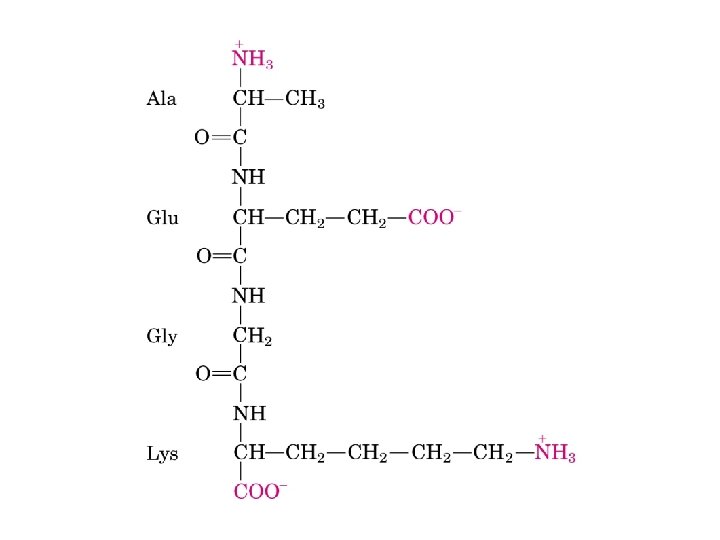



- Slides: 39