Sra Vskyt v prod se sra nachz v

















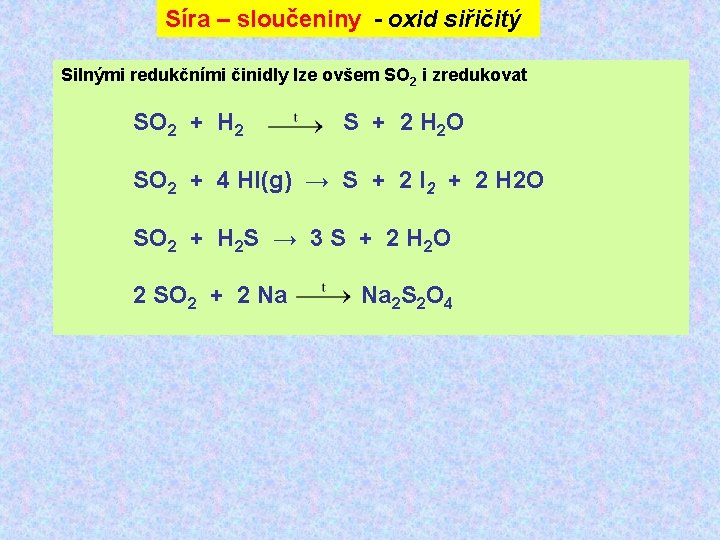










- Slides: 43

Síra Výskyt • v přírodě se síra nachází v podobě elementární • vázaná: sírany (sádrovec Ca. SO 4∙ 2 H 2 O, baryt Ba. SO 4 aj. ) sulfidy (sfalerit Zn. S, galenit Pb. S, pyrit Fe. S 2 aj. ) v atmosféře H 2 S, SO 2 součást esenciálních aminokyselin (cystin, cystein a methionin) • přírodní síra je směsí izotopů S 8 32 S, 33 S, 34 S, 36 S

Síra • • • • S Chemický vzorec: Tvrdosť: 1, 5 – 2 Vryp: biely, niekedy svetložltý Farba: žltá, medovožltá, žltohnedá až žltozelená Priehľadnosť: priesvitná Lesk: na kryštálových plochách diamantový, na lomových plochách matný Štiepateľnosť: slabá Lom: lastúrnatý, nerovný Kryštalografická sústava: ortorombická Výskyt: Viglašská Huta, Dubník, Smolník Sprievodné minerály: kalcit, aragonit, celestín Podobné minerály: žltý sfalerit Testy: Síra sa taví pri nízkej teplote a vylučuje SO 2. Použitie: výroba H 2 SO 4, chemikálií, výbušnín, použitie v papierenskom priemysle, v gumárstve, na výrobu zápaliek, do prostriedkov proti škodcom Zaujímavosti: V minulosti sa používala na výrobu strelného prachu.

PYRIT • • • • Fe. S Chemické zloženie: 2 Tvrdosť: 6 -6, 5 Vryp: zelenočierny Farba: žltá, mosadznežltá (niekedy zachádza do pestrých nábehových farieb) Priehľadnosť: opakná Lesk: kovový Štiepateľnosť: nedokonalá Lom: lastúrnatý, nerovný Kryštalografická sústava: kubická Výskyt: hojný, je to najrozšírenejší sulfidický minerál: Hnúšťa, Banská Štiavnica, Smolník, Zlatá Baňa, . . . Sprievodné minerály: sfalerit, galenit, kremeň, kalcit Podobné minerály: markazit (má iný tvar kryštálov a viac zelený vryp) Testy: pri nárazoch s tvrdými kovovými predmetmi iskrí, pomerne ľahko sa taví Použitie: na výrobu H 2 SO 4 a leštiacich práškov, niekedy je zdrojom Co, Cu, Au, Se, . . . , viazaných na pyritové rudy v prímesiach, zriedka bývajú menšie samostatné a dokonalé kryštály spracované ako drahé kamene Zaujímavosti: Pre svoju farebnú podobnosť (spolu s chalkopyritom) sa nazýva aj „Mačacie zlato“ – „Fool’s gold“

GALENIT • • • • Chemické zloženie: Pb. S Tvrdosť: 2, 5 Vryp: šedočierny, lesklý do modrého odtieňa sfarbený Farba: svetloolovená alebo tmavoolovená, na čerstvom lome s modrastým odtieňom Priehľadnosť: opakná Lesk: kovový, na štiepnych plochách silný Štiepateľnosť: veľmi dobrá Lom: pololastúrovitý Kryštalografická sústava: kubická Výskyt: Banská Štiavnica, Zlatá Baňa, pri Ochtinej Sprievodné minerály: sfalerit, chalkopyrit, baryt, sulfidy striebra Podobné minerály: Vzhľadom na farbu, lesk, dokonalú štiepateľnosť je galenit nezameniteľný. Testy: Rozpúšťa sa v HCl, pričom vzniká nepríjemne páchnuci H 2 S. Použitie: Je to hlavná ruda olova. Jeho hlavné využitie je teda v tom, že sa z neho získava olovo, ktoré sa ďalej využíva.

CHALKOPYRIT • • • • Cu. Fe. S Chemické zloženie: 2 Tvrdosť: 3, 5 - 4 Vryp: zelenočierny Farba: mosadznežltá, niekedy so zeleným nádychom, zlatožltá (časté nábehové farby) Priehľadnosť: opakná Lesk: kovový Štiepateľnosť: nedokonalá Lom: lastúrnatý, nerovný Kryštalografická sústava: tetragonálna Výskyt: Smolník, Gelnica, Slovinky, Rožňava, Zlatá Baňa, Banská Štiavnica, Hodruša Sprievodné minerály: pyrit, sfalerit, kalcit, fluorit, tetraedrit Podobné minerály: baryt, dolomit, kremeň Testy: Rozpúšťa sa v HNO 3 a plameň sfarbuje do zelena. Použitie: Je to najdôležitejšia ruda medi. Použitie má v elektropriemysle, v chemickom a strojárenskom priemysle, občas sa používa ako drahý kameň. Zaujímavosti:

Síra výroba Elementární síra se nejčastěji získává ze sirných ložisek (hlavní naleziště USA, bývalém SSSR, Kanada, Polsko, Japonsko) Frashův způsob získávání síry z podzemí roztavením přehřátou vodní parou a vytlačením roztavené síry na povrch horkým vzduchem. Tato síra je velmi čistá, obvykle více než 99, 5 %. Jiné způsoby výroby síry oxidací sulfanu ze zemního plynu, příp. se sirných sloučenin přítomných v ropě.

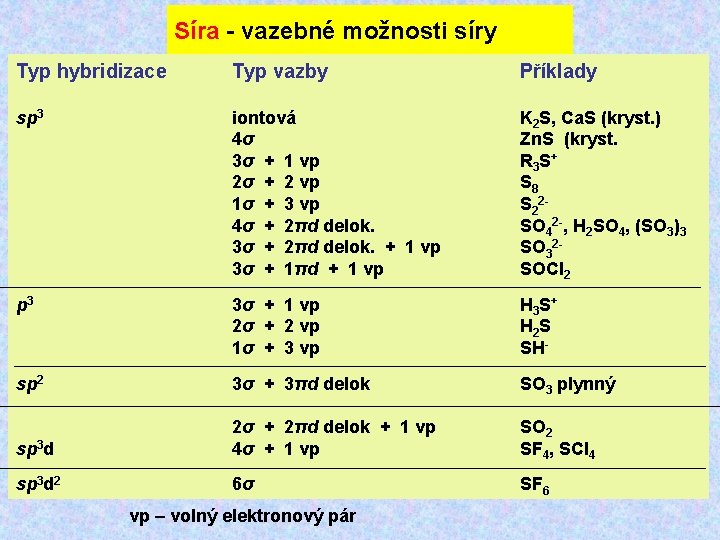
Síra – vazebné poměry Ø elektronové konfigurace valenční sféry pro kyslík i síru jsou shodné (ns 2 np 4) Ø tvorba aniontu S 2 - je obtížná – jen u sulfidů nejelektropozitivnějších kovů s nízkou ionizační energií (alkalické kovy). Ø důvodem je nízká elektronegativita síry (jen 2, 4) a záporná hodnota elektronové afinity (pro přechod S → S 2 - je – 3, 4 e. V). Proto síra ochotněji vytváří kovalentní vazby. Ø síra volné nd-orbitaly. Při vytváření σ-vazeb může tedy vystupovat až jako šestivazná. Pro vytváření σ-vazeb může síra použít p-orbitaly, častěji však hybridní sp 2, sp 3 d a sp 3 d 2 orbitaly. Ø vedle σ-vazeb je síra schopna vytvářet i πpd interakce se silně elektronegativními prvky (F, O, Cl) díky přítomnosti 3 d-vakantních orbitalů. Ø tyto π-vazby jsou obvykle delokalizované a projevují se zkrácením vazebných partnerů pod hodnotu součtu kovalentních poloměrů. Ø hodnota energie vazby S—S je dosti vysoká (264 k. J mol-1), proto známe řadu sloučenin, v nichž je tato vazba přítomna. Ø díky nízké elektronegativitě síry je velmi snížena schopnost vazby S—H tvořit vodíkové můstky

Síra - vazebné možnosti síry Typ hybridizace Typ vazby Příklady sp 3 iontová 4σ 3σ + 1 vp 2σ + 2 vp 1σ + 3 vp 4σ + 2πd delok. 3σ + 2πd delok. + 1 vp 3σ + 1πd + 1 vp K 2 S, Ca. S (kryst. ) Zn. S (kryst. R 3 S + S 8 S 22 SO 42 -, H 2 SO 4, (SO 3)3 SO 32 SOCl 2 p 3 3σ + 1 vp 2σ + 2 vp 1σ + 3 vp H 3 S + H 2 S SH- sp 2 3σ + 3πd delok SO 3 plynný sp 3 d 2σ + 2πd delok + 1 vp 4σ + 1 vp SO 2 SF 4, SCl 4 sp 3 d 2 6σ SF 6 vp – volný elektronový pár

Síra - molekula Síra tvoří několik allotropických modifikací. Ø Jedinou stálou modifikací je kosočtverečná síra normálním tlaku do teploty 95, 3 o. C. Sα, stálá při Ø Nad touto teplotou přechází na jednoklonnou modifikaci stability 95, 3 – 119 o. C, kdy taje. Sβ s oblastí S Ø Obě modifikace jsou tvořeny cykly 8, liší se vzájemným uspořádáním molekul v krystalové mříži. Ø V cyklech S 8 mají vazebné úhly S—S—S hodnotu 107, 8 o, lze tedy pro atomy síry uvažovat hybridní stav sp 3 (atomy leží síry v S 8 cyklech střídavě ve dvou rovinách).

Síra – vlastnosti při zahřívání t. t. = 119 °C t. v. = 444, 6 °C Ø 119 -161 o. C - síra jako žlutá kapalina. Ø > 161 o. C prudce roste viskozita a reaktivita síry Ø dochází totiž k štěpení cyklů S 8 za vzniku řetězovitých biradikálů S-(S)6 -S (tzv. Sπ) Ø tyto biradikály se ihned spojují do různě dlouhých řetězců, což je spojeno se změnou viskozity (zvýšením) a tmavnutím taveniny. Ø prudkým ochlazením taveniny (vylití do vody) se získá plastická síra Sμ , tvořená právě těmito dlouhými řetězci. Ø Sμ je nestálá, během několika dní samovolně přechází na Sα. Ø mimo tyto tři hlavní modifikace byly popsány ještě Sρ, cyklická židličková modifikace S 6 a další cyklické struktury, např. S 7, S 10, S 12, S 18 aj. Ø > 444, 6 o. C dochází k dalšímu štěpení na S 6, S 4 Ø > 900 o. C vzniká paramagnetická síra S 2 (viz kyslík).

Síra – vlastnosti a reaktivita Rozpustnost síry závisí na modifikaci: Sα je dobře rozpustná: • v sirouhlíku, • hůře v CCl 4, • benzenu, • špatně v alkoholu, • ve vodě je nerozpustná. Reaktivita síry Ø je značná, zvláště při vyšší teplotě (vznik radikálů štěpením cyklů). Ø slučuje se téměř se všemi prvky vyjma vzácných plynů, dusíku, telluru, jodu, platiny, iridia a zlata. Ø stabilní sloučeniny netvoří pouze se vzácnými plyny a jodem. Ø s většinou kovů reaguje síra ochotně za tvorby sulfidů už při mírném zahřátí, Ø Zn. S a Hg. S vznikají už při pokojové teplotě – likvidace rtuti.

Síra – sloučeniny - sulfan Sulfan H 2 S je bezbarvý plyn (teplota tání je -85, 6 o. C, varu -60, 3 o. C) Ø ve velmi zředěném stavu zapáchající po shnilých vejcích, koncentrovaný relativně příjemně páchne Ø prudce jedovatý (více než HCN !). Ø příprava a výroba H 2 + S H 2 S H = -20 k. J. mol-1 Ø rozklad některých sulfidů (Fe. S, Ca. S, Ba. S) silnými neoxidujícími kyselinami Fe. S + 2 HCl → Fe. Cl 2 + H 2 S Ø redukce konc. H 2 SO 4 některými kovy (Zn) či organickými látkami. Ø v přírodě vzniká hnitím bílkovin a je obsažen i v některých minerálních vodách Je rozpustný ve vodě:

Síra – sloučeniny - sulfan Sulfan má redukční vlastnosti (volné elektronové páry na atomu síry), oxiduje se většinou na elementární síru; v kyslíku hoří na SO 2 H 2 S + Cl 2 → 2 HCl + S H 2 S + H 2 O 2 → 2 H 2 O + S H 2 S + 2 Fe. Cl 3 → 2 Fe. Cl 2 + 2 HCl + S H 2 S + konc. H 2 SO 4 → S + SO 2 + 2 H 2 O

Síra – sloučeniny - sulfidy Sulfan se rozpouští ve vodě na asi 0, 1 M roztok (sirovodíková voda), Ø je slabou dvojsytnou kyselinou (K 1 = 0, 87∙ 10 -7 ; K 2 = 0, 79∙ 10 -13) Ø tvoří dvě řady solí (hydrogensulfidy a sulfidy). hydrogensulfidy jsou vesměs dobře rozpustné ve vodě. Prakticky je známe pouze od alkalických kovů a zemin. sulfidy známe téměř ode všech kovů, rozpustné jsou pouze sulfidy alkalických kovů, částečně i alkalických zemin. Sulfid amonný známe pouze v roztoku. V důsledku hydrolýzy reagují roztoky těchto solí zásaditě : S 2 - + H 2 O SH- + OH-

Síra – sloučeniny - sulfidy Ø těžké kovy tvoří sulfidy vesměs nerozpustné, Ø připravené srážením, bývají barevné. Ø v přírodě se nacházející sulfidy mívají odlišné, většinou tmavé zbarvení. Ø sulfidy některých trojmocných kovů se snadno hydrolyzují (Al 2 S 3, Cr 2 S 3, Ln 2 S 3). Sulfidy v kvalitativní analýze – „sirovodíková škola“ Ø různá rozpustnost v kyselinách umožňuje i analytické využití srážení, eventuálně. dělení sulfidů. Ø některé sulfidy lze srážet v kyselém prostředí (tedy plynným sulfanem), např. Pb. S, Ag 2 S, Hg. S, Cd. S, Cu. S, As 2 S 3, Sn. S 2, Ø jiné lze vysrážet pouze v alkalickém prostředí, např. Fe. S, Mn. S, Co. S, Ni. S aj. Cu. SO 4 + H 2 S → Cu. S + H 2 SO 4 Mn. SO 4 + (NH 4)2 S → Mn. S + (NH 4)2 SO 4

Síra – sloučeniny - sulfidy Některé sulfidy reagují s nadbytkem alkalických sulfidů za tvorby thiosolí Sn. S 2 + (NH 4)2 S → (NH 4)2 Sn. S 3 trithiocíničitan Ø v přírodě se nacházející sulfidy slouží často jako rudný materiál pro výrobu kovů (Pb. S, Zn. S, Hg. S, Bi 2 S 3, As 2 S 3 aj. ) – SO 2 pro výrobu kyseliny sírové Ø jako vedlejší produkt vznikající SO 2 se zpracovává většinou na H 2 SO 4. Ø praktické využití mají též sulfidy (a polysulfidy) alkalických kovů, vápenatý (koželužství) a barnatý (výroba lithoponu), vyráběné nejčastěji redukcí síranů : Ca. SO 4 (Ba. SO 4) + 4 C Ca. S (Ba. S) + 4 CO

Síra – sloučeniny - polysulfidy Tavením sulfidů alkalických kovů, příp. zemin, se sírou (v případě sulfidu amonného probíhá reakce i ve vodném roztoku) vznikají žluté až žlutohnědé polysulfidy, např. Na 2 Sn (n = 2 - 6). Tyto látky můžeme odvozovat od polysulfanů H 2 Sn. H 2 S 2 H 2 S 3 H 2 S 4 H 2 S 5 p. K 1 p. K 2 6, 83 5, 0 4, 2 3, 8 3, 5 ~ 14 9, 7 7, 5 6, 3 5, 7 Polysulfidy mají spíše iontový charakter. V krystalickém stavu jsou stálé, některé, hlavně disulfidy, nacházíme i v přírodě (Fe. S 2, Co. S 2, Ni. S 2). Polysulfidy sodné a vápenaté slouží v koželužství („sirná játra“ – také patinování mědi) a při průmyslové výrobě thiosíranů.

Síra – sloučeniny - oxidy V literatuře byla popsána celá řada oxidů síry o složení: Sn. O, Sn. O 2 (n = 5 -10), S 2 O, SO i peroxid SO 4. Všechny tyto látky jsou málo stálé a zcela postrádají praktické použití. Nejdůležitější jsou oxid siřičitý a oxid sírový.

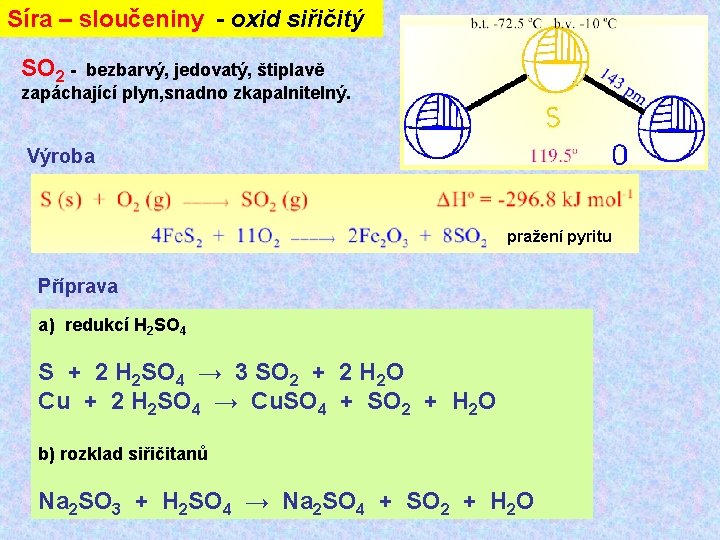
Síra – sloučeniny - oxid siřičitý SO 2 - bezbarvý, jedovatý, štiplavě zapáchající plyn, snadno zkapalnitelný. Výroba pražení pyritu Příprava a) redukcí H 2 SO 4 S + 2 H 2 SO 4 → 3 SO 2 + 2 H 2 O Cu + 2 H 2 SO 4 → Cu. SO 4 + SO 2 + H 2 O b) rozklad siřičitanů Na 2 SO 3 + H 2 SO 4 → Na 2 SO 4 + SO 2 + H 2 O

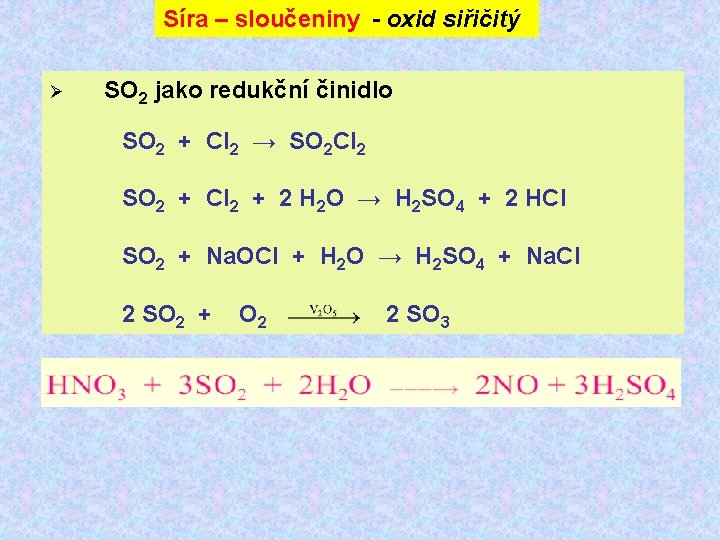
Síra – sloučeniny - oxid siřičitý Ø SO 2 jako redukční činidlo SO 2 + Cl 2 → SO 2 Cl 2 SO 2 + Cl 2 + 2 H 2 O → H 2 SO 4 + 2 HCl SO 2 + Na. OCl + H 2 O → H 2 SO 4 + Na. Cl chlorid sulfurylu 2 SO 2 + O 2 2 SO 3
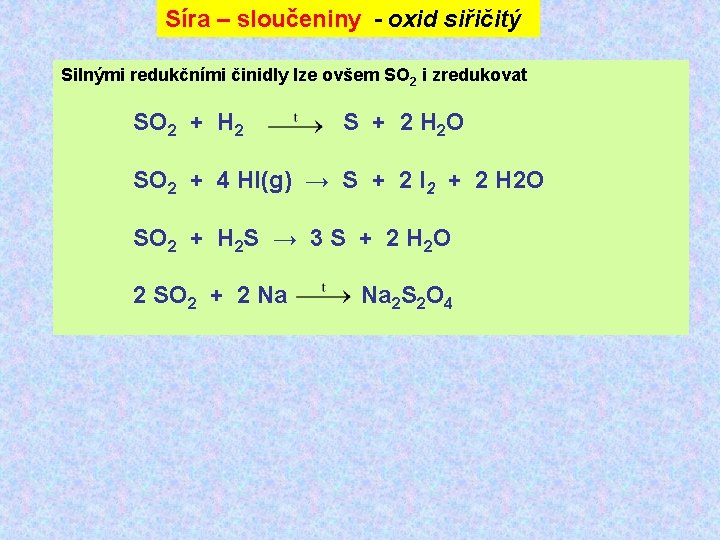
Síra – sloučeniny - oxid siřičitý Silnými redukčními činidly lze ovšem SO 2 i zredukovat SO 2 + H 2 S + 2 H 2 O SO 2 + 4 HI(g) → S + 2 I 2 + 2 H 2 O SO 2 + H 2 S → 3 S + 2 H 2 O 2 SO 2 + 2 Na 2 S 2 O 4

Síra – sloučeniny - oxid siřičitý jako rozpouštědlo SO 2 jako aprotické rozpouštědlo Ø kapalný SO 2 je vynikající aprotické rozpouštědlo pro velké množství kovalentních sloučenin (PCl 3, CS 2, SOX 2, Br 2, aminy, alkoholy, estery, organické kyseliny). Ø Z iontových sloučenin rozpouští jodidy alkalických kovů, ostatní soli jen omezeně. Ø solvolytické reakce v kapalném SO 2 WCl 6 + SO 2 → WOCl 4 + SOCl 2 Rozpustnost ve vodě Ø rozpustnost: ve 100 cm 3 při 20 o. C až 3900 cm 3 Ø vodný roztok lze spíše charakterizovat jako SO 2∙x. H 2 O než kyselinu siřičitou. Ø při 0 o. C lze získat klathrát o přibližném složení SO 2∙ 6 H 2 O

Síra – sloučeniny - použití oxidu siřičitého v výroba kyseliny sírové, v výroba siřičitanů, v v průmyslu celulózy (sulfitové louhy), v odbarvování látek, konzervaci ovoce aj. Pozn. Přítomnost SO 2 v ovzduší představuje (vedle NOx) snad největší ohrožení životního prostředí.

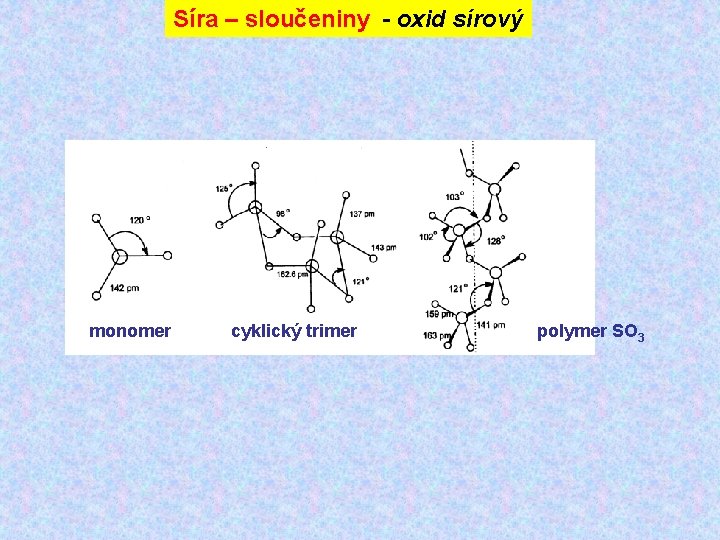
Síra – sloučeniny - oxid sírový monomer cyklický trimer polymer SO 3

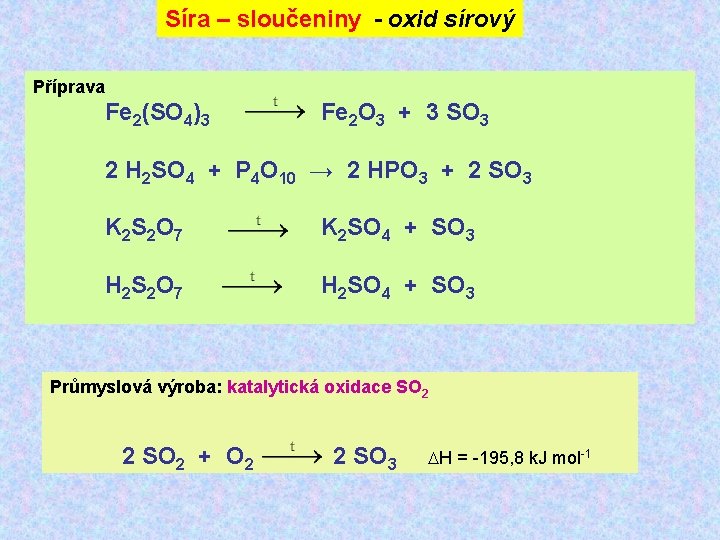
Síra – sloučeniny - oxid sírový Příprava Fe 2(SO 4)3 Fe 2 O 3 + 3 SO 3 2 H 2 SO 4 + P 4 O 10 → 2 HPO 3 + 2 SO 3 K 2 S 2 O 7 K 2 SO 4 + SO 3 H 2 S 2 O 7 H 2 SO 4 + SO 3 Průmyslová výroba: katalytická oxidace SO 2 2 SO 2 + O 2 2 SO 3 H = -195, 8 k. J mol-1

Síra – sloučeniny - vlastnosti a použití SO 3 Ø Chemická reaktivita oxidu sírového je velká. Ø Extremně vysoká je jeho afinita k vodě, i konstitučně vázané, a jeho oxidační vlastnosti. Ø Většina vyrobeného oxidu sírového se zpracovává dále na kyselinu sírovou (výroba síranů, hnojiv, textilní průmysl, průmysl ropy aj. ), Ø H 2 S 2 O 7 („oleum“) pro sulfonace aj.

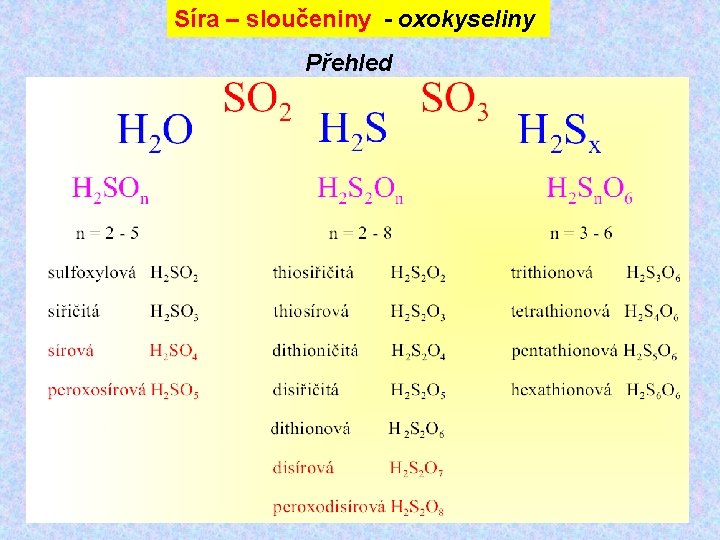
Síra – sloučeniny - oxokyseliny Přehled

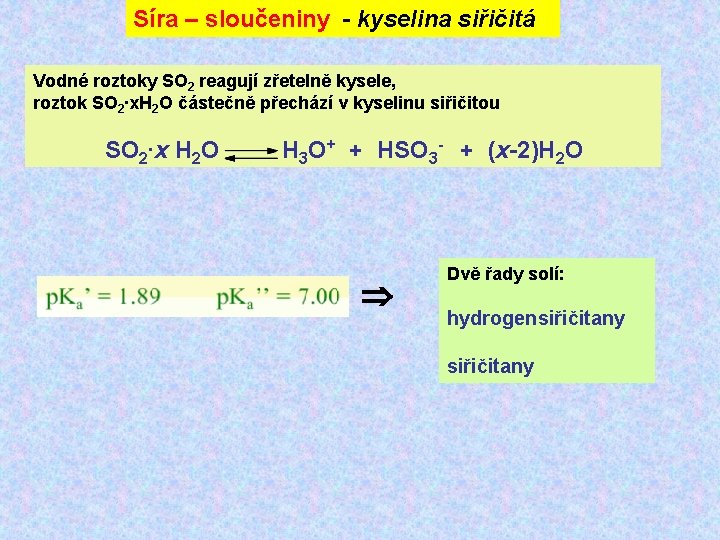
Síra – sloučeniny - kyselina siřičitá Vodné roztoky SO 2 reagují zřetelně kysele, roztok SO 2∙x. H 2 O částečně přechází v kyselinu siřičitou SO 2∙x H 2 O H 3 O+ + HSO 3 - + (x-2)H 2 O Dvě řady solí: hydrogensiřičitany

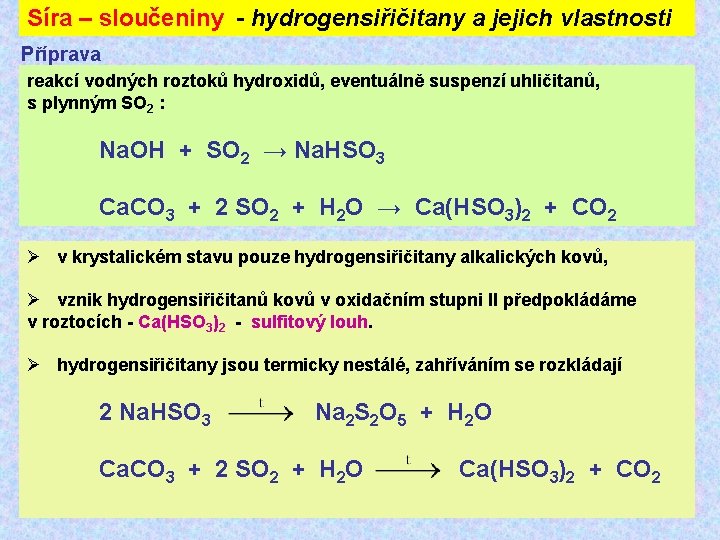
Síra – sloučeniny - hydrogensiřičitany a jejich vlastnosti Příprava reakcí vodných roztoků hydroxidů, eventuálně suspenzí uhličitanů, s plynným SO 2 : Na. OH + SO 2 → Na. HSO 3 Ca. CO 3 + 2 SO 2 + H 2 O → Ca(HSO 3)2 + CO 2 Ø v krystalickém stavu pouze hydrogensiřičitany alkalických kovů, Ø vznik hydrogensiřičitanů kovů v oxidačním stupni II předpokládáme v roztocích - Ca(HSO 3)2 - sulfitový louh. Ø hydrogensiřičitany jsou termicky nestálé, zahříváním se rozkládají 2 Na. HSO 3 Na 2 S 2 O 5 + H 2 O Ca. CO 3 + 2 SO 2 + H 2 O Ca(HSO 3)2 + CO 2

Síra – sloučeniny - kyselina sírová Ø H 2 SO 4 je bezbarvá olejovitá kapalina Ø neomezeně mísitelná s vodou za uvolňování značného množství tepla (asi 880 k. J mol-1). Ø při ředění je proto potřebí dbát opatrnosti a nalévat vždy za míchání a chlazení kyselinu do vody (hrozí totiž až explosivní vystříknutí kapalné směsi). Ø uvolňování tepla je hlavně důsledek disociace nedisociované kyseliny. Ø do prodeje přichází kyselina sírová jako 98, 3 % (azeotrop o t. varu 338 o. C) Ø kyselina sírová je silná dvojsytná kyselina (K 2 = 1, 29∙ 10 -2), Ø tvoří dvě řady solí – hydrogensírany a sírany

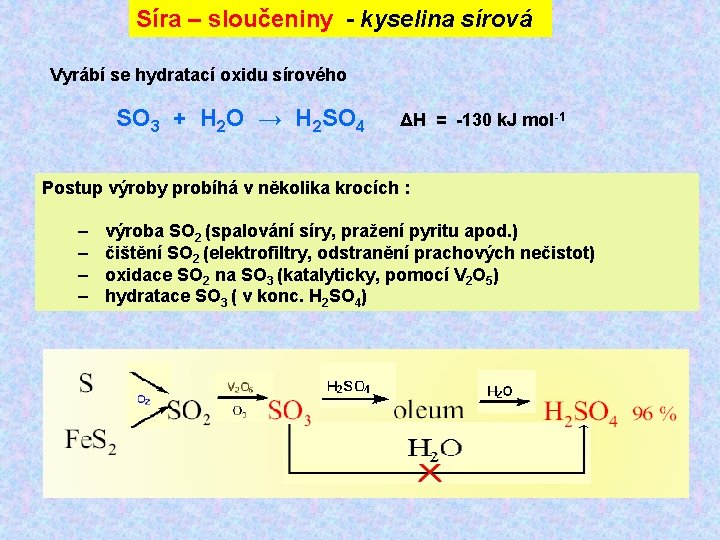
Síra – sloučeniny - kyselina sírová Vyrábí se hydratací oxidu sírového SO 3 + H 2 O → H 2 SO 4 ΔH = -130 k. J mol-1 Postup výroby probíhá v několika krocích : – – výroba SO 2 (spalování síry, pražení pyritu apod. ) čištění SO 2 (elektrofiltry, odstranění prachových nečistot) oxidace SO 2 na SO 3 (katalyticky, pomocí V 2 O 5) hydratace SO 3 ( v konc. H 2 SO 4)

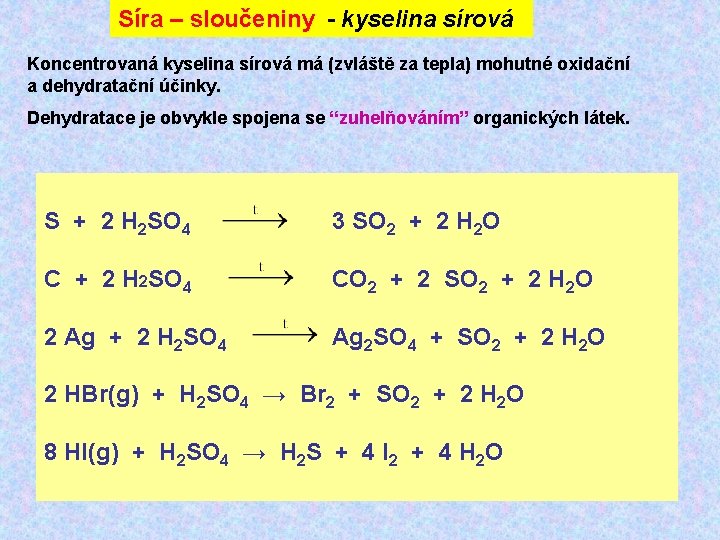
Síra – sloučeniny - kyselina sírová Koncentrovaná kyselina sírová má (zvláště za tepla) mohutné oxidační a dehydratační účinky. Dehydratace je obvykle spojena se “zuhelňováním” organických látek. S + 2 H 2 SO 4 3 SO 2 + 2 H 2 O C + 2 H 2 SO 4 CO 2 + 2 SO 2 + 2 H 2 O 2 Ag + 2 H 2 SO 4 Ag 2 SO 4 + SO 2 + 2 H 2 O 2 HBr(g) + H 2 SO 4 → Br 2 + SO 2 + 2 H 2 O 8 HI(g) + H 2 SO 4 → H 2 S + 4 I 2 + 4 H 2 O

Síra – sloučeniny - hydrogensírany MIHSO 4 Ø vesměs dobře rozpustné; Ø v krystalickém stavu lze získat pouze soli alkalických kovů. Ø nejsou termicky stálé, za zvýšené teploty se rozkládají na disírany : 2 KHSO 4 K 2 S 2 O 7 + H 2 O Ø používají se pro na tzv. kyselé tavení – převádění obtížně rozpustných oxidů (Al 2 O 3, Ti. O 2, Zr. O 2 aj. ) na rozpustné sírany.

Síra – sloučeniny - sírany Ø SO 42 - - známe téměř ode všech kovů. Ø jsou většinou dobře rozpustné, pokud není barevný kation, jsou bezbarvé. Ø špatně rozpustné jsou sírany alkalických zemin, Pb. SO 4, omezeně rozpustný je Ag 2 SO 4. Příprava H 2 SO 4 + 2 KOH → K 2 SO 4 + 2 H 2 O Zn + zřed. H 2 SO 4 → Zn. SO 4 + H 2 Hg + konc. H 2 SO 4 → Hg. SO 4 + SO 2 + 2 H 2 O Ba. Cl 2 + H 2 SO 4 → Ba. SO 4 + 2 HCl Zn. CO 3 + H 2 SO 4 → Zn. SO 4 + CO 2 + H 2 O Na 2 SO 3 + H 2 O 2 → Na 2 SO 4 + H 2 O

Síra – sloučeniny - sírany Použití síranů (NH 4)2 SO 4 - hnojivo Na 2 SO 4∙ 10 H 2 O (Glauberova sůl) výroba Na 2 CO 3 skalice MIISO 4∙n. H 2 O (M = Zn, Fe, Co, Mn n = 7), event. M = Cu, Mn, Cr; n = 5), kamence MIMIII(SO 4)2∙ 12 H 2 O (MI = Na, K, NH 4, Rb, Cs aj. ; MIII = Al, Cr, Fe, Mn, Ti, V aj. ) sádra Ca. SO 4∙ 1/2 H 2 O baryt Ba. SO 4 (rtg. vyšetření, součást lithoponu)

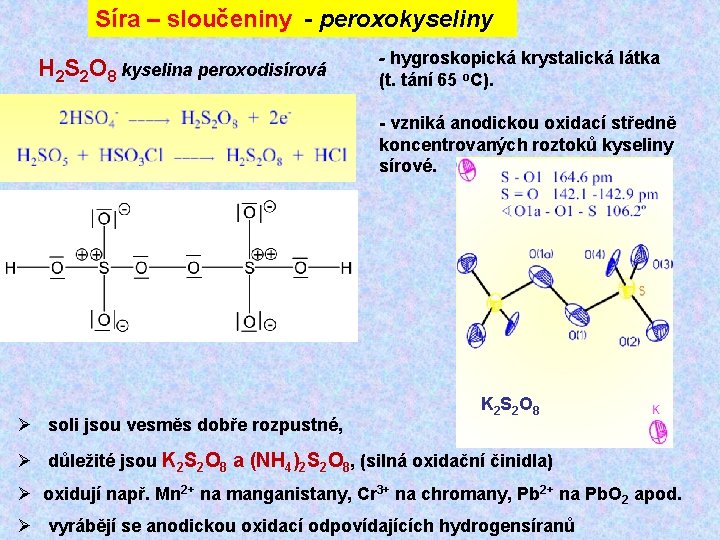
Síra – sloučeniny - peroxokyseliny H 2 S 2 O 8 kyselina peroxodisírová - hygroskopická krystalická látka (t. tání 65 o. C). - vzniká anodickou oxidací středně koncentrovaných roztoků kyseliny sírové. Ø soli jsou vesměs dobře rozpustné, K 2 S 2 O 8 Ø důležité jsou K 2 S 2 O 8 a (NH 4)2 S 2 O 8, (silná oxidační činidla) Ø oxidují např. Mn 2+ na manganistany, Cr 3+ na chromany, Pb 2+ na Pb. O 2 apod. Ø vyrábějí se anodickou oxidací odpovídajících hydrogensíranů

Síra – sloučeniny - peroxokyseliny Kyselina peroxodisírová je důležitým meziproduktem při výrobě peroxidu vodíku. Hydrolýzou poskytuje jako konečné produkty H 2 SO 4 a H 2 O 2. Tato hydrolýza probíhá stupňovitě : H 2 S 2 O 8 H 2 SO 5 + H 2 SO 4 2 H 2 SO 4 + H 2 O 2 Kyselina peroxosírová Vzhledem k nízké stabilitě kyseliny i jejích solí MIHSO 5 (odštěpují kyslík) postrádají tyto látky praktické použití.

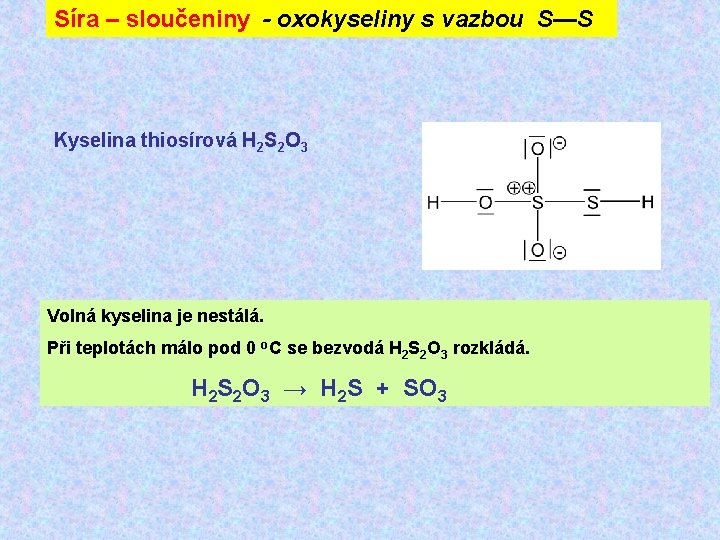
Síra – sloučeniny - oxokyseliny s vazbou S—S Kyselina thiosírová H 2 S 2 O 3 Volná kyselina je nestálá. Při teplotách málo pod 0 o. C se bezvodá H 2 S 2 O 3 rozkládá. H 2 S 2 O 3 → H 2 S + SO 3

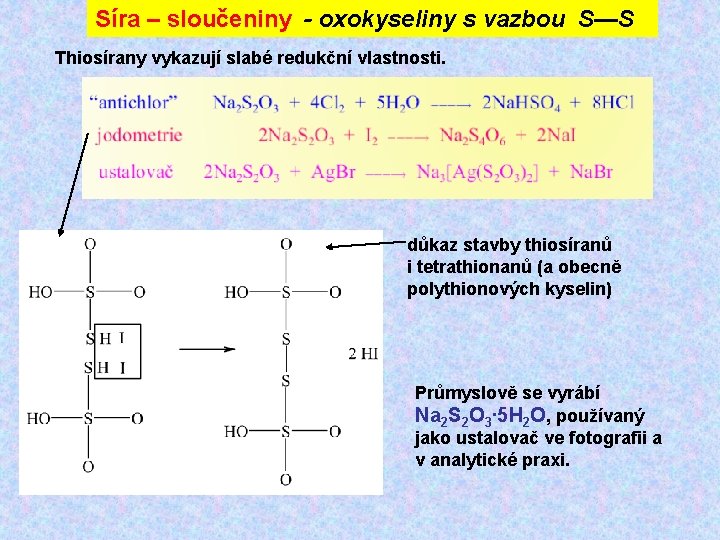
Síra – sloučeniny - oxokyseliny s vazbou S—S Thiosírany vykazují slabé redukční vlastnosti. důkaz stavby thiosíranů i tetrathionanů (a obecně polythionových kyselin) Průmyslově se vyrábí Na 2 S 2 O 3∙ 5 H 2 O, používaný jako ustalovač ve fotografii a v analytické praxi.

Síra – sloučeniny - halogenidy kyselin Halogenidy kyseliny siřičité – halogenidy thionylu SOF 2 SOCl. F SOCl 2 SOBr 2 plyn, t. varu -44 o. C plyn, t. varu 12 o. C kapalina, t. varu 76 o. C červenožlutá kapalina, t. varu 140 o. C Nejdůležitější látkou je thionylchlorid SOCl 2, vysoce reaktivní kapalina štiplavého zápachu SO 2 + PCl 5 → SOCl 2 + POCl 3 SO 3 + SCl 2 → SOCl 2 + SO 2 Praktický význam mají jeho reakce s hydroxylovými sloučeninami : H 2 O + SOCl 2 → SO 2 + 2 HCl ROH + SOCl 2 → SO 2 + RCl + HCl RCOOH + SOCl 2 → SO 2 + RCOCl + HCl V anorganické chemii SOCl 2 jako elegantní dehydratační činidlo (při dehydrataci krystalohydrátů chloridů kovů), Jako nevodné ionizující rozpouštědlo (podobně jako kapalný SO 2).

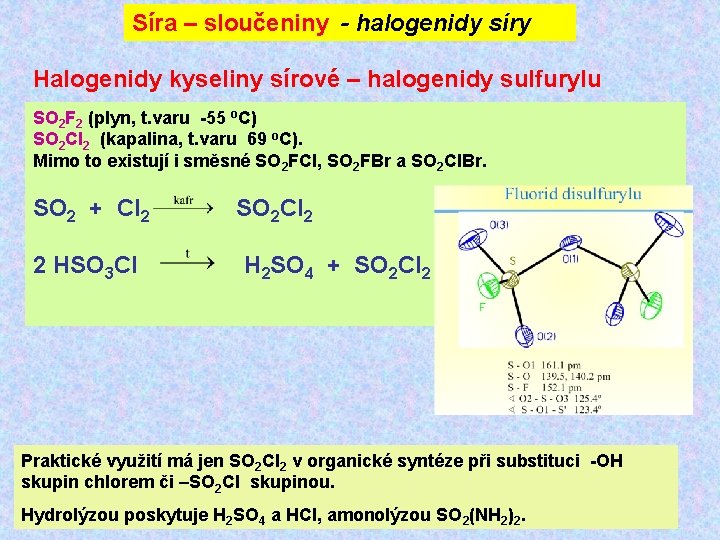
Síra – sloučeniny - halogenidy síry Halogenidy kyseliny sírové – halogenidy sulfurylu SO 2 F 2 (plyn, t. varu -55 o. C) SO 2 Cl 2 (kapalina, t. varu 69 o. C). Mimo to existují i směsné SO 2 FCl, SO 2 FBr a SO 2 Cl. Br. SO 2 + Cl 2 SO 2 Cl 2 2 HSO 3 Cl H 2 SO 4 + SO 2 Cl 2 Praktické využití má jen SO 2 Cl 2 v organické syntéze při substituci -OH skupin chlorem či –SO 2 Cl skupinou. Hydrolýzou poskytuje H 2 SO 4 a HCl, amonolýzou SO 2(NH 2)2.

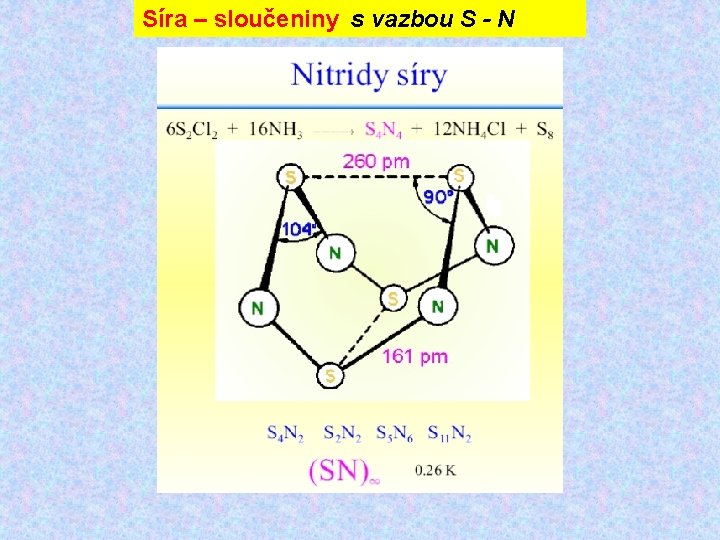
Síra – sloučeniny s vazbou S - N

Síra – sloučeniny s vazbou S - N