Sooladele iseloomulikud Katrin Soika Avaldatud Creative Commonsi litsentsi



















- Slides: 30

Sooladele iseloomulikud Katrin Soika Avaldatud Creative Commonsi litsentsi „Autorile viitamine + jagamine samadel tingimustel 3. 0 Eesti (CC BY-SA 3. 0)“ alusel, vt http: //creativecommons. org/licenses/by-sa/3. 0/ee/

Sisukord Soolade saamisvõimalusi Metall + hape (selgitus, näide) Alus + hape (selgitus) Hape + aluseline oksiid (selgitus) Sool + metall (selgitus, katse, animatsioon, video) Sool +sool (selgitus, animatsioon (I, II) , lahustuvus (I), videod, katse, tabel) Sool + alus (selgitus, animatsioon, lahustuvus, videod, katse, tabel)

lähteained lahustuvad saaduses sade Soolade saamisvõimalusi 1. metall + hape→ sool + vesinik (aktiivsus) 2. alus + hape → sool + vesi (alati) 3. hape + aluseline oksiid→ sool + vesi (alati) 4. sool + metall → sool + metall (aktiivsus) 5. sool + sool → sool + sool (sade) 6. sool + alus → sool + alus (sade)

metall + hape = sool + vesinik NB! Tuleb jälgida metallide pingerida! K Ba Ca Na Mg Al Mn Zn Cr Fe Ni Sn Pb H Cu Hg Ag Pt Au reageerivad lahjendatud hapetega http: //en. wikipedia. org/wiki/File: Zn_reaction_ with_HCl. JPG EI REAGEERI lahjendatud hapetega

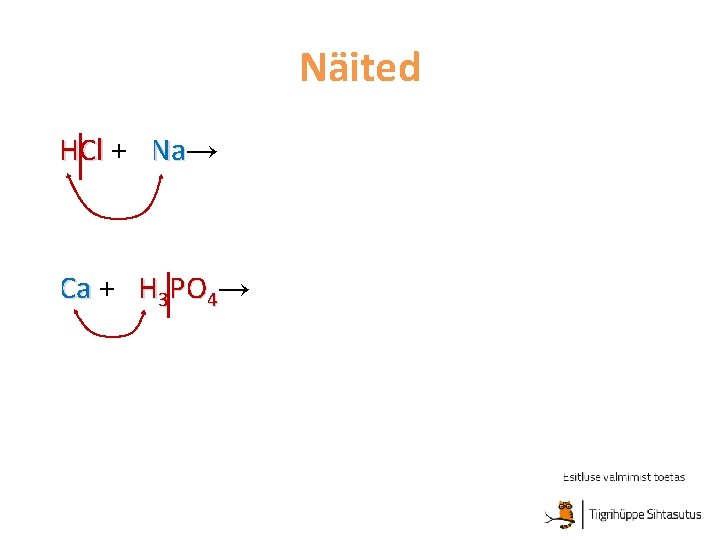
Näited 2 HCl + 2 Na→ Na 2 Na. Cl+ H 2↑ 6 Ca + 2 H 3 PO 4→ 2 Ca 3(PO 4)2 + 3 H 2↑

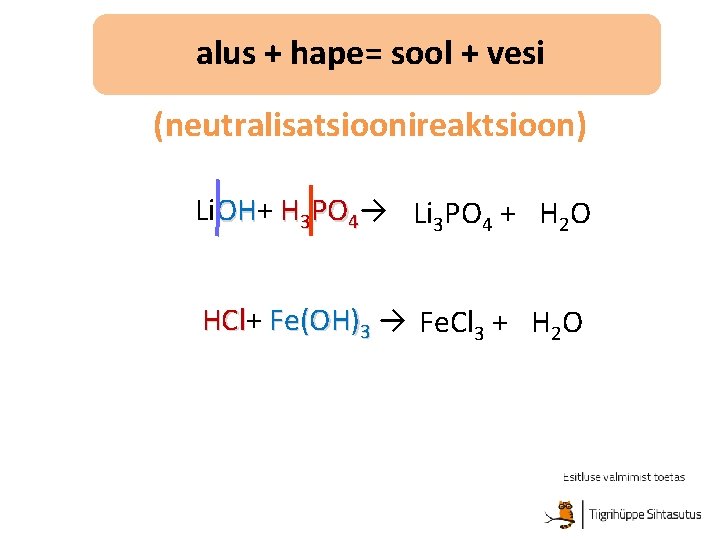
alus + hape= sool + vesi (neutralisatsioonireaktsioon) 3 Li. OH+ OH H 3 PO 4→ Li 3 PO 4 + 3 H 2 O 3 HCl+ Cl Fe(OH)3 → Fe. Cl 3 + 3 H 2 O

hape + aluseline oksiid = sool + vesi 2 Hl + Ba. O → Bal 2 + H 2 O 3 K 2 O + 2 H 3 PO 4 → 2 K 3 PO 4 + 3 H 2 O

sool + metall = sool + metall NB! Tuleb jälgida metallide pingerida! K Ba Ca Na Mg Al Mn Zn Cr Fe Ni Sn Pb H Cu Hg Ag Pt Au Metall peab olema pingereas soola katioonist eespool (vasakul). Ag + Cu(NO 3 )2 → Ei toimu (Ag on pingereas taga) 2 Ag. NO 3 + Cu → 2 Ag↓ + Cu(NO 3 )2

Kontrolli seda reeglit katseliselt Töövahendid: Rauast nael, vask(II)sulfaat, 2 katseklaasi, vaselaastud, raud(II)sulfaat. Töökäik: Vala ühte katseklaasi vask(II)sulfaati ning aseta sinna rauast nael. Teise katseklaasi vala raud(II)sulfaat ja lisa sinna vaselaaste. Jälgi, kummas katseklaasis reaktsioon toimub. Põhjenda!

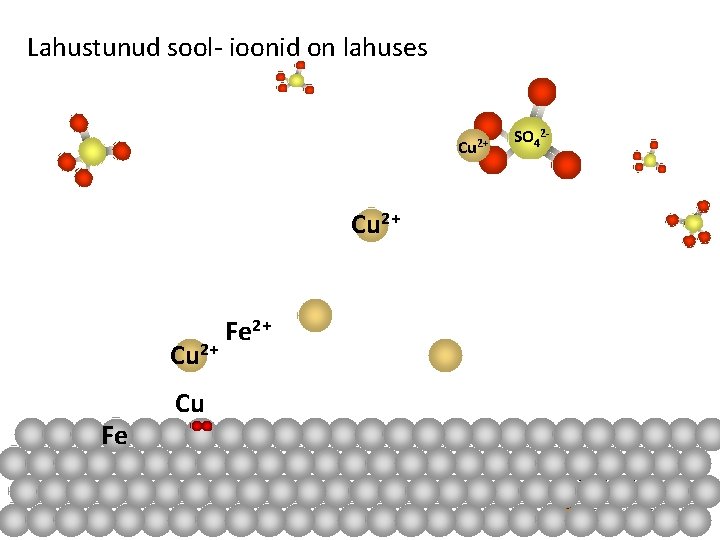
Lahustunud sool- ioonid on lahuses Cu 2+ Fe Cu Fe 2+ SO 42 -

Kirjuta eelneva animatsiooni põhjal toimuva reaktsioonivõrrand. Fe + Cu. SO Cu 4 → Cu↓ Cu + Fe. SO Fe 4

Video- hõbe(I)nitraat + vask http: //www. youtube. com/watch? v=8 BDSz 65 Q Wjc

sool + sool= sool + sool JÄLGI LAHUSTUVUST!

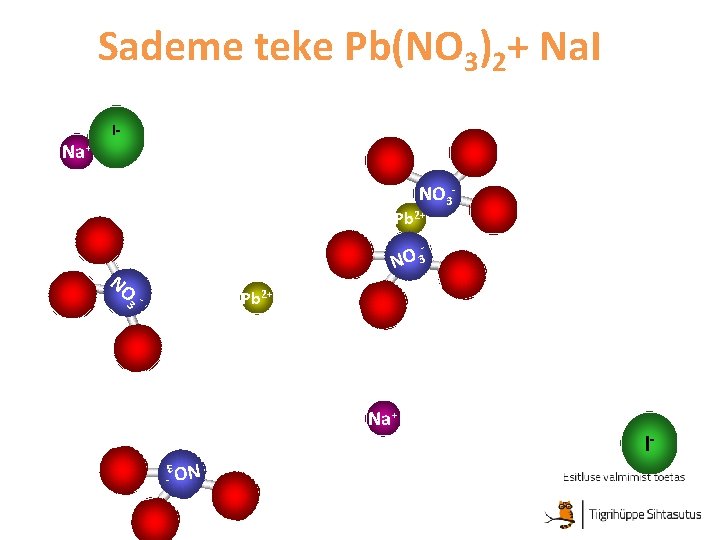
Sademe teke Pb(NO 3)2+ Na. I I- Na+ NO 3 - Pb 2+ NO 3 NO Pb 2+ 3 - Na+ I- NO 3 -

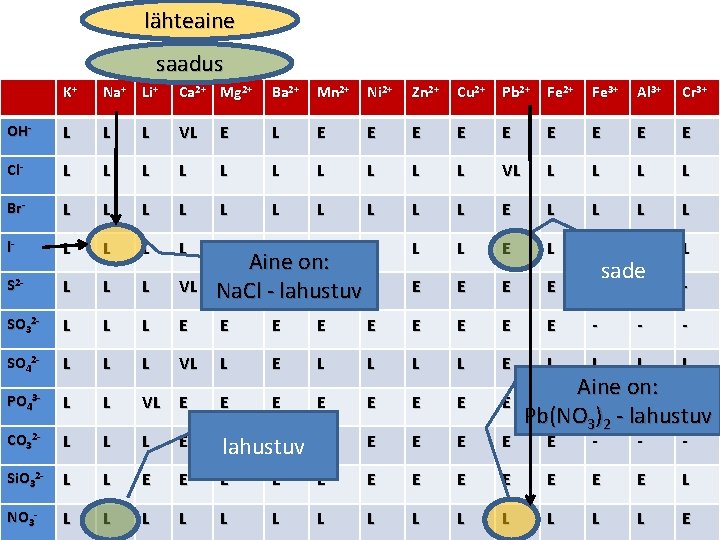
lähteaine saadus K+ Na+ Li+ Ca 2+ Mg 2+ Ba 2+ Mn 2+ Ni 2+ Zn 2+ Cu 2+ Pb 2+ Fe 3+ Al 3+ Cr 3+ OH- L LBr- L VL E E E E E Cl- L L L L L VL L L Br- L L L L L Pb 2+ L E L L l- L L L L L- L E L L S 2 - L LNO L - NO 3 E E E - - SO 32 - L - - SO 42 - L PO 43 - K+ VL Aine on: L L E E Na. Cl Pb 2+- lahustuv NO 3 - sade Reaktsioon toimub, sest saadus (sade) tekib! L L E E E E E Lahuse koostis on muutunud. 3 L L L CO 32 - L Si. O 32 NO 3 - VL L E VL E E E E L L E NO 3 Elahustuv E E E E E L L L L L - L K+ L L E E L L L E Aine on: E E Pb(NO 3)2 - lahustuv E - - Br

Video- plii(II)jodiidi tekkimisest http: //www. youtube. com/watch? v=G 8 qnaq 6 Eh c 8 http: //www. youtube. com/watch? v=Ob 4 yi 4 d. JGz M&feature=related

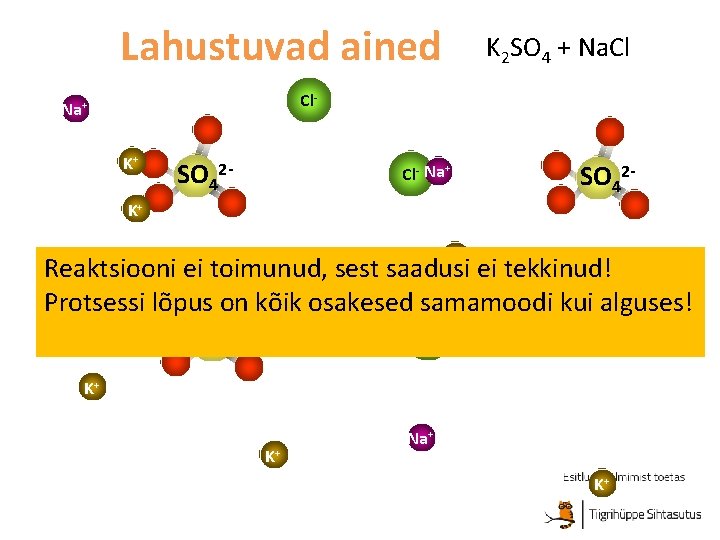
Lahustuvad ained K 2 SO 4 + Na. Cl Cl- Na+ K+ SO 42 - Cl- Na+ SO 42 - K+ K+ Reaktsiooni ei toimunud, sest saadusi ei tekkinud! Protsessi lõpus on kõik osakesed samamoodi kui alguses! Cl. SO 42 K+ K+ Na+ K+

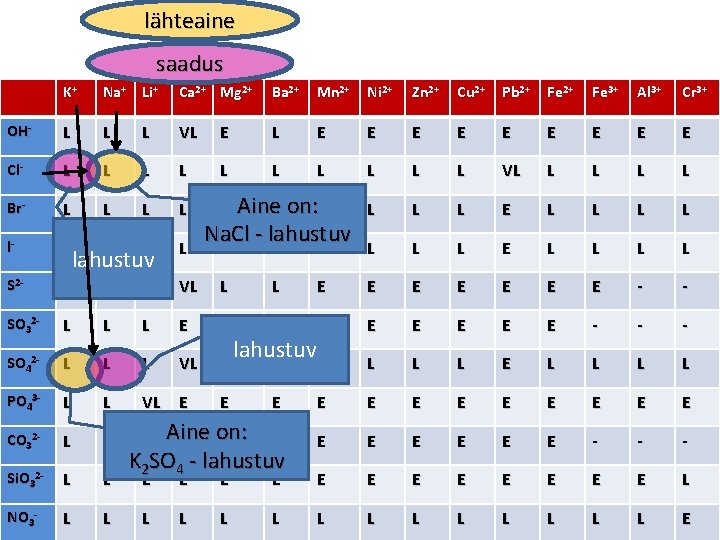
lähteaine saadus K+ Na+ Li+ Ca 2+ Mg 2+ Ba 2+ Mn 2+ Ni 2+ Zn 2+ Cu 2+ Pb 2+ Fe 3+ Al 3+ Cr 3+ OH- L LBr- L VL E E E E E Cl- L L L L L VL L L Br- L L L Pb 2+ L E L L l- L L L- L E L L S 2 - L LNO L NO 3 E E E - - SO 32 - L - - SO 42 - L PO 43 - K+ lahustuv VL 3 - Aine. L on: L Na. Cl - lahustuv L L L Pb 2+ E NO 3 - Reaktsioon toimub, sest saadus (sade) tekib! L L E E E E E Lahuse koostislahustuv on muutunud. L L VL L E L L L L VL E E E CO 32 - L L Aine on: E E E K 2 SO 4 - lahustuv E E E - - Br - Si. O 32 - L L NO 3 - L L L E E E L L L E - L NO 3 E K+

Katse Töövahendid: K 2 S, Na 2 CO 3; Fe. Cl 2; Cu. SO 4 , KCl, Mg. SO 4, Ba(NO 3)2, Pb(NO 3)2, tilkanalüüsi plaat, tilgapudelid, pipetid. Töökäik: a) Kirjuta kõikide toimuvate reaktsioonide tasakaalustatud reaktsioonivõrrandid, b) kontrolli võrrandite õigsust reaktsiooniga, c) pane igasse TAP pesasse 3 -4 tilka soolalahus. Lisa soolalahusele 3 -4 tilka kaaliumsulfiidi, d) kirjelda, mida oli reaktsiooni toimumisel näha ning põhjenda!

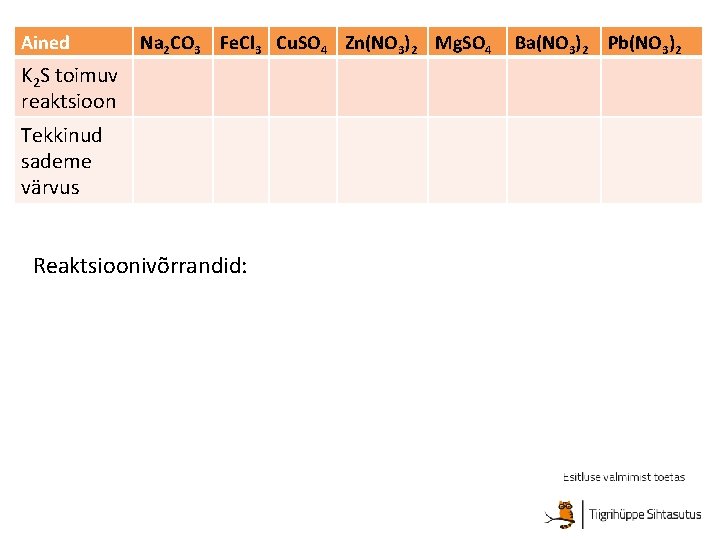
Ained Na 2 CO 3 Fe. Cl 3 Cu. SO 4 Zn(NO 3)2 Mg. SO 4 K 2 S toimuv reaktsioon Tekkinud sademe värvus Reaktsioonivõrrandid: Ba(NO 3)2 Pb(NO 3)2

sool + alus= sool + alus JÄLGI LAHUSTUVUST!

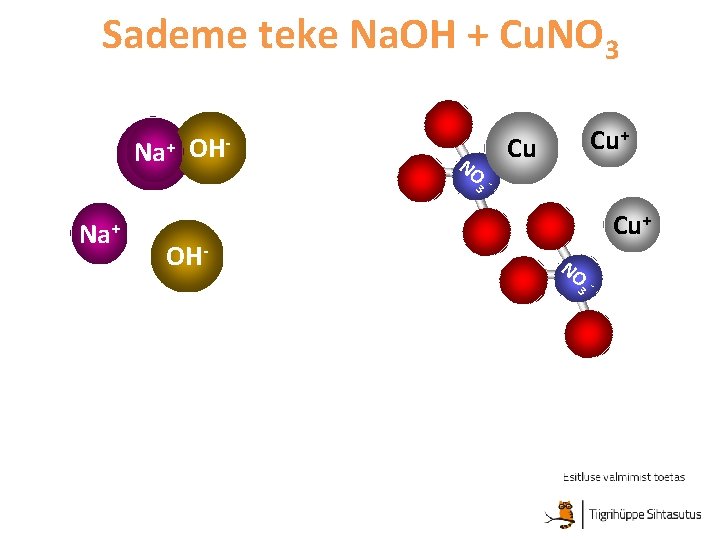
Sademe teke Na. OH + Cu. NO 3 Na+ Na OH- NO Cu+ Cu 3 - Na+ OH- Cu+ NO 3 -

Eelmise näite põhjal: + - + - 2 Na. OH+ Cu(NO 3)2→ 2 Na. NO 3 + Cu(OH)2↓ LAHUSTUVAD! SADE! Tekkis aine, mis läks ühtsest liikumisest välja.

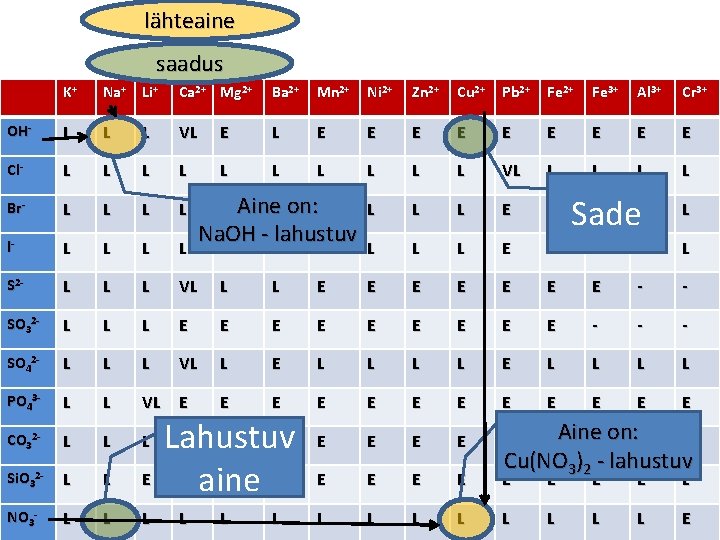
lähteaine saadus K+ Na+ Li+ Ca 2+ Mg 2+ Ba 2+ Mn 2+ Ni 2+ Zn 2+ Cu 2+ Pb 2+ Fe 3+ Al 3+ Cr 3+ OH- L LBr- L VL E E E E E Cl- L L L L L VL L L Br- L L L Pb 2+ L E L L L Sade L l- L L L- L E L L S 2 - L LNO L NO 3 E E E - - SO 32 - L - - SO 42 - L PO 43 - K+ Aine. L on: L Na. OH - lahustuv L L L VL 3 - L L L Pb 2+ E NO 3 - Reaktsioon toimub, sest saadus (sade) tekib! L L E E E E E Lahuse koostis on muutunud. L L VL E CO 32 - L L L Si. O 32 - L L E NO 3 - L L L L E E E E E Aine - on: Br - - - E E E E L L L L L E E Lahustuv E aine E E NO 3 - L L L K+ Cu(NO 3)2 - lahustuv

Video http: //www. chemicum. com/? vid=60&lan=EE

Katse Töövahendid: Na. OH, Na 2 CO 3; Fe. Cl 2; Cu. SO 4 , Ag. NO 3, Mg. SO 4, Ba(NO 3)2, Pb(NO 3)2, tilkanalüüsi plaat, tilgapudelid, pipetid. Töökäik: a) Kirjuta kõikide toimuvate reaktsioonide võrrandid, b) kontrolli võrrandite õigsust reaktsiooniga, c) pane igasse TAP pesasse 3 -4 tilka soolalahust. Lisa soolalahusele 3 -4 tilka leelist, d) kirjelda, mida oli reaktsiooni toimumisel näha ning põhjenda! Lisa ül. Mõtle, milliseid sademeid saaks tekitada kahe soola reageerimisel. Vii reaktsioonid läbi ja kirjuta võrrandid.

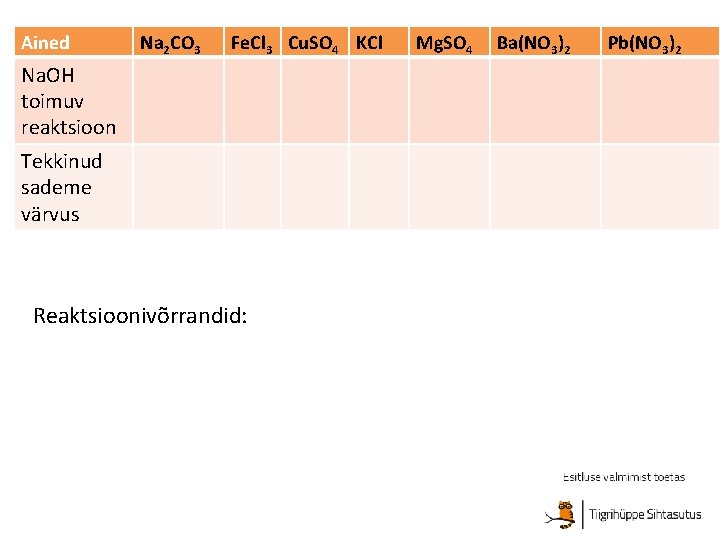
Ained Na 2 CO 3 Fe. Cl 3 Cu. SO 4 KCl Na. OH toimuv reaktsioon Tekkinud sademe värvus Reaktsioonivõrrandid: Mg. SO 4 Ba(NO 3)2 Pb(NO 3)2

1) 2) 3) 4) 5) 6) 7) 8) Kirjuta toimuvad reaktsioonivõrrandid Naatriumhüdroksiid + raud(III)kloriid Kaaliumsulfiid + vask(II)nitraat Väävelhape + kaalium Alumiinium + soolhape Jood + kaalium Hõbe(I)sulfaat + kaaliumnitraat Lämmastik + naatrium Alumiiniumhüdroksiid + kaaliumnitraat

Vastused

Materjalid Videod: http: //www. youtube. com/