REACCION Y ECUACIN QUIMICA SEMANA No 4 1






















- Slides: 26

REACCION Y ECUACIÓN QUIMICA SEMANA No. 4 1

Reacción Química: Proceso en el cual se produce un cambio químico, es decir se consume una o más sustancias a medida que se forman una o más sustancias nuevas. 2

Reactivos: Sustancias presentes en el inicio de la reacción. Productos: Las sustancias que la reacción produce. REACTIVOS PRODUCTOS 3

Ecuación Química Representa de una manera simbólica, lo que ocurre en una reacción. Glucosa + Oxígeno Dióxido de carbono+ Agua C 6 H 12 O 6(s) + 6 O 2(g) 6 CO 2(g) + 6 H 2 O(g) 4

Símbolos de las reacciones: (g)= gas (s)=sólido (l)=líquido (ac)=acuoso Catalizador: Mn. O 2 Reversible Gas liberado Irreversible Precipitado Calor para reaccionar Calor de reacción 65°C 5

BALANCEO DE ECUACIONES En una ecuación química balanceada la cantidad de átomos de cada elemento representados como reactivos y productos tiene que ser el mismo. Utilizaremos moles (6. 022 x 1023 partículas unitarias en un mol) 6

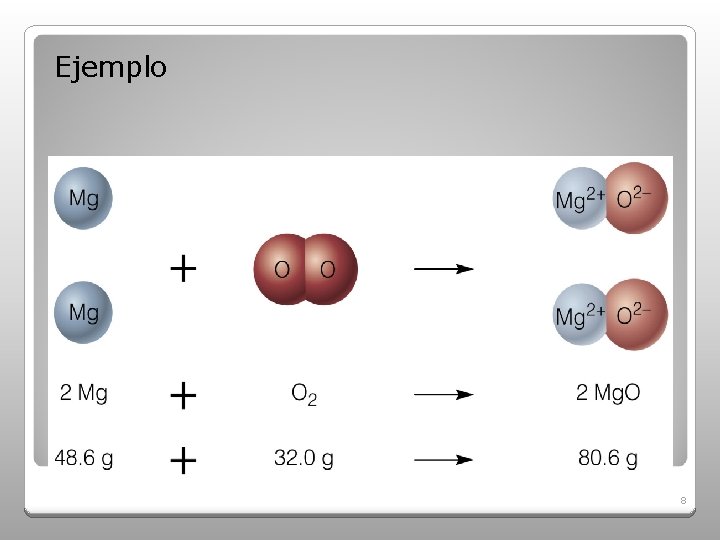
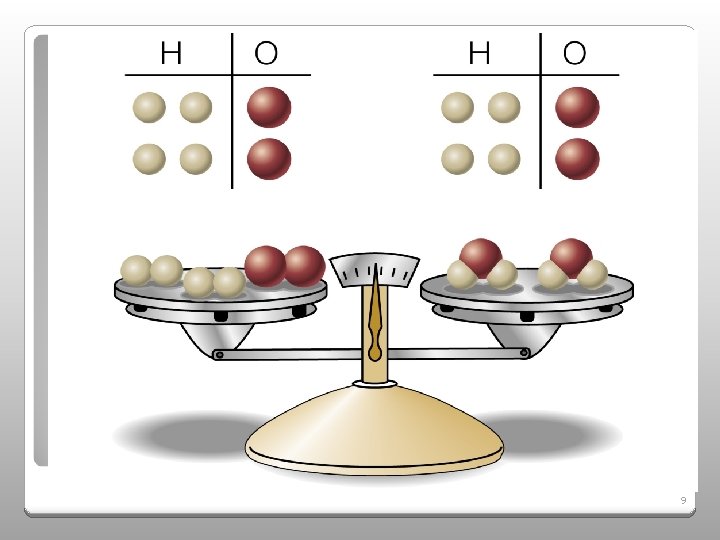
Cada ecuación indica las proporciones de masa y el no. de partículas. La masa total de los reactivos es igual a la masa total de los productos. (Ley de conservación de masas). 7

Ejemplo REACTIVOS Y PRODUCTOS 8

9

Procedimiento Sugerido para balancear ecuaciones por tanteo. 1. Metales 2. No metales 3. Hidrógeno 4. Oxígeno Ejercicios. -Cuando sea necesario buscar mínimo común multiplo. -No empezar por el elemento que esté solo. -combustión: 1. C 2. H 3. O -Iones poliatómicos: como unidades individuales, cuando esté una sola vez de cada lado. 10

Clasificación de las reacciones A. Según la forma en que se combinan o descomponen los reactivos. Reacciones de Combustión: Los compuestos que contienen Carbono, Hidrógeno y Oxígeno arden con el aire (consumiendo Oxígeno) y forman CO 2 +H 2 O +energía. CH 4 + 2 O 2 CO 2 + 2 H 2 O + energìa 11

Reacciones de Combinación o Síntesis Cuando un elemento reacciona o se combina con otro elemento para formar un compuesto (se ha sintetizado una nueva sustancia). A +B N 2(g) +3 H 2 (g) AB 2 NH 3(g) 12

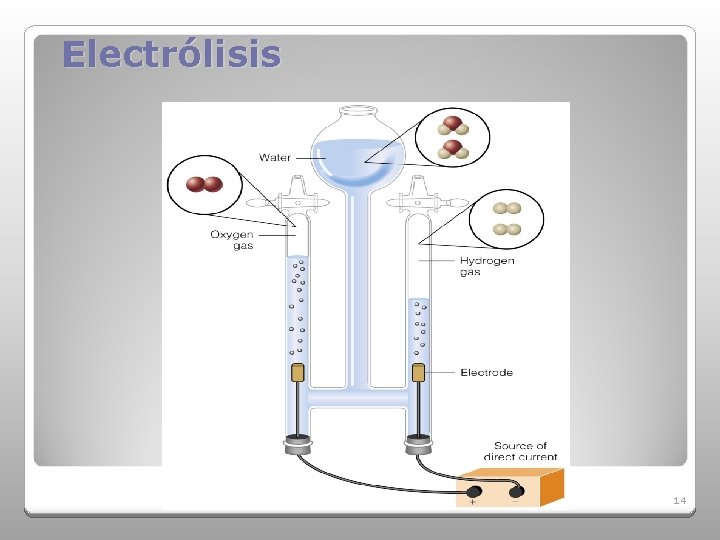
Reacciones de descomposición: Son aquellas en las que un solo compuesto simbolizado AB se descompone en dos o más sustancias sencillas. AB 2 H 2 O(l) A + B 2 H 2(g) + O 2(g) (electrólisis) 13

Electrólisis 14

• Reacciones de Simple sustitución o desplazamiento simple Un elemento simbolizado A, reacciona con un compuesto simbolizado BC, desplazando a otro elemento. A + BC AC + B A + BC AB + C Cu(s) + 2 Ag. NO 3 Cu(NO 3)2 +2 Ag (s) 15

• Reacciones de doble sustitución (metátesis) Se presentan cuando dos compuestos AB y CD, intercambian compañero para formar dos compuestos diferentes AC + BD Ej. AB + CD AD + BC H 2 SO 4 + Na 2 S H 2 S(g) + Na 2 SO 4 16

Neutralización: es una reacción de doble sustitución. Acido + Base HCl(ac)+ Na. OH(ac) Sal + Agua Na. Cl(ac) + H 2 O(l) La reacción de neutralización es la reacción de Iones H+ con los iones OH para formar moléculas covalentes estables de agua. 17

B. Reacciones clasificadas por el flujo de calor: Exotérmicas: la reacción desprende calor al ambiente. Combustión de Metano. Aumenta la temperatura del ambiente + (Entalpía) Ej. CH 4(g) +2 O 2(g) CO 2(g) + H 2 O(g)+ Calor 18

Endotérmicas: El sistema reaccionante absorbe el calor del ambiente. Ej. Fusión del Hielo Aplicación de calor al efectuar la reacción. 19

C. Clasificación de acuerdo al sentido de la Reacción a. Reversible: es aquella que puede llevarse a cabo en uno y otro sentido. Se dice que las reacciones están en equilibrio. A+ B AB 20

b. Irreversible: es aquella reacción química que puede llevarse a cabo en un solo sentido. Ej. A B 21

NÚMERO DE OXIDACIÓN También llamado Estado de Oxidación. Es el NÚMERO que se asigna a cada tipo de átomo o ión o a un elemento con base a un conjunto de reglas. El NÚMERO De Oxidación representa el NÚMERO de electrones que la especie gana, pierde o comparte. Iones monoatómicos: Na+ Mg+2 Cl Iones poliatómicos: 22

Reglas para asignar número de Oxidación 1. Todo elemento no combinado o unido consigo mismo, se le asigna número de oxidación de cero. Ej. K, Fe, H 2, O 2. 2. El H cuando se encuentra combinado se le asigna +1, a excepción de los hidruros (Metal + H) se le asigna -1. 23

3. Al O combinado se le asigna -2, exceptuando peróxidos, se le asigna -1. 4. Los metales de familias A al combinarse presentan principalmente: IA +1 IIA +2 IIIA +3(excepto Ta +1 y+3). 5. La suma de los numeros de oxidación debe ser cero para un compuesto. (Se asigna # oxidación positivo al elemento menos electronegativo y negativo al mas electronegativo. Ej. de cargas totales. 24

6. Para partículas iónicas: a. Monoatómicas: el número de oxidación es igual a su carga. b. Iones poliatómicos: la suma de los números de oxidación debe ser igual a la carga del ión. Ejercicios: K 2 Cr 2 O 7 Cl. O 325

26