Sesin 11 EL COCIENTE ARBITRARIO DE REACCIN Qc

Sesión 11 • EL COCIENTE ARBITRARIO DE REACCIÓN (Qc y Qp) • EL PRINCIPIO DE LE CHATELIER-BRAUN “Porque después de todo he comprobado que no se goza bien de lo gozado sino después de haberlo padecido” Francisco Ruiz Bernárdez, Poeta argentino

2 Objetivos: l Identificar los factores que afectan al equilibrio químico y cómo lo afectan. l Utilizar el Principio de Le Chatêlier y el concepto de cociente arbitrario de reacción, para realizar predicciones cualitativas acerca del desplazamiento del equilibrio como respuesta a efectos perturbadores de dicho equilibrio.
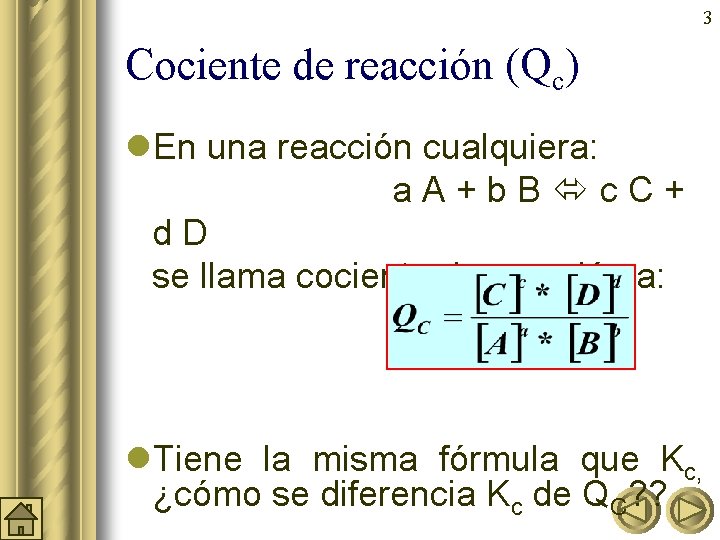
3 Cociente de reacción (Qc) l. En una reacción cualquiera: a. A+b. B c. C+ d. D se llama cociente de reacción a: l. Tiene la misma fórmula que Kc, ¿cómo se diferencia Kc de QC? ?

Cociente de reacción (QC) l Si QC = Kc entonces el sistema está en equilibrio. l Si QC < Kc el sistema evolucionará hacia la derecha, es decir, aumentarán las concentraciones de los productos y disminuirán las de los reactivos hasta que QC se iguale con Kc. l Si QC > Kc el sistema evolucionará hacia la izquierda, es decir, aumentarán las concentraciones de los reactivos y disminuirán las de los productos hasta que QC se iguale con Kc 4

5 Cociente de reacción (QP) l. En una reacción cualquiera: a. A+b. B c. C+ d. D se llama cociente de reacción a: Al igual que en KP en el cálculo de este cociente sólo se toman en

Cociente de reacción (QP) l Si QP = KP entonces el sistema está en equilibrio. l Si QP < KP el sistema evolucionará hacia la derecha, es decir, aumentarán las presiones parciales de los productos y disminuirán las de los reactivos hasta que QP se iguale con KP. l Si QP > KP el sistema evolucionará hacia la izquierda, es decir, aumentarán las presiones parciales de los reactivos y disminuirán las de los productos hasta que QP se iguale con KP 6

Ejemplo: En un recipiente de 3 litros se introducen 7 0. 6 moles de HI, 0. 3 moles de H 2 y 0. 3 moles de I 2 a 490ºC. Si Kc = 0. 022 a 490ºC para 2 HI(g) H 2(g) + I 2(g) a) ¿se encuentra en equilibrio? ; b) En caso que no, ¿cuántos moles de HI, H 2 e I 2 habrá en el equilibrio? a) [H 2] · [I 2] Q = —————— = 2 [HI] 0. 3/3 · 0. 3/3 —————— = 0. 25 2 (0. 6/3) Como Q > Kc el sistema no se encuentra en equilibrio y la reacción se desplazará hacia la izquierda. b) Al plantear el eq. y resolver la ec. resultante se obtiene: ξ = -0. 163 ó x = -0. 054 n. HI = 0. 926 y n. H = n. I = 0. 137

Modificaciones del equilibrio l Si un sistema se encuentra en equilibrio (Q = K) y se produce una perturbación: – Cambio en la concentración de alguno de los reactivos o productos. – Cambio en la presión (o volumen) – Cambio en la temperatura. El sistema deja de estar en equilibrio y trata de volver a él. 8

9 Cambio en la concentración de alguno de los reactivos o productos. l. Si, una vez establecido un equilibrio, cambia la presión o concentración de algún reactivo o producto, el equilibrio se rompe y se tiende hacia un nuevo equilibrio.

10 Cambio en la presión (o volumen) l Al ↑ “P” (o ↓ V) aumenta la concentración y eso lleva consigo un cambio en “ξ”, es decir, el equilibrio se desplaza hacia donde haya menos moles de gas. l Lógicamente, si la presión disminuye, el efecto es el contrario. l Si el número de moles de gas es igual ¿Qué pasará?

11 Cambio en la temperatura. l Se observa que, al aumentar T el sistema se desplaza hacia donde se consuma calor, es decir, hacia la izquierda en las reacciones exotérmicas y hacia la derecha en las endotérmicas. l Si disminuye T el sistema se desplaza hacia donde se desprenda calor (derecha en las exotérmicas e izquierda en las endotérmicas).

12 Principio de Le Chatelier l “Un cambio o perturbación en cualquiera de las variables que determinan el estado de equilibrio químico, produce un desplazamiento del equilibrio en el sentido de contrarrestar o minimizar el efecto causado por la perturbación”.

IM Variaciones en el equilibrio PO MU Y RT Variación en el equilibrio AN l [reactivos] > 0 TE l [reactivos] < 0 l [productos] > 0 l [productos] < 0 l T > 0 (exotérmicas) l T > 0 (endotérmicas) l T < 0 (exotérmicas) l T < 0 (endotérmicas) l P > 0 Hacia donde hay menor nº de moles estequiométricos de gas. l P < 0 Hacia donde hay más nº de moles estequiométricos de gas. 13
- Slides: 13