Propojen metabolickch drah Jana varcov Alice Skoumalov Vznamn

Propojení metabolických drah Jana Švarcová Alice Skoumalová

Významné metabolické dráhy z hlediska integrace metabolismu: ü Syntéza a degradace glykogenu ü Glykolýza ü Glukoneogeneze ü Syntéza a oxidace MK ü Lipogeneze, lipolýza ü Syntéza a degradace proteinů ü Močovinový cyklus Kde probíhají Kdy probíhají Jak jsou kontrolovány ?
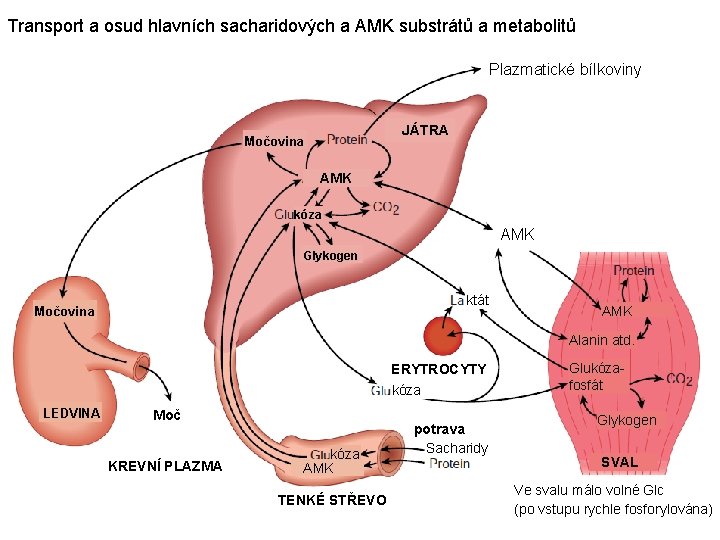
Transport a osud hlavních sacharidových a AMK substrátů a metabolitů Plazmatické bílkoviny JÁTRA Močovina AMK kóza AMK Glykogen ktát Močovina AMK Alanin atd. ERYTROCYTY kóza LEDVINA Moč KREVNÍ PLAZMA kóza AMK TENKÉ STŘEVO potrava Sacharidy Glukózafosfát Glykogen SVAL Ve svalu málo volné Glc (po vstupu rychle fosforylována)

Metabolické stavy 1. Resorpční fáze ü po dobu vstřebávání živin z GIT (~ 2 h) glukóza je hlavní energetický zdroj 2. Postresorpční fáze ü mezi jídly (~ 2 h po jídle - do dalšího jídla) mastné kyseliny jsou hlavní energetický zdroj 3. Hladovění ü více než 3 dny mozek začne metabolizovat ketolátky
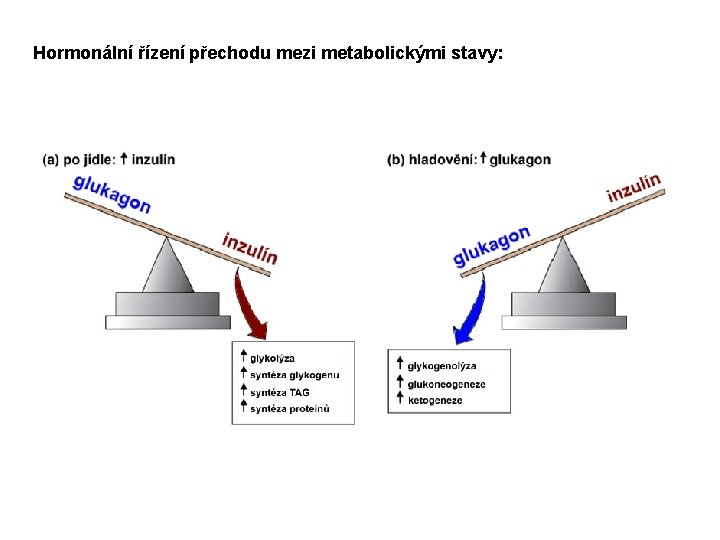
Hormonální řízení přechodu mezi metabolickými stavy:

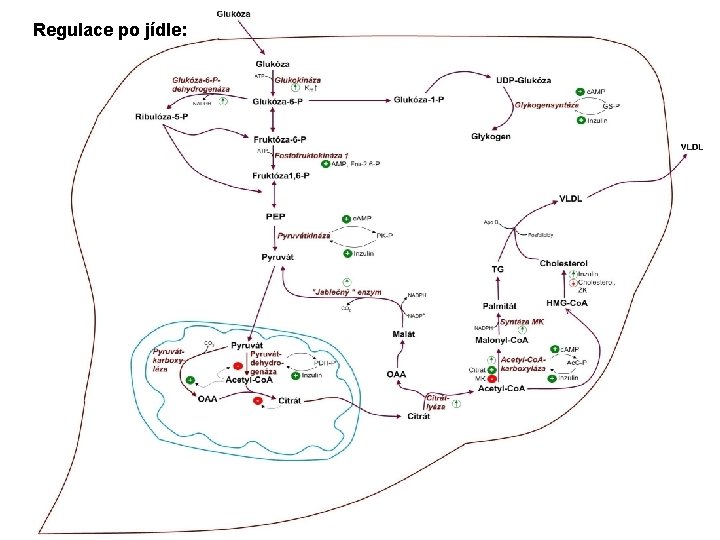
Regulace po jídle:
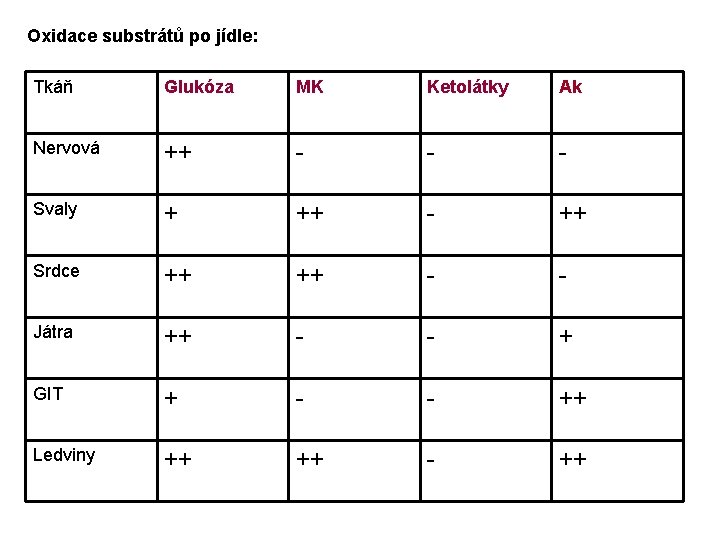
Oxidace substrátů po jídle: Tkáň Glukóza MK Ketolátky Ak Nervová ++ - - - Svaly + ++ - ++ Srdce ++ ++ - - Játra ++ - - + GIT + - - ++ Ledviny ++ ++ - ++

Resorpční fáze: ü vstřebání glukózy a aminokyselin do portální cirkulace ü vstřebání triacylglycerolů v chylomikronech do systémové cirkulace ü zvýšení koncentrace glukózy v portální krvi pankreas: jaterní tkáň: zvýšená sekrece inzulínu, snížená sekrece glukagonu syntéza jaterního glykogenu syntéza triacylglycerolů syntéza proteinů svalová tkáň: syntéza svalového glykogenu syntéza proteinů tuková tkáň: syntéza triacylglycerolů ukládání triacylglycerolů z chylomikronů

Resorpční fáze: 1 oxidace živin z potravy: ü oxidace glukózy, mastných kyselin, aminokyselin ZISK ENERGIE ü konečné produkty metabolické přeměny živin: 2 tvorba zásob: ü syntéza glykogenu (játra, svaly) ü syntéza triacylglycerolů (tuková tkáň) ü syntéza proteinů (játra, kosterní svaly) CO 2, H 2 O, ATP, močovina

Klinická korelace 56 letý pacient s váhou 120 kg při výšce 175 cm - BMI 39, 18, centrální typ obezity - nízká fyzická aktivita, zadýchává se - zvýšený krevní tlak Diagnóza: Obezita Laboratorní vyšetření: celkový cholesterol ↑ Rodinná anamnéza: hypercholesterolémie, AIM Rizika: metabolický syndrom, kardiovaskulární choroby, DM typ II Terapie: redukce váhy
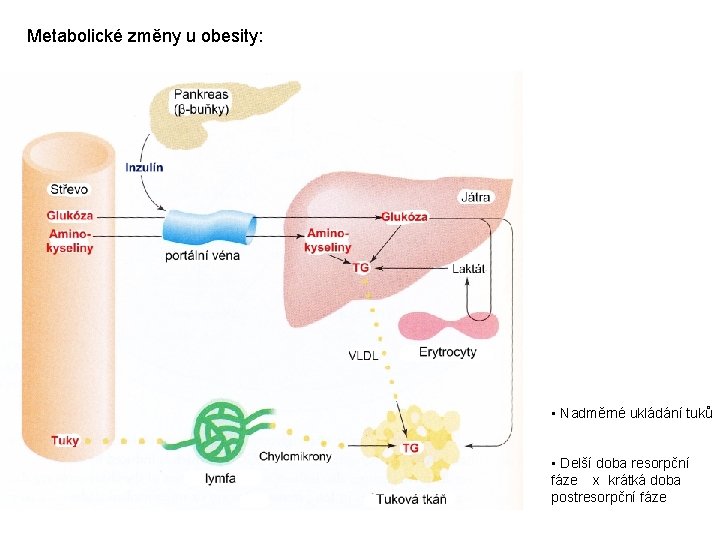
Metabolické změny u obesity: • Nadměrné ukládání tuků • Delší doba resorpční fáze x krátká doba postresorpční fáze

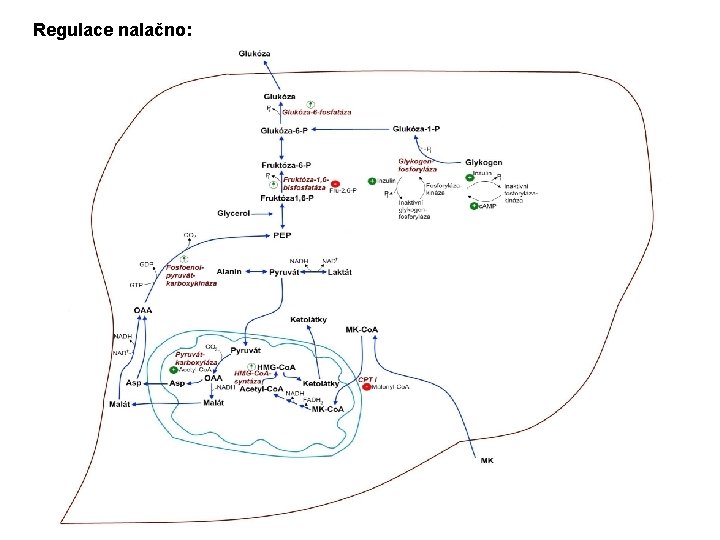
Regulace nalačno:

Postresorpční fáze: pankreas: snížená sekrece inzulínu, zvýšená sekrece glukagonu Tuková tkáň – hlavní zdroj energie během hladovění (TAG – adipocyty) A) aktivace lipolýzy v tukové tkáni ü uvolnění mastných kyselin a glycerolu ü stoupající hladina volných mastných kyselin v plazmě ü využití mastných kyselin jako energetického substrátu šetření glukózy (zejména srdce a kosterní svaly) ü zvýšení hladiny volných mastných kyselin v játrech syntéza ketolátek (energie pro srdce, svaly, ledviny) B) aktivace glukoneogeneze ü syntéza glukózy de novo (játra, ledviny) ü zajištění zásobení mozkové tkáně glukózou

Postresorpční fáze: 1 oxidace substrátů ze zásob: ü glukózy (tkáně závislé na glukóze) ü mastných kyselin (svaly, játra) !!! NELZE syntetizovat Glc z MK ü ketolátek (svaly, ledviny): tvorba ketolátek z mastných kyselin uvolněných z triacylglycerolů 2 homeostáza glukózy: ü degradace jaterního glykogenu ü glukoneogeneze 3 degradace proteinů a syntéza močoviny
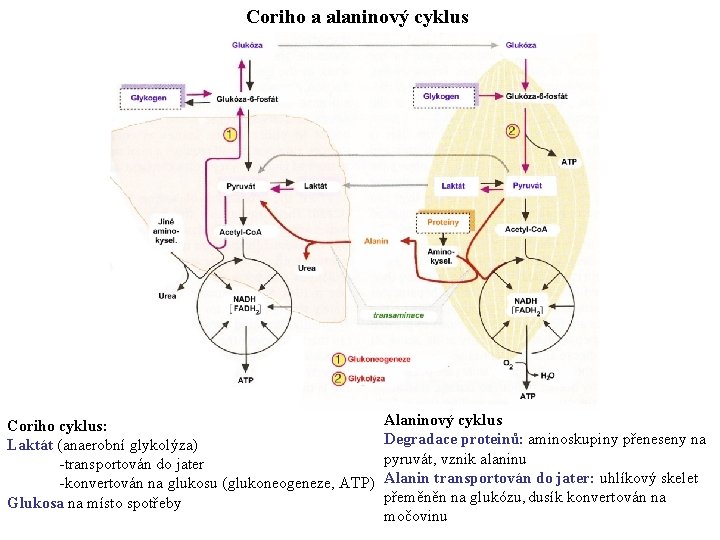
Coriho a alaninový cyklus Coriho cyklus: Laktát (anaerobní glykolýza) -transportován do jater -konvertován na glukosu (glukoneogeneze, ATP) Glukosa na místo spotřeby Alaninový cyklus Degradace proteinů: aminoskupiny přeneseny na pyruvát, vznik alaninu Alanin transportován do jater: uhlíkový skelet přeměněn na glukózu, dusík konvertován na močovinu
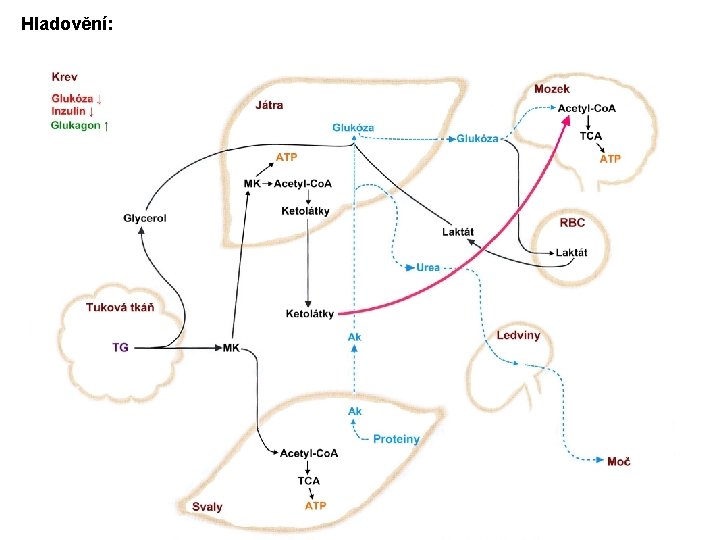
Hladovění:

Hladovění: pankreas: snížená sekrece inzulínu, zvýšená sekrece glukagonu A) svaly sníží oxidaci ketolátek ⇒ zdrojem energie jsou MK ü játra – stále vysoký stupeň oxidace MK → zvýší se koncentrace ketolátek v krvi ü mozek začne oxidovat ketolátky B) snížení glukoneogeneze z proteinů šetření glukózy (energie pro RBC) šetření proteiny ü snížená produkce močoviny ( jaterní glykogen vyčerpán ∼ 30 hodin lačnění ⇒ glukoneogeneze jediný proces dostupnosti Glc) ⇒ pool AMK (rozklad proteinů) – hlavní zdroj uhlíků pro glukoneogenezi
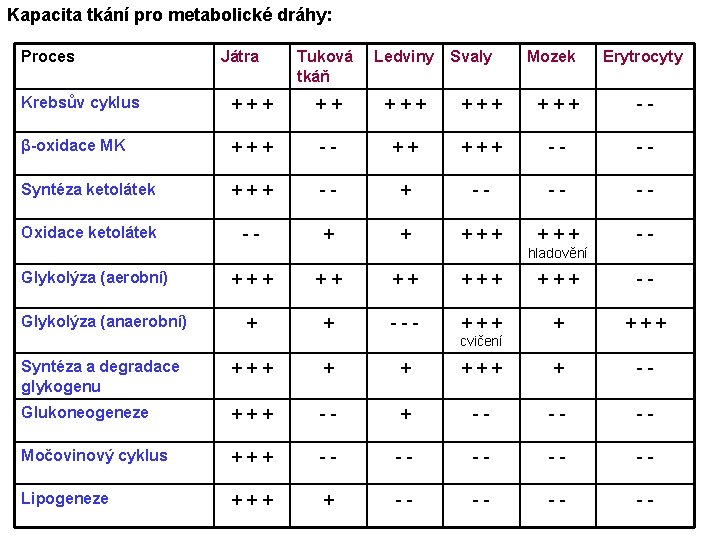
Kapacita tkání pro metabolické dráhy: Proces Játra Tuková tkáň Ledviny Svaly Mozek Erytrocyty Krebsův cyklus +++ +++ +++ -- β-oxidace MK +++ -- ++ +++ -- -- Syntéza ketolátek +++ -- -- -- Oxidace ketolátek -- + + +++ -- hladovění Glykolýza (aerobní) Glykolýza (anaerobní) +++ +++ -- + + --- +++ + +++ cvičení Syntéza a degradace glykogenu +++ + + +++ + -- Glukoneogeneze +++ -- -- -- Močovinový cyklus +++ -- -- -- Lipogeneze +++ + -- --
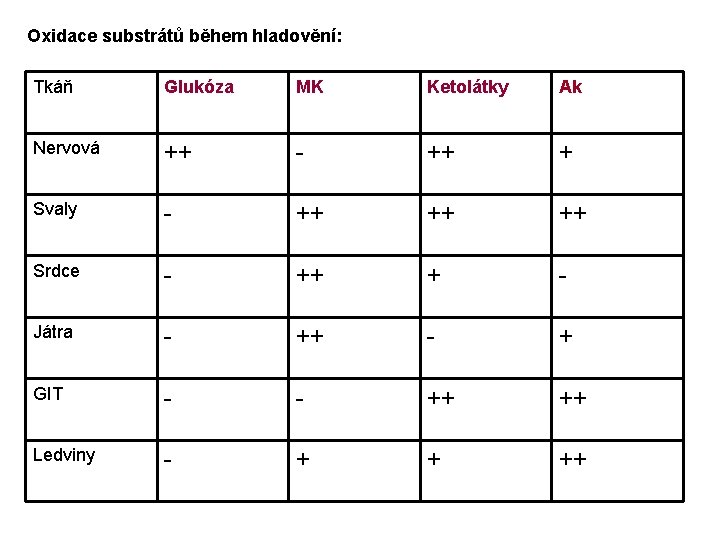
Oxidace substrátů během hladovění: Tkáň Glukóza MK Ketolátky Ak Nervová ++ - ++ + Svaly - ++ ++ ++ Srdce - ++ + - Játra - ++ - + GIT - - ++ ++ Ledviny - + + ++
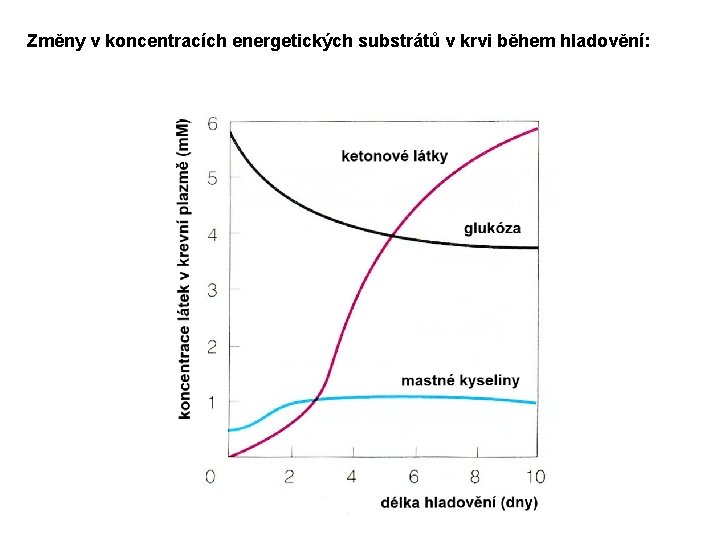
Změny v koncentracích energetických substrátů v krvi během hladovění:

Klinická korelace 23 letá pacientka s 40 kg při výšce 175 cm s potřebou dále hubnout - BMI 13, 06 - stále unavená - 5 měsíců amenorhea Diagnóza: Mentální anorexie Hospitalizace (snížená teplota, puls a tlak) Laboratorní vyšetření: krev glukóza 3, 6 mmol/l ketolátky 4200 μM/l (norma 70) moč Terapie: výživa, psychiatr ketolátky
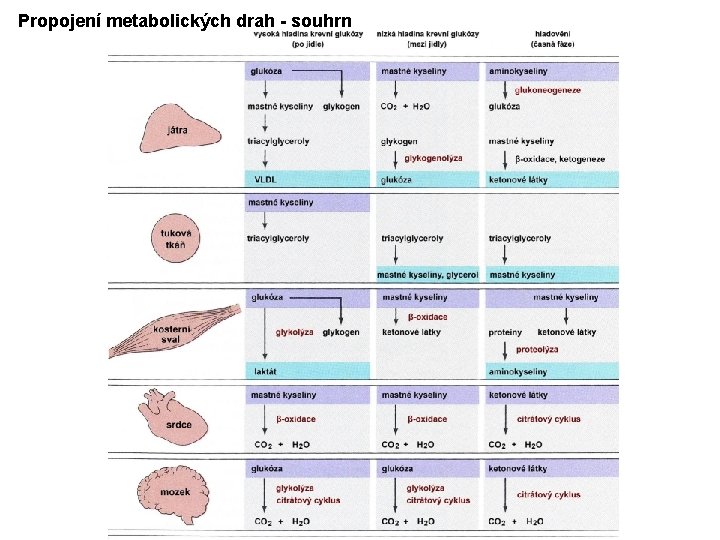
Propojení metabolických drah - souhrn
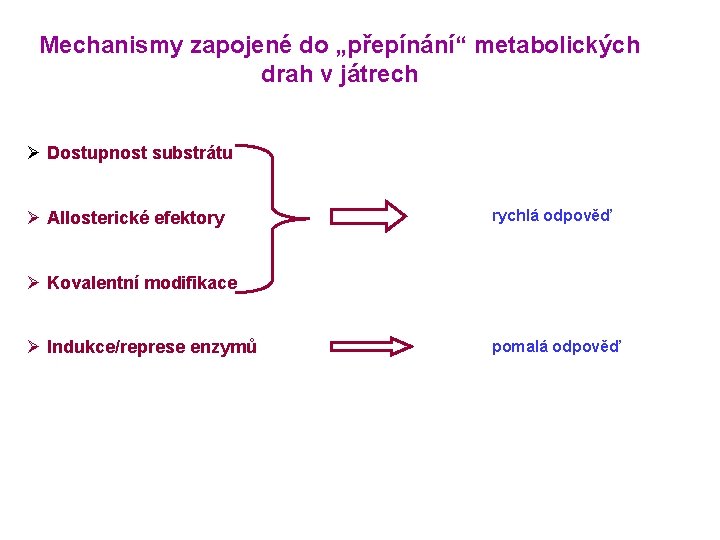
Mechanismy zapojené do „přepínání“ metabolických drah v játrech Ø Dostupnost substrátu Ø Allosterické efektory rychlá odpověď Ø Kovalentní modifikace Ø Indukce/represe enzymů pomalá odpověď
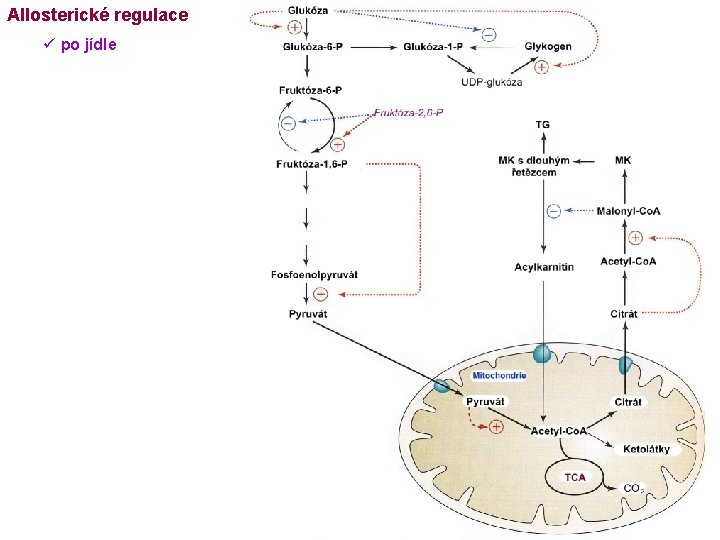
Allosterické regulace ü po jídle
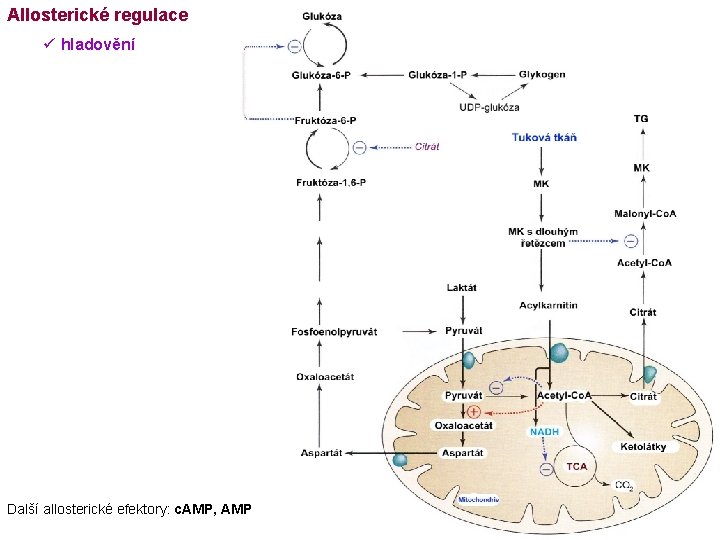
Allosterické regulace ü hladovění Další allosterické efektory: c. AMP, AMP
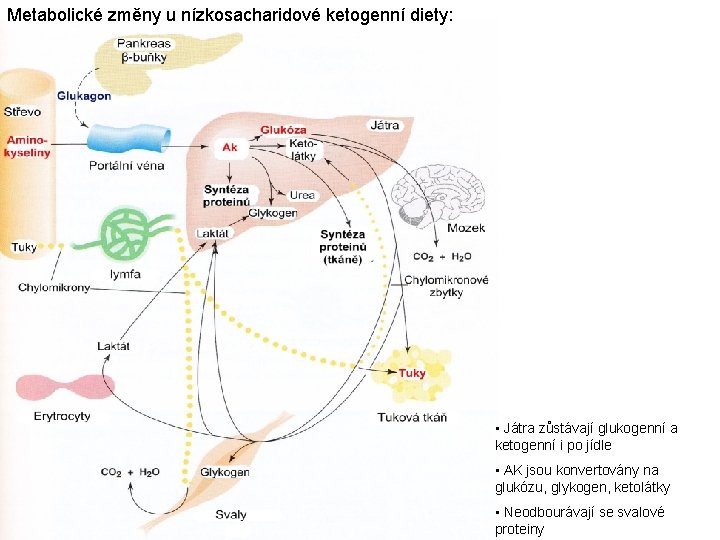
Metabolické změny u nízkosacharidové ketogenní diety: • Játra zůstávají glukogenní a ketogenní i po jídle • AK jsou konvertovány na glukózu, glykogen, ketolátky • Neodbourávají se svalové proteiny
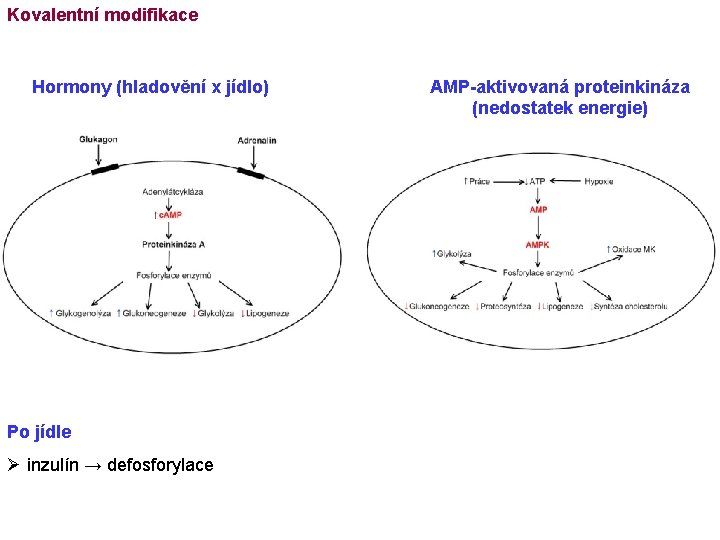
Kovalentní modifikace Hormony (hladovění x jídlo) Po jídle Ø inzulín → defosforylace AMP-aktivovaná proteinkináza (nedostatek energie)
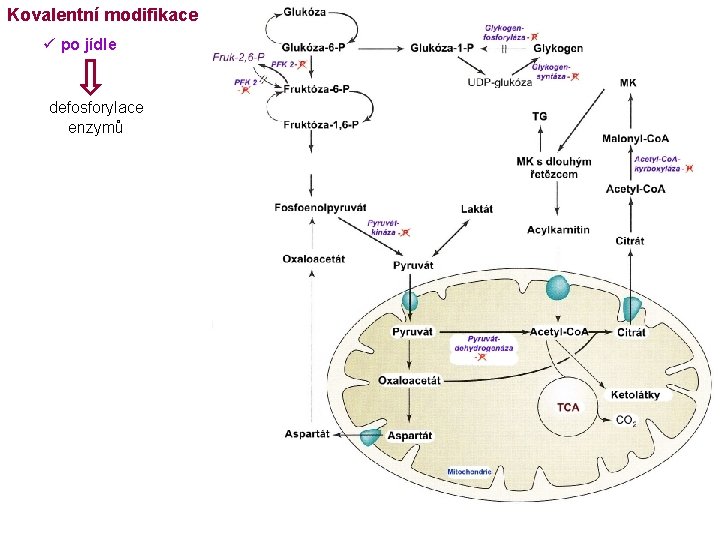
Kovalentní modifikace ü po jídle defosforylace enzymů
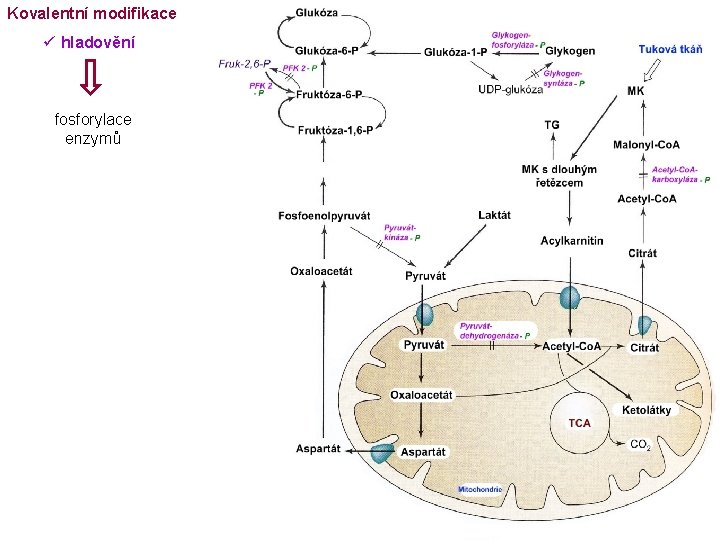
Kovalentní modifikace ü hladovění fosforylace enzymů
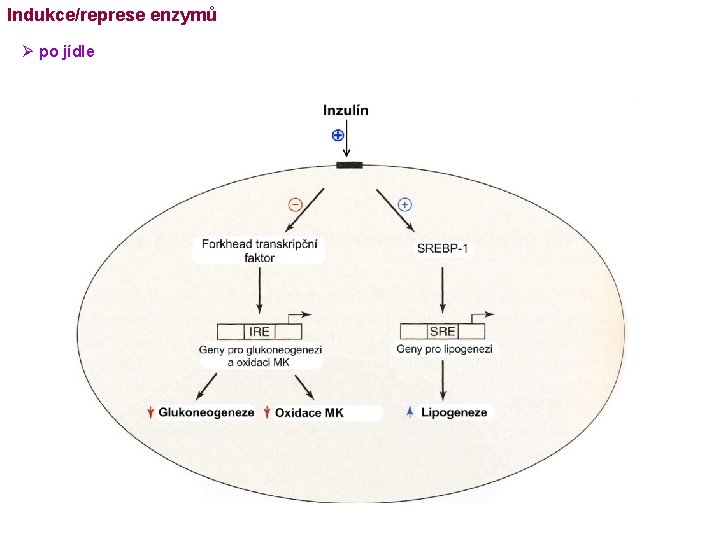
Indukce/represe enzymů Ø po jídle
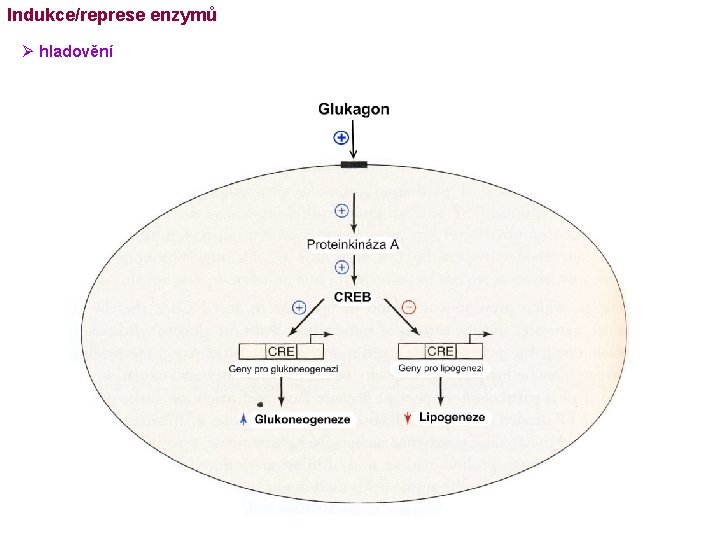
Indukce/represe enzymů Ø hladovění
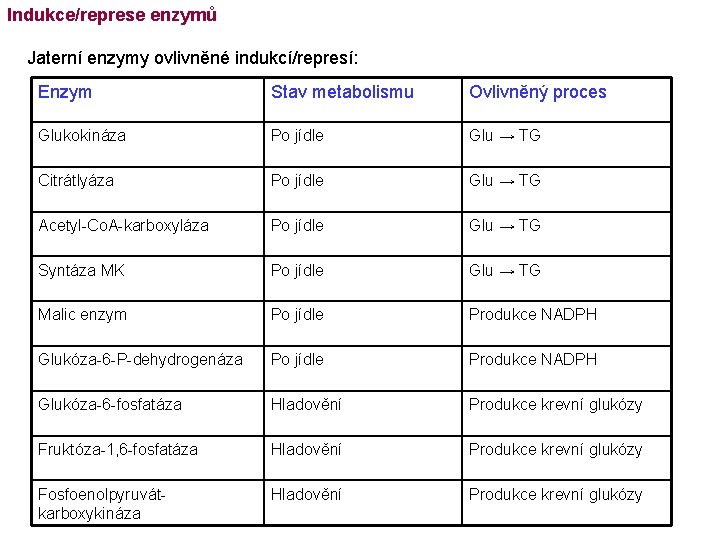
Indukce/represe enzymů Jaterní enzymy ovlivněné indukcí/represí: Enzym Stav metabolismu Ovlivněný proces Glukokináza Po jídle Glu → TG Citrátlyáza Po jídle Glu → TG Acetyl-Co. A-karboxyláza Po jídle Glu → TG Syntáza MK Po jídle Glu → TG Malic enzym Po jídle Produkce NADPH Glukóza-6 -P-dehydrogenáza Po jídle Produkce NADPH Glukóza-6 -fosfatáza Hladovění Produkce krevní glukózy Fruktóza-1, 6 -fosfatáza Hladovění Produkce krevní glukózy Fosfoenolpyruvátkarboxykináza Hladovění Produkce krevní glukózy
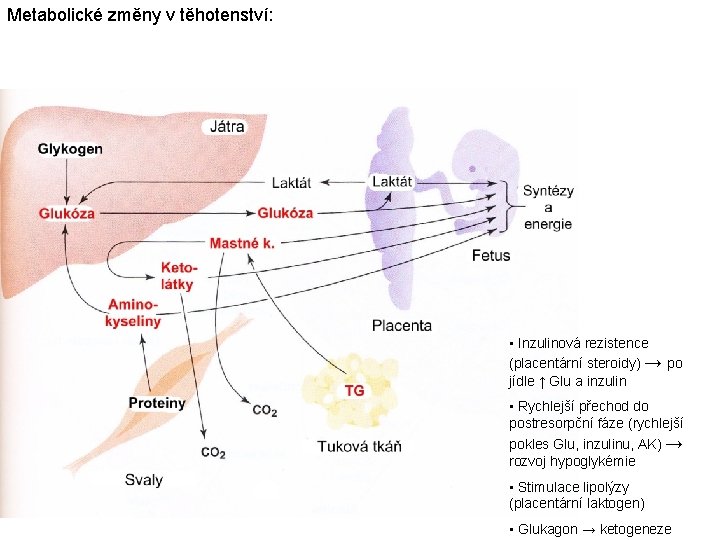
Metabolické změny v těhotenství: • Inzulinová rezistence (placentární steroidy) → po jídle ↑ Glu a inzulin • Rychlejší přechod do postresorpční fáze (rychlejší pokles Glu, inzulinu, AK) → rozvoj hypoglykémie • Stimulace lipolýzy (placentární laktogen) • Glukagon → ketogeneze
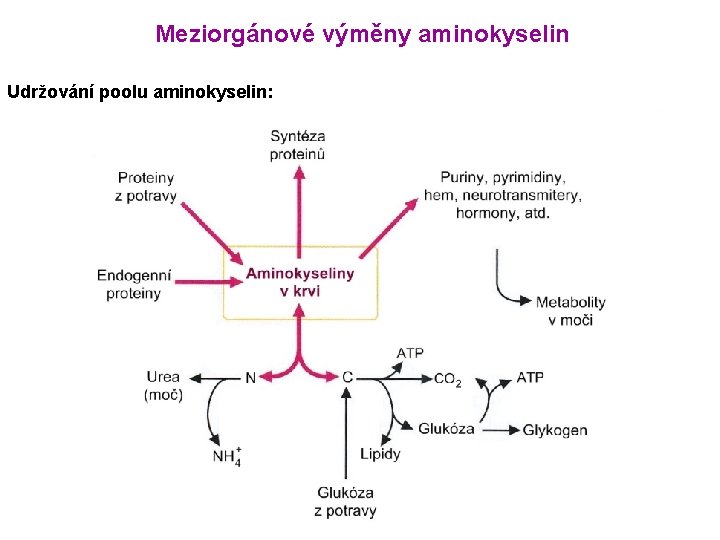
Meziorgánové výměny aminokyselin Udržování poolu aminokyselin:
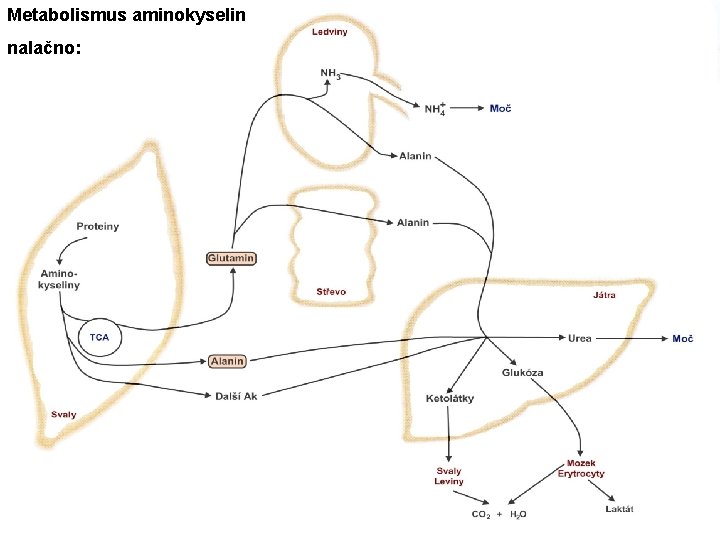
Metabolismus aminokyselin nalačno:
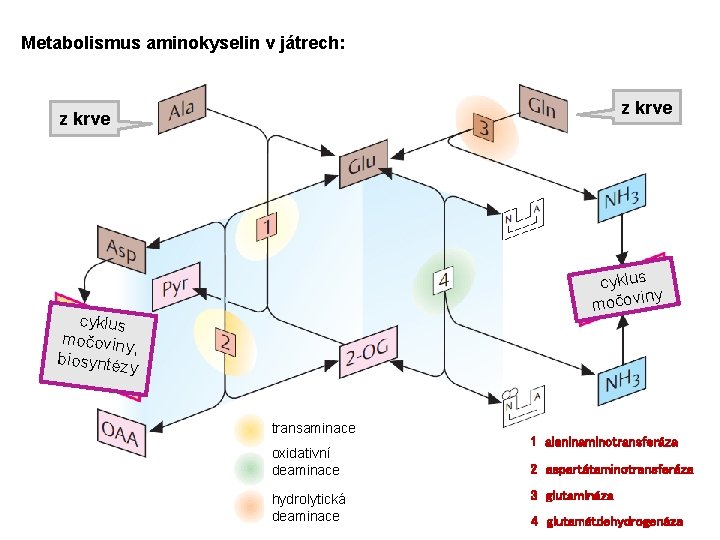
Metabolismus aminokyselin v játrech: z krve cyklus iny močov cyklus močoviny , biosyntéz y transaminace oxidativní deaminace hydrolytická deaminace 1 alaninaminotransferáza 2 aspartátaminotransferáza 3 glutamináza 4 glutamátdehydrogenáza
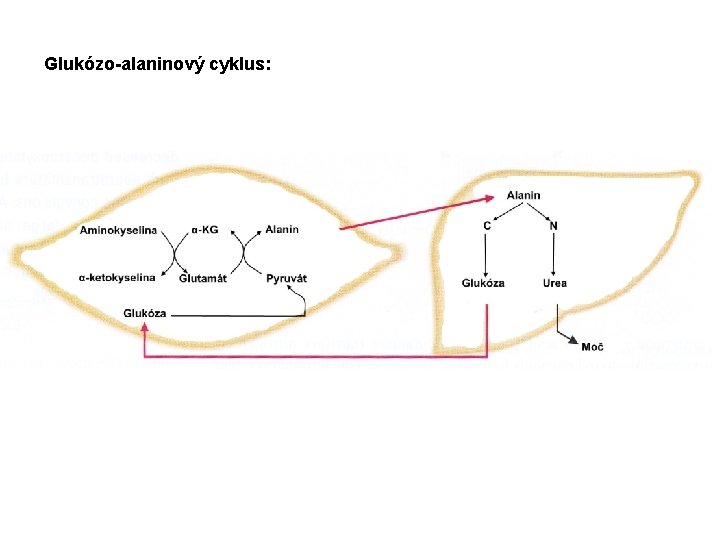
Glukózo-alaninový cyklus:
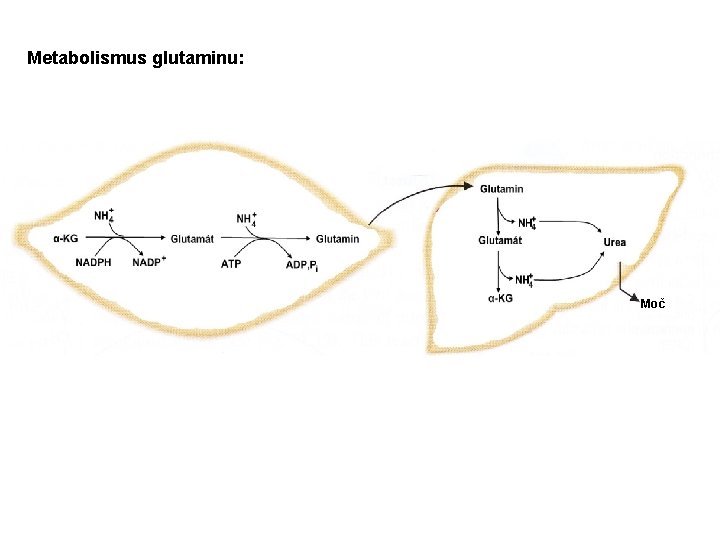
Metabolismus glutaminu: Moč
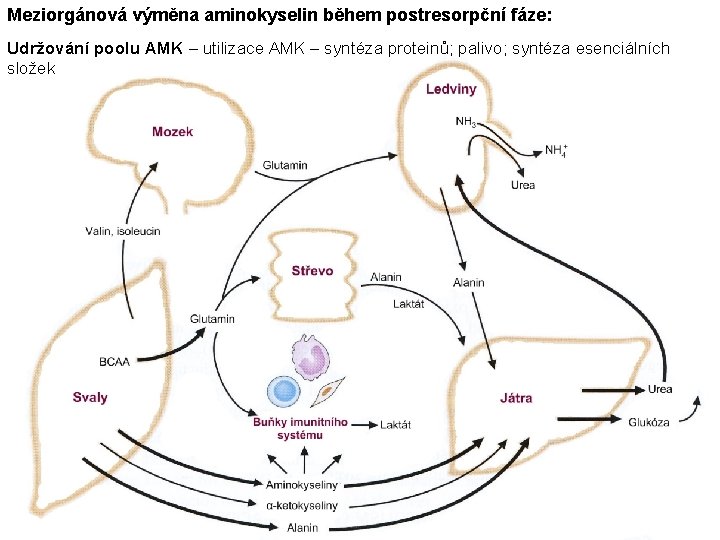
Meziorgánová výměna aminokyselin během postresorpční fáze: Udržování poolu AMK – utilizace AMK – syntéza proteinů; palivo; syntéza esenciálních složek
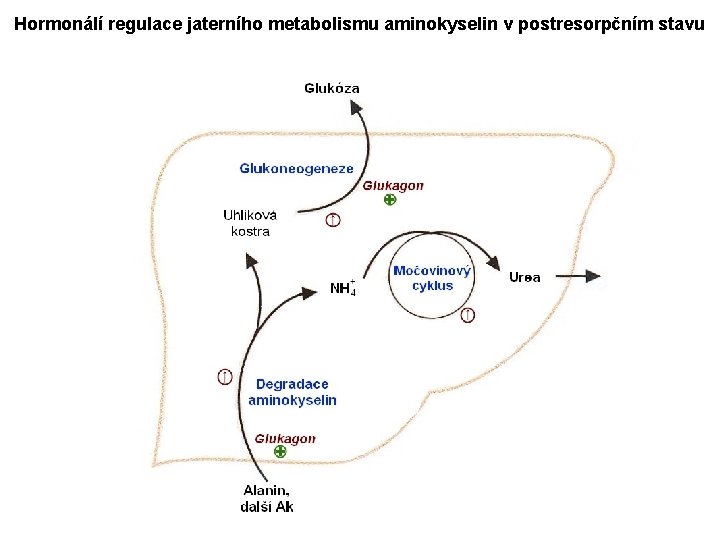
Hormonálí regulace jaterního metabolismu aminokyselin v postresorpčním stavu

Principy řízení toku aminokyselin mezi tkáněmi: ü NH 3 je toxické → alanin, glutamin ü Glutaminový pool • exkrece protonů (NH 4+) • živina (střevo, ledviny, buňky imunitního systému) • zdroj dusíku pro biosyntetické reakce (buňky imunitního systému) • transport glutamátu v mozku ü BCAA (valin, leucin, isoleucin) → konverze na meziprodukty TCA (většina tkání) ü Aminokyseliny jsou hlavní substráty pro glukoneogenezi ü Turnover proteinů determinuje velikost poolu aminokyselin

Funkce glutaminu: Zdroj energie (střevo, ledviny, imunitní systém) Proteosyntéza Exkrece protonů Donor dusíku pro syntézu purinů, pyrimidinů, NAD+, aminocukrů, asparaginu Donor glutamátu pro syntézu glutationu, GABA, ornitinu, argininu, prolinu

Souhrn: ü Metabolismus „přepíná“ mezi více metabolickými stavy v závislosti na jídle Ø aby byl dostatek substrátů pro oxidace (i během hladovění) Ø aby organismus vydržel déle bez jídla (šetření proteiny) Ø řízeno hormonálně ü Mechanismy řízení „přepínání“ metabolismu (dostupnost substrátu, allostericky, fosforylací, množství enzymu) ü Změny v cyklu jídlo/hlad u různých metabolických stavů ü Různé orgány spolupracují ve vzájemných přeměnách aminokyselin

Schémata použitá v prezentaci: Marks´ Basic Medical Biochemistry, A Clinical Approach, third edition, 2009 (M. Lieberman, A. D. Marks) Textbook of Biochemistry with Clinical Correlations, sixth edition, 2006 (T. M. Devlin) Barevný atlas biochemie, překlad 4. vydání, 2009 (J. Koolman, K. H. Röhm)
- Slides: 46