LTALNOS KMIA elads altkemk 17 ea Eladk Szalay













































- Slides: 56

ÁLTALÁNOS KÉMIA előadás (altkemk 17 ea) Előadók: Szalay Péter, Szalay Roland, Tarczay György (ELTE, Szervetlen Kémiai Tanszék) Egyetemi honlap: www. elte. hu Intézeti honlap: www. chem. elte. hu




























Viszontlátásra a kémiai folyamatok energetikájának tárgyalásánál!

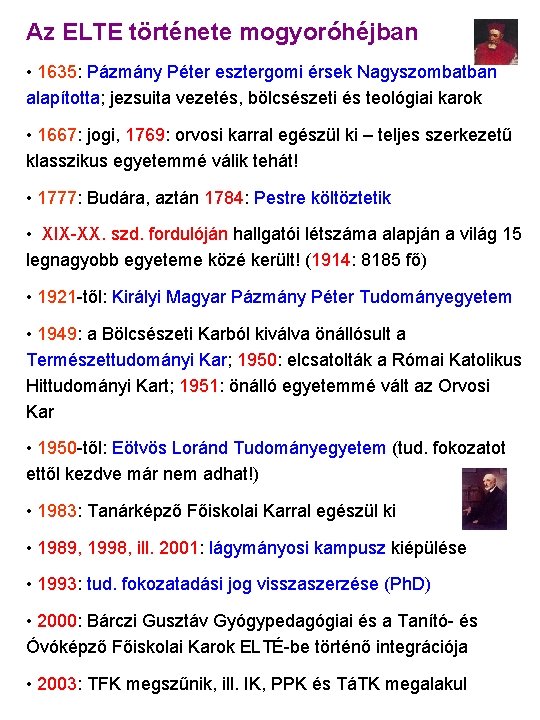
Az ELTE története mogyoróhéjban • 1635: Pázmány Péter esztergomi érsek Nagyszombatban alapította; jezsuita vezetés, bölcsészeti és teológiai karok • 1667: jogi, 1769: orvosi karral egészül ki – teljes szerkezetű klasszikus egyetemmé válik tehát! • 1777: Budára, aztán 1784: Pestre költöztetik • XIX-XX. szd. fordulóján hallgatói létszáma alapján a világ 15 legnagyobb egyeteme közé került! (1914: 8185 fő) • 1921 -től: Királyi Magyar Pázmány Péter Tudományegyetem • 1949: a Bölcsészeti Karból kiválva önállósult a Természettudományi Kar; 1950: elcsatolták a Római Katolikus Hittudományi Kart; 1951: önálló egyetemmé vált az Orvosi Kar • 1950 -től: Eötvös Loránd Tudományegyetem (tud. fokozatot ettől kezdve már nem adhat!) • 1983: Tanárképző Főiskolai Karral egészül ki • 1989, 1998, ill. 2001: lágymányosi kampusz kiépülése • 1993: tud. fokozatadási jog visszaszerzése (Ph. D) • 2000: Bárczi Gusztáv Gyógypedagógiai és a Tanító- és Óvóképző Főiskolai Karok ELTÉ-be történő integrációja • 2003: TFK megszűnik, ill. IK, PPK és TáTK megalakul

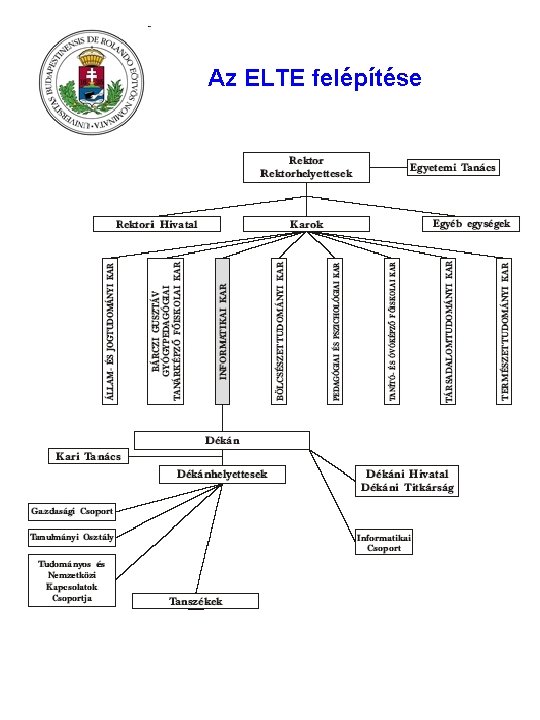
Az ELTE felépítése







unesdoc. unesco. org/images/000829/082946 eb. pdf




Bóna Ervin: A kémiai tudományok és kutatási ágak rendszerezési kérdései (Akadémiai Kiadó, 1971) Terjedelem: 115 p. ; 25 cm ETO jelzet: 54: 168. 521 Ár: 30 Ft







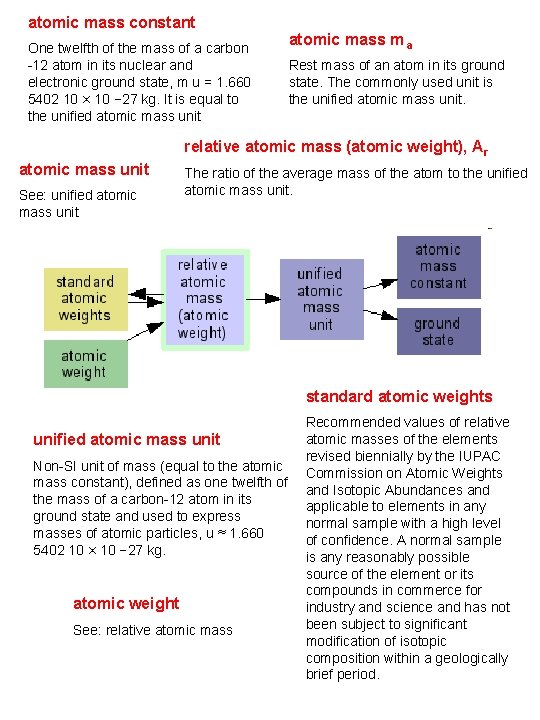
atomic mass constant One twelfth of the mass of a carbon -12 atom in its nuclear and electronic ground state, m u = 1. 660 5402 10 × 10 − 27 kg. It is equal to the unified atomic mass unit atomic mass m a Rest mass of an atom in its ground state. The commonly used unit is the unified atomic mass unit. relative atomic mass (atomic weight), Ar atomic mass unit See: unified atomic mass unit The ratio of the average mass of the atom to the unified atomic mass unit. standard atomic weights unified atomic mass unit Non-SI unit of mass (equal to the atomic mass constant), defined as one twelfth of the mass of a carbon-12 atom in its ground state and used to express masses of atomic particles, u ≈ 1. 660 5402 10 × 10 − 27 kg. atomic weight See: relative atomic mass Recommended values of relative atomic masses of the elements revised biennially by the IUPAC Commission on Atomic Weights and Isotopic Abundances and applicable to elements in any normal sample with a high level of confidence. A normal sample is any reasonably possible source of the element or its compounds in commerce for industry and science and has not been subject to significant modification of isotopic composition within a geologically brief period.

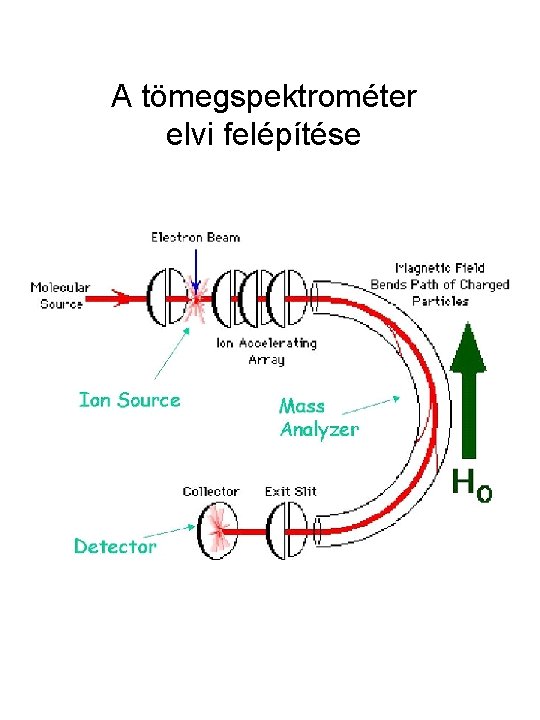
A tömegspektrométer elvi felépítése

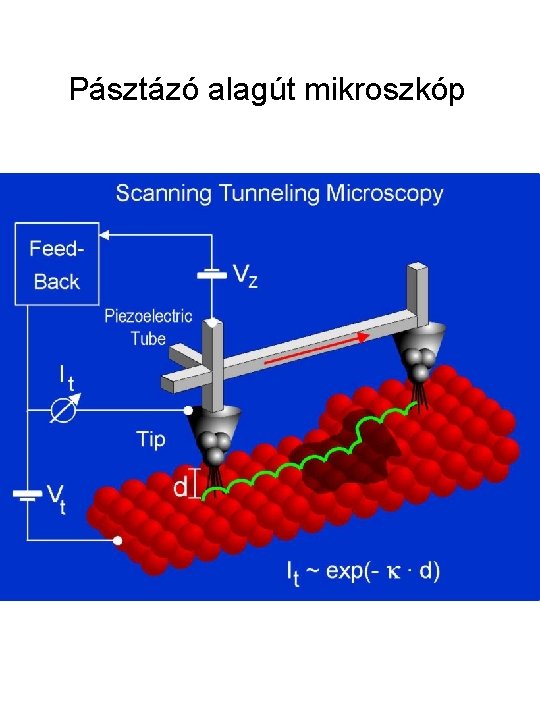
Pásztázó alagút mikroszkóp

Xenonatom-írás Ni-felületen

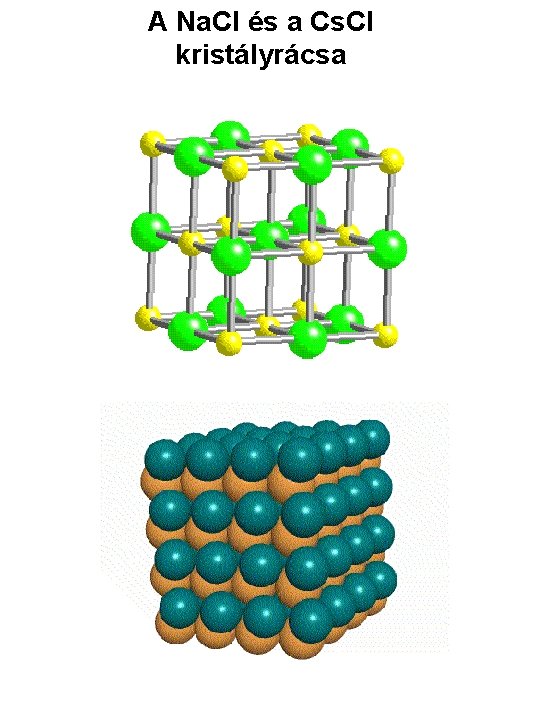
A Na. Cl és a Cs. Cl kristályrácsa

http: //www. kfki. hu/~cheminfo/hun/eloado/egyenlet/egy. htm HOGYAN RENDEZZÜNK REAKCIÓEGYENLETEKET? Tóth Zoltán Tartalomjegyzék A reakcióegyenletek rendezése alapvetõ fontosságú mind a kémiai ismeretek megszerzése, mind azok alkalmazása szempontjából. A különbözõ típusú és bonyolultságú reakcióegyenletek rendezésének régóta ismertek általános módszerei, de a Journal of Chemical Education hasábjain ebben a témában évrõl-évre megjelenõ cikkek is jelzik, hogy azokat mindig lehet finomítani, alakítani. Az egyenletrendezési eljárások kutatásának kettõs célja van: egyrészt a már ismert módszerek finomításával, egyszerûsítésével, elemzésével segítséget nyújtani az egyenletrendezés különbözõ szinten történõ tanításához, másrészt a matematika és a számítástechnika eszközeinek felhasználásával a kémiai kutatás számára is hasznosítható eljárásokat fejleszteni ki. Amikor egy anyagi rendszerben kémiai reakció megy végbe, egy dologban biztosak lehetünk, hogy a különbözõ típusú atomok száma a reakció során nem változik meg. Az atomok megmaradásának törvényét a különbözõ alkotó elemekre felírt anyagmérleg-egyenletekkel fejezhetjük ki. Ezek megoldásaként kapjuk a rendezett reakcióegyenletben szereplõ sztöchiometriai együtthatókat. A reakcióegyenletek rendezésének általános módszere tehát, az anyagmérleg alapján történõ rendezés. A kémiai átalakulás lényegének kiemelésére szoktunk használni olyan reakcióegyenleteket is, amelyekben nem (vagy nemcsak) semleges részecskék (molekulák, esetleg atomok) szerepelnek, hanem töltéssel rendelkezõ részecskék (anionok, kationok, elektronok) is. Az ilyen egyenletek rendezésekor az anyagmérleg mellett figyelembe kell venni a töltésmegmaradás elvét leíró töltésmérleget is. A töltésmérleg figyelembevétele nem feltétlenül szükséges, de hasznos lehet a semleges részecskékbõl álló reakcióegyenletek rendezésekor is. Ilyenkor a töltésmegmaradás elvét az alkotó atomok névleges töltésére (oxidációs számára) írhatjuk fel. A bevezetõben már említettem, hogy a reakcióegyenletek rendezése alapvetõ fontosságú a kémiával foglalkozó diák és kutató számára, de azt látnunk kell, hogy a különbözõ egyenletrendezési módszerek (még ha olyan alapvetõ természeti törvényeken alapulnak is mint a tömegmegmaradás elve és a töltésmegmaradás elve) matematikai-logikai eljárások, és nem érdemes ezeknek különösebb kémiai jelentést tulajdonítani. Kémiai jelentése csak a rendezett reakcióegyenletnek van, az egyenletrendezési eljárásnak nincs. A tanulmány elkészítését az OTKA (T-023144/1997. ) is támogatta. Tartalomjegyzék: 1. fejezet Reakcióegyenletek rendezése alapfokon 1. 1. Rendezés "ránézésre", próbálgatással 1. 2. Egy egyszerû algoritmus: a láncszabály 2. fejezet Reakcióegyenletek rendezése középfokon 2. 1. Rendezés az oxidációs szám alapján 2. 2. Rendezés többismeretlenes egyenletrendszerrel: az algebrai módszer 3. fejezet Reakcióegyenletek rendezése felsõfokon 3. 1. Egy konvenció határain túl: rendezés szokatlan oxidációs számokkal 3. 2. Egyenletrendezés számítógéppel Függelék F. 1. Néhány nem mindennapi reakcióegyenlet F. 2. Egy felmérés és tanulságai Vissza az Elôadóba


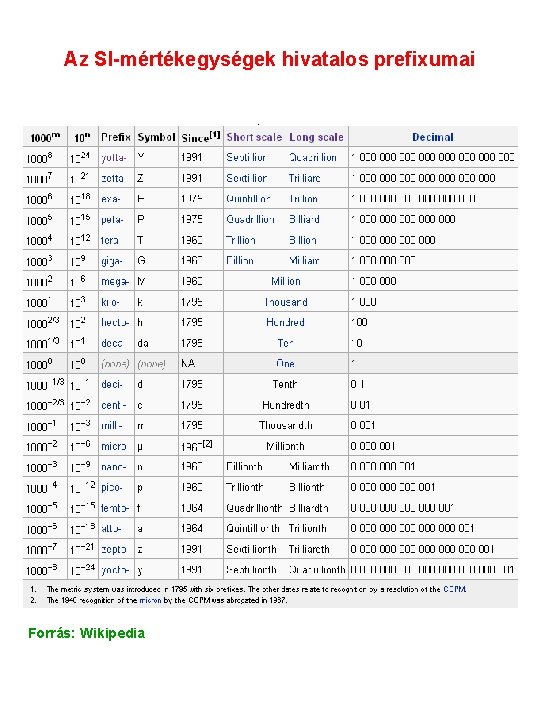
Az SI-mértékegységek hivatalos prefixumai Forrás: Wikipedia