Kmiai Ksrletbemutat Eladk Nagy Pter ELTE TTK Kmia

Kémiai Kísérletbemutató Előadók: Nagy Péter ELTE TTK Kémia MSC Bacsó András ELTE TTK Kémia BSC

Kémia Versenyek • • • Hevesy György Kémia Verseny (7 -8. oszt. ) Curie Kémia Verseny (7 -12. oszt) Irinyi József Kémia Verseny (9 -10. oszt. ) Kémia OKTV (11 -12. oszt. ) VegyÉSZtorna (levelező, 9 -12. oszt. ) KöKéL (levelező, 7 -12. oszt. ) (K, H és OH feladatok, egyéb versenyek pl. : fordítás …)

Nemzetközi Kémiai Diákolimpia • • • „A kémiaversenyek csúcsa” 2010: Tokió, Japán 2011: Ankara, Törökország 2012: Washington DC, USA Hogyan lehet bekerülni? OKTV helyezés (1 -15. ), KöKéL helyezés alapján a válogató 1. hetére onnan kb. 12 ember a 2. hétre 4 fős a csapat

Egy kis fizikai kémia Feladat: Hogyan vegyük ki száraz kézzel a pénzérmét? (A vizet nem szabad elforralni vagy kiönteni. ) Használható segédeszközök: Erlenmayer lombik borszeszégő

Saturnus fája Ólom-acetát oldatba cinklemezt mártunk. Egy kis idő múlva ólomfa képződik. Magyarázat: Pb 2+ + Zn = Pb + Zn 2+ Képen: Diana fája ugyanez csak ezüsttel

Exoterm és Endoterm • Exotermre még sok példa lesz • Endoterm: bárium-hidroxid és ammónium-nitrát reakciója Ba(OH)2 + 2 NH 4 NO 3 = Ba(NO 3)2 + 2 NH 3 + 2 H 2 O Olyan endoterm a reakció, hogy a lombik odafagy a falapra.

Exoterm és Endoterm Kérdés: Mi történik? Melyik folyamat exoterm és melyik endoterm? Válasz: A pasztilla oldódik vízben és a jód egy része szublimál. A Na. OH pasztilla oldódása vízben exoterm. A jód szublimációja pedig endoterm.

Égés (exoterm kísérletek) • Égés tiszta oxigénben: 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2 • Lehetséges-e az égés víz alatt? (Mi kell az égéshez) • Lehetséges-e az égés széndioxidban? 2 Mg + CO 2 = 2 Mg. O + C • Bengáli tűz (sárga: Na, zöld: Ba, ibolya: K, vörös: Sr, villanás: Al)

Gyufa • Mártógyufa: A tömény kénsav vizet von el a keményítőből, illetve oxidáló hatású klórdioxidot hoz létre, ezért gyullad be a gyufa. • Dörzsgyufa: 3 S + 2 KCl. O 3 = 3 SO 2 + 2 KCl

Színes • Rézkolmplexek az ammónia oldja a réz hidroxid csapadékot: Cu(OH)2 + 4 NH 3 = [Cu(NH 3)4]2+ + 2 OHcc. HCl: Cu 2+ + 4 Cl- = [Cu. Cl 4]2 • Nikkelkomplexek: Ni 2+ + 6 NH 3 = [Ni(NH 3)6]2+ + 3 en = [Ni(en)3]2+ + 6 NH 3 [Ni(en)3]2+ + 2 dmg = [Ni(dmg)2]2+ + 3 en • (en: etilén-diamin; dmg: dimetil-glioxim)
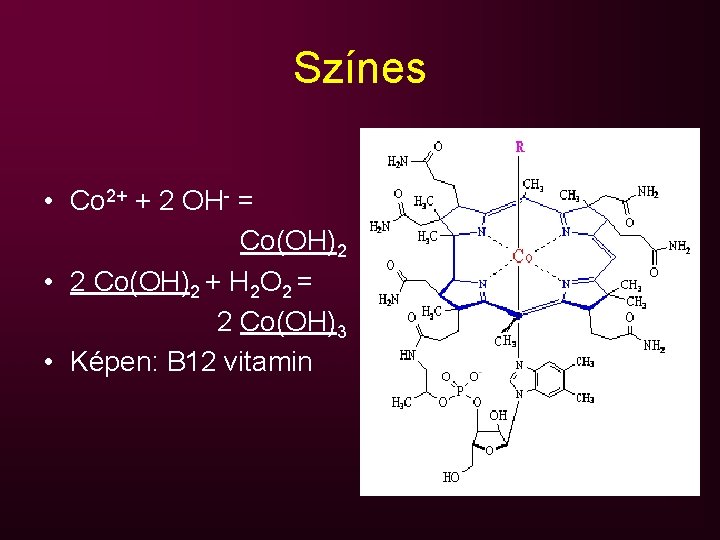
Színes • Co 2+ + 2 OH- = Co(OH)2 • 2 Co(OH)2 + H 2 O 2 = 2 Co(OH)3 • Képen: B 12 vitamin
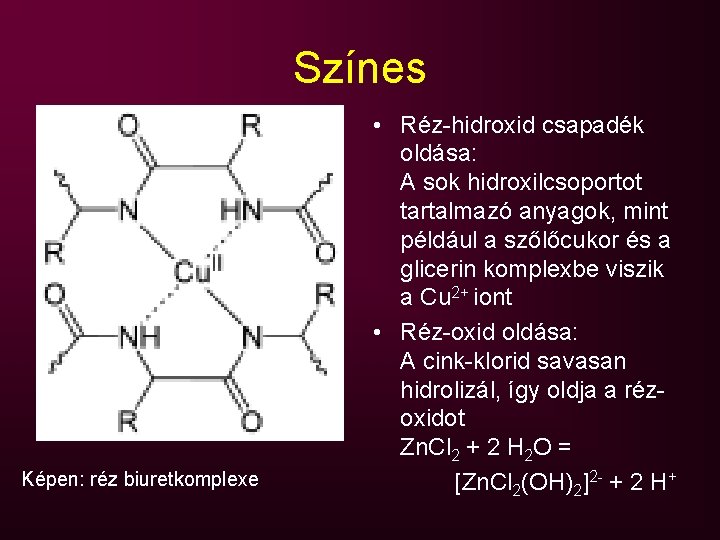
Színes Képen: réz biuretkomplexe • Réz-hidroxid csapadék oldása: A sok hidroxilcsoportot tartalmazó anyagok, mint például a szőlőcukor és a glicerin komplexbe viszik a Cu 2+ iont • Réz-oxid oldása: A cink-klorid savasan hidrolizál, így oldja a rézoxidot Zn. Cl 2 + 2 H 2 O = [Zn. Cl 2(OH)2]2 - + 2 H+

Ezüstkomplexek 2 Ag+ + CO 32– Ag 2 CO 3 + 2 OH– Ag 2 O + H 2 O + CO 32– Ag 2 O + H 2 O + 2 Cl – 2 Ag. Cl + 2 OH– Ag. Cl + 2 NH 3(aq) [Ag(NH 3)2]+ + Cl– [Ag(NH 3)2]+ + Br– Ag. Br + 2 NH 3 Ag. Br + 2 S 2 O 32– [Ag(S 2 O 3) 2]3– + Br– [Ag(S 2 O 3) 2]3– + I– Ag. I + 2 S 2 O 32– 2 Ag. I + S 2– Ag 2 S + 2 I–

Oldódás • Alapelv: Hasonló a hasonlóban oldódik jobban. • A kálium dikromát a vízben oldódik, mivel ionos, a jód a benzinben és a triklórmetánban is oldódik, mivel apoláris. • Összerázás után a benzines és a triklórmetános fázis elegyedik.

Reakciósebesség • Landolt-reakió I. : 3 HSO 3 + HIO 3 = 3 HSO 4 + HI HIO 3 + 5 HI = 3 H 2 O + 3 I 2 + H 2 O + HSO 3 = HSO 4 + 2 HI • Landolt II. : Hg 2+ iont is juttatunk a rendszerhez, ezért Hg. I 2 csapadékot (narancsvörös) észlelünk. • Landolt III. : malonsavat adunk a rendszerhez ami lassan reagál a jóddal emiatt színtelenedik el.

A víz mint katalizátor • 2 Al + 3 I 2 = 2 Al. I 3 A reakció exoterm ezért a jód egy része szublimál • A reakciót a jég is katalizálja, azaz lehet jéggel tüzet gyújtani Zn + NH 4 NO 3 = N 2 + Zn. O + 2 H 2 O

Kísérletek hidrogén peroxiddal • A mangán dioxid katalizálja a hidrogén peroxid bomlását. • KI oxidálása 2 KI + H 2 O 2 = 2 KOH + I 2 • Ólom-szulfid oxidálása Pb. S + 4 H 2 O 2 = Pb. SO 4 + 4 H 2 O • Higany-oxid redukciója: 2 Hg. O + H 2 O 2 = Hg 2 O + H 2 O + O 2 Hg 2 O + H 2 O 2 = 2 Hg + H 2 O + O 2

Oxigénátvivő katalizátorok • Metilénkék: Redukált alakja színtelen, oxidált alakja kék színű. Ha a rázással oxigén oldódik a vízbe, a metilénkék oxidálódik, de a cukor és a lúgos közeg mellett idővel visszaredukálódik • Indigókármin: Hasonló mechanizmus, csak itt van egy vörös átmeneti szín a kezdeti zöld és a végső sárga között

Érdekességek • Fekete kígyók: Az alkohol égni kezd, a felszabaduló hő hatására, a cukor elszenesedik a szódabikarbóna pedig bomlik, és a keletkező szén-dioxid felfújja. 2 Na. HCO 3 = Na 2 CO 3 + CO 2 + H 2 O • A kis tűzhányó: (NH 4)2 Cr 2 O 7 = N 2 + Cr 2 O 3 + 4 H 2 O

Alkoholszonda • Alkoholszonda: 2 Cr 2 O 72 - + 3 CH 3 CH 2 OH + 16 H+ = 4 Cr 3+ + 3 CH 3 COOH + 11 H 2 O

Fény • Szikraeső: A kálium-permanganátból oxigén fejlődik, ezért a vas és a szén ég, a szén-dioxid részecskéi pedig izzó vasrészecskéket visznek magukkal • A kén cinkkel és vassal is hevesen reagál, Zn. S és Fe. S képződik

Kemilumineszcencia • Olyan kémiai reakciók melyek fénykibocsátással járnak. • Pirogallol: vörös • Luminol + réz-szulfát + hidrogén-peroxid: kék • Luminol + vörösvérlúgsó: zöldes

Köszönjük a figyelmet!
- Slides: 23