LEKI O DZIAANIU PRZECIWWIRUSOWYM Leki przeciwwirusowepodzia wg mechanizmu










































































- Slides: 82

LEKI O DZIAŁANIU PRZECIWWIRUSOWYM

Leki przeciwwirusowe-podział wg mechanizmu działania • Leki bezpośrednio wpływające na wirusa: wiruicydy • Leki hamujące replikację wirusa na poziomie komórkowych: leki antywirusowe • Leki modyfikujące odpowiedź gospodarza: immunomodulatory

WIRIUCYDY PREPARATY: -detergenty -organiczne rozpuszczalniki: estry, chloroform, UV METODY: inaktywacja fotodynamiczna, krioterapia, laseroteraplia

Leki przeciwwirusowe • Etapy cyklu replikacyjnego wirusów = mechanizm działania większości leków przeciwwirusowych.

Etapy cyklu replikacyjnego wirusów • 1) Adsorbcja-proces przylegania wirusów do powierzchni komórki poprzez połączenie za specyficznym receptorem • 2) Penetracja-proces wnikania wirusów do komórki po jego uprzednim połączeniu się z receptorem • 3) Odpłaszczanie wirusa-uwolnienie materiału genetycznego

Etapy cyklu replikacyjnego wirusów • 4) Produkcja białek wczesnychpotrzebnych do replikacji genomu wirusa i modyfikujących metabolizm komórki • 5) Replikacja genomu- różne mechanizmy zależne od rodzaju wirusa • 6) Produkcja białek późnych –na podstawie nowopowstałych genomów • 7) Składanie wirionów- tworzenie nukleokapsydów

LEKI IMMUNOMODULUJĄCE • Zwiększają odpowiedź immunologiczną gospodarza np. - egzogenne przeciwciała - tymozyna - szczepionki terapeutyczne

Leki hamujące replikację wirusówna etapie adsorbcji i penetracji • 1) inhibitory wejścia/fuzji np. enfuvirtide (Fuzeon)- blokuje łączenie wirusa HIV i cząsteczką CD 4 • 2) inhibitory koreceptorów np. maraviroc (Selzentry)-blokuje łączenie wirusa HIV z koreceptorem CCR 5

Leki hamujące replikacja wirusówna etapie procesu odpłaszczania • Amantadyna (Viregyt K) • Rimantadyna (Flumanide) Amantadyna-lek lizozymotropowy-wpływa na kanał jonowy M 2 w aparacie Golgiego odpowiedzialny za aktywację wirusa (przed jego uwolnieniem w komórce) Działa na wirusa grypy typu A Niewielki efekt terapeutyczny

Leki hamujące replikację genomu wirusówpoprzez hamowanie enzymów koniecznych w cyklu namnażania wirusów Enzymy replikacyjne wirusów: • 1) Polimeraza kwasów nukleinowych • 2) Proteaza (retrowirusy) • 3) Integraza (retrowirusy) • 4) Neuraminidaza (ortomyksowirusy)

Inhibitory odwrotnej transkryptazy • Nukleozydowe NRTI • Nukleotydowe Nt. RTI • Nienukleozydowe NNRTI Odwrotna transkryptaza bierze udział w procesie transkrypcji wiruswego RNA na DNA. • Leki z grupy NRTI/Nt. RTI współzawodniczą z naturalnymi nukleozydami o specyficzne miejsce wiązania na odwrotnej transktryptazie. Zablokowanie przez NRTI odwrotnej transktyptazy hamuje dalszą budowę DNA. • NNRTI wiążą się bezpośrednio z odwrotną transkryptazą, hamując zdolność odwrotnej transkryptazy do dodawania nowych nukleotydów do nowopowstałego łańcucha DNA.

Nukleozydowe inhibitory odwrotnej transkryptazy (NRTI) • • • Zidovudine Emtricitabine Lamivudine Didanosine Stavudine Abacavir AZT FTC 3 TC dd. I d 4 T ABC „ Retrovir” „Emtriva” „Epivir” „Videx” „Zerit” „Ziagen”

Nukleotydowe inhibitory odwrotnej transkryptazy (Nt. RTI) Tenofovir TDF , , Viread”

Nienukleozydowe inhibirory odwrotnej transktyptazy • • newirapina NVP (Viramune) efavirenz EVF (Stocrin) rilpiwiryna RPV (Edurant) etraviryna ETV (Intelence)

Inhibitory odwrotnej transkryptazy stosowane w leczeniu zakażenia HBV • • • NRTI: Nt. RTI Entekawir (Baraclude) Tenofovir (Viread) Emtrycytabina Adefovir (Hepsera) Lamiwudyna (Zeffix) Clewudyna Telbivudyna (Tyzeca)

Leki hamujące replikację genomu wirusówpoprzez hamowanie enzymów koniecznych w cyklu namnażania wirusów • Inhibitory integrazy HIV (integracja wirusowego DNA z jądrowym DNA): - raltegravir - elvitegravir - dolutegravir • Inhibitory protezy HIV (hamują rozszczepianie proteolityczne dużych poliprotein Gag-Pol na białka strukturalne i enzymy wirusowe tj. odwrotna transkryptaza, integraza, proteaza).

Inhibitory proteazy HIV ( PI ) • Saquinavir SQV „Invirase” • Indinavir IDV „Crixivan” • Atazanavir ATV „Reyataz” • Fosamprenavir FPV „Telzir” • Ritonavir RTV „Norvir” • Lopinavir LPV „Kaletra” • Tipranavir TPV „Aptivus” • Darunavir DRV „Prezista”

Leki hamujące replikację genomu wirusów- Inhibitory enzymów cyklu replikacyjnego HCV • Inhibitorami specyficznych enzymów HCV: – NS 3 -4 A proteazy serynowej - NS 5 B RNA polimerazy - Białka NS 5 A NS 3 -4 A proteaza HCV rozszczepia poliproteiny HCV uwalniając białka HCV niezbędne do jego replikacji. Zastosowanie w trójlekowej terapii (Peg IFN/RBV/Boc lub Tel) poprawa SVR do 66% w genotypie 1, a terapii(Peg. IFN/RBV/SIM) do 90%.

Inhibitory neuraminidazy • Neuramidaza wirusowa powoduje uwolnienie kwasu sialinowego z powierzchni komórki powodując uwalnianie cząsteczki wirusowej. • Po zahamowaniu neuraminidazy hemaglutyniny wirusa grypy przyklejają nowe cząsteczki wirusa do kwasu sialinowego na powierzchni komórki powodując zbijanie się wirusa grypy, uniemożliwiając opuszczenie zakażonej komórki. • Oseltamivir - TAMIFLU • Zanamivir - Relenza

Tamiflu-oseltamivir Ø Aktywny wobec wirusów grypy typu A i B Ø Rekomendowany przez WHO w leczeniu i profilaktyce ptasiej i świńskiej grypy Ø Rejestracja od 1 roku życia Ø Dwie postaci: kapsułki po 75 mg - 10 kapsułek zawiesina 12 mg/ml - op. 100 ml

Dawkowanie Tamiflu w leczeniu grypy • • < 15 kg > 15 kg do 23 kg > 23 kg do 40 kg > 40 kg - 30 mg 2 xdziennie - 45 mg 2 xdziennie - 60 mg 2 xdziennie - 75 mg 2 xdziennie

Zanamivir-Relenza • Aktywny wobec wirusa grypy • Słaba biodostępność RELENZA ( proszek do inhalacji ) – stosowany jedynie w postaci inhalacji

Inhibitory dojrzewania • Bevirinat (lek w badaniach klinicznych)-blokuje dojrzewanie HIV poprzez hamowanie ostatniego etapu powstawania białka GAG. • Powstałe wiriony są defektywne, nie mają zdolności zakażania innych komórek.

Leki przeciwwirusowe • Największą grupę leków przeciwwirusowych stanowią analogi naturalnych nukleozydów. • Większość z nich to proleki, które stają się aktywne po fosforylacji przez kinazy białkowe wirusów.

SYNTETYCZNE ANALOGI GUANOZYNY ACYKLOWIR GANCYKLOWIR RYBAWIRYNA

ACYKLOWIR Analog dezoksyguanozyny • Aktywny wobec wirusów: HSV, VZV, CMV, EBV • Wchodzi w reakcję z polimerazą DNA wirusa, powoduje jej zablokowanie • Łatwo przenika do tkanek w tym OUN, wydalany jest przez nerki Zahamowanie replikacji wirusa

Zastosowanie kliniczne ACIKLOVIRU • Zakażenia wirusem ospy wietrznej (VZV) i półpaśca (VZV) oraz zakażenia skóry i błon śluzowych wirusem opryszczki (HSV 1 i 2) (także opryszczka narządów płciowych). • Stosowany w leczeniu opryszczkowego zapalenia mózgu.

Acyclowir-dawkowanie W ospie wietrznej dorośli i dzieci > 40 kg 800 mg 4 x/dobę przez 5 – 7 dni, dzieci młodsze: 80 mg/kg/dobę doustnie W półpaścu dorośli 800 mg co 4 godziny(5 x/dobę ) przez 7 dni doustnie W opryszczce wargowej dorośli 200 mg co 4 godziny (5 x/dobę przez 5 - 10 dni ) doustnie W opryszczkowym zapaleniu mózgu 10 mg/kg m. c. co 8 godzin wlew dożylny przez 21 dni

ACYKLOWIR • ZOVIRAX fiolki 0, 250 i 0, 500 tabl. 0, 2 0, 4 0, 8 , zawiesina doustna: 0, 2 i 0, 4/5 ml, • ACIX fiolki 0, 250 0, 500 • HERPESIN tabl. 0, 200 0, 400 mg fiolki 0, 250 • HEVIRAN tabl. 0, 2 0, 4 i 0, 8 • ANTIVIR tabl. 0, 2,

ACYKLOWIR • • Acyclovir - 3% maść do oczu, Cusiviral - 3% i maść do oczu, Virolex - 3% maść do oczu, Zovirax - 3 % maść do oczu

ACYKLOWIR • • • Antivir – 5% krem, Awirol - 5% krem, Cusiviral - 5% krem, Virolex - 5% krem, Zovirax - 5% krem

Immunoglobulina przeciw wirusowi VZV • VARITECT • Ampułki po 5 ml, 20 ml i 50 ml • Dawkowanie: profilaktycznie 1 ml /kg mc, leczniczo 2 ml / kg mc

GANCYKLOWIR • Nukleozydowy syntetyczny analog guaniny • Aktywny wobec wirusa CMV

Gancyklowir Ø Ze względu na znaczną toksyczność stosowany jest jedynie u chorych z obniżoną odpornością: W ciężkich zakażeniach CMV: • zapalenie siatkówki • zapalenie płuc • zapalenia przewodu pokarmowego

GANCYKLOWIR • Preparaty : CYMEVENE (fiolki 0, 5, kaps. 0, 25) CYMEVEN (fiolki 0, 5 ) CYMEVAN(flakony 0, 5 ) CYTOVENE, VALCYTE( iv i po, implanty doszklistkowe )

GANCYKLOWIR - dawkowanie • 5 mg/kg mc 2 x na dobę przez 14 -21 dni we wlewie dożylnym co najmniej przez 1 godzinę (stężenie leku nie większe niż 10 mg/ml ) • Leczenie podtrzymujące (dorośli ) doustnie 3 x 1 g lub 6 x 500 mg

Działania niepożądane Ø Uszkodzenie szpiku: neutropenia, małopłytkowość, niedokrwistość, eozynofilia Ø Zaburzenia żołądkowo-jelitowe i zapalenie trzustki Ø Zaburzenia neurologiczne (drgawki, bóle głowy) i psychiczne Ø Zwiększenie stężenia kreatyniny i mocznika, zwiększenie aktywności LDH i AST, ALT, FA, hipopokaliemia, hiponatremia, hipoglikemia, kwasica Ø Zab. rytmu serca, duszność

Immunoglobulina przeciw CMV CYTOTECT • Głównie Ig. G, śladowe Ig. A i Ig. M fiolki: 1 g/10 ml, 2 g/20 ml, 5 g/50 ml Podaje się we wlewie doż. , maksymalna dawka jednorazowa 150 mg/kg m. c.

Rybawiryna • Analog guanozyny • Aktywna wobec wirusów RNA (HCV, RSV wirusy wywołujące gorączki krwotoczne) • Nie wykazuje aktywności p-HCV w monoterapii

Rybawiryna • Hamuje replikację HCV przez zmianę aktywności dehydrogenazy monofosforanu inozyny • Modyfikuje aktywność RNA zależnej polimerazy • Poprawia aktywność interferonu poprzez stymulację genów ISGs (interferon stimulated genes)

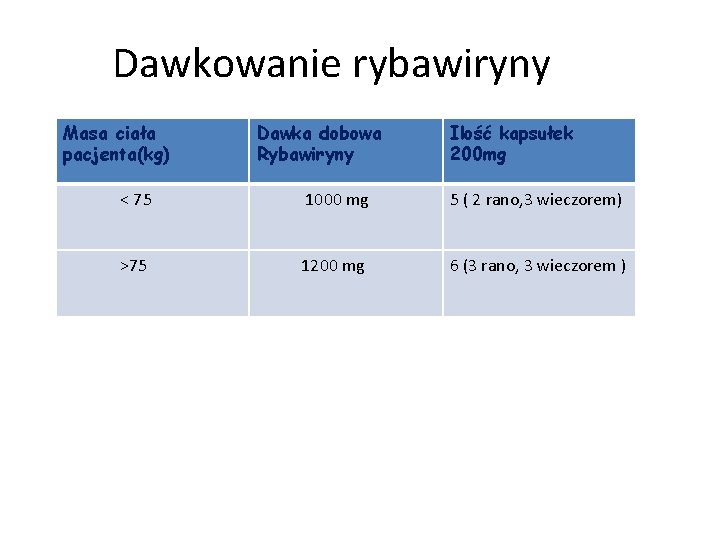
Rybawiryna (Copegus, Rebetol) • Należy podawać rano i wieczorem z posiłkiem • Nie stosować w monoterapii • Stosować zawsze w skojarzeniu z peginterferonem α albo interferonem alfa

Dawkowanie rybawiryny Masa ciała pacjenta(kg) Dawka dobowa Rybawiryny Ilość kapsułek 200 mg < 75 1000 mg 5 ( 2 rano, 3 wieczorem) >75 1200 mg 6 (3 rano, 3 wieczorem )

INTERFERONY • Są to małocząsteczkowe glikoproteiny wytwarzane przez komórki organizmu zakażonego wirusem. • INTERFERONY α ß Ύ

Interferony Działanie: wspomagają rozpoznawanie antygenów wirusowych, zwiększają aktywność komórek T, NK i makrofagów. Hamują replikację wirusa w zakażonej komórce. Działanie: - przeciwwirusowe - immunomodulacyjne - antyproliferacyjne

INTERFERONY charakterystyka W leczeniu zakażenia HCV mają zastosowanie: • Rekombinowane IFN alfa (różniące się składem aminokwasów) • Pegylowane IFN alfa ( zawierające rekombinowane IFN alfa, różniące się wielkością cząsteczki pegylującej) • Naturalne IFN alfa z ludzkich leukocytów

Interferony pegylowane • Peg IFN alfa: alfa 2 a z cząsteczką Peg o wielkości 40 k. D(metabolizm wątrobowy) (PEGASYS) • Peg. IFN alfa: alfa 2 b z cząsteczką Peg o wielkości 12 k. D (wydalanie przez nerki) (PEGINTRON)

Działnia niepożądane w leczeniu skojarzonym (Peg. IFN i RBV) • • Odczyn w miejscu podania Ból głowy, gorączka, objawy grypopodobne Zmniejszenie masy ciała Depresja, myśli samobójcze, drażliwość, bezsenność, niepokój, zaburzenia koncentracji • Łysienie, świąd, suchość skóry • Niedoczynność lub nadczynność tarczycy • Niedokrwistość, leukopenia, granulocytopenia, trombocytopenia

Zakażenie HCV • 200 mln ludzi jest zakażonych HCV na świecie. • 200 tys ludzi jest zakażonych HCV w Polsce. • Przewlekle zakażenie HCV prowadzi u co 5 osoby do marskości wątroby, a u około 4% chorych z tej grupy stwierdza się rocznie raka wątrobowo-komórkowego.

Leczenie zakażeń HCV • Wskazania • Chorzy z ostrym i przewlekłym zapaleniem wątroby t. C oraz wyrównaną marskością wątroby. • Chorzy z pozawątrobowymi objawami zakażenia HCV. • Chorzy z marskością wątroby niewyrównaną (ew. DAA).

Leczenie ostrego wirusowego zapalenia wątroby typu C MONOTERAPIA • INTERFERONY naturalne (Alfaferon ) • INTERFERONY rekombinowane ( IFN α 2 a – Roferon, IFN α 2 b Intron A ) • INTERFERONY pegylowane

Leczenie PZWC • Do programu kwalifikowani są świadczeniobiorcy w wieku powyżej 3 roku życia, chorzy na przewlekłe wirusowe zapalenie wątroby typu C i spełniający poniższe kryteria: • 1) obecność wiremii HCV RNA w surowicy krwi lub w tkance wątrobowej; • 2) obecność przeciwciał anty-HCV; • 3) zmiany zapalne i włóknienie w obrazie histopatologicznym wątroby określone z wykorzystaniem elastografii wątroby wykonanej techniką umożliwiającą pomiar ilościowy w k. Pa lub określone z wykorzystaniem biopsji wątroby.

Leczenie PZWC (genotyp 2 i 3) Ø Terapia dwulekowa przez 24 tygodnie: • IFN alfa pegylowany • Rybawiryna • Terapia alternatywna: SOF i RBV przez 12 tygodni: (przy nieskuteczności lub nietolerancji Peg. IFN i RBV)

Leczenie PZWC (genotyp 1) • Terapia trójlekowa (Peg. IFN/RBV/inhibitor proteazy) • Terapie bezinterferonowe: 2 D +/-RBV 3 D+/- RBV

Leczenie przewlekłego wirusowega zapalenia wątroby typu C • Terapia skojarzona (terapia trójlekowa): genotyp 1 IFN α pegylowany i Rybawiryna i Inhibitor protezy NS 3 A: Symeprewir (genotyp 1 b i 4)/Boceprewir (genotyp 1) / Telaprewir (genotyp 1)

Nowe leki w zakażeniu HCV • Simeprevir (OLYSIO)


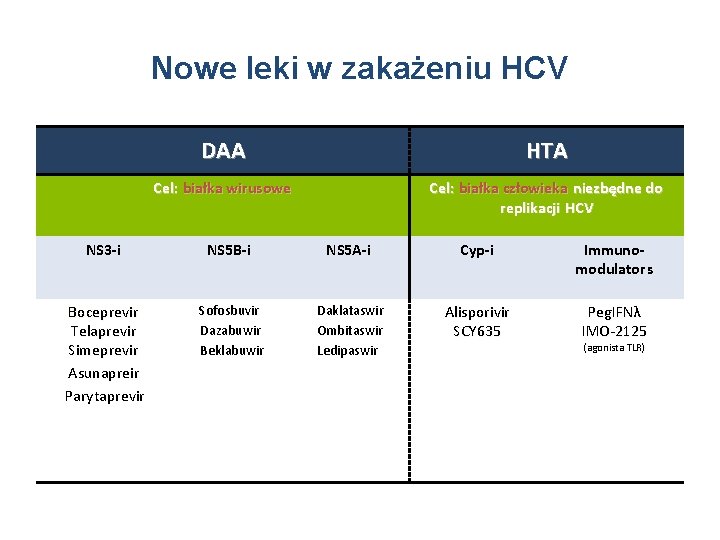
Nowe leki w zakażeniu HCV NS 3 -i Boceprevir Telaprevir Simeprevir Asunapreir Parytaprevir DAA HTA Cel: białka wirusowe Cel: białka człowieka niezbędne do replikacji HCV NS 5 B-i Sofosbuvir Dazabuwir Beklabuwir NS 5 A-i Daklataswir Ombitaswir Ledipaswir Cyp-i Immunomodulator s Alisporivir SCY 635 Peg. IFNλ IMO-2125 (agonista TLR)

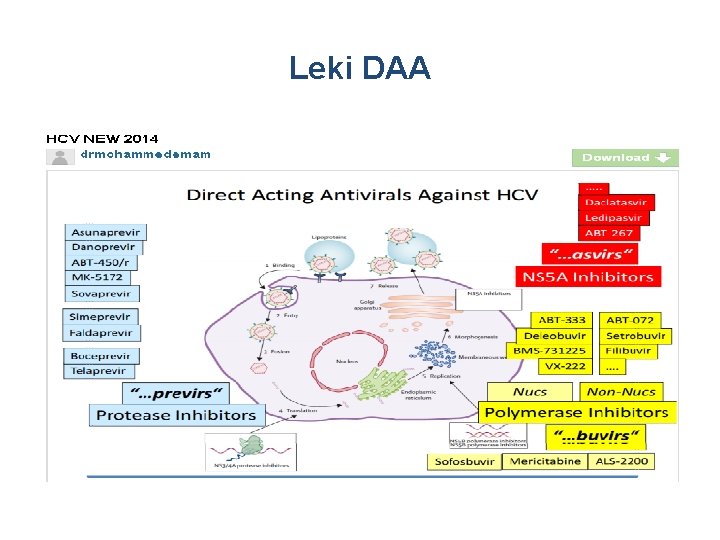
Leki DAA

Inhibitory proteazy NS 3 • • • Boceprewir Telaprewir Symeprewir Asunaprewir Parytaprewir

Inhibitory polimerazy NS 5 B Nienukleozydowe: Dazabuwir Beklabuwir Nukleotydowe: Sofosbuwir

Inhibitory białka niestrukturalnego NS 5 A • Daklataswir • Ombitaswir • Ledipaswir

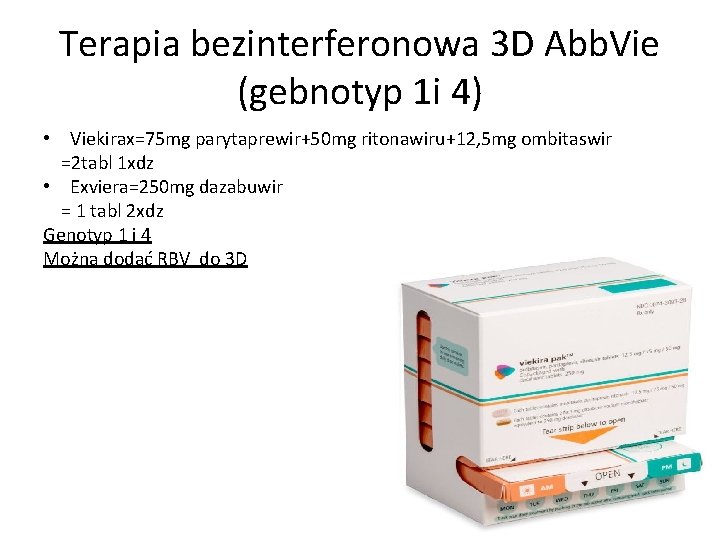
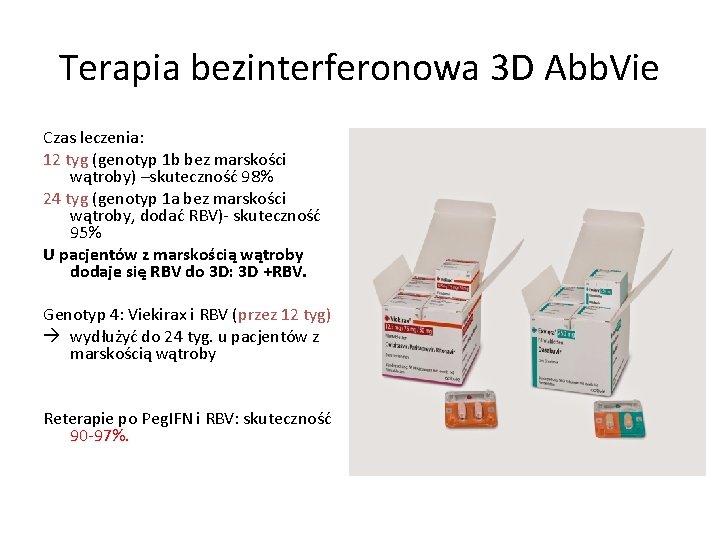
Terapia bezinterferonowa 3 D Abb. Vie (gebnotyp 1 i 4) • Viekirax=75 mg parytaprewir+50 mg ritonawiru+12, 5 mg ombitaswir =2 tabl 1 xdz • Exviera=250 mg dazabuwir = 1 tabl 2 xdz Genotyp 1 i 4 Można dodać RBV do 3 D

Terapia bezinterferonowa 3 D Abb. Vie Czas leczenia: 12 tyg (genotyp 1 b bez marskości wątroby) –skuteczność 98% 24 tyg (genotyp 1 a bez marskości wątroby, dodać RBV)- skuteczność 95% U pacjentów z marskością wątroby dodaje się RBV do 3 D: 3 D +RBV. Genotyp 4: Viekirax i RBV (przez 12 tyg) wydłużyć do 24 tyg. u pacjentów z marskością wątroby Reterapie po Peg. IFN i RBV: skuteczność 90 -97%.

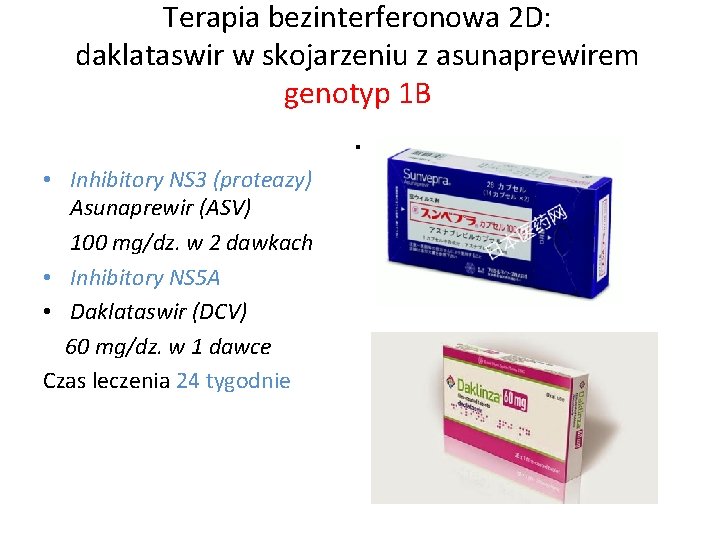
Terapia bezinterferonowa 2 D: daklataswir w skojarzeniu z asunaprewirem genotyp 1 B . • Inhibitory NS 3 (proteazy) Asunaprewir (ASV) 100 mg/dz. w 2 dawkach • Inhibitory NS 5 A • Daklataswir (DCV) 60 mg/dz. w 1 dawce Czas leczenia 24 tygodnie

Daklatazwir (DCV) • Lek może być stosowany u pacjentów z genotypem 1 w terapii bez interferonu, w skojarzeniu z sofosbuwirem (DCV + SOFOSBUWIR) przez 12 tygodni, przy czym u chorych wcześniej leczonych inhibitorem proteazy należy terapię przedłużyć do 24 tygodni i rozważyć dodanie RBV.

Nowe leki w zakażeniu HCV • SOFOSBUVIR (SOVALDI)1 x 1 tabl a 400 mg - może być stosowany z pegylowanym interferonem alfa i rybawiryną do leczenia wszystkich genotypów wirusa HCV (Peg. IFN i RBV i SOF). - u chorych z genotypem 1 lub 4 wirusa oraz niekorzystnym polimorfizmem IL 28 B taka terapia 3 -lekowa okazuje się skuteczna 3 razy częściej niż terapia 2 -lekowa – odsetek wyleczeń 87% (a przy korzystnym polimorfizmie CC uzyskano nawet 99%).

SOFOSBUVIR • Dopuszczono również stosowanie sofosbuviru bez interferonu, z samą rybawiryną lub innymi DAA. • Dla genotypu 3 uzyskiwano dobrą skuteczność takiej terapii bezinterferonowej tylko z RBV, jeśli trwała ona 24 tygodnie (93% w grupie uprzednio nieleczonych i 77% w grupie uprzednio leczonych nieskutecznie).

Schematy bezinterferonowe dla SOF • sofosbuvir + simeprevir+/RBV • sofosbuvir + daclatasvir +/- RBV (przy nieskuteczności terapii trójlekowej) • sofosbuvir + RBV (genotyp 2 i 3 przy przeciwwskazaniach do IFN, niewyrównana funkcja wątroby) • sofofosbivir +ledipasvir skuteczność terapii bliska 100%.

Schematy bezinterferonowe • SOFOSBUVIR +LEDIPASVIR (jedna tabletka HARVONI)+/-RBV • Zarejestrowany dla chorych z genotypem 1 wirusa wcześniej nieleczonych jak i uprzednio leczonych nieskutecznie, w tym chorych z wyrównaną marskością wątroby. Terapia ma 12 tygodni lub 24 tygodni (F 4).

Przeszłość w leczeniu HCV Peg IFN +Boceprevir +RBV= 18 tabletek na dobę i zastrzyk 1 x w tygodniu

Przyszłość w leczeniu HCV • Harvoni = sofosbuvir + ledipasvir (w jednej tabletce)

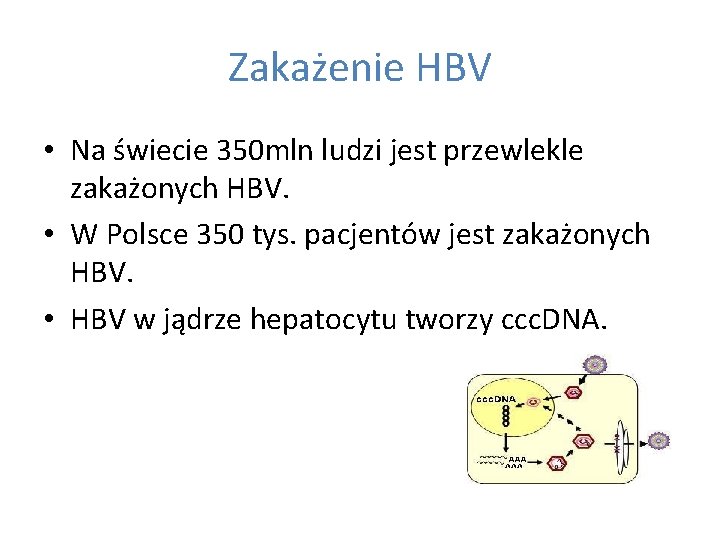
Zakażenie HBV • Na świecie 350 mln ludzi jest przewlekle zakażonych HBV. • W Polsce 350 tys. pacjentów jest zakażonych HBV. • HBV w jądrze hepatocytu tworzy ccc. DNA.

Leczenie przewlekłego wirusowego zapalenia wątroby typu B Ø Głównym celem terapii– • uzyskanie trwałego zaniku HBV-DNA • i następnie eliminacja HBs. Ag • aby zapobiec marskości wątroby i pierwotnemu rakowi wątroby

Leczenie PZWB

Leczenie PZWB • Pacjenci z marskością wątroby oraz z wykrywalnym HBV DNA są leczeni niezależnie od poziomu transaminaz. • Pacjenci oczekujący na przeszczep narządowy są leczeni niezależnie od poziomu wiremii HBV DNA i stwierdzonego poziomu aktywności AIAT.

Leki zarejestrowane do leczenia HBV • Interferon rekombinowany alfa 2 a i alfa 2 b • Interferon pegylowany (Peg. IFN) alfa 2 a • Analogi nukleozydowe i nukleotydowe: ADEFOWIR ENTEKAWIR LAMIVUDINA TELBIWUDYNA TENOFOWIR

Leczenie PZWB • Lekiem pierwszego rzutu w terapii pacjentów z przewlekłym wirusowym zapaleniem wątroby typu B dotychczas nieleczonych są interferony stosowane w monoterapii przez 48 tygodni, o ile nie ma przeciwwskazań do ich podania. Preferowanym interferonem ze względu na wyniki leczenia jest interferon pegylowany alfa-2 a.

Leczenie PZWB • Kryteria wyłączenia z leczenia interferonem • brak odpowiedzi po 12 tygodniach leczenia definiowanej jako zmniejszenie poziomu wiremii HBV DNA o co najmniej 1 log 10;

Leczenie PZWB • W przypadkach niemożności zastosowania interferonów lub ich nieskuteczności należy rozważyć stosowanie analogów nukleozydowych lub nukleotydowych. • U pacjentów HBe. Ag (-) leczenie należy rozpocząć od entekawiru albo tenofowiru albo lamiwudyny, a u osób HBe. Ag (+) leczenie należy rozpocząć od adefowiru albo entekawiru albo tenofowiru.

Leczenie PZWB • Kryteria skuteczności terapii analogiami: -obniżenie wiremii HBV DNA co najmniej o 1 log 10 w 12 tygodniu leczenia -niewykrywalna wiremia HBV w 24 tygodniu terapii

Leczenie PZWB • W innym wypadku należy rozważyć zmianę leku po uzyskaniu wyniku wirogramu i sprawdzeniu adherencji pacjenta.

Leczenie PZWB • Leczenie analogami można zakończyć u osób leczonych dłużej niż rok, po stwierdzeniu: • 1) serokonwersji w układzie "s" lub • 2) dwukrotnie ujemnych wyników oznaczenia HBV DNA wykonanych w odstępach co najmniej 3 miesięcy.
 Kuriuo paprastuoju mechanizmu galima laimėti darbo
Kuriuo paprastuoju mechanizmu galima laimėti darbo Kur naudojami skridiniai
Kur naudojami skridiniai Gnp suwnicy
Gnp suwnicy Fungovanie trhového mechanizmu
Fungovanie trhového mechanizmu Paprastasis mechanizmas
Paprastasis mechanizmas Polieny leki
Polieny leki Color coding leki
Color coding leki Leki neutralizujące nadmiar kwasów żołądkowych
Leki neutralizujące nadmiar kwasów żołądkowych Selam leki tselot
Selam leki tselot Selam leki prayer
Selam leki prayer Wlanea
Wlanea Leki antypsychotyczne
Leki antypsychotyczne Dalacin c a karmienie piersią
Dalacin c a karmienie piersią Farmakoterapia cukrzycy
Farmakoterapia cukrzycy Leki adrenergiczne
Leki adrenergiczne Fotosensytyzacja
Fotosensytyzacja Leki sekretolityczne
Leki sekretolityczne Leki ganglioplegiczne
Leki ganglioplegiczne Atypowa żarłoczność psychiczna
Atypowa żarłoczność psychiczna








































