Kiseonik Marija Stanojevi II 8 Kiseonik Najrasprostranjeniji element






















- Slides: 26

Kiseonik Marija Stanojević II 8

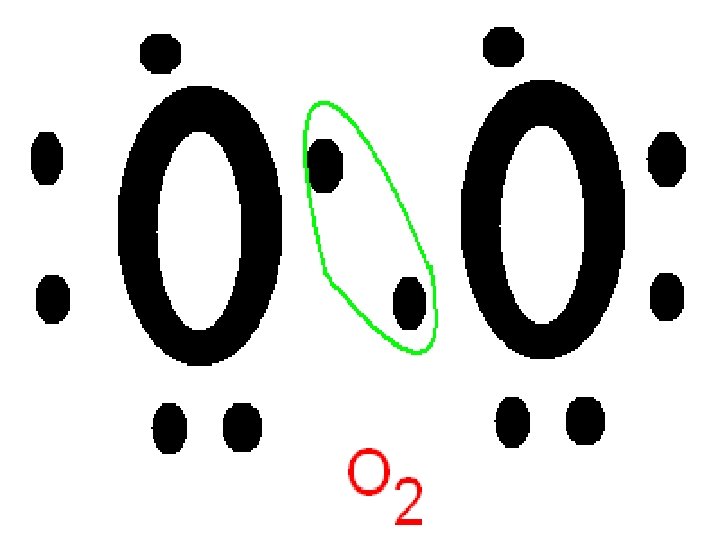
Kiseonik ØNajrasprostranjeniji element u prirodi ØSlobodan se javlja u obliku: Ø O 2 (donji slojevi atmosfere) Ø O 2 (gornji slojevi atmosfere) ØJedini se sa svim elementima u prirodi, direktno se ne jedini samo sa plemenitim metalima i halogonim elementima – oksidi (proces oksidacije je egzoterman proces)

Dobijanje kiseonika ØU laboratoriji: ØZagrevanjem oksidacionog sredstva, npr. KMn. O 4, KCl. O 3, Hg. O. . . Ø 2 KMn. O 4 + H 2 SO 4 + 5 H 2 O 2 → 2 Mn. SO 4 + K 2 SO 4 + 8 H 2 O +5 O 2 Ø KCl. O 3 → 2 KCL + 3 O 2 ØU industriji: Øfraksciona destilacija tečnog vazduha Øelektroliza vode


Primene kiseonika ØSav živi svet koristi kiseonik za disanje - bez njega ne bismo mogli da živimo ØKiseonik se pomaže sagorevanju laktoze u našim mišićima i omogućava nam pomeranje udova, trčanje i bavljenje sportom ØUdisanje kiseonika iz boce sa kiseonikom jako povoljno utiče na srce svih ljudi koji imaju bilo kakvih zdravstvenih tegoba i problema sa srcem ØKiseonik iz boce je takođe veonma koristan i za ljude koji boluju od raka pluća

Primene kiseonika ØKiseonik se koristi u prehrambenoj industriji ØU metalnoj industriji kiseonik se koristi za intezifikaciju procesa sagorevanja u industrijskim pećima za proizvodnju metala i nemetala ØU metalurgiji obojenih metala (bakar, aluminijum i olovo) tehnički gasovi se primenjuju u mnogim procesima proizvodnje i prerade ovih metala, a kiseonik ima najveću primenu u procesu sagorevanja

Oksidi - najvažnija jedinjenja kiseonika ØOksidi su jedinjenja kiseonika sa drugim elementima ØU zavisnosti od oksidacionog broja kiseonika imamo tri vrste oksida: Øobični oksidi – oksidaciono stanje -2 Øperoksidi – oksidaciono stanje -1 Øsuperoksidi – oksidaciono stanje -1/2 ØOksidi mogu biti: Øbazni Økiseli Øamfoterni

Dobijanje oksida Ø Ø Ø Sagorevanje elemenata na vazduhu: 2 Mg + O 2 → 2 Mg. O Sagorevanje elemenata u struji vodene pare: Mg + H 2 O → Mg. O + H 2 Razlaganje hidroksida dejstvom toplote: 2 Al (OH)3 → Al 2 O 3 + H 2 O Žarenje karbonata: Ca. CO 3 → Ca + CO 2 Razlaganje nitrata dejstvom toplote: Cu (NO 3) → Cu. O + 2 NO 2 + ½ O 2 Oksiodacija metala sa HNO 3 Ø Ø Ø dejstvom koncentrovane HNO 3 na Cu: Cu + 4 HNO 3 → Cu(NO 3) + 2 2 NO 2 + 2 H 2 O dejstvom razblažene HNO 3 na Cu: 3 Cu + 8 HNO 3 → 3 Cu(NO 3) + 2 NO 2 + 4 H 2 O Ø Redukcija oksida u kome je elemenat u višem oksidacionom stanju: Ø Ø CO 2 + C→ 2 CO Ø Razlaganje mešovitih oksida: 2 Pb 3 O 4 → 6 Pb. O + O 2

Bazni oksidi – anhidridi baza ØOksidi metala: Li 2 O, K 2 O, Mg. O, Ca. O, Ni. O, Fe. O. . . ØMetali I grupe sa kiseonikom grade: Øokside (Li 2 O, Na 2 O, K 2 O) Ø 4 Li (s) + O 2 (g) → 2 Li 2 O (s) Øperokside (Na 2 O 2, K 2 O 2) Ø 2 Na (s) + O 2 (g) → Na 2 O 2 (s) Øsuperokside (KO 2) ØK (s) + O 2 (g) → KO 2 (s) ØMetali II grupe sa kiseonikom grade: Øokside (Mg. O, Ca. O, Sr. O, Ba. O) Ø 2 Ca (s) + O 2 (g) → 2 Ca. O (s) Øperokside (Ba. O 2) ØBa (s) + O 2 (g) → Ba. O 2 (s)

Bazni oksidi – anhidridi baza ØMetali III grupe sa kiseonikom grade Øokside (In 2 O 3, Tl 2 O 3) ØIn (s) + O 2 (g) → In 2 O 3 (s) ØMetal bizmut iz pete grupe jedini gradi bazni oksid sa kiseonikom ØBi (s) + O 2 (g) → Bi 2 O 3 (s) ØReakcije sa vodom i kiselinama: ØNa 2 O (s) + H 2 O (l) → 2 Na. OH (aq) ØCa. O (s) + H 2 O (l) → Ca (OH)2 (aq) ØCa. O (s) + 2 HCl(aq) → Ca. Cl 2 (aq) + H 2 O (l)

Bazni oksidi – anhidridi baza ØDobijanje baznih oksida: Ø 2 Mg (s) + O 2 (g) → 2 Mg. O (s) ØMg (OH)2 (s) → Mg. O (s) + H 2 O (g) ØMg. CO 3 (s) → Mg. O (s) + CO 2 (g) (zagrevanjem) Ø 2 Pb (NO 3)2 (s) → 2 Pb. O (s) + 4 NO 2 (g) + O 2 (g) (zagrevanjem) ØHg. Cl 2 (aq) + 2 Na. OH (aq) → Hg. O (s) + H 2 O (l) + 2 Na. Cl (aq)

Kiseli oksidi - anhidridi kiselina ØOksidi nemetala : N 2 O 5, CO 2, SO 3, SO 2, P 2 O 5, Cl 2 O 7. . . ØOksidi metala: Cr. O 3, Mn 2 O 7. . . (visok oksidacioni broj metala) ØOksidi metaloida: B 2 O 3, Si. O 2, Ge. O 2. . . ØJedinjenja kovalentnog karaktera Ø Jedinjenja kiseonika i elemenata IV, V, VI i VII grupe Ø Većina ih je u gasovitom agregatnom stanju

Kiseli oksidi - anhidridi kiselina ØDobijanje: Ø 2 C(s) + O 2(g) → 2 CO(g) ØP 4(s) + 3 O 2(g) → P 4 O 6(s) ØS 8(s) + 8 O 2(g) → 8 SO 2(g)

Kiseli oksidi - anhidridi kiselina ØReakcije sa vodom i bazama: ØCO 2(g) + H 2 O(l) → H 2 CO 3(aq) ØSO 2(g) + H 2 O(l) → H 2 SO 3(aq) ØN 2 O 5(g) + H 2 O(l) → 2 HNO 3(aq) ØCO 2(g) + 2 Na. OH(aq) → Na 2 CO 3(aq) + H 2 O(l) ØReakcije oksida metala i oksida nemetala: ØCa. O(s) + SO 3(l) → Ca. SO 4(s) Ø 6 Na 2 O(s) + P 4 O 10(s) → 4 Na 3 PO 4(s)

Amfoterni oksidi ØAl 2 O 3, Zn. O, Be. O, Pb. O, As 2 O 3, Sn. O, Cr 2 O 3. . . ØImaju istovremeno osobine i baznih i kiselih oksida. ØReakcije sa kiselinama i bazama: ØAl 2 O 3 (s) + 6 HCl (aq) → 2 Al. Cl 3 (aq) + 3 H 2 O (l) ØAl 2 O 3 (s) + 2 Na. OH (aq) + 3 H 2 O → 2 Na Al(OH)4 (aq)

Amfoterni oksidi ØPeriodni sistem: Ø u periodi kiselost oksida raste, a baznost opada: ØPrimer: IV perioda ØK 2 O Ca. O Ga 2 O 3 Ge. O 2 As 2 O 5 Se. O 3 Br 2 O 7 baz. > baz. amfot. kis. < kis. Ø u grupi bazni karakter oksida raste, a kiseli opada: ØPrimer: V grupa ØN 2 O 3 P 2 O 3 As 2 O 3 Sb 2 O 3 Bi 2 O 3 kis. > kis. amfot. baz.

Amfoterni oksidi ØAko element gradi više oksida: Økiseli karakter je najjače izražen kod oksida u kome je element u najvišem oksidacionom stanju ØPrimer Ø As 2 O 3 – amfoteran i As 2 O 5 – kiseo Ø Ako metal gradi više oksida: ØCr. O – bazni, Cr 2 O 3 – amfoteran, Cr. O 3 - kiseo

Neutralni oksidi ØOksidi nemetala: N 2 O, NO, CO ØGasoviti oksidi ØNe reaguju sa vodom, ni sa kiselinama, ni sa bazama ØNe grade baze, ni kiseline

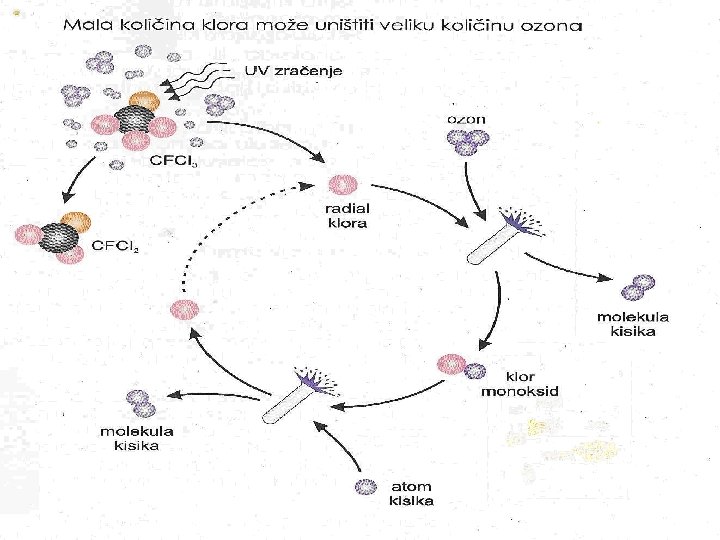
Ozon ØJedinjenje kiseonika sa formulom O 3 ØDobijanje: 3 O 2 → 2 O 3 bolje se rastvara u vodi od O 2 ØNastaje spajanjem tri atoma kiseonika i ima formulu O 3 ØNalazi se u gornjim slojevima atmosfere ØRazgradnjom freona oslobađaju se joni hlora i broma koji se vežu s atomom kiseonika iz molekula ozona

Ozonski omotač ØDaje plavetnilo nebu ØOzonski sloj je deo stratosfere na visini od 12 – 50 km ØPlaneta nazvana HD 209458 b - "OZIRIS“, koja se ne nalazi u Sunčevom sistemu takođe ima atmosferu u kojoj se nalazi kiseonik ØSmatra se da ima još takvih planeta van Sunčevog sistema


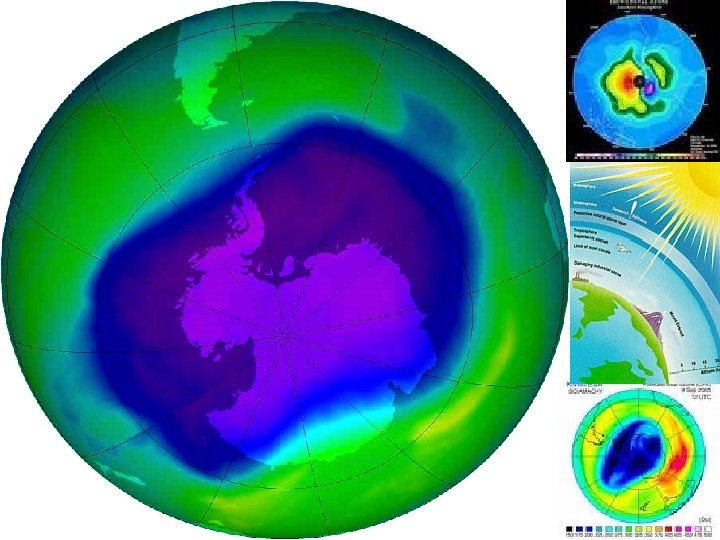
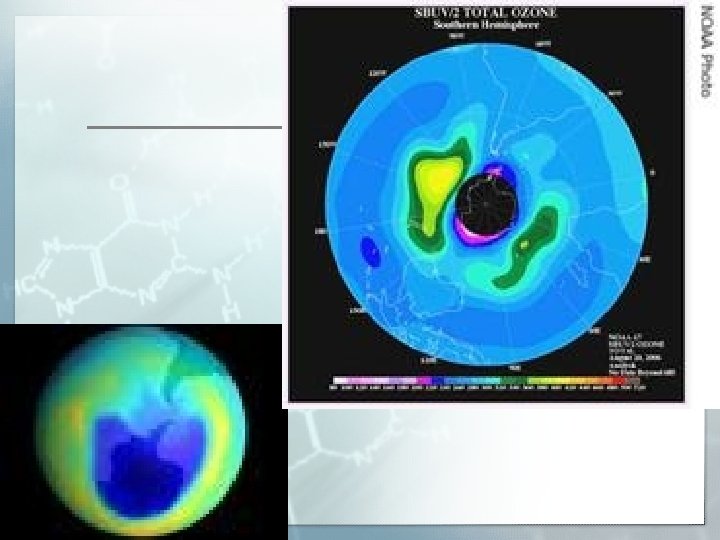
Ozonske rupe ØPrve pretpostavke o tome što sve ljudska delatnost može naneti ozonskom omotaču objavljene su početkom 1970 -ih godina ØPrva ozonska rupa nađena je na južnoj hemisferi ØOzon se oštećuje u proseku 4 -5% za deset godina ØRanih osamdesetih dokazano je oštećenje ozonskog omotača nad Antarktikom pomoću NASA-inog satelita ØGodine 1999. godine izmerena je najveća "rupa", veličine 27 miliona kvadratnih kilometara. Ali 2000. godine ona se još povećala na 30 miliona.

Ozonske rupe ØUsled prevelike i nekontrolisane upotrebe: Øfreona (hemikalija koja se koristi u dezodoransima i lakovima za kosu, ili kao rashladni mediji u hladnjacima, ledenicama, klima-uređajima) Øhalona (upotrebljava se kao sredstvo za gašenje požara u protupožarnim uređajima) danas dolazi do oštećivanja ozonskog sloja. Ø Oštećeni ozonski štit propušta do tla više ultraljubičastog zračenja koje uzrokuje učestalost očnih bolesti i raka kože kod ljudi, a može oštetiti i belančevine i DNK kod ljudi, biljaka i životinja.

Primena ozona ØOzon izaziva vedro raspoloženje, bolji imunitet i lep ten ØPojačava imuni sistem i energetski potencijal organizma ØPrirodan je antibiotik i za kratko vreme uništava viruse, bakterije i gljivice ØPodiže nivo intelektualnih sposobnosti, pojačava pažnju i ubrzava razmišljanje. ØKoristi se za dezinfekciju rana. ØU kozmetici se upotrebljava za pravljenje krema za podmlađivanje

Primena ozona ØLeči apscese, rane, osteomijelitis, zaustavlja cirozu jetre i propadanje očnog živca. ØOzon se ubrizgava u mišić kroz krv, radi veće izdržljivosti ØZa lečenje se koristi i ozonirana voda, koja se dobija propuštanjem ozona kroz vodu. ØLeči zglobove, smanjuje otok i poboljšava cirkulaciju ØKoristi se za dezinfekciju ØDobar je za osvežavanje i podmlađivanje kože

Hvala na pažnji!!!