Imunoglobulny Ig protiltky Protiltka Antibody Antikrper srov glykoproteny
Imunoglobulíny (Ig) protilátky

Protilátka Antibody Antikörper sérové glykoproteíny živočíšneho pôvodu súčasť imunoglobulínovej veľkorodiny 1891 P. EHRLICH Antikörper • AGLUTINÍNY reagujú s antigénmi erytrocytov, baktérií a rôznych častíc • ANTITOXÍNY neutralizujú rôzne toxíny • PRECIPITÍNY reagujú pri imunoprecipitácii • LYZÍNY navodzujú lýzu terčových buniek

Objavy imunoglobulínov • 1845 H. BENCE-JONES dimér ľahkých reťazcov (myelómové proteíny) • 1937 A. TISELIUS voľná elektroforéza • 1939 A. TISELIUS, E. A. KABÁT -globulínová frakcia • 1964 komisia expertov WHO, Praha názvoslovie Ab IMUNOGLOBULÍNY (Ig) (immunoglobulins) • • • Ig. M 1944 Ig. G 1950 Ig. A 1960 Ig. D 1965 Ig. E 1966 J. WALDENSTRÖM makroglobulinémia R. R. PORTER fragmentácia Ab papaínom G. M. EDELMAN fragmentácia (β-merkaptoetanol) J. H. HEREMANS D. W. ROWE a J. L. FAHEY K. ISHIZAKA, BENICH a JOHANSSON
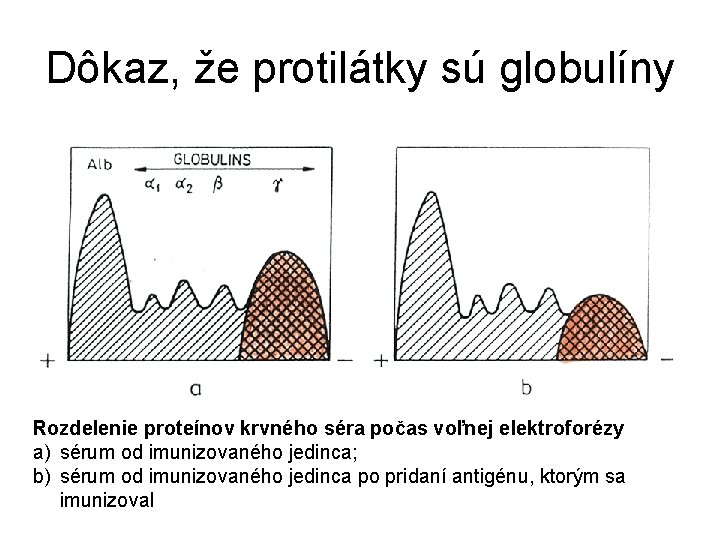
Dôkaz, že protilátky sú globulíny Rozdelenie proteínov krvného séra počas voľnej elektroforézy a) sérum od imunizovaného jedinca; b) sérum od imunizovaného jedinca po pridaní antigénu, ktorým sa imunizoval
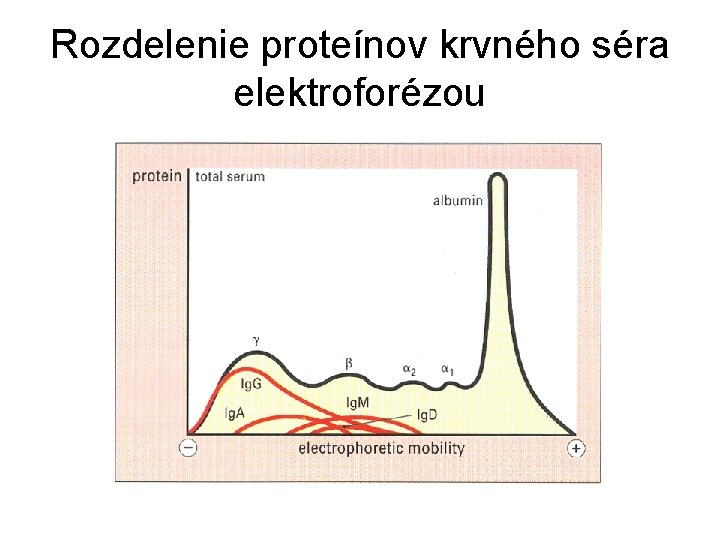
Rozdelenie proteínov krvného séra elektroforézou

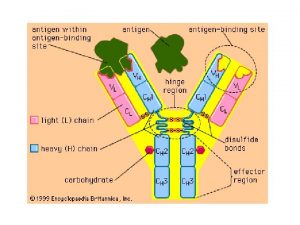
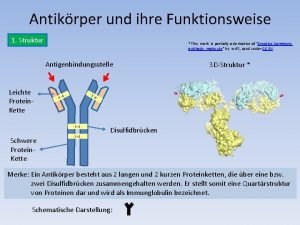
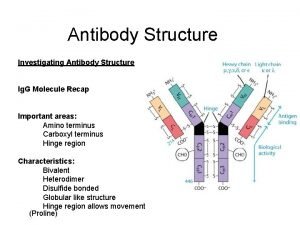
Štruktúra imunoglobulínov • • • 4 polypeptidové reťazce - 2 ľahké (Light) a 2 ťažké (Heavy) L reťazec ~ 215 aminokyselín H reťazec ~ dvojnásobok - γ (445), α (472), δ (512), ε (558), μ (576) vzájomná väzba pomocou disulfidových väzieb jedna molekula Ig má vždy identické L a H reťazce: γ (Ig. G), α (Ig. A), δ (Ig. D), ε (Ig. E), μ (Ig. M) – zatriedenie do tried L reťazce: κ (K typ), λ (L-typ) pomer κ: λ je u ľudí 65: 35, u myší 97: 3 iné reťazce: J reťazec (joining) – sekrečný Ig. A a Ig. M sekrečný komponent (SC)
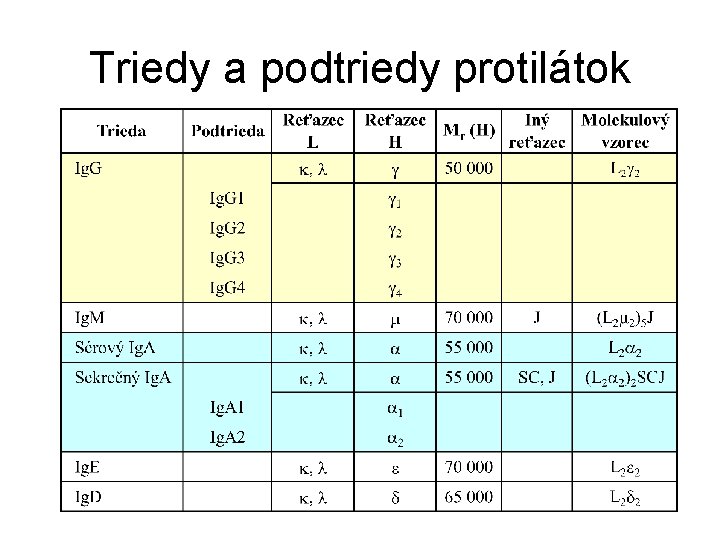
Triedy a podtriedy protilátok
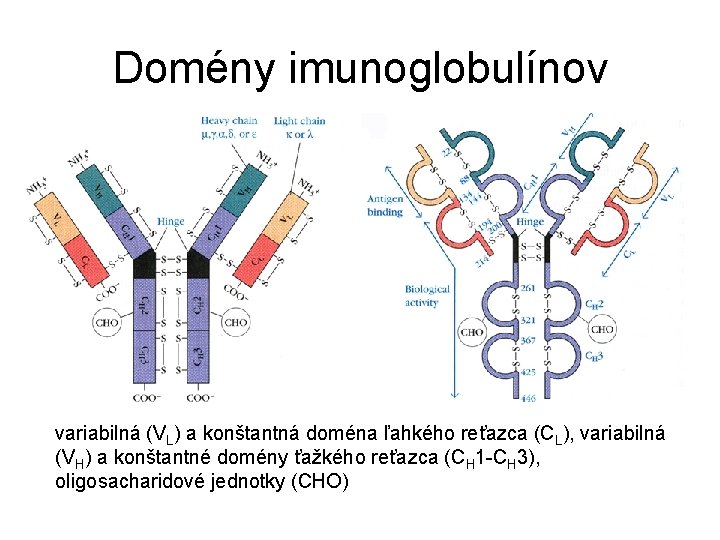
Domény imunoglobulínov variabilná (VL) a konštantná doména ľahkého reťazca (CL), variabilná (VH) a konštantné domény ťažkého reťazca (CH 1 -CH 3), oligosacharidové jednotky (CHO)

Domény imunoglobulínov • každá doména pozostáva zo 70 -110 aminokyselín • majú globulárny tvar stabilizovaný vnútroreťazcovou disulfidovou väzbou Domény: • variabilné „V“ – majú hypervariabilné úseky a v nich oblasti určujúce komplementárnosť (CDR), ktoré sa bezprostredne zúčastňujú na interakcii s antigénom a kostrové oblasti (FR – framework region) – každá V doména má 3 CDR (6 -10 aminokyselín) vytvárajúce epitop • konštantné „C“ – sekvencia aminokyselín sa nemení 3 typy domén: • 1. typ – variabilná doména L reťazca (VL), variabilná doména H reťazca (VH) • 2. typ – konštantná doména L reťazca (CL), konštantná doména H reťazca (CH 1, CH 3 a niekedy CH 4) • 3. typ – konštantná doména H reťazca (CH 2 je izolovaná, lebo vo vzájomnej interakcii im bránia postranné oligosacharidové reťazce)

Domény imunoglobulínov Pántová oblasť • oblasť so zvýšeným ohýbaním aminokyselinových reťazcov • určuje tvar (Y alebo T) • túto oblasť nemajú Ig. E a Ig. M, ale majú CH 4 doménu Disulfidové väzby • každá trieda má rôzny počet S-S väzieb • od počtu závisí možnosť rotovať Interakcie medzi doménami (vodíkové väzby a van der Waalsove sily) • longitudinálne (pozdĺžne) – vnikajú moduly VH-CH 1, VL-CL – ohýbajú dané moduly o 10 -45° • laterálne (bočné) – vnikajú moduly VH-VL, CH 1 -CL, CH 3 -CH 3 – určujú trojrozmernú štruktúru
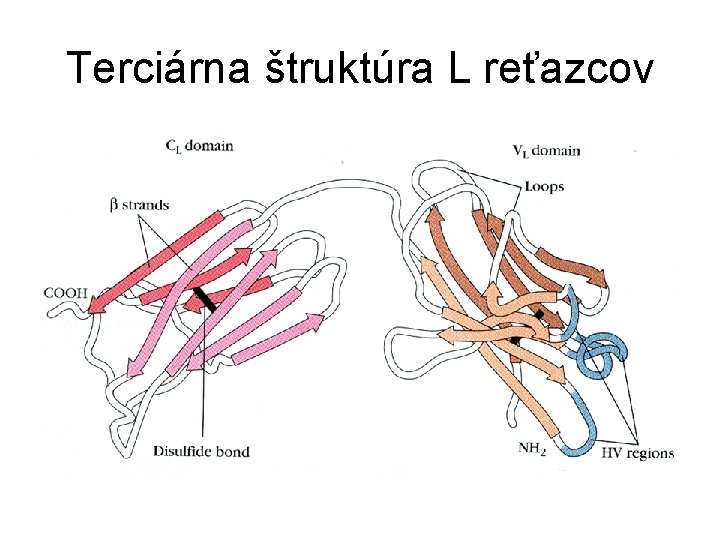
Terciárna štruktúra L reťazcov


SACHARIDOVÁ ZLOŽKA IMUNOGLOBULÍNOV GLUKOZAMÍN (Glc. N) • konštantné domény ťažkých reťazcov (CH), Mr = 2500 -3000 • N-glykozidová väzba na asparagín polypeptidového reťazca so sekvenciou Asn-X-Ser/Thr (X = akákoľvek aminokyselina) GALAKTOZAMÍN (Gal. N) • pántové oblasti ľudských Ig. A 1 a Ig. D (CH), Mr = 750 • O-glykozidová väzba na serín alebo treonín Biologické funkcie oligosacharidov • uľahčenie sekrécie a zvýšenie rozpustnosti (cez lektínové receptory) • priestorová medzera medzi reťazcami a doménami (CH 2) • prenos signálov z väzbového miesta k efektorovým doménam v Fc • väzba komplementu a cytotropné interakcie s lymfoidnými bunkami • regulácia katabolizmu (regulácia činnosti proteáz) • sprostredkovávajú väzbu protilátok na lektínové miesto na hepatocytoch
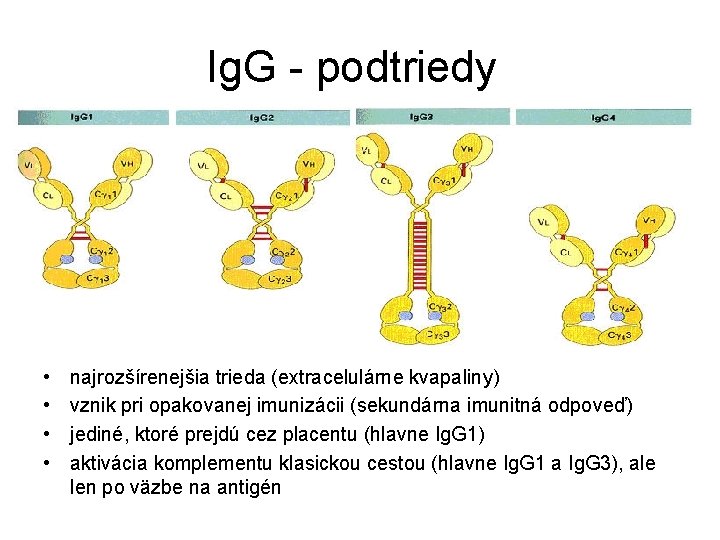
Ig. G - podtriedy • • najrozšírenejšia trieda (extracelulárne kvapaliny) vznik pri opakovanej imunizácii (sekundárna imunitná odpoveď) jediné, ktoré prejdú cez placentu (hlavne Ig. G 1) aktivácia komplementu klasickou cestou (hlavne Ig. G 1 a Ig. G 3), ale len po väzbe na antigén
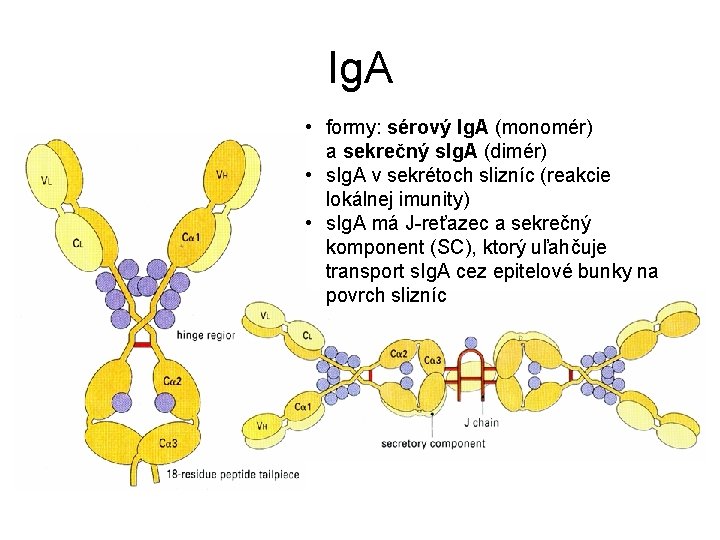
Ig. A • formy: sérový Ig. A (monomér) a sekrečný s. Ig. A (dimér) • s. Ig. A v sekrétoch slizníc (reakcie lokálnej imunity) • s. Ig. A má J-reťazec a sekrečný komponent (SC), ktorý uľahčuje transport s. Ig. A cez epitelové bunky na povrch slizníc
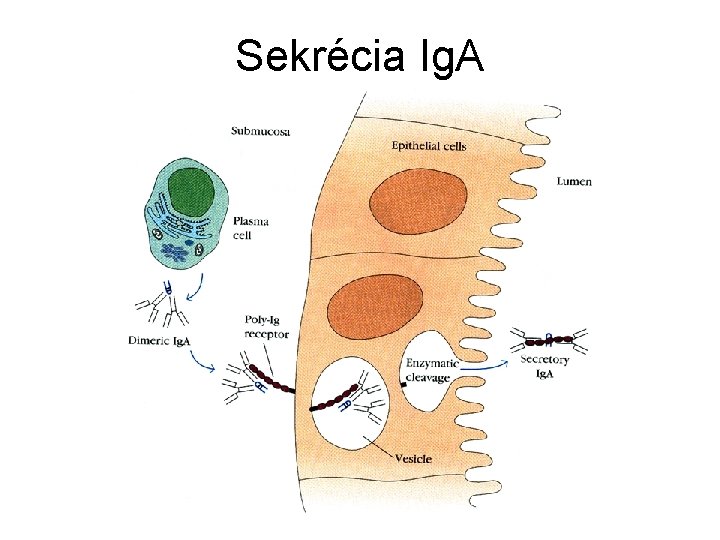
Sekrécia Ig. A
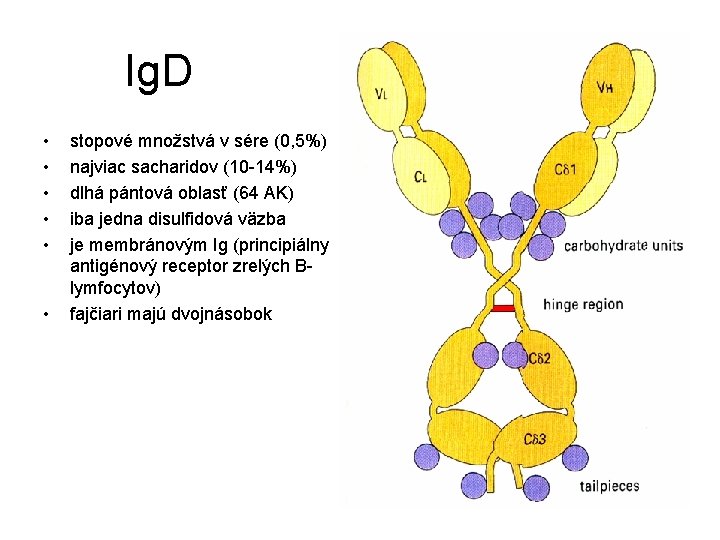
Ig. D • • • stopové množstvá v sére (0, 5%) najviac sacharidov (10 -14%) dlhá pántová oblasť (64 AK) iba jedna disulfidová väzba je membránovým Ig (principiálny antigénový receptor zrelých Blymfocytov) fajčiari majú dvojnásobok
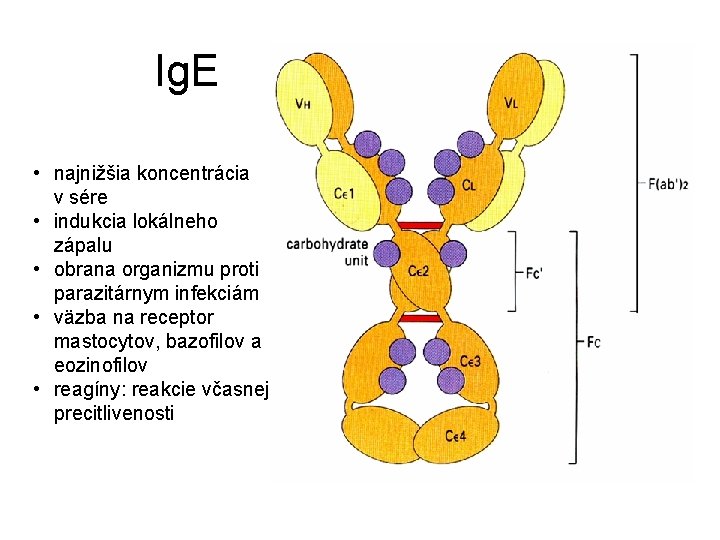
Ig. E • najnižšia koncentrácia v sére • indukcia lokálneho zápalu • obrana organizmu proti parazitárnym infekciám • väzba na receptor mastocytov, bazofilov a eozinofilov • reagíny: reakcie včasnej precitlivenosti
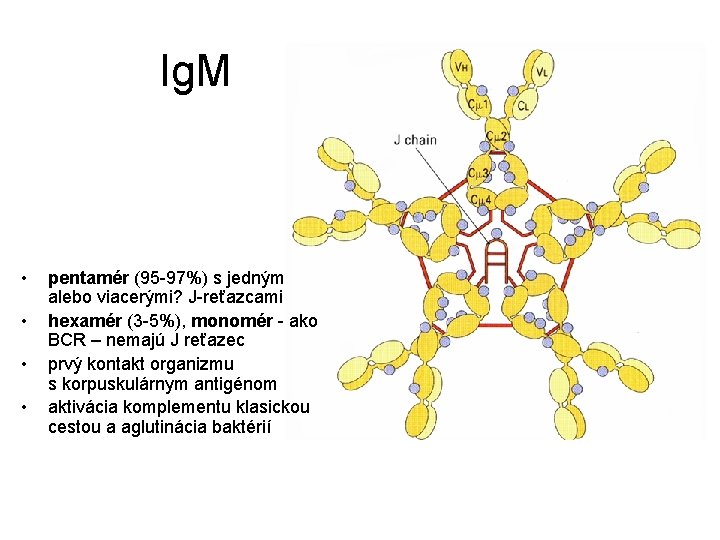
Ig. M • • pentamér (95 -97%) s jedným alebo viacerými? J-reťazcami hexamér (3 -5%), monomér - ako BCR – nemajú J reťazec prvý kontakt organizmu s korpuskulárnym antigénom aktivácia komplementu klasickou cestou a aglutinácia baktérií
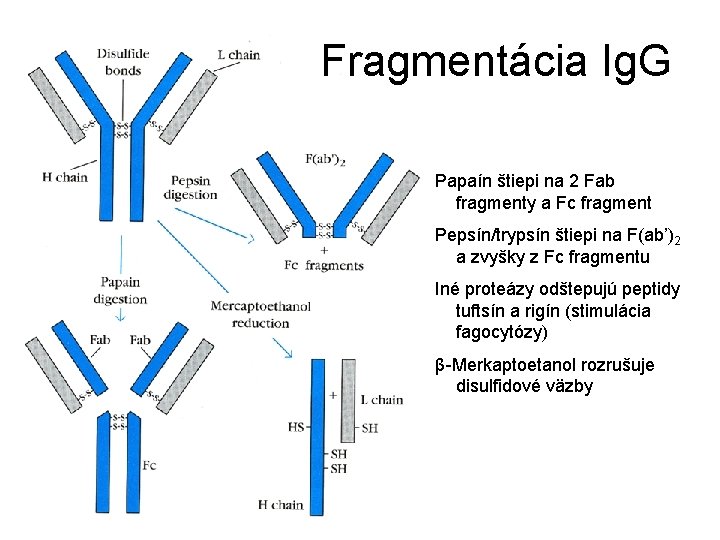
Fragmentácia Ig. G Papaín štiepi na 2 Fab fragmenty a Fc fragment Pepsín/trypsín štiepi na F(ab’)2 a zvyšky z Fc fragmentu Iné proteázy odštepujú peptidy tuftsín a rigín (stimulácia fagocytózy) β-Merkaptoetanol rozrušuje disulfidové väzby

Väzba epitop - paratop

Väzba epitop - paratop AFINITA PROTILÁTKY • sila väzby medzi jedným antigénovým determinantom (epitopom) a jedným väzbovým miestom protilátky (paratopom) AVIDITA PROTILÁTKY • sila väzby medzi celou molekulou multivalentného antigénu a protilátky VALENCIA • počet väzbových miest protilátky (paratopov) a antigénových determinantov (epitopov), prostredníctvom ktorých sa antigén môže viazať na protilátku • Ig. G, Ig. D, Ig. E, Ig. A (sérový) 2 väzbové miesta (bivalentné) • Ig. A (sekrečný) 4 väzbové miesta • Ig. M (pentamér) 10 väzbových miest (max. 5 valencií)
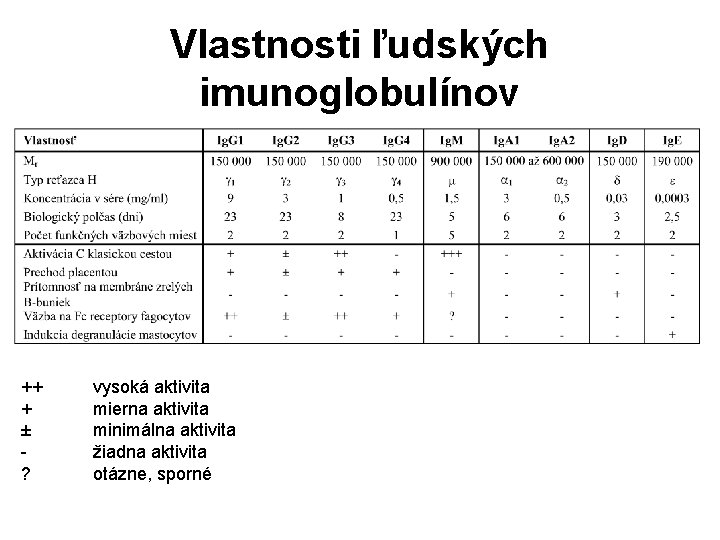
Vlastnosti ľudských imunoglobulínov ++ + ± ? vysoká aktivita mierna aktivita minimálna aktivita žiadna aktivita otázne, sporné

Biologické funkcie imunoglobulínov Rozpoznávacia • protilátková špecifickosť Výkonná (efektorová) • aktivácia komplementu • cytotropné reakcie (väzba na Fc receptor) • regulácia fagocytózy (tuftsín, rigín) • regulácia chemotaxie a respiračného vzplanutia neutrofilov a makrofágov (hlavne tuftsín) • prechod cez placentu (iba Ig. G)
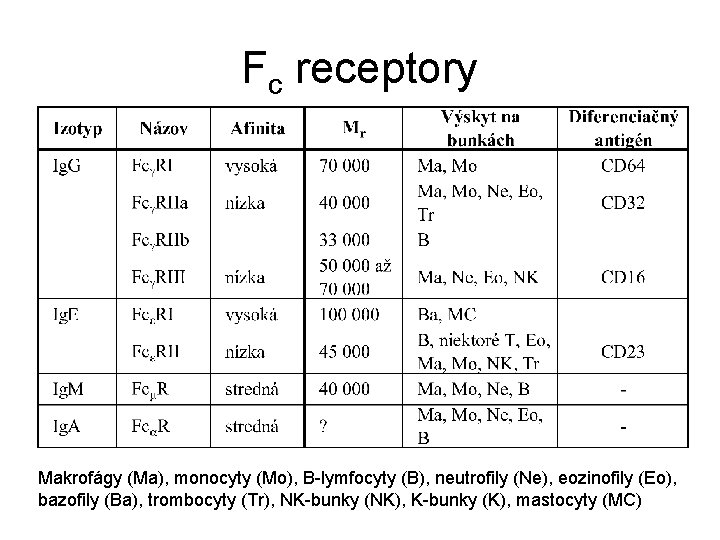
Fc receptory Makrofágy (Ma), monocyty (Mo), B-lymfocyty (B), neutrofily (Ne), eozinofily (Eo), bazofily (Ba), trombocyty (Tr), NK-bunky (NK), K-bunky (K), mastocyty (MC)
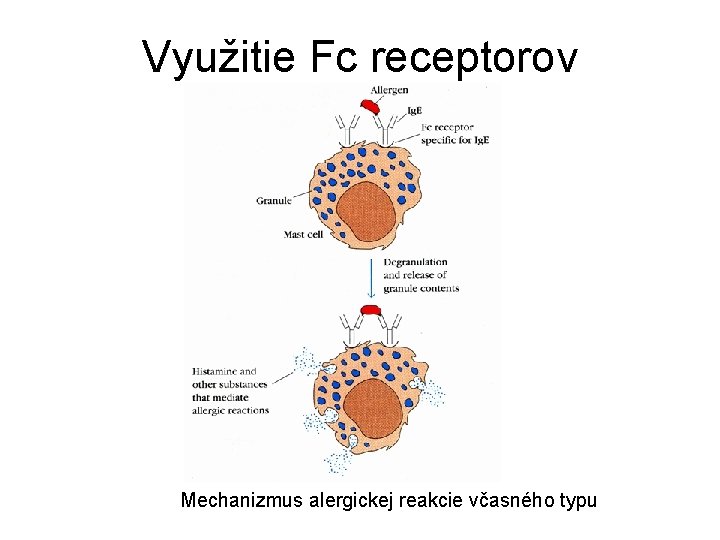
Využitie Fc receptorov Mechanizmus alergickej reakcie včasného typu

Varianty imunoglobulínov IZOTYPY • triedy resp. podtriedy (CH) a typy resp. podtypy imunoglobulínov (CL) • rovnaké u všetkých jedincov určitého živočíšneho druhu • produkty rôznych štruktúrnych génov • určujú sa pomocou xenogénnych antisér ALOTYPY • geneticky určené znaky (alotopy) v antigénovej štruktúre Ig (CH, CL) • len u niektorých jedincov určitého živočíšneho druhu • produkty rôznych alel toho istého štruktúrneho génu • význam: populačné štúdie, genetická charakterizácia jedinca, zisťovanie náchylnosti na choroby a úspešnosti alogénnej transplantácie kostnej drene IDIOTYPY • súbor determinantov v hypervariabilných úsekoch imunoglobulínov (idiotopov) vo väzbovom mieste určitej protilátky (VH, VL) • súkromné idiotypy – v organizme určitého jedinca • všeobecné alebo krížovo reagujúce idiotypy – u mnohých jedincov
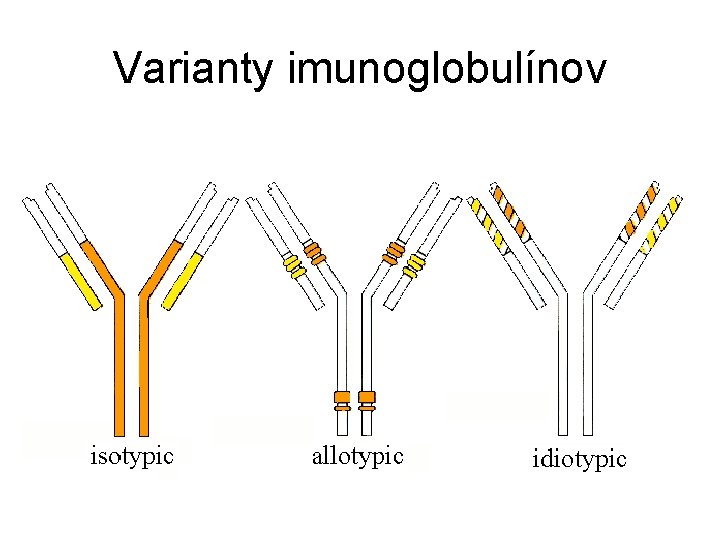
Varianty imunoglobulínov
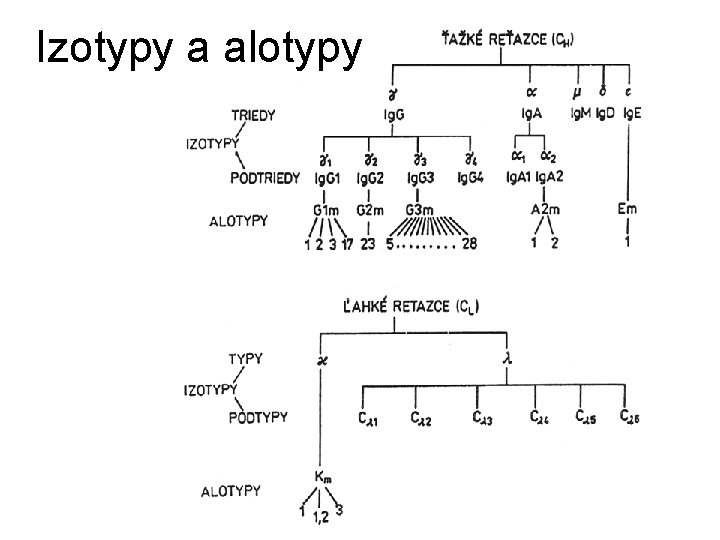
Izotypy a alotypy
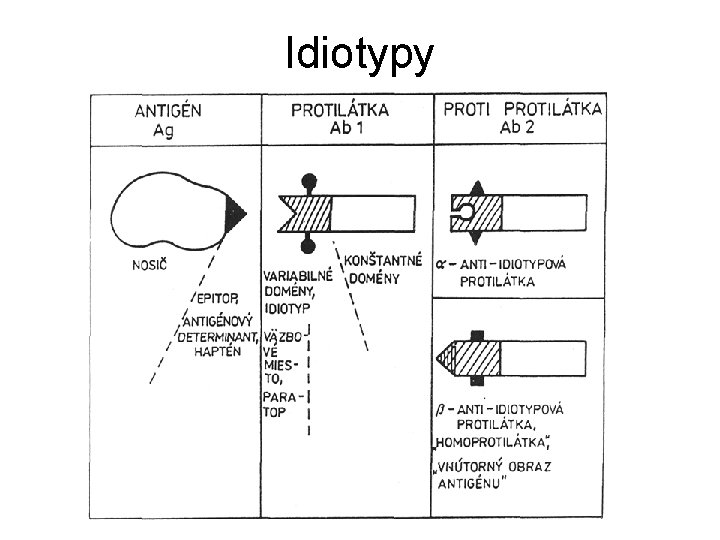
Idiotypy

Idiotypová anti-idiotypová sieť • reguluje mechanizmy humorálnej a bunkovej imunity • kontroluje výskyt protilátok po zneškodnení agensu • ďalšie proti-protilátky vznikajú v oveľa menšom množstve (o 2 -3 rády) • tvorba protilátok, keď nie sú potrebné môže vyústiť do patologických stavov
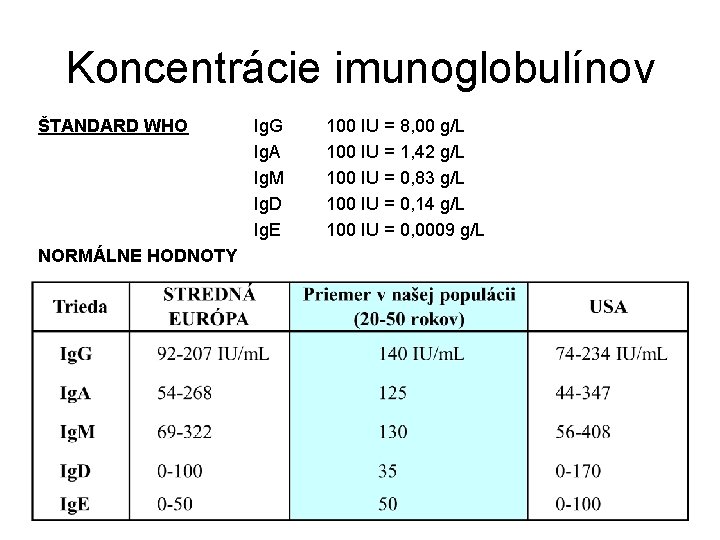
Koncentrácie imunoglobulínov ŠTANDARD WHO NORMÁLNE HODNOTY Ig. G Ig. A Ig. M Ig. D Ig. E 100 IU = 8, 00 g/L 100 IU = 1, 42 g/L 100 IU = 0, 83 g/L 100 IU = 0, 14 g/L 100 IU = 0, 0009 g/L
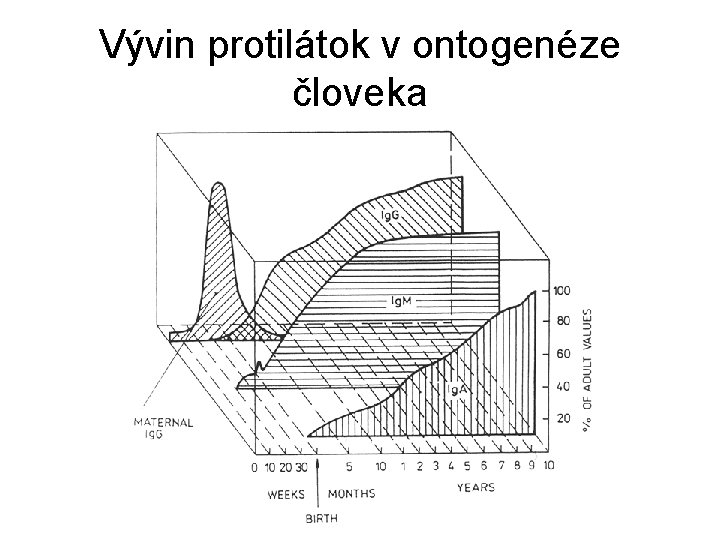
Vývin protilátok v ontogenéze človeka
- Slides: 33