Antikrper gegen Vedolizumab knnen ab Woche 2 nachgewiesen

Antikörper gegen Vedolizumab können ab Woche 2 nachgewiesen werden und verschwinden während der Therapie Bian S. 1, Tang H. T. 1, Peeters M. 1, Compernolle G. 1, Dreesen E. 1, Van Assche G. A. 2, Ferrante M. 2, Vermeire S. 2, Gils A. 1 Sa 1883, DDW-Kongress 06. – 09. Mai 2017; Chicago, United States 1 2 Department of Pharmaceutical and Pharmacological Sciences, KU Leuven, Belgium Department of Gastroenterology and Hepatology, University Hospitals Leuven, Belgium, Belgium Grafiken und Daten modifiziert nach Grafiken und Daten von Bian et al. Antibodies Towards Vedolizumab Appear from Week 2 Onwards and Disappear upon Treatment. Gastroenterology, Volume 152, Issue 5, S. 382, Abstract Sa 1883 1

Antikörpernachweis von Anti-Vedolizumab-Antikörpern durch einen Arzneimittel-resistenten Test während der Vedolizumab-Therapie Ziele und Methoden • Ziele - Entwicklung eines sensitiveren, Arzneimittel-resistenten AVA-Tests zur besseren Detektion der AVA - Bestimmung der Anzahl an Patienten mit AVA sowie Bestimmung der VDZ-Talspiegel und CRP-Werte • Hintergrund - VDZ-Talspiegel liegen während der Induktionstherapie bei >30 µg/m. L und bei >10 µg/m. L während der Erhaltungstherapie - Diese VDZ-Talspiegel machen es schwierig in Immunoassays AVA zu detektieren • Methode - Komplexbildung von AVA unter VDZ-Überschuss und Fällung des VDZ/AVA-Komplexes Ansäuerung des Präzipitats und Detektion von freien AVA unter Verwendung von biotinyliertem VDZ 20 VDZ-naive Patienten wurden zur Bestimmung des Cut-offs untersucht Die Kreuzreaktivität mit Serum von 2 AIA und 2 AAA positiven Patienten, sowie Serum mit hohen Konzentrationen des rheumatoiden Faktors (150 U/m. L) wurde untersucht • Analysen - Serumproben von 75 VDZ-Patienten (46 MC, 29 CU) wurden während der Induktion (Woche 6) und Erhaltung (Woche 22) bei AVA-positiven Patienten hinsichtlich VDZ-Talspiegel, AVA- und CRP-Level untersucht AVA = Anti-Vedolizumab-Antikörper; VDZ = Vedolizumab; AIA = Anti-Infliximab-Antikörper; AAA = Anti-Adalimumab-Antikörper; MC = Morbus Crohn; CU = Colitis ulcerosa; CRP = C-reaktives Protein Grafiken und Daten modifiziert nach Grafiken und Daten von Bian et al. , DDW-Kongress 2017, Chicago, USA, Sa 1883

Antikörpernachweis von Anti-Vedolizumab-Antikörpern durch einen Arzneimittel-resistenten Test während der Vedolizumab-Therapie Sensitivität des Arzneimittel-resistenten AVA-Tests • Die MA-VDZ 19 C 11 Dosis-abhängige Kurve umfasste einen Bereich von 25 – 1. 600 ng/m. L in einer 1/125 -Verdünnung des getesteten Serums • Der Test ermöglichte einen Nachweis von AVA-Konzentrationen bis zu 200 µg/m. L 5 Bestätigung der Arzneimittelresistenz des AVA-Tests • Zugaben von verschiedenen Mengen an VDZ zu 40 µg/m. L MA-VDZ 19 C 11 führte bei 3 Patienten zu vergleichbaren Ergebnissen - Zugabe von 1 µg/m. L VDZ: 89 ± 7 % - Zugabe von 10 µg/m. L VDZ: 90 ± 11 % - Zugabe von 100 µg/m. L VDZ: 82 ± 5 % • Die Ergebnisse bestätigen die Arzneimittelresistenz des AVA-Tests AVA = Anti-Vedolizumab-Antikörper; VDZ = Vedolizumab Grafiken und Daten modifiziert nach Grafiken und Daten von Bian et al. , DDW-Kongress 2017, Chicago, USA, Sa 1883

Antikörpernachweis von Anti-Vedolizumab-Antikörpern durch einen Arzneimittel-resistenten Test während der Vedolizumab-Therapie Vergleich zwischen den verschiedenen AVA-Tests • Unter den 75 getesteten Patienten war in den Analysen mit dem herkömmlichen AVA-Test 1 Patient (1, 3 %) mit positivem AVA-Nachweis in Woche 6 • Analysen der 75 Patienten mit dem Arzneimittel-resistenten AVA-Test zeigten, dass 4 Patienten (5, 3 %) an ≥ 2 Zeitpunkten AVA-positiv waren 5 AVA = Anti-Vedolizumab-Antikörper; VDZ = Vedolizumab Grafiken und Daten modifiziert nach Grafiken und Daten von Bian et al. , DDW-Kongress 2017, Chicago, USA, Sa 1883
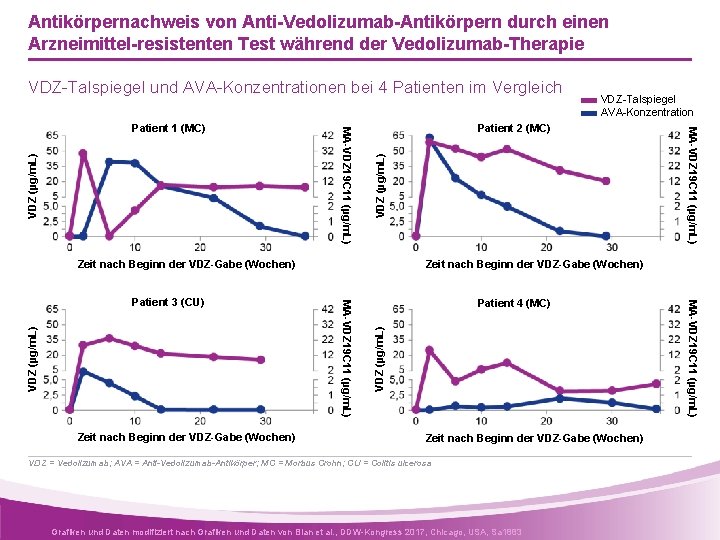
Antikörpernachweis von Anti-Vedolizumab-Antikörpern durch einen Arzneimittel-resistenten Test während der Vedolizumab-Therapie VDZ-Talspiegel und AVA-Konzentrationen bei 4 Patienten im Vergleich VDZ (µg/m. L) Patient 2 (MC) Zeit nach Beginn der VDZ-Gabe (Wochen) VDZ (µg/m. L) Patient 4 (MC) Zeit nach Beginn der VDZ-Gabe (Wochen) VDZ = Vedolizumab; AVA = Anti-Vedolizumab-Antikörper; MC = Morbus Crohn; CU = Colitis ulcerosa Grafiken und Daten modifiziert nach Grafiken und Daten von Bian et al. , DDW-Kongress 2017, Chicago, USA, Sa 1883 MA-VDZ 19 C 11 (µg/m. L) Zeit nach Beginn der VDZ-Gabe (Wochen) MA-VDZ 19 C 11 (µg/m. L) Patient 3 (CU) MA-VDZ 19 C 11 (µg/m. L) Patient 1 (MC) VDZ-Talspiegel AVA-Konzentration
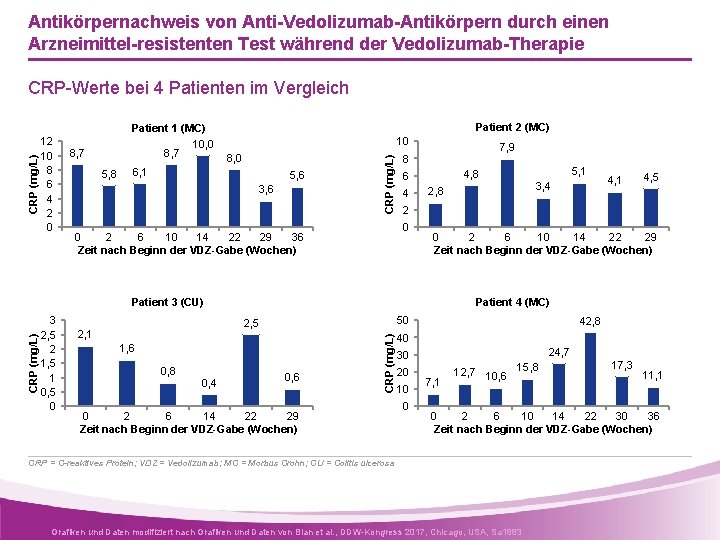
Antikörpernachweis von Anti-Vedolizumab-Antikörpern durch einen Arzneimittel-resistenten Test während der Vedolizumab-Therapie 12 10 8 6 4 2 0 Patient 1 (MC) 10, 0 8, 7 5, 8 Patient 2 (MC) 10 8, 0 6, 1 5, 6 3, 6 CRP (mg/L) CRP-Werte bei 4 Patienten im Vergleich 4, 8 6 4 2, 8 0, 4 0, 6 CRP (mg/L) 50 1, 6 0, 8 4, 1 4, 5 Patient 4 (MC) 2, 5 2, 1 3, 4 0 2 6 10 14 22 29 Zeit nach Beginn der VDZ-Gabe (Wochen) Patient 3 (CU) 3 2, 5 2 1, 5 1 0, 5 0 5, 1 2 0 0 2 6 10 14 22 29 36 Zeit nach Beginn der VDZ-Gabe (Wochen) 7, 9 8 0 2 6 14 22 29 Zeit nach Beginn der VDZ-Gabe (Wochen) 42, 8 40 24, 7 30 20 10 0 7, 1 12, 7 10, 6 15, 8 17, 3 11, 1 0 2 6 10 14 22 30 36 Zeit nach Beginn der VDZ-Gabe (Wochen) CRP = C-reaktives Protein; VDZ = Vedolizumab; MC = Morbus Crohn; CU = Colitis ulcerosa Grafiken und Daten modifiziert nach Grafiken und Daten von Bian et al. , DDW-Kongress 2017, Chicago, USA, Sa 1883

Antikörpernachweis von Anti-Vedolizumab-Antikörpern durch einen Arzneimittel-resistenten Test während der Vedolizumab-Therapie Fazit • Durch die Verwendung des Arzneimittel-resistenten AVA-Tests wurden 5, 3 % der Patienten als AVA-positiv identifiziert. • Keiner der 4 AVA-positiven Patienten benötigte eine Intensivierung der VDZ-Therapie. • Die Antikörper (AVA) erschienen ab Woche 2 und verschwanden über die Zeit, was den transienten Charakter der Antikörper bestätigt. AVA = Anti-Vedolizumab-Antikörper Grafiken und Daten modifiziert nach Grafiken und Daten von Bian et al. , DDW-Kongress 2017, Chicago, USA, Sa 1883

Entyvio® 300 mg, Pulver für ein Konzentrat zur Herstellung einer Infusionslösung Wirkstoff: Vedolizumab Zusammensetzung: Arzneilich wirksamer Bestandteil: Jede Durchstechflasche enthält 300 mg Vedolizumab; nach Rekonstitution enthält 1 ml Infusionslösung 60 mg Vedolizumab. Sonstige Bestandteile: L-Histidin, L-Histidin-Monohydrochlorid, L-Arginin-Hydrochlorid, Saccharose, Polysorbat 80. Anwendungsgebiete: Colitis ulcerosa: Behandlung von erwachsenen Patienten mittelschwerer bis schwerer aktiver Colitis ulcerosa, die entweder auf konventionelle Therapie oder einen der Tumornekrosefaktor-alpha (TNFα)-Antagonisten unzureichend angesprochen haben, nicht mehr darauf ansprechen oder eine Unverträglichkeit gegen eine entsprechende Behandlung aufweisen. Morbus Crohn: Behandlung von erwachsenen Patienten mittelschwerem bis schwerem aktiven Morbus Crohn, die entweder auf konventionelle Therapie oder einen der Tumornekrosefaktor-alpha (TNFα)-Antagonisten unzureichend angesprochen haben, nicht mehr darauf ansprechen oder eine Unverträglichkeit gegen eine entsprechende Behandlung aufweisen. Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile. Aktive schwere Infektionen wie Tuberkulose, Sepsis, Cytomegalievirus, Listeriose und opportunistische Infektionen, wie z. B. progressive multifokale Leukoenzephalopathie (PML) (siehe Abschnitt 4. 4 Fachinformation). Nebenwirkungen: Sehr häufig: Nasopharyngitis, Kopfschmerzen, Arthralgie; Häufig: Bronchitis, Gastroenteritis, Infektionen der oberen Atemwege, Grippe, Sinusitis, Pharyngitis, Parästhesie, Hypertonie, oropharyngeale Schmerzen, verstopfte Nase, Husten, anale Abszesse, Analfissur, Übelkeit, Verdauungsstörungen, Verstopfung, aufgeblähter Bauch, Blähungen, Hämorrhoiden, Hautausschlag, Juckreiz, Ekzem, Erythem, Nachtschweiß, Akne, Muskelkrämpfe, Rückenschmerzen, Muskelschwäche, Müdigkeit, Schmerzen in den Extremitäten, Fieber; Gelegentlich: Infektion der Atemwege, Vulvovaginalkandidose, Mundsoor, Follikulitis, Reizungen an der Infusionsstelle (einschl. : Schmerzen und Reizungen an der Einstichstelle), infusionsbedingte Reaktionen, Schüttelfrost, Kältegefühl. Bei einem Patienten mit Morbus Crohn wurde während der 2. Infusion ein schwerwiegendes unerwünschtes IR-Ereignis berichtet (die berichteten Symptome waren Dyspnoe, Bronchospasmus, Urtikaria, Hitzewallungen, Hautausschlag und erhöhter Blutdruck und Herzfrequenz), das mit Absetzen der Infusion und Behandlung mit Antihistaminika und intravenös verabreichtem Hydrocortison erfolgreich behandelt wurde. Infektionen: In kontroll. Studien und der Open-Label-Fortsetzungsstudie mit Vedolizumab bei Erwachsenen wurden schwerwiegende Infektionen wie Tuberkulose, Sepsis (einige mit tödlichem Ausgang), Salmonellen-Sepsis, Listerien-Meningitis und Cytomegalievirus-Colitis berichtet. Malignität: Bisherige Ergebnisse aus dem klinischen Programm lassen nicht auf ein erhöhtes Risiko für maligne Erkrankungen schließen, jedoch war das Auftreten von Krebserkrankungen gering und die langfristige Exposition war begrenzt. Langzeituntersuchungen zur Sicherheit dauern noch an. Wechselwirkungen sowie weitere Hinweise: siehe Fachinformation. Verschreibungspflichtig. EU-Zulassungsinhaber: Takeda Pharma A/S, Taastrup, Dänemark Kontaktadresse d. Pharm. Unternehmens in Deutschland: Takeda Gmb. H, Byk-Gulden-Straße 2, 78467 Konstanz, Tel. : 0800 8253325, medinfo@takeda. de. Stand: 11/2015
- Slides: 8