Gliederung 1 Einleitung 2 Geschichte 3 Vorkommen 4

























- Slides: 34


Gliederung 1. Einleitung 2. Geschichte 3. Vorkommen 4. Darstellung 5. Verwendung 6. 6. Elementares Silber 7. 7. Silberverbindungen 8. 8. Alltagsrelevanz – Schulrelevanz?

1. Einleitung • Ag (lat. argentum) • Namensgebend für Argentinien • Alchemie: Halbmond als chem. Symbol (der Mondgöttin Luna geweiht) • Cu, Ag, Au: Münzmetalle • Cu, Ag, Au und Platingruppenmetalle: Edelmetalle

2. Geschichte • 4000 v. Chr. : Silberentdeckung, Nebenprodukt bei der ägypischen Goldgewinnung • 3400 v. Chr. : Au/ Ag-Ringe als Zahlungsmittel • 700 v. Chr. : Beginn der Münzprägung in Griechenland • 16. Jh. n. Chr. : Blütezeit der mitteldeutschen Silberproduktion (Freiberg) • Um 1540: Entdeckung der Silbervorkommen in Südamerika • 19. Jh. : USA wird zweitgrößter Silberproduzent

2. Geschichte Versuch 1: Nachweis von Silber in Legierungen +1 Oxidation: Reduktion: 0 +6 +3 Chromat-Dichromat-Gleichgewicht: Fällung von schwerlöslichem Silberchromat Ag 2 Cr. O 4 (braunrot) und Silberdichromat Ag 2 Cr 2 O 7 (rot) Rautenförmige Kristalle


3. Vorkommen • Silbergehalt der Erdkruste: 0, 1 g/t (0, 1 ppm) „Silberlocke“ • Gediegen • Silbererze: Ag 2 S (Silberglanz, Argentit) Cu. Ag. S (Kupfersilberglanz) Argentit Ag. Cl (Hornsilber) • Silberhaltige Erze: Silber, kristallin Pb. S (Bleiglanz) enthält 0, 01 -1% Silber in Form von Ag 2 S Cu. Fe. S 2 (Kupferkies) Hornsilber

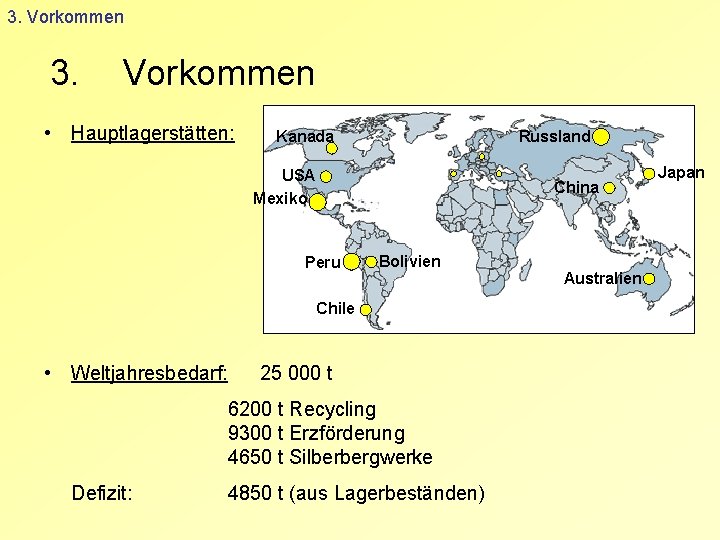
3. Vorkommen 3. Vorkommen • Hauptlagerstätten: Kanada Russland USA Mexiko China Peru Bolivien Chile • Weltjahresbedarf: 25 000 t 6200 t Recycling 9300 t Erzförderung 4650 t Silberbergwerke Defizit: 4850 t (aus Lagerbeständen) Australien Japan

4. Darstellung • Aus Silbererzen: Cyanidlaugerei Rohsilber • Aus Blei- und Kupfererzen: „Parkesieren“ „Pattinsonieren“ Kupellation Rohsilber • Feinreinigung: Elektrolytische Raffination Feinsilber • Rückgewinnung von Silber aus Sekundärrohstoffen

4. Darstellung Cyanidlaugerei • Ausgangsmaterial: Silbererze (Ag, Ag. Cl, Ag 2 S) • Gemahlenes Erz wird mit 0, 1 - 0, 2 %-iger heißer Natriumcyanidlösung unter Einblasen von Luft ausgelaugt: 0 +1 0 -0, 31 V 0 V Ag/[Ag(CN)2]- H 2/2 H+ 0, 40 V 2 OH-/O 2 (p. H 14) -2 0, 80 V Ag/Ag+

4. Darstellung Cyanidlaugerei • Hornsilber: • Silberglanz: -2 0 +6 -2 • Zementation: +1 0 +2 0 Rohsilber

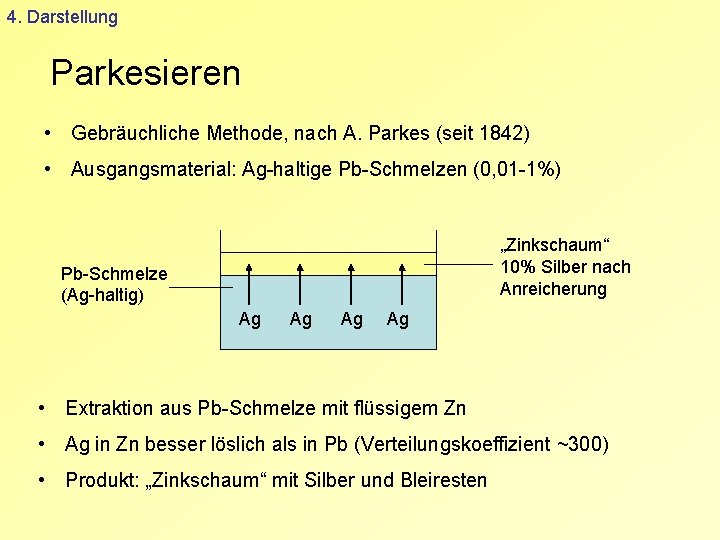
4. Darstellung Parkesieren • Gebräuchliche Methode, nach A. Parkes (seit 1842) • Ausgangsmaterial: Ag-haltige Pb-Schmelzen (0, 01 -1%) „Zinkschaum“ 10% Silber nach Anreicherung Pb-Schmelze (Ag-haltig) Ag Ag • Extraktion aus Pb-Schmelze mit flüssigem Zn • Ag in Zn besser löslich als in Pb (Verteilungskoeffizient ~300) • Produkt: „Zinkschaum“ mit Silber und Bleiresten

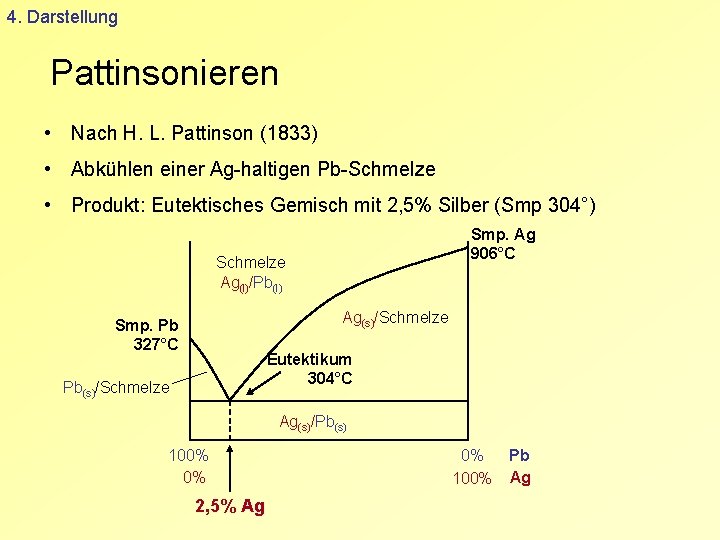
4. Darstellung Pattinsonieren • Nach H. L. Pattinson (1833) • Abkühlen einer Ag-haltigen Pb-Schmelze • Produkt: Eutektisches Gemisch mit 2, 5% Silber (Smp 304°) Smp. Ag 906°C Schmelze Ag(l)/Pb(l) Ag(s)/Schmelze Smp. Pb 327°C Eutektikum 304°C Pb(s)/Schmelze Ag(s)/Pb(s) 100% 0% 2, 5% Ag 0% 100% Pb Ag

4. Darstellung Isolierung des angereicherten Silbers: • Ausgangsmaterial: Produkte des Parkesierens bzw. Pattinsonierens • Treibarbeit („Kupellation“) überführt Pb in Pb. O, dieses wird flüssig abgezogen • Zink wird durch Destillation entfernt (Sdp. Zn: 908, 5 °C, Sdp. Ag: 2212°C) Rohsilber (95%)

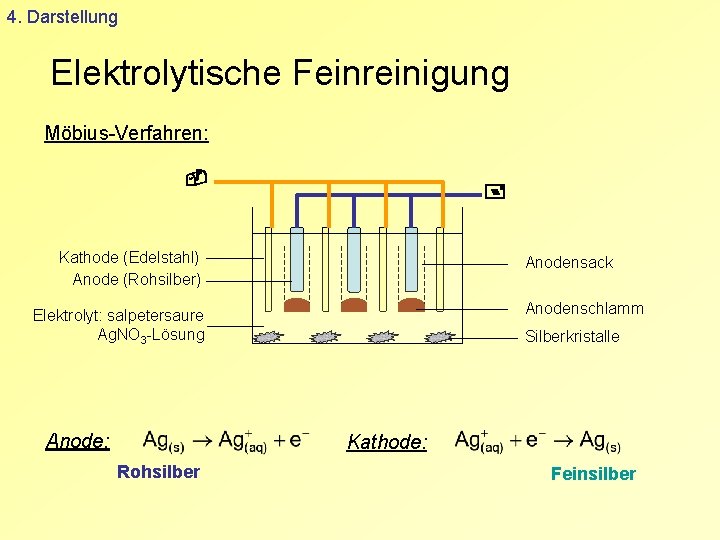
4. Darstellung Elektrolytische Feinreinigung Möbius-Verfahren: Kathode (Edelstahl) Anode (Rohsilber) Anodensack Anodenschlamm Elektrolyt: salpetersaure Ag. NO 3 -Lösung Anode: Silberkristalle Kathode: Rohsilber Feinsilber

4. Darstellung Versuch 2: Fraktale Silberstrukturen • Anode: • Kathode: -2 +1 0 0

4. Darstellung Feinsilber und Legierungen „Feinheit“ = Anteil des Silbers am Gesamtgewicht in Promille Feinsilber-Qualitäten: Feinheit 835 (83, 5 %): 835 Teile Feinsilber, 165 Teile Legierungsmetalle Feinheit 925 (92, 5 %): „Sterling-Silber“ Feinheit 999 (99, 9 %): Reines Feinsilber Preis: ca. 6 $ pro Feinunze (ca. 200 €/kg) 1 Feinunze (oz) = 31, 104 g

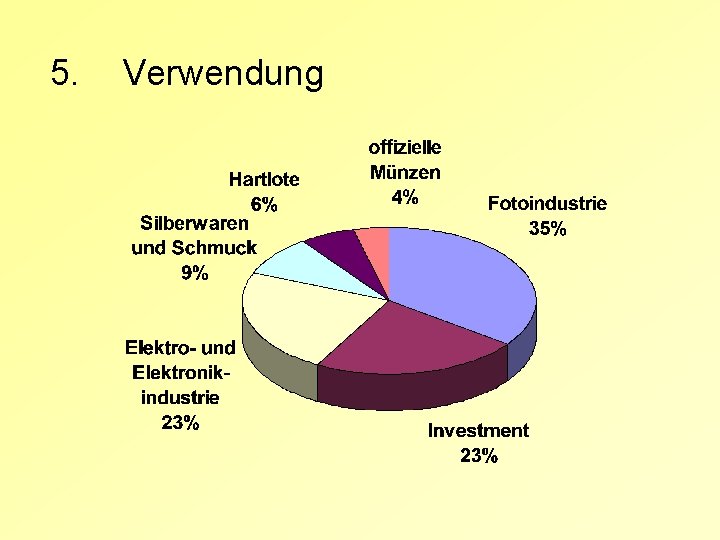
5. Verwendung

6. Elementares Silber Eigenschaften: • 1. Nebengruppe (11. Gruppe) • Isotope: 107 Ag (51, 83%) und 109 Ag (48, 17%) 47 107, 87 Ag Silber • Smp. 960, 8°C, Sdp. 2212°C • Kubisch dichteste Kugelpackung • Sehr duktil (Silberfolien, dünne Drähte) • Beste elektrische und Wärmeleitfähigkeit unter den Metallen [Kr] 4 d 10 5 s 1

6. Elementares Silber als Edelmetall • E 0 (Ag/Ag+) = +0, 7991 V • Oxidationsbeständig gegenüber Luft-O 2 • Bildung einer passivierenden, durchsichtigen Ag 2 O-Schicht (10 -20 nm) • Löst sich nur in oxidierenden Säuren (HNO 3) • „Anlaufen“ von Silber an der Luft unter Einwirkung schwefelhaltiger Spurengase

6. Elementares Silber Versuch 3: Sulfidieren einer Silbergabel • Reaktionsverlauf: 0 0 +1 -2 schwarz • Unter Einwirkung schwefelhaltiger Spurengase: 0 • 0 +1 -2 Begünstigte Adsorption und Reaktion der Spurengase an der Ag 2 O -Schicht

6. Elementares Silber Versuch 4: Reinigen einer angelaufenen Silbergabel Passivierung des Aluminiums wird aufgehoben: Oxidation des Aluminiums (E 0 (Al/Al 3+)= -1, 7 V): 0 +3 Reduktion von Ag 2 S: +1 0 Wasserstoffentwicklung: +1 0

6. Elementares Silber Antibakterielle Wirkung • Verunreinigungen (Lokalströme) und Ag 2 O-Schicht führen zur Löslichkeit des Silbers • Ag+ wirkt bakterizid, fungizid, antiseptisch • 2 g Ag+ sterilisieren 1 Mio. Kubikmeter Wasser Oligodynamische Wirkung • Wirkung: Blockade von Thioenzymen • Anwendungen: Chirurgische Instrumente Medikamente Essbesteck und -geschirr Trinkwasserreinigung

6. Elementares Silber Versuch 5: Nachweis von Silber in Trinkwasserfiltern • Trinkwasserfilter: mechanischer Filter Ionenaustauscher Aktivkohle Silber (als keimtötende Substanz) Aufschluss mit HNO 3: 0 +2 +5 0 +1 +4 -2 braun Nachweis als Ag. Cl: +2 farblos

6. Elementares Silber Versilbern • Galvanisches Versilbern von Metallgegenständen: Kathodische Abscheidung von Ag aus einer Lösung von K[Ag(CN)2] • Stromloses Versilbern: Bei unedleren Metallen möglich • Glasversilberung: Auf chemischem Wege, zur Spiegelherstellung

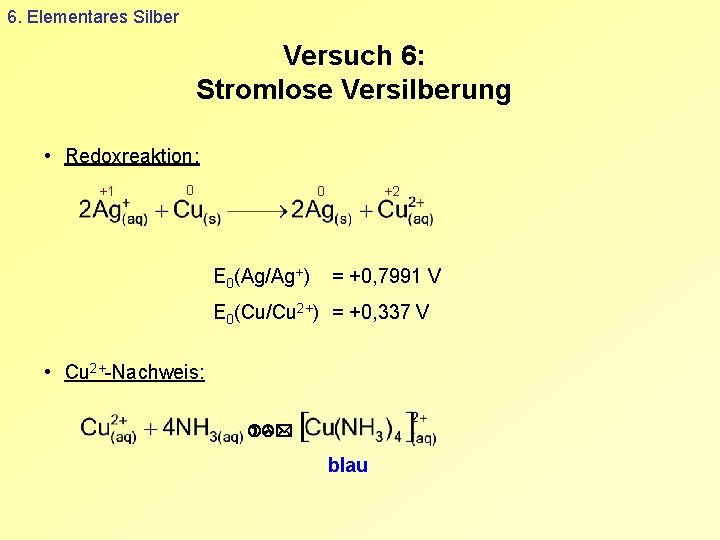
6. Elementares Silber Versuch 6: Stromlose Versilberung • Redoxreaktion: +1 0 0 E 0(Ag/Ag+) +2 = +0, 7991 V E 0(Cu/Cu 2+) = +0, 337 V • Cu 2+-Nachweis: blau

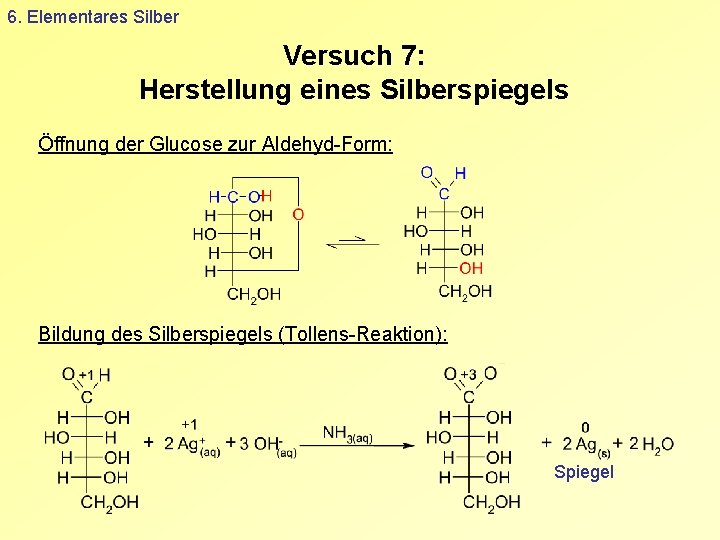
6. Elementares Silber Versuch 7: Herstellung eines Silberspiegels Öffnung der Glucose zur Aldehyd-Form: Bildung des Silberspiegels (Tollens-Reaktion): Spiegel

6. Elementares Silber Spiegelherstellung – Historisches • Altes Ägypten: polierte Bronze- und Kupferspiegel • Die Römer: Glas mit Gold und Lack beschichtet • Mittelalter (ab 13. Jh. ): Zinn-Amalgam-Spiegel • 1835, Justus v. Liebig: Silberspiegel • Heute: Silberspiegel mit Schutzschicht aus Kupfer oder nur mit Schutzlack

7. Silberverbindungen • Stabilste Oxidationsstufe: +1 • Oxidationsstufen +2, +3 sind selten (Bsp. : Ag. IIF 2, Ag. IIIO 2) • Elektronenkonfiguraton des Ag+: 4 d 10 • Farblos und diamagnetisch • Koordinationszahl in Ag(I)-Komplexen: 2 (lineare Anordnung der Liganden, Bsp. : [Ag(CN)2]-) • Lösliche Ag(I)-Salze: Ag. F, Ag. NO 3, Ag. Cl. O 4 • Der Rest: schwerlöslich (relevant: Silberhalogenide)

7. Silberverbindungen Silbernitrat – Ag. NO 3 • Wichtigstes Silbersalz • Ausgangsprodukt zur Herstellung aller anderen Silberverbindungen • Gut wasserlöslich (215 g/100 g Wasser bei 20°C) • Darstellung: Auflösen von Silber in Salpetersäure: 0 +5 +1 +2 • Wirkt auf der Haut oxidierend und ätzend, bildet schwarze Flecken. „Höllenstein“: Anwendung in der Medizin zur Entfernung von Warzen und Wucherungen Bildung von Ag (schwarz) und HNO 3

7. Silberverbindungen Schwerlösliche Silberhalogenide Darstellung: - Aus den Elementen - Durch Fällung aus Ag. NO 3 -Lösung mittels Halogenid Eigenschaften: Farbe Löslichkeitsprodukt KL [mol 2/L 2] Ag. Cl Weiß 1, 7 · 10 -10 Ag. Br Hellgelb 5 · 10 -13 Ag. I 8, 5 · 10 -17 Gelb • Kovalenter Charakter nimmt mit zunehmender OZ zu (HSAB): abnehmende Löslichkeit Farbvertiefung (Charge-Transfer) • Lichtempfindlichkeit

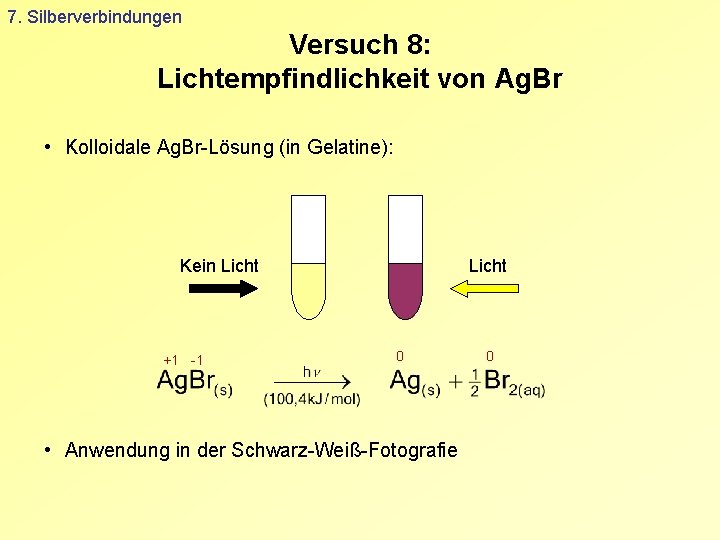
7. Silberverbindungen Versuch 8: Lichtempfindlichkeit von Ag. Br • Kolloidale Ag. Br-Lösung (in Gelatine): Kein Licht +1 -1 Licht 0 • Anwendung in der Schwarz-Weiß-Fotografie 0

8. Alltagsrelevanz – Schulrelevanz? Akkumulatoren Fotografie Recycling (Röntgenfilme, Elektroschrott) Elektronik, Elektrotechnik Haushalt (Trinkwasserfilter, Besteck) Schmuck Medizin
