Fondamenti di chimica organica Janice Gorzynski Smith University
















- Slides: 29

Fondamenti di chimica organica Janice Gorzynski Smith University of Hawai’i Capitolo 14 Coniugazione, risonanza e dieni Prepared by Rabi Ann Musah State University of New York at Albany Copyright © The Mc. Graw-Hill Companies, Inc. Permission required for reproduction or display. J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8 1

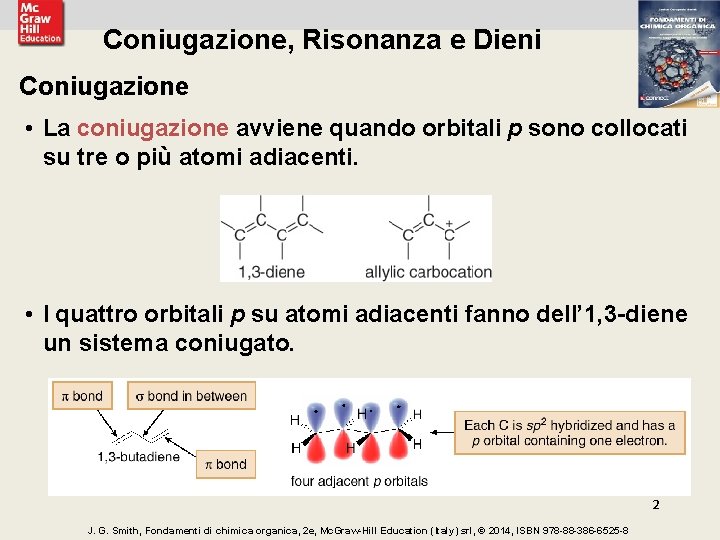
Coniugazione, Risonanza e Dieni Coniugazione • La coniugazione avviene quando orbitali p sono collocati su tre o più atomi adiacenti. • I quattro orbitali p su atomi adiacenti fanno dell’ 1, 3 -diene un sistema coniugato. 2 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Coniugazione • Avere tre o più orbitali p su atomi adiacenti permette la sovrapposizione degli orbitali p e la delocalizzazione degli elettroni. 3 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Coniugazione • L’ 1, 4 -pentadiene è un diene isolato. • I legami nell’ 1, 4 -pentadiene sono troppo lontani tra loro per essere coniugati. 4 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Coniugazione • Il carbocatione allilico è un altro esempio di sistema coniugato. • La coniugazione stabilizza il carbocatione allilico. 5 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Coniugazione • Disegnare le strutture di risonanza per il carbocatione allilico è un modo di utilizzare le strutture di Lewis per mostrare come la coniugazione delocalizza gli elettroni. • Il vero carbocatione allilico è un ibrido delle due strutture di risonanza. • Nell’ibrido, la carica positiva è delocalizzata su due atomi di carbonio terminali. • La delocalizzazione della densità elettronica abbassa l’energia dell’ibrido, stabilizzando il carbocatione allilico e rendendolo più stabile di un normale carbocatione 1°. 6 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Coniugazione • Dati sperimentali mostrano che la stabilità del carbocatione allilico è paragonabile a quella di un carbocatione 2° polisostituito. 7 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

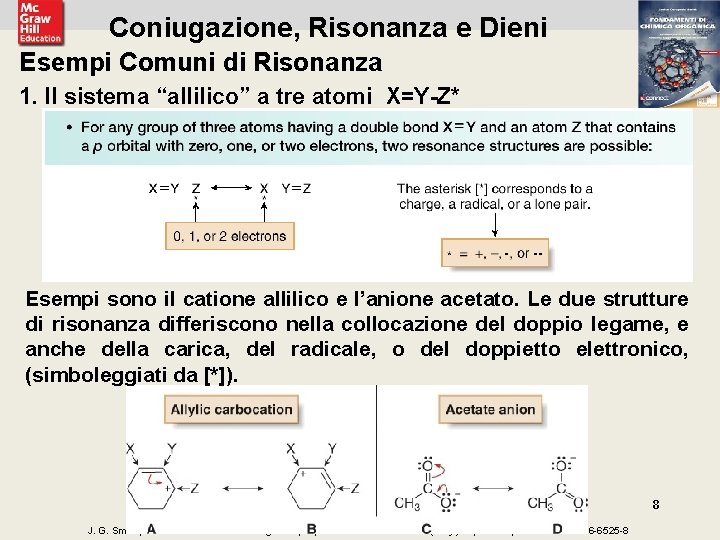
Coniugazione, Risonanza e Dieni Esempi Comuni di Risonanza 1. Il sistema “allilico” a tre atomi X=Y-Z* Esempi sono il catione allilico e l’anione acetato. Le due strutture di risonanza differiscono nella collocazione del doppio legame, e anche della carica, del radicale, o del doppietto elettronico, (simboleggiati da [*]). 8 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Esempi Comuni di Risonanza 2. Doppi legami coniugati • Composti ciclici, completamente coniugati, come il benzene, hanno due strutture di risonanza, disegnate muovendo gli elettroni in circolo intorno all’anello. • Per altri dieni coniugati possono essere disegnate tre strutture di risonanza, due delle quali comportano separazione di carica. 9 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Esempi Comuni di Risonanza 3. Cationi con una carica positiva adiacente a un doppietto elettronico La carica totale è la stessa nelle due strutture di risonanza. Basandosi sulla carica formale, un gruppo X neutro in una struttura deve portare una carica (+) nell’altra. 10 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

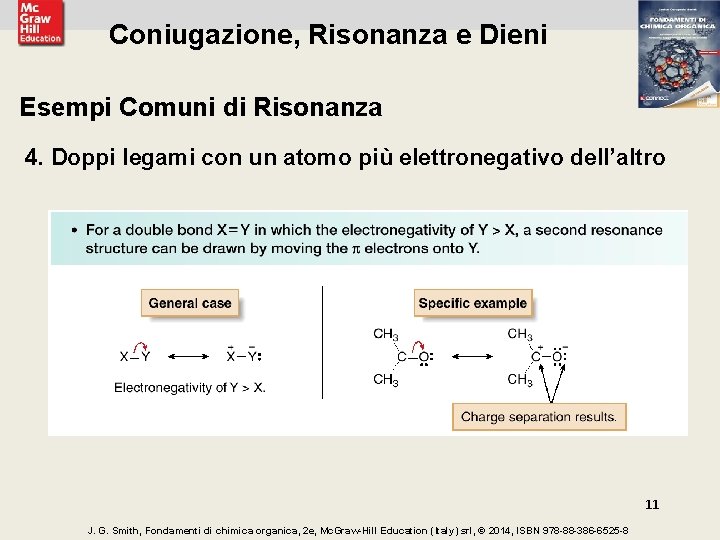
Coniugazione, Risonanza e Dieni Esempi Comuni di Risonanza 4. Doppi legami con un atomo più elettronegativo dell’altro 11 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

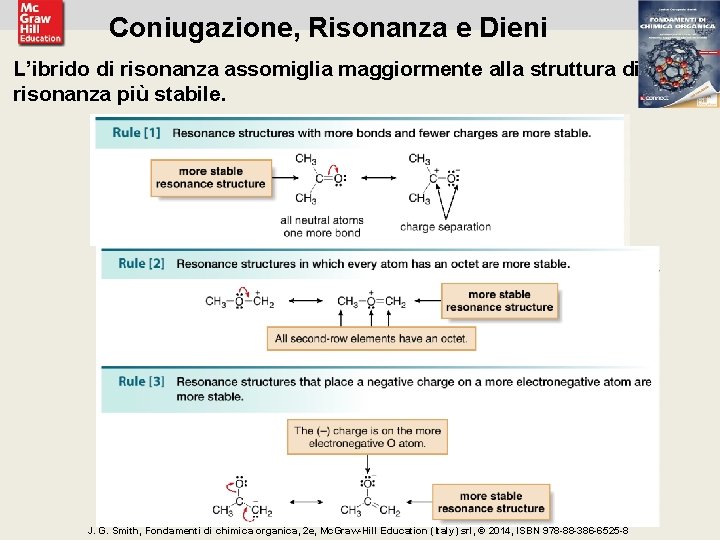
Coniugazione, Risonanza e Dieni L’ibrido di risonanza assomiglia maggiormente alla struttura di risonanza più stabile. 12 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

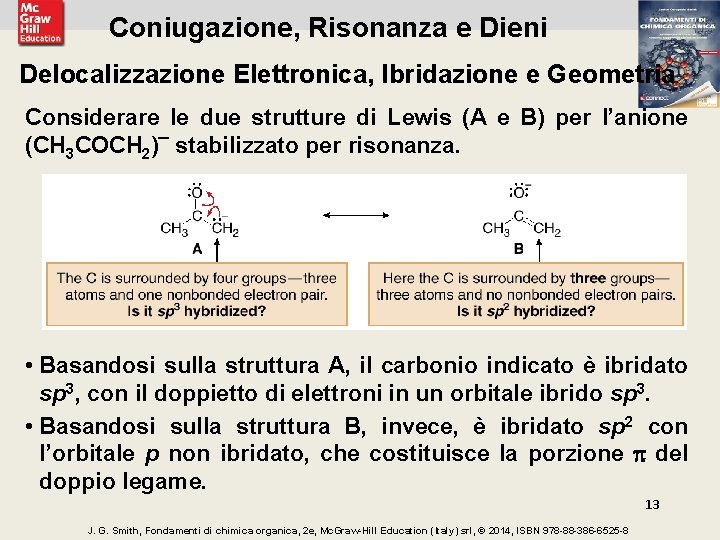
Coniugazione, Risonanza e Dieni Delocalizzazione Elettronica, Ibridazione e Geometria Considerare le due strutture di Lewis (A e B) per l’anione (CH 3 COCH 2)¯ stabilizzato per risonanza. • Basandosi sulla struttura A, il carbonio indicato è ibridato sp 3, con il doppietto di elettroni in un orbitale ibrido sp 3. • Basandosi sulla struttura B, invece, è ibridato sp 2 con l’orbitale p non ibridato, che costituisce la porzione del doppio legame. 13 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Delocalizzazione Elettronica, Ibridazione e Geometria • Il doppietto elettronico, su un atomo di carbonio adiacente al gruppo C=O, può essere delocalizzato se ha un orbitale p che si può sovrapporre a due altri orbitali p su due atomi adiacenti. Quindi l’atomo di carbonio terminale è ibridato sp 2 con geometria trigonale planare. • Tre orbitali p adiacenti formano un anione coniugato. 14 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

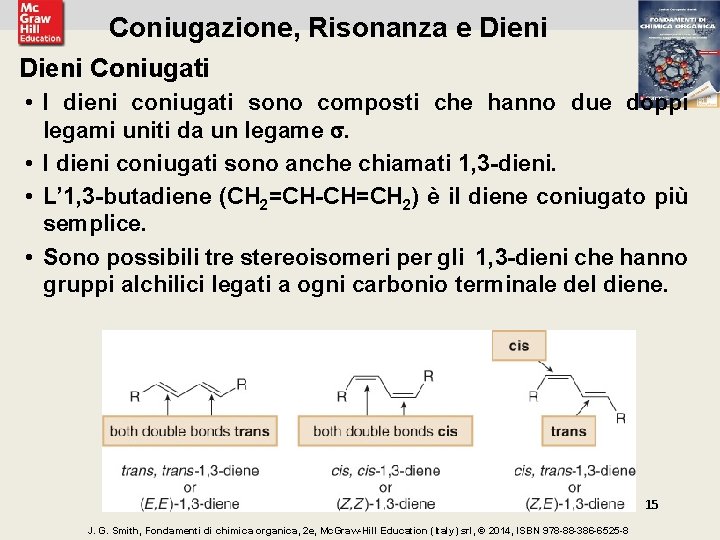
Coniugazione, Risonanza e Dieni Coniugati • I dieni coniugati sono composti che hanno due doppi legami uniti da un legame . • I dieni coniugati sono anche chiamati 1, 3 -dieni. • L’ 1, 3 -butadiene (CH 2=CH-CH=CH 2) è il diene coniugato più semplice. • Sono possibili tre stereoisomeri per gli 1, 3 -dieni che hanno gruppi alchilici legati a ogni carbonio terminale del diene. 15 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

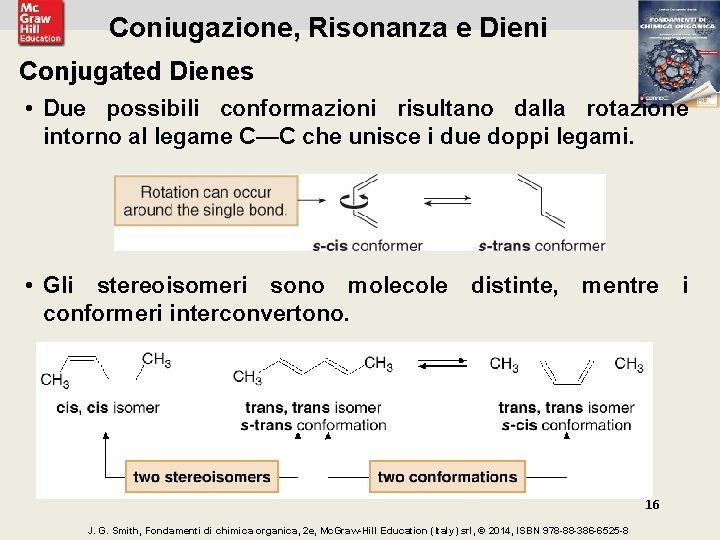
Coniugazione, Risonanza e Dieni Conjugated Dienes • Due possibili conformazioni risultano dalla rotazione intorno al legame C—C che unisce i due doppi legami. • Gli stereoisomeri sono molecole distinte, mentre i conformeri interconvertono. 16 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

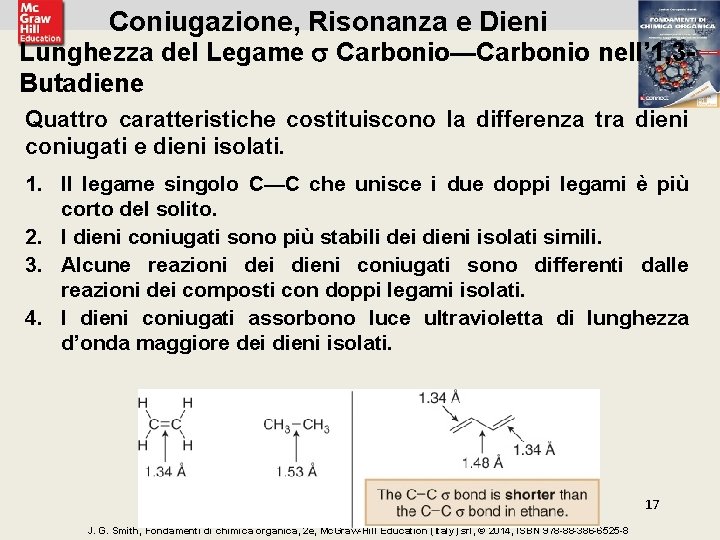
Coniugazione, Risonanza e Dieni Lunghezza del Legame Carbonio—Carbonio nell’ 1, 3 Butadiene Quattro caratteristiche costituiscono la differenza tra dieni coniugati e dieni isolati. 1. Il legame singolo C—C che unisce i due doppi legami è più corto del solito. 2. I dieni coniugati sono più stabili dei dieni isolati simili. 3. Alcune reazioni dei dieni coniugati sono differenti dalle reazioni dei composti con doppi legami isolati. 4. I dieni coniugati assorbono luce ultravioletta di lunghezza d’onda maggiore dei dieni isolati. 17 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

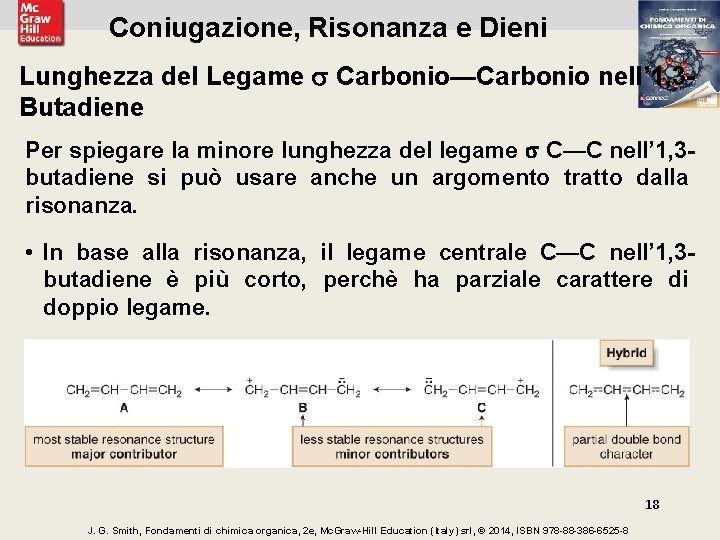
Coniugazione, Risonanza e Dieni Lunghezza del Legame Carbonio—Carbonio nell’ 1, 3 Butadiene Per spiegare la minore lunghezza del legame C—C nell’ 1, 3 butadiene si può usare anche un argomento tratto dalla risonanza. • In base alla risonanza, il legame centrale C—C nell’ 1, 3 butadiene è più corto, perchè ha parziale carattere di doppio legame. 18 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Addizione Elettrofila : Addizione 1, 2 e 1, 4. • I legami nei dieni coniugati danno reazioni di addizione, che differiscono per due ragioni dalle reazioni di addizione ai doppi legami isolati. 1. L’addizione elettrofila nei dieni coniugati dà una miscela di prodotti. 2. I dieni coniugati danno una reazione di addizione particolare, che non avviene né con gli alcheni, né con i dieni isolati. • Ricordare che l’addizione elettrofila di un equivalente di HBr ad un diene isolato dà un prodotto e segue la regola di Markovnikov. 19 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Addizione Elettrofila : Addizione 1, 2 e 1, 4. • Con un diene coniugato, l’addizione elettrofila di un equivalente di HBr dà due prodotti. • Il prodotto di addizione 1, 2 deriva da un’addizione secondo Markovnikov di HBr su due atomi di carbonio adiacenti (C 1 e C 2) del diene. • Il prodotto di addizione 1, 4 deriva da un’addizione di HBr su due atomi di carbonio terminali (C 1 e C 4) del diene. L’addizione 1, 4 è anche chiamata addizione coniugata. • Le estremità dell’ 1, 3 -diene sono chiamate arbitrariamente C 1 20 e C 4, indipendentemente dalla nomenclatura IUPAC. J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Addizione Elettrofila : Addizione 1, 2 e 1, 4. L’addizione di HX a un diene coniugato forma prodotti di addizione 1, 2 e 1, 4 a causa dell’intermedio carbocationico allilico stabilizzato 21 per risonanza. J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Prodotti a Controllo Cinetico e Termodinamico • La quantità di prodotti di addizione 1, 2 e 1, 4 formati nelle addizioni elettrofile ai dieni coniugati dipende molto dalle condizioni di reazione. 22 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

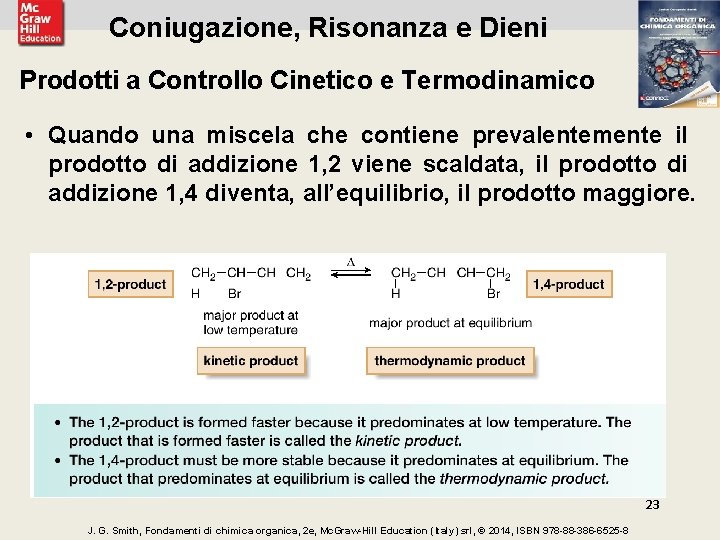
Coniugazione, Risonanza e Dieni Prodotti a Controllo Cinetico e Termodinamico • Quando una miscela che contiene prevalentemente il prodotto di addizione 1, 2 viene scaldata, il prodotto di addizione 1, 4 diventa, all’equilibrio, il prodotto maggiore. 23 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Prodotti a Controllo Cinetico e Termodinamico • Nelle reazioni studiate il prodotto più stabile è anche formato più velocemente, cioè il prodotto cinetico e il prodotto termodinamico sono lo stesso composto. • L’addizione elettrofila di HBr all’ 1, 3 -butadiene è differente, perchè il prodotto più stabile è formato più lentamente, cioè i prodotti cinetico e termodinamico sono differenti. • Perchè il prodotto più stabile si forma più lentamente? 24 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

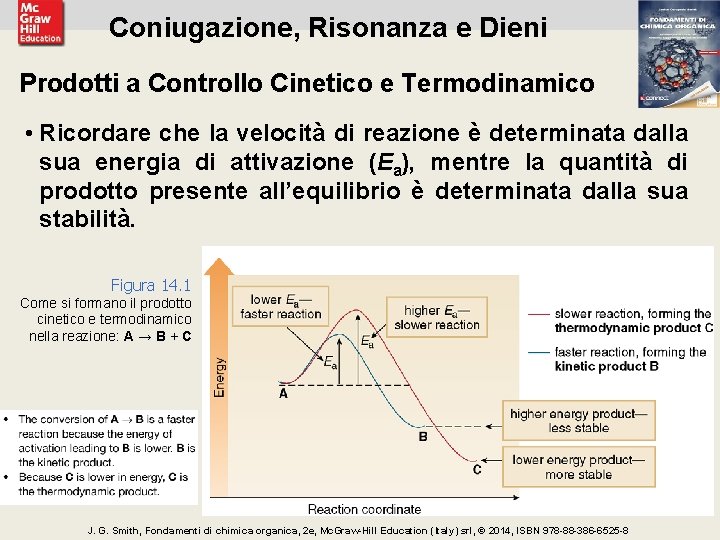
Coniugazione, Risonanza e Dieni Prodotti a Controllo Cinetico e Termodinamico • Ricordare che la velocità di reazione è determinata dalla sua energia di attivazione (Ea), mentre la quantità di prodotto presente all’equilibrio è determinata dalla sua stabilità. Figura 14. 1 Come si formano il prodotto cinetico e termodinamico nella reazione: A → B + C 25 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni Prodotti a Controllo Cinetico e Termodinamico • Il prodotto 1, 4 (1 -bromo-2 -butene) è più stabile perchè ha due gruppi alchilici legati al doppio legame carbonio, mentre il prodotto 1, 2 (3 -bromo-1 -butene) ne ha uno solo. 26 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

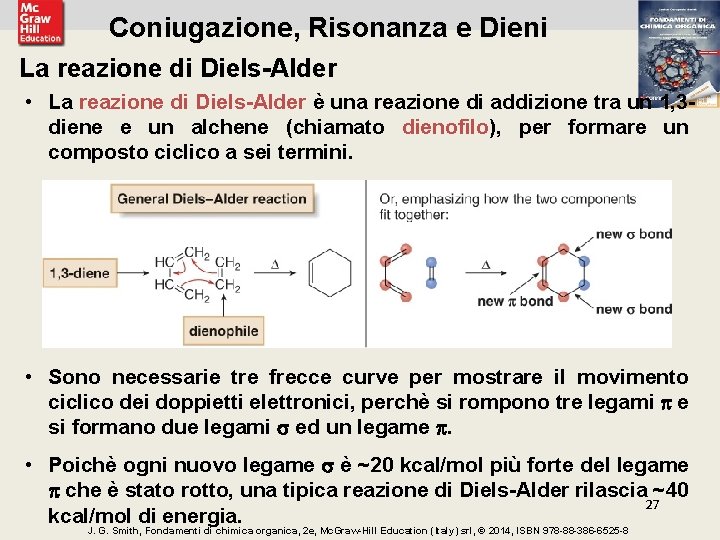
Coniugazione, Risonanza e Dieni La reazione di Diels-Alder • La reazione di Diels-Alder è una reazione di addizione tra un 1, 3 diene e un alchene (chiamato dienofilo), per formare un composto ciclico a sei termini. • Sono necessarie tre frecce curve per mostrare il movimento ciclico dei doppietti elettronici, perchè si rompono tre legami e si formano due legami ed un legame . • Poichè ogni nuovo legame è ~20 kcal/mol più forte del legame che è stato rotto, una tipica reazione di Diels-Alder rilascia ~40 27 kcal/mol di energia. J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

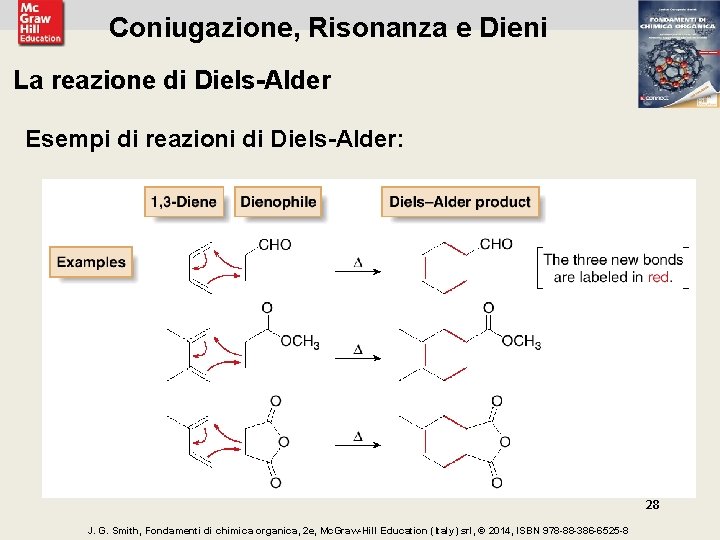
Coniugazione, Risonanza e Dieni La reazione di Diels-Alder Esempi di reazioni di Diels-Alder: 28 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8

Coniugazione, Risonanza e Dieni La reazione di Diels-Alder Tutte le reazioni di Diels-Alder hanno in comune le seguenti caratteristiche: 1. Sono iniziate dal calore; ciò significa che la reazione di Diels-Alder è una reazione termica. 2. Formano nuovi cicli a sei termini. 3. Si rompono tre legami C—C e si formano due nuovi legami C—C e un nuovo legame C—C. 4. Il meccanismo è concertato; cioè tutti i vecchi legami si rompono e tutti i nuovi legami si formano in un solo stadio. 29 J. G. Smith, Fondamenti di chimica organica, 2 e, Mc. Graw-Hill Education (Italy) srl, © 2014, ISBN 978 -88 -386 -6525 -8