Fondamenti di chimica organica Janice Gorzynski Smith University





- Slides: 18

Fondamenti di chimica organica Janice Gorzynski Smith University of Hawai’i Capitolo 12 Ossidazione e riduzione Prepared by Rabi Ann Musah State University of New York at Albany Copyright © The Mc. Graw-Hill Companies, Inc. Permission required for reproduction or display. Fondamenti di chimica organica Janice Gorzynski Smith 1 Copyright © 2009 – The Mc. Graw-Hill Companies srl

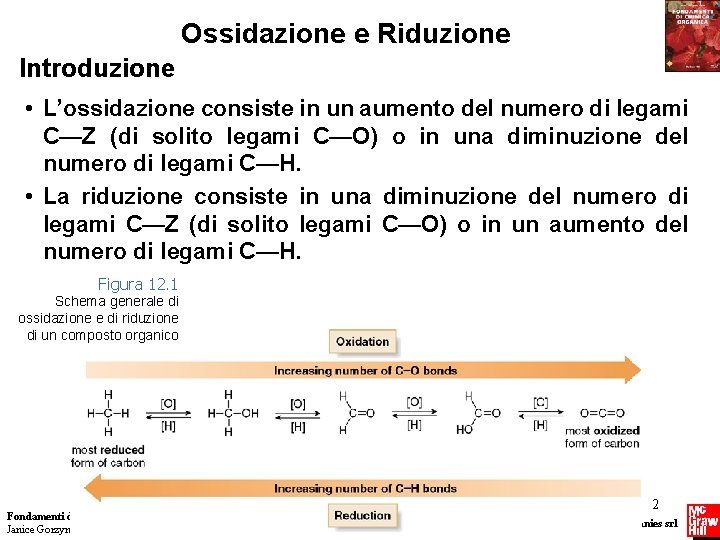
Ossidazione e Riduzione Introduzione • L’ossidazione consiste in un aumento del numero di legami C—Z (di solito legami C—O) o in una diminuzione del numero di legami C—H. • La riduzione consiste in una diminuzione del numero di legami C—Z (di solito legami C—O) o in un aumento del numero di legami C—H. Figura 12. 1 Schema generale di ossidazione e di riduzione di un composto organico Fondamenti di chimica organica Janice Gorzynski Smith 2 Copyright © 2009 – The Mc. Graw-Hill Companies srl

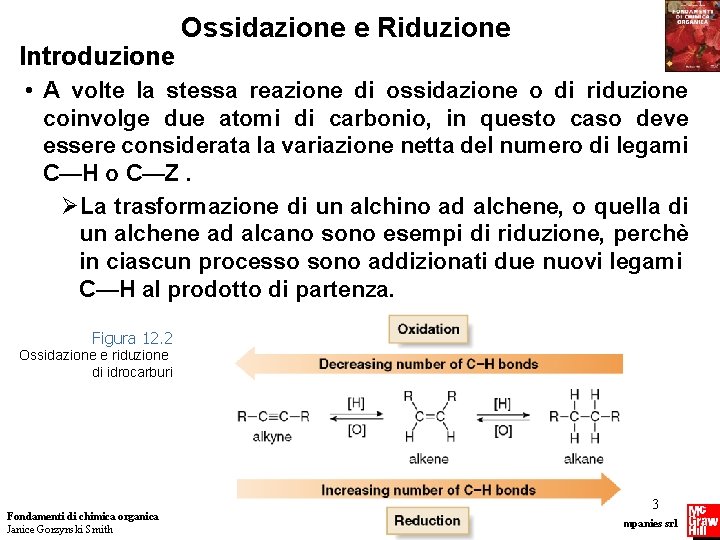
Introduzione Ossidazione e Riduzione • A volte la stessa reazione di ossidazione o di riduzione coinvolge due atomi di carbonio, in questo caso deve essere considerata la variazione netta del numero di legami C—H o C—Z. ØLa trasformazione di un alchino ad alchene, o quella di un alchene ad alcano sono esempi di riduzione, perchè in ciascun processo sono addizionati due nuovi legami C—H al prodotto di partenza. Figura 12. 2 Ossidazione e riduzione di idrocarburi Fondamenti di chimica organica Janice Gorzynski Smith 3 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Ossidazione e Riduzione Agenti Riducenti • Esistono tre tipi di riduzioni, che differiscono nel numero di H 2 aggiunto. • L’agente riducente più semplice è H 2. Riduzioni di questo tipo sono condotte in presenza di un catalizzatore metallico. • Un secondo modo è l’aggiunta a un substrato di due protoni e due elettroni, cioè H 2 = 2 H+ + 2 e-. ØRiduzioni di questo tipo usano metalli alcalini come sorgente di elettroni e ammoniaca liquida come sorgente di protoni. ØQueste sono dette riduzioni con metallo in soluzione. Fondamenti di chimica organica Janice Gorzynski Smith 4 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Ossidazione e Riduzione Agenti Riducenti • Il terzo modo per addizionare H 2 è l’aggiunta di un idruro (H¯) e di un protone (H+). • I più comuni agenti riducenti contengono un atomo di idrogeno legato al boro o all’alluminio. Esempi sono il sodio boroidruro (Na. BH 4) e il litio alluminio idruro (Li. Al. H 4). • Na. BH 4 e Li. Al. H 4 cedono H¯ al substrato, mentre il protone è fornito da H 2 O o da un alcol. Fondamenti di chimica organica Janice Gorzynski Smith 5 Copyright © 2009 – The Mc. Graw-Hill Companies srl

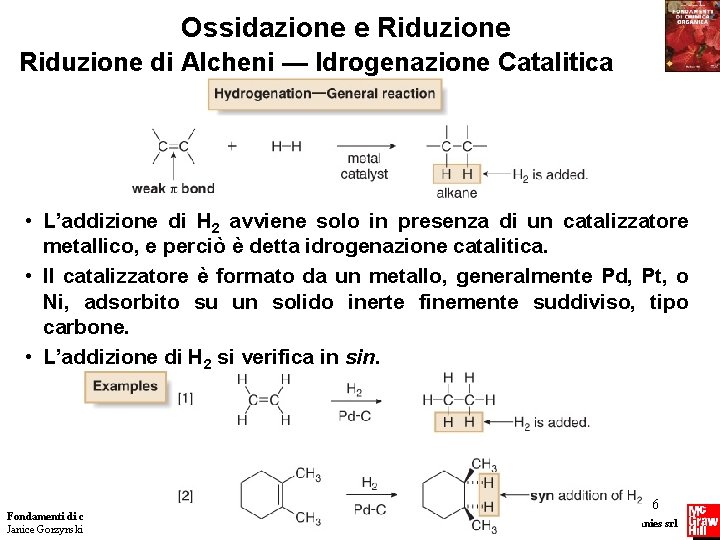
Ossidazione e Riduzione di Alcheni — Idrogenazione Catalitica • L’addizione di H 2 avviene solo in presenza di un catalizzatore metallico, e perciò è detta idrogenazione catalitica. • Il catalizzatore è formato da un metallo, generalmente Pd, Pt, o Ni, adsorbito su un solido inerte finemente suddiviso, tipo carbone. • L’addizione di H 2 si verifica in sin. Fondamenti di chimica organica Janice Gorzynski Smith 6 Copyright © 2009 – The Mc. Graw-Hill Companies srl

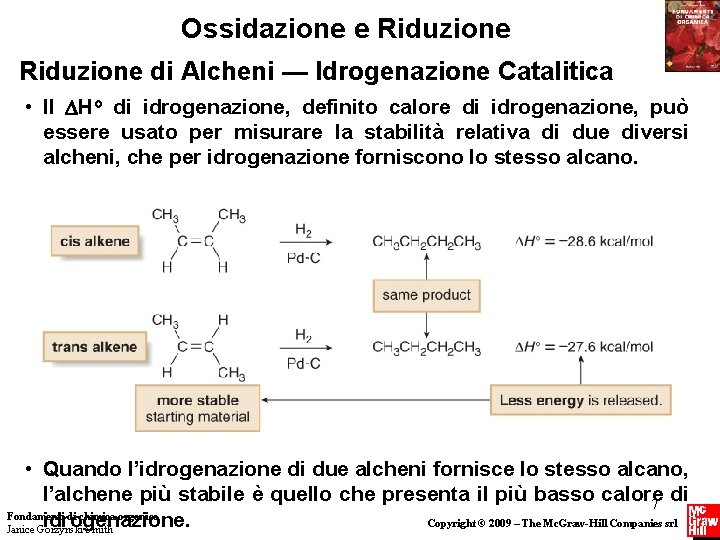
Ossidazione e Riduzione di Alcheni — Idrogenazione Catalitica • Il Ho di idrogenazione, definito calore di idrogenazione, può essere usato per misurare la stabilità relativa di due diversi alcheni, che per idrogenazione forniscono lo stesso alcano. • Quando l’idrogenazione di due alcheni fornisce lo stesso alcano, l’alchene più stabile è quello che presenta il più basso calore di 7 Fondamenti di chimica organica idrogenazione. Copyright © 2009 – The Mc. Graw-Hill Companies srl Janice Gorzynski Smith

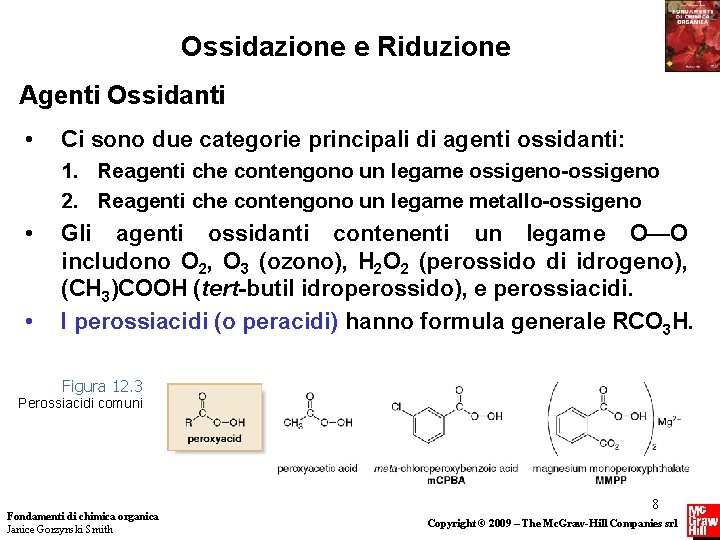
Ossidazione e Riduzione Agenti Ossidanti • Ci sono due categorie principali di agenti ossidanti: 1. Reagenti che contengono un legame ossigeno-ossigeno 2. Reagenti che contengono un legame metallo-ossigeno • • Gli agenti ossidanti contenenti un legame O—O includono O 2, O 3 (ozono), H 2 O 2 (perossido di idrogeno), (CH 3)COOH (tert-butil idroperossido), e perossiacidi. I perossiacidi (o peracidi) hanno formula generale RCO 3 H. Figura 12. 3 Perossiacidi comuni Fondamenti di chimica organica Janice Gorzynski Smith 8 Copyright © 2009 – The Mc. Graw-Hill Companies srl

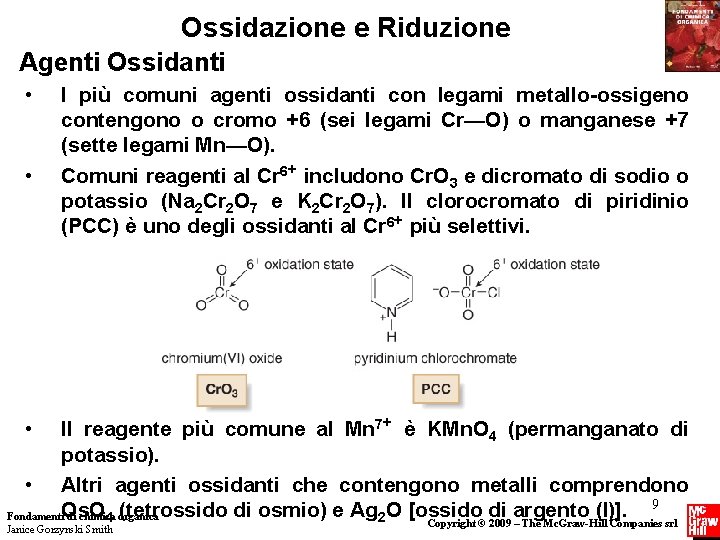
Ossidazione e Riduzione Agenti Ossidanti • • I più comuni agenti ossidanti con legami metallo-ossigeno contengono o cromo +6 (sei legami Cr—O) o manganese +7 (sette legami Mn—O). Comuni reagenti al Cr 6+ includono Cr. O 3 e dicromato di sodio o potassio (Na 2 Cr 2 O 7 e K 2 Cr 2 O 7). Il clorocromato di piridinio (PCC) è uno degli ossidanti al Cr 6+ più selettivi. Il reagente più comune al Mn 7+ è KMn. O 4 (permanganato di potassio). • Altri agenti ossidanti che contengono metalli comprendono 9 (tetrossido di osmio) e Ag 2 O [ossido di argento (I)]. Fondamenti. Os. O di chimica 4 organica Copyright © 2009 – The Mc. Graw-Hill Companies srl • Janice Gorzynski Smith

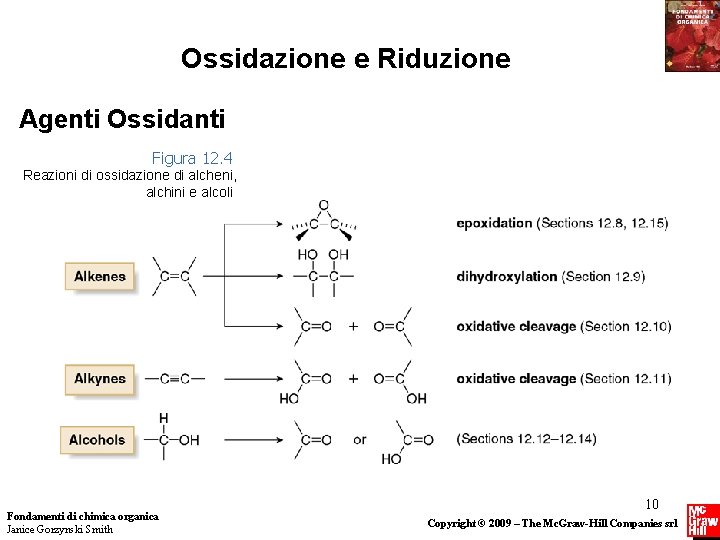
Ossidazione e Riduzione Agenti Ossidanti Figura 12. 4 Reazioni di ossidazione di alcheni, alchini e alcoli Fondamenti di chimica organica Janice Gorzynski Smith 10 Copyright © 2009 – The Mc. Graw-Hill Companies srl

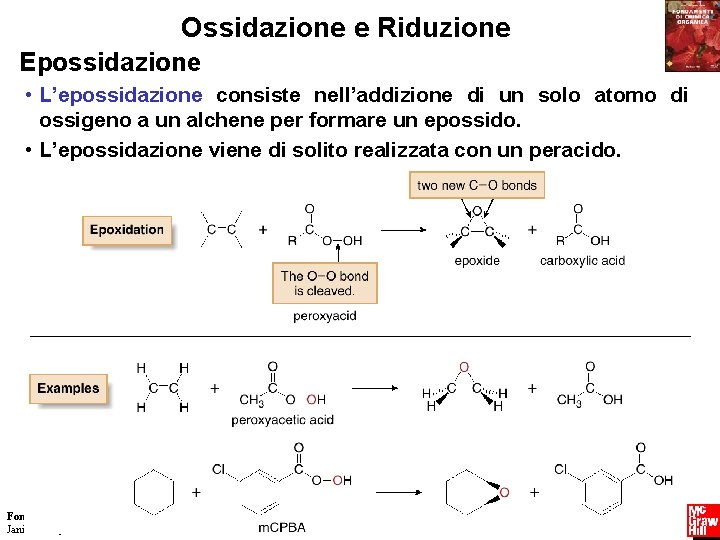
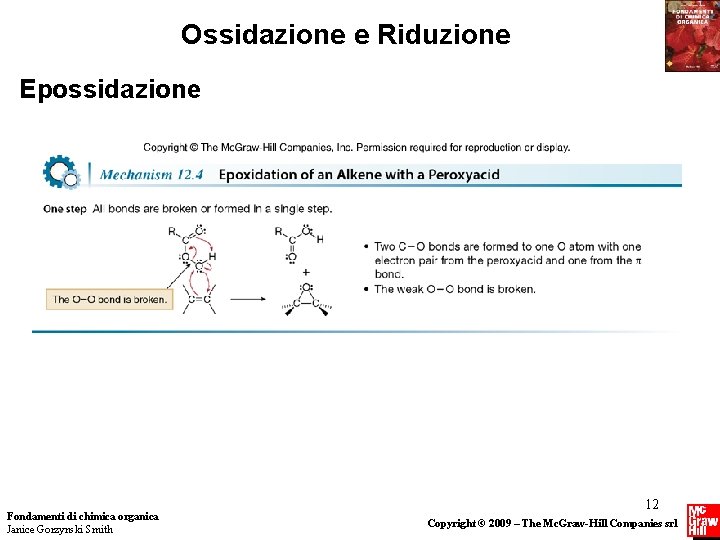
Ossidazione e Riduzione Epossidazione • L’epossidazione consiste nell’addizione di un solo atomo di ossigeno a un alchene per formare un epossido. • L’epossidazione viene di solito realizzata con un peracido. Fondamenti di chimica organica Janice Gorzynski Smith 11 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Ossidazione e Riduzione Epossidazione Fondamenti di chimica organica Janice Gorzynski Smith 12 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Ossidazione e Riduzione Diidrossilazione • La diidrossilazione è l’addizione di due gruppi ossidrilici a un doppio legame, con formazione di un 1, 2 -diolo o glicole. • A seconda del tipo di reagente, i due nuovi gruppi OH possono essere addizionati da parti opposte (addizione anti) o dalla stessa parte (addizione sin) del doppio legame. Fondamenti di chimica organica Janice Gorzynski Smith 13 Copyright © 2009 – The Mc. Graw-Hill Companies srl

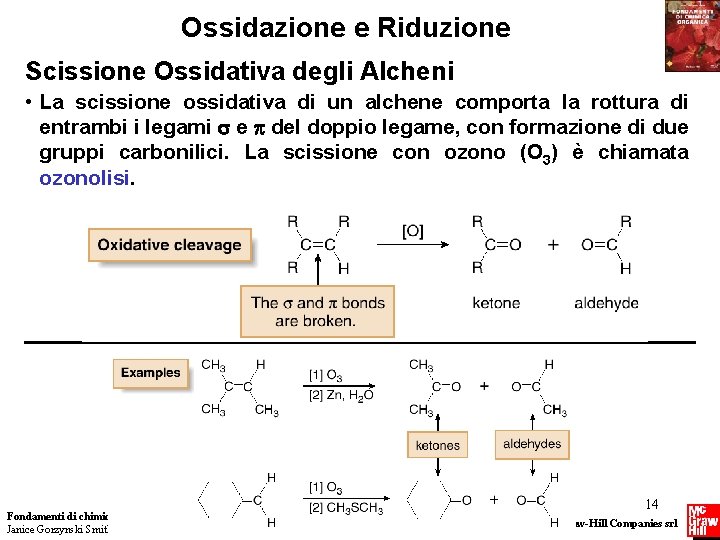
Ossidazione e Riduzione Scissione Ossidativa degli Alcheni • La scissione ossidativa di un alchene comporta la rottura di entrambi i legami e del doppio legame, con formazione di due gruppi carbonilici. La scissione con ozono (O 3) è chiamata ozonolisi. Fondamenti di chimica organica Janice Gorzynski Smith 14 Copyright © 2009 – The Mc. Graw-Hill Companies srl

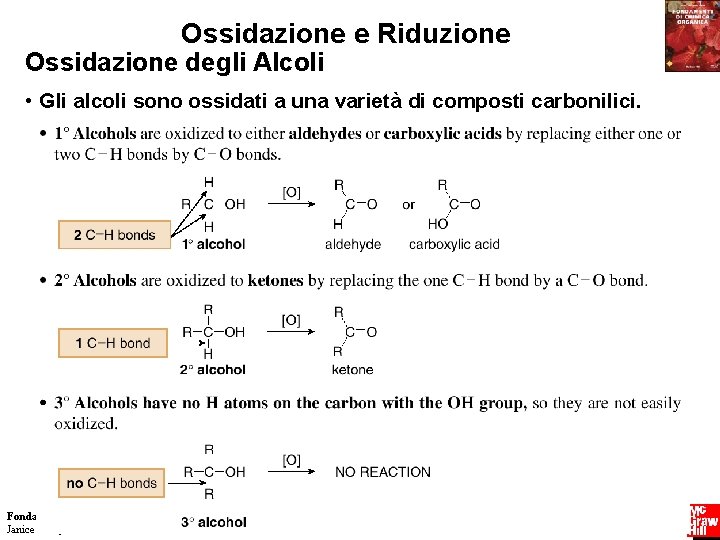
Ossidazione e Riduzione Ossidazione degli Alcoli • Gli alcoli sono ossidati a una varietà di composti carbonilici. Fondamenti di chimica organica Janice Gorzynski Smith 15 Copyright © 2009 – The Mc. Graw-Hill Companies srl

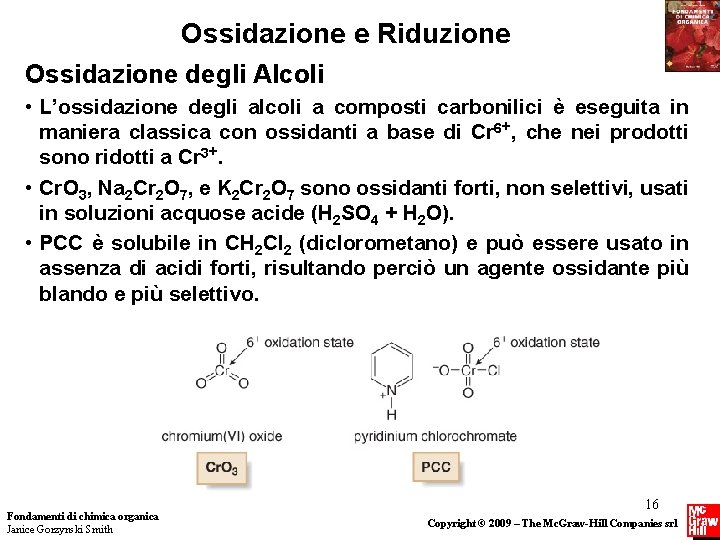
Ossidazione e Riduzione Ossidazione degli Alcoli • L’ossidazione degli alcoli a composti carbonilici è eseguita in maniera classica con ossidanti a base di Cr 6+, che nei prodotti sono ridotti a Cr 3+. • Cr. O 3, Na 2 Cr 2 O 7, e K 2 Cr 2 O 7 sono ossidanti forti, non selettivi, usati in soluzioni acquose acide (H 2 SO 4 + H 2 O). • PCC è solubile in CH 2 Cl 2 (diclorometano) e può essere usato in assenza di acidi forti, risultando perciò un agente ossidante più blando e più selettivo. Fondamenti di chimica organica Janice Gorzynski Smith 16 Copyright © 2009 – The Mc. Graw-Hill Companies srl

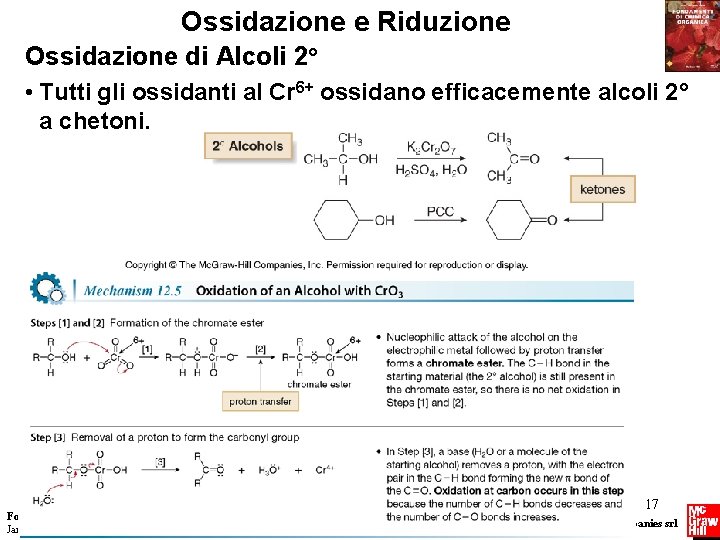
Ossidazione e Riduzione Ossidazione di Alcoli 2° • Tutti gli ossidanti al Cr 6+ ossidano efficacemente alcoli 2° a chetoni. Fondamenti di chimica organica Janice Gorzynski Smith 17 Copyright © 2009 – The Mc. Graw-Hill Companies srl

Ossidazione e Riduzione Ossidazione di Alcoli 1° • Gli alcoli 1° sono ossidati ad aldeidi o ad acidi carbossilici, in funzione del reagente usato. Fondamenti di chimica organica Janice Gorzynski Smith 18 Copyright © 2009 – The Mc. Graw-Hill Companies srl