Eletroqumica II ELETRLISE Ao contrrio das pilhas a




















- Slides: 31

Eletroquímica (II)

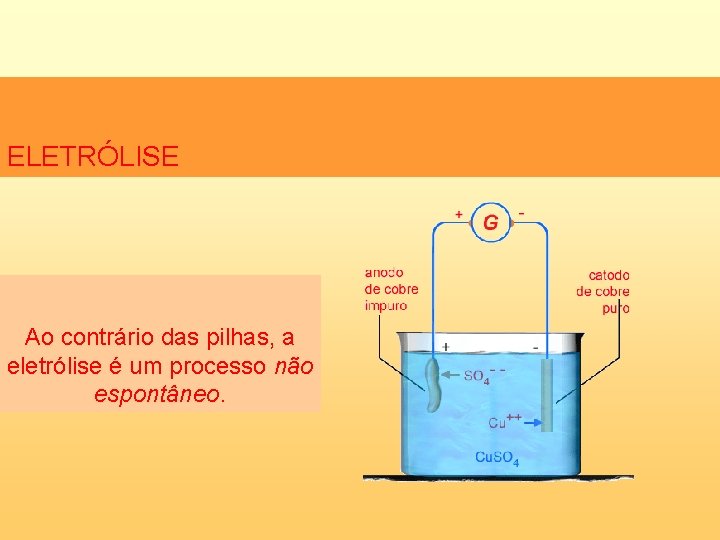
ELETRÓLISE Ao contrário das pilhas, a eletrólise é um processo não espontâneo.

ELETRÓLISE Na eletrólise ocorre uma reação de oxi-redução não espontânea que consome corrente elétrica de uma bateria ligada ao sistema.

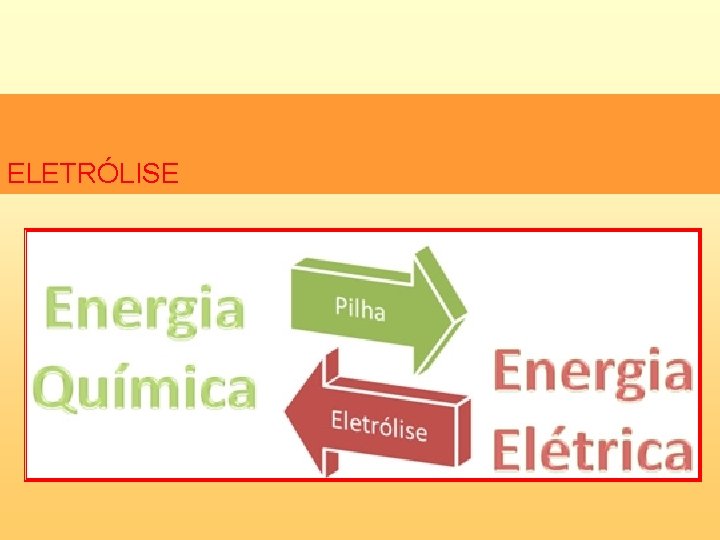
ELETRÓLISE

ELETRÓLISE X PILHA 1. NODO a) Na pilha fornece elétrons, sinal (-); b) Na eletrólise recebe elétrons dos ânions do eletrólito, sinal (+). 2. CÁTODO a) Na pilha recebe elétrons, sinal (+); b) Na Eletrólise fornece elétrons dos cátions do eletrólito, sinal (-).

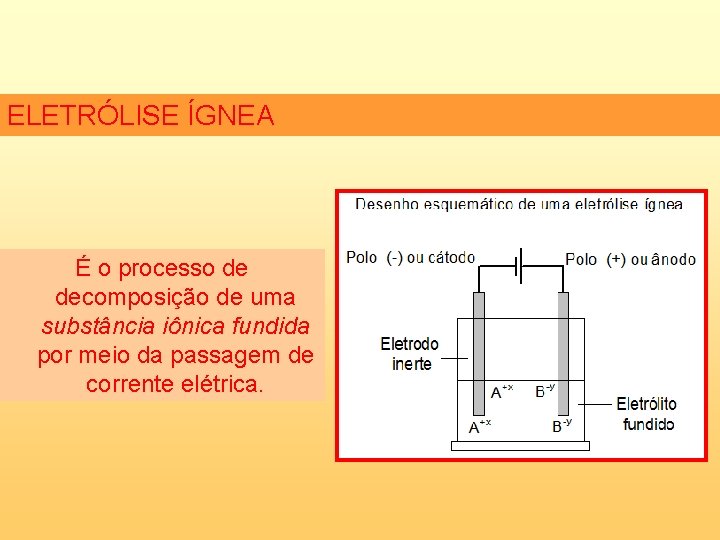
ELETRÓLISE ÍGNEA É o processo de decomposição de uma substância iônica fundida por meio da passagem de corrente elétrica.

ELETRÓLISE ÍGNEA A eletrólise ígnea exige eletrodos inertes que possuam elevado ponto de fusão. Geralmente são usados a platina ou grafita. A eletrólise do Na. Cℓ é um processo economicamente importante. O Na. Cℓ se funde à temperatura de 808 ºC. Na. Cℓ(sólido) Na. Cℓ (líquido) Ocorre, então, dissociação. . . Na. Cℓ Na 1+ + Cℓ 1 -

ELETRÓLISE ÍGNEA Os íons Cℓ 1 - se dirigem para o ânodo (pólo positivo), perdem seus elétrons e são transformados em gás cloro, Cℓ 2. 2 Cℓ 1 - Cℓ 2 + 2 e- (oxidação) Os íons Na 1+ se dirigem para o cátodo (pólo negativo), recebem um elétron e são transformados em sódio metálico (Na 0). * 2 Na 1+ + 2 e- 2 Na 0 (redução) *Duplica-se para igualar o número de elétrons na redução e na oxidação.

ELETRÓLISE ÍGNEA Considerando-se. . . 2 Na. Cℓ(l) 2 Na 1+(l) + 2 Cℓ 1 -(l) Cℓ 2(g) + 2 e- (oxidação) 2 Na 1+(l) + 2 e- 2 Na 0(l) (redução) A equação global da eletrólise é. . . 2 Na. Cℓ(l) Cℓ 2(g) + 2 Na 0(l)

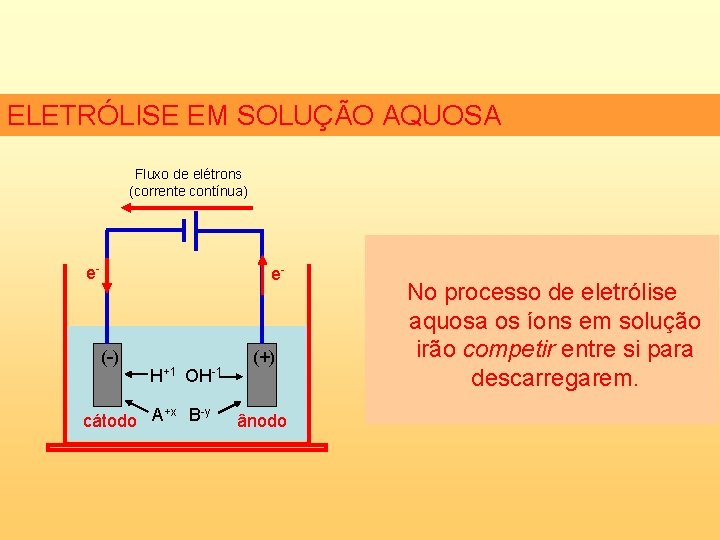
ELETRÓLISE EM SOLUÇÃO AQUOSA Fluxo de elétrons (corrente contínua) e- e- (-) H+1 OH-1 -y +x cátodo A B (+) ânodo No processo de eletrólise aquosa os íons em solução irão competir entre si para descarregarem.

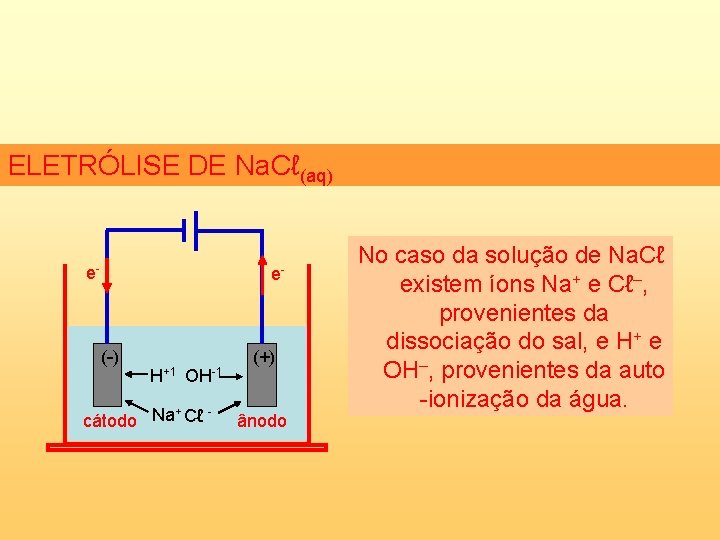
ELETRÓLISE DE Na. Cℓ(aq) e- e- (-) H+1 OH-1 + cátodo Na Cℓ (+) ânodo No caso da solução de Na. Cℓ existem íons Na+ e Cℓ–, provenientes da dissociação do sal, e H+ e OH–, provenientes da auto -ionização da água.

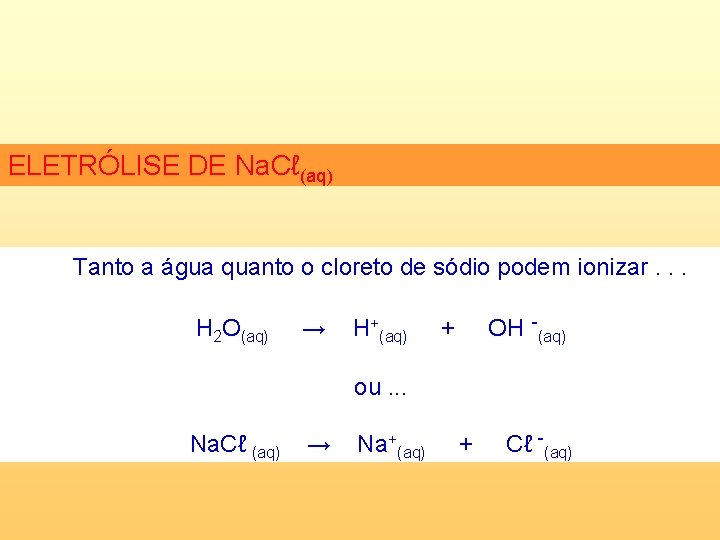
ELETRÓLISE DE Na. Cℓ(aq) Tanto a água quanto o cloreto de sódio podem ionizar. . . H 2 O(aq) → H+(aq) + OH -(aq) ou. . . Na. Cℓ (aq) → Na+(aq) + Cℓ -(aq)

ELETRÓLISE DE Na. Cℓ(aq) Significa que temos teremos uma competição. . . H 2 O(aq) → H+(aq) + OH -(aq) Competição Na. Cℓ (aq) → Na+(aq) + Cℓ -(aq)

ELETRÓLISE DE Na. Cℓ(aq) O que a experiência mostra? O POLO NEGATIVO DESCARREGA EM PRIMEIRO LUGAR, O CÁTION DE REDUÇÃO MAIS FÁCIL O POLO POSITIVO DESCARREGA EM PRIMEIRO LUGAR O NION DE OXIDAÇÃO MAIS FÁCIL

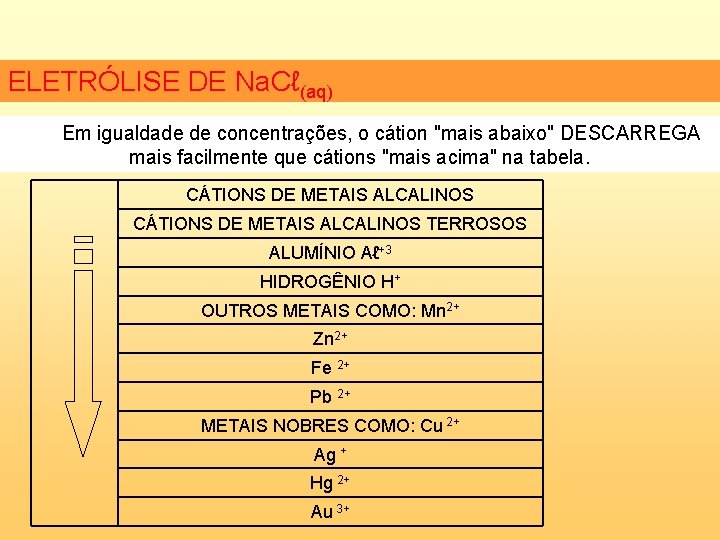
ELETRÓLISE DE Na. Cℓ(aq) Em igualdade de concentrações, o cátion "mais abaixo" DESCARREGA mais facilmente que cátions "mais acima" na tabela. CÁTIONS DE METAIS ALCALINOS TERROSOS ALUMÍNIO Aℓ+3 HIDROGÊNIO H+ OUTROS METAIS COMO: Mn 2+ Zn 2+ Fe 2+ Pb 2+ METAIS NOBRES COMO: Cu 2+ Ag + Hg 2+ Au 3+

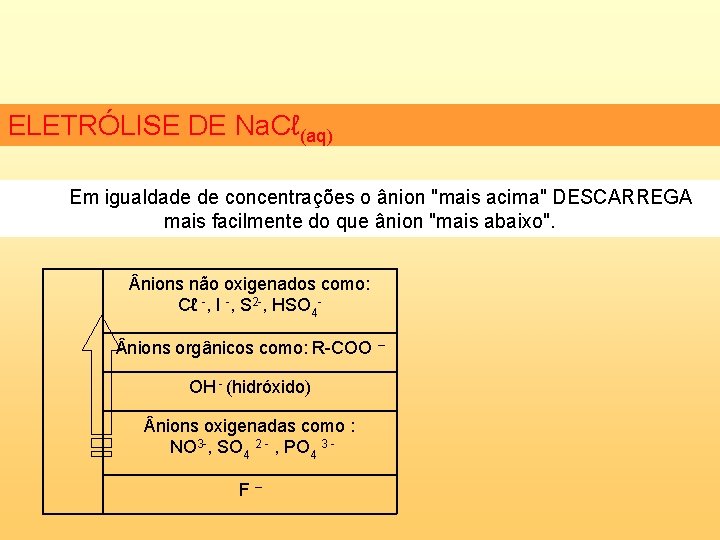
ELETRÓLISE DE Na. Cℓ(aq) Em igualdade de concentrações o ânion "mais acima" DESCARREGA mais facilmente do que ânion "mais abaixo". nions não oxigenados como: Cℓ -, I -, S 2 -, HSO 4 nions orgânicos como: R-COO – OH - (hidróxido) nions oxigenadas como : NO 3 -, SO 4 2 - , PO 4 3 - F –

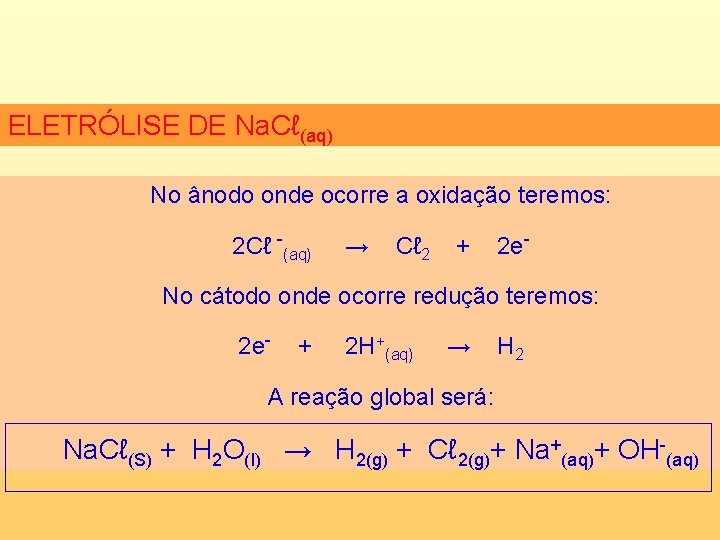
ELETRÓLISE DE Na. Cℓ(aq) No ânodo onde ocorre a oxidação teremos: 2 Cℓ -(aq) → Cℓ 2 + 2 e- No cátodo onde ocorre redução teremos: 2 e- + 2 H+(aq) → H 2 A reação global será: Na. Cℓ(S) + H 2 O(l) → H 2(g) + Cℓ 2(g)+ Na+(aq)+ OH-(aq)

ELETRÓLISE do KI(aq) No processo dessa eletrólise aquosa os íons em solução também irão competir entre si para descarregarem. No caso da solução de KI existem íons K+ e I–, provenientes da dissociação do sal, e H+ e OH–, provenientes da auto-dissociação da água.

ELETRÓLISE do KI(aq) De forma semelhante, observando-se a prioridade de descarga, na eletrólise do KI aquoso há formação de H 2(no cátodo) e I 2(no ânodo) e liberação de Na+OH-(aq). Experimento dos alunos Cassiane e Pedro.

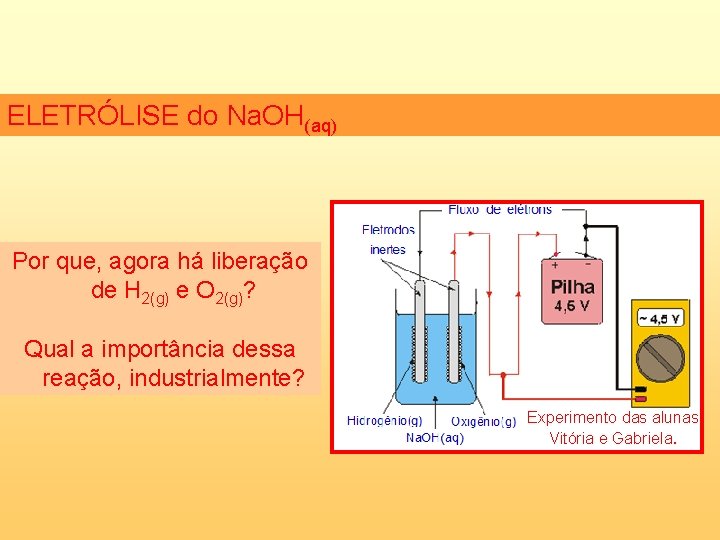
ELETRÓLISE do Na. OH(aq) Por que, agora há liberação de H 2(g) e O 2(g)? Qual a importância dessa reação, industrialmente? Experimento das alunas Vitória e Gabriela.

ELETRÓLISE QUANTITIVA Michael Faraday formulou duas leis que regem o aspecto quantitativo da eletrólise Michael Faraday (1791 — 1867)

ELETRÓLISE QUANTITIVA A primeira lei de FARADAY “A massa, “m”, de uma substância, formada ou transformada numa eletrólise, é diretamente proporcional à carga elétrica, Q, que atravessa o circuito. ” m = K 1. Q

ELETRÓLISE QUANTITIVA Sabe-se (da Física) que. . . Q = i. t Substituindo na lei de Faraday, temos. . . m = K 1. i. t * i é a intensidade da corrente elétrica e t é o tempo de reação.

ELETRÓLISE QUANTITIVA A segunda lei de FARADAY “A massa, m, de uma substância, formada ou transformada numa eletrólise, é diretamente proporcional ao equivalente-grama, E, dessa substância. ” m = K 2. E

ELETRÓLISE QUANTITIVA De forma semelhante ao raciocínio anterior. . . Sabendo que m = K 2. E E que Q = i. t Então. . . m = K 2. E. i. t

ELETRÓLISE QUANTITIVA Associando as duas leis e considerando K=1/96500 teremos. . . Constante de Faraday = 96500 C, ou seja, quantidade de carga elétrica transportada por 1 mol de elétrons (6, 02 x 1023 elétrons).

ELETRÓLISE QUANTITIVA: EXEMPLIFICANDO Uma solução de cloreto de prata é eletrolisada durante 965 segundos por uma corrente elétrica de 1 ampère (A). Qual a massa de prata depositada no cátodo? Dado da tabela periódica: Ag = 108 g / mol 1. ª parte *Um mol de elétrons transferidos pela Ag.

ELETRÓLISE QUANTITIVA Uma solução de cloreto de prata é eletrolisada durante 965 segundos por uma corrente elétrica de 1 ampère (A). Qual a massa de prata depositada no cátodo? Dado da tabela periódica: Ag = 108 g / mol 2. ª parte *C = A. s

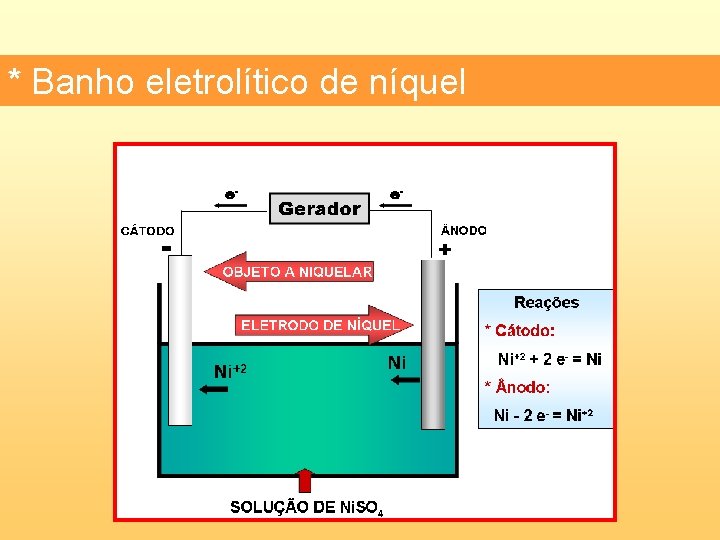
ELETRÓLISE (GALVANOPLASTIA) * Banhos eletrolíticos de metais - cromo, níquel, zinco, cobre, ouro, prata, . . .

* Banho eletrolítico de níquel

F I M Colégio INEDI Prof. Luiz Antônio Tomaz