Pilhas Entendese por ELETROQUMICA o ramo da Qumica





























- Slides: 38

Pilhas

Entende-se por ELETROQUÍMICA o ramo da Química que estuda so fenômenos químicos que envolvem transferência de elétrons. Quando um processo químico ocorre espontaneamente e produz transferência de elétrons é chamado de pilha ou bateria, mas quando o processo químico é provocado por uma corrente elétrica é denominado eletrólise.

ELETROQUÍMICA

PILHAS E BATERIAS Para calculadoras Para lanternas Para celulares Para automóveis

ELETRÓLISE laboratório indústria

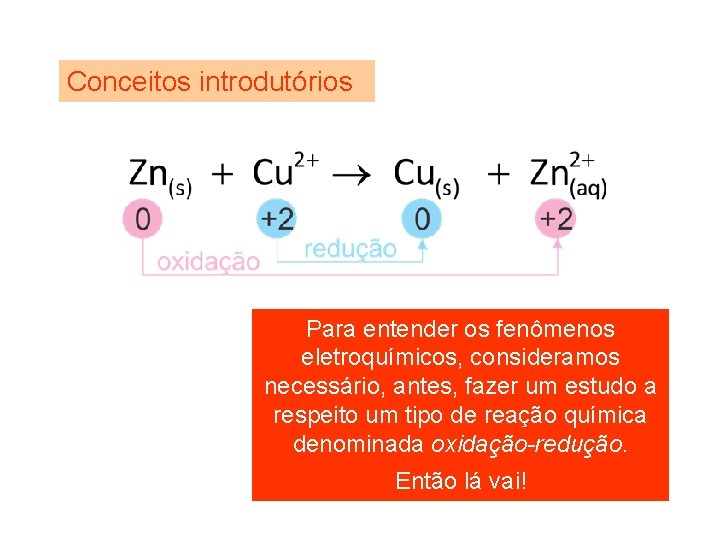
Conceitos introdutórios Para entender os fenômenos eletroquímicos, consideramos necessário, antes, fazer um estudo a respeito um tipo de reação química denominada oxidação-redução. Então lá vai!

Reação química OXIDAÇÃO-REDUÇÃO (REDOX) Na imagem ao lado, dizse`, normalmente, que o objeto “enferrujou”. Quimicamente, porém, seria mais adequado falarse em um processo de “oxidação-redução”.

Reação química OXIDAÇÃO-REDUÇÃO ou REDOX A oxidação-redução é, na verdade, uma reação química em que se observa “transferência de elétrons” de uma espécie química para outra.

Uma experiência realizada no laboratório Após certo tempo, a solução muda de cor e um “pó” avermelhado (Cu) parece ocupar o lugar do prego (Fe).

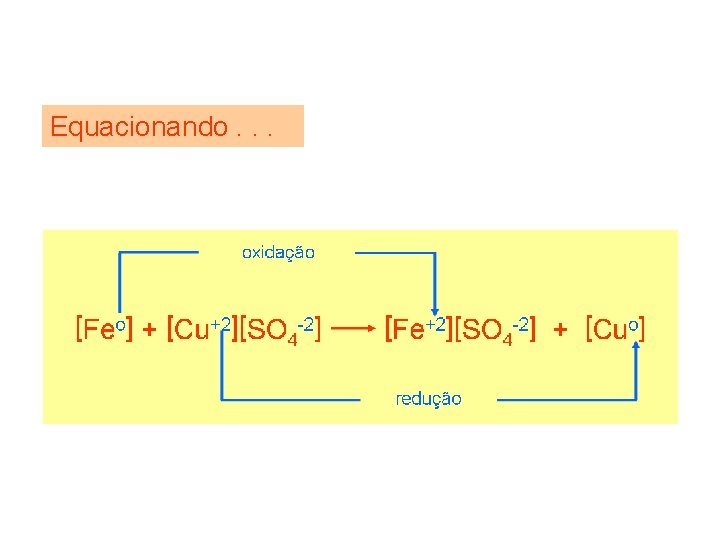
Equacionando para melhor compreensão. . . Fe + Cu. SO 4 cinza azul *Tende a tornar-se incolor. Fe. SO 4 + Cu esverdeada* avermelhado

Equacionando. . .

Explicando. . . O ferro, inicialmente neutro (NOX=0), perde 2 elétrons, os quais são transferidos para o cobre, tornado-se carregado (NOX=+2). É a oxidação do ferro!

Explicando. . . O cobre, inicialmente carregado (NOX = +2), recebe 2 elétrons e tornando-se neutro (NOX=0). É a redução do cobre!

Outros conceitos. . . Agente oxidante É a espécie que sofre redução. No exemplo, o agente oxidante é o cobre (Cu+2). Cu+2 + 2 e- Cuo

Outros conceitos. . . Agente redutor É a espécie que sofre oxidação. No exemplo, o agente redutor é o cobre (Feo). Feo Fe+2 + 2 e-

A equação global. . . Feo + Cu+2 Fe+2 + Cuo Esta é chamada de equação global. Nela só aparecem os íons ou átomos que mudaram o seu número de oxidação (NOX).

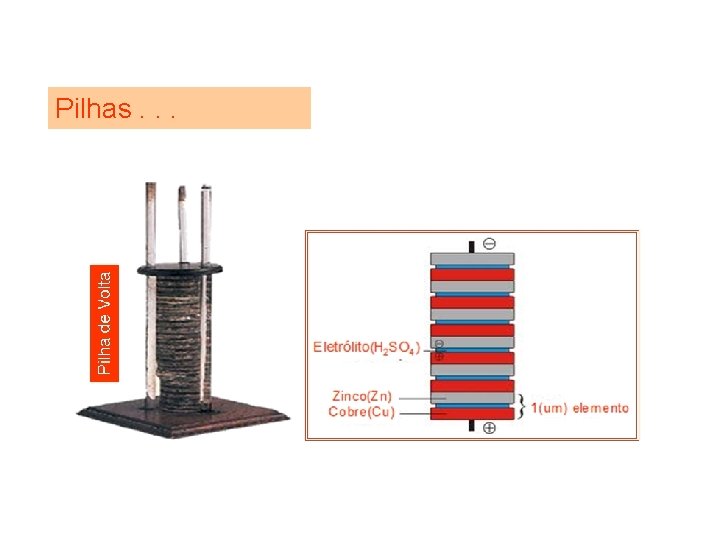
Pilhas. . . Pilha de Volta A pilha de Volta, como o próprio nome indica, foi inventada em 1800 pelo físico italiano Alessandro Volta (1745 -1827).

Pilhas. . .

Pilha de Daniell A pilha de Daniell baseia-se na seguinte reação (forma iônica simplificada). . . Zno + Cu+2(aq) Zn+2(aq) + Cuo

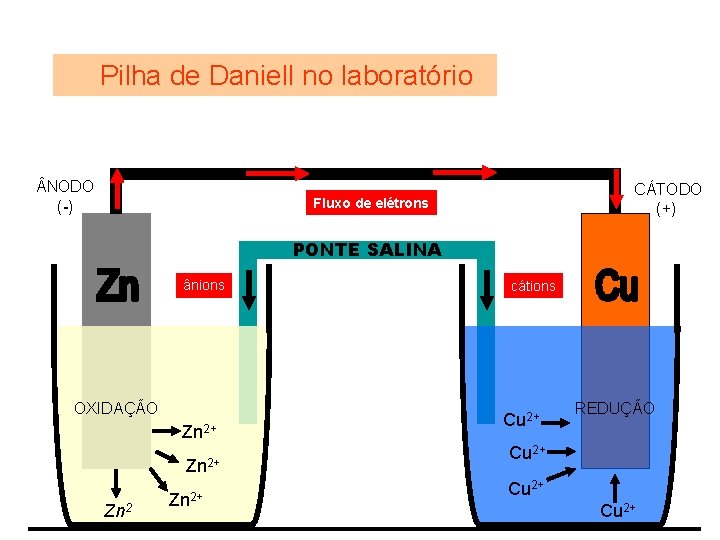
Pilha de Daniell no laboratório NODO (-) CÁTODO (+) Fluxo de elétrons PONTE SALINA ânions OXIDAÇÃO Zn 2+ cátions Cu 2+ REDUÇÃO Cu 2+

Pilha de Daniell percebeu que os elétrons poderiam ser transferidos do zinco (Zn) para os cátions cobre (Cu+2) por um fio condutor externo e, com isso, produzir uma corrente elétrica.

Pilha de Daniell Com o passar do tempo, haverá excesso de cátions na solução de sulfato de zinco e falta de cátions na solução de sulfato de cobre. Isso faz com que a pilha pare de funcionar. Isso é, então, compensado pela ponte salina.

Representação de uma pilha (IUPAC) A IUPAC determina como representar uma pilha. M 1 o / M 1+x // M 2+y / M 2 o Zno / Zn+2 // Cu+2 / Cuo * As barras paralelas representam a ponte salina.

Potencial de redução Na pilha de Daniell o zinco (Zno) tende a se oxidar, enquanto o cobre (Cuo), a se reduzir. Por quê? O zinco apresenta menor potencial de redução (- 0, 76 V), enquanto cobre apresenta maior potencial de redução (+ 0, 34 V).

Potencial de redução Valores são obtidos experimentalmente e permitem que. . . 1. Seja calculada a diferença de potencial da pilha 2. Façamos previsão de quem se oxida ou quem se reduz

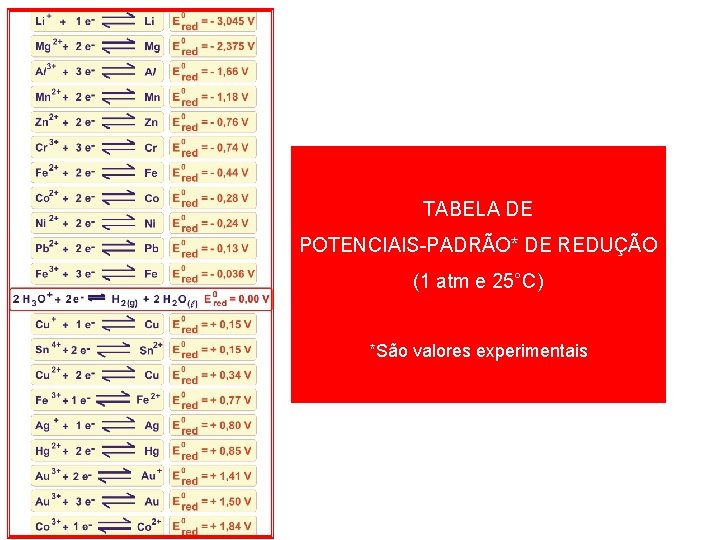
TABELA DE POTENCIAIS-PADRÃO* DE REDUÇÃO (1 atm e 25°C) *São valores experimentais

Entendendo. . . Quanto maior for a medida do potencial de oxidação, maior é a tendência do metal ceder elétrons Quanto maior for a medida do potencial de redução, maior é a tendência do metal ganhar elétrons

Exemplificando. . . Zn 2+ + 2 e- Zno E° = – 0, 76 V Cu 2+ + 2 e- Cuo E° = + 0, 34 V

Exemplificando. . . O cobre tem maior potencial de redução, logo ganhará elétrons (sofrerá redução); o zinco perderá elétrons (sofrerá oxidação). Zno Zn 2+ + 2 e. Cuo Zno + Cu 2+ E° = + 0, 76 V E° = + 0, 34 V Zn 2+ + Cuo ΔE = + 1, 10 V

Exercitando. . . Sejam as seguintes semi-reações e os seus potenciais padrão de redução, determine a “d. d. p. ” da pilha formada: Sn+2 + 2 e. Sno Eo = - 0, 14 V Ag+1 +1 e. Ago Eo = + 0, 80 V (a) + 0, 54 V. (b) + 0, 66 V. (c) + 1, 46 V. (d) + 0, 94 V. (e) + 1, 74 V.

Exercitando. . . Sejam as seguintes semi-reações e os seus potenciais padrão de redução, determine a “ d. d. p “ da pilha formada: Sn+2 + 2 e. Sno Eo = - 0, 14 V Ag+1 +1 e. Ago Eo = + 0, 80 V (a) + 0, 54 V. (b) + 0, 66 V. (c) + 1, 46 V. (d) + 0, 94 V. (e) + 1, 74 V. O potencial de redução da prata é maior que o do estanho Sno 2 Ag+1 + 2 e. Sno + 2 Ag+1 Sn+2 + 2 e 2 Ago Eo = + 0, 14 V Eo = + 0, 80 V Sn+2 + 2 Ago ∆Eo = + 0, 94 V

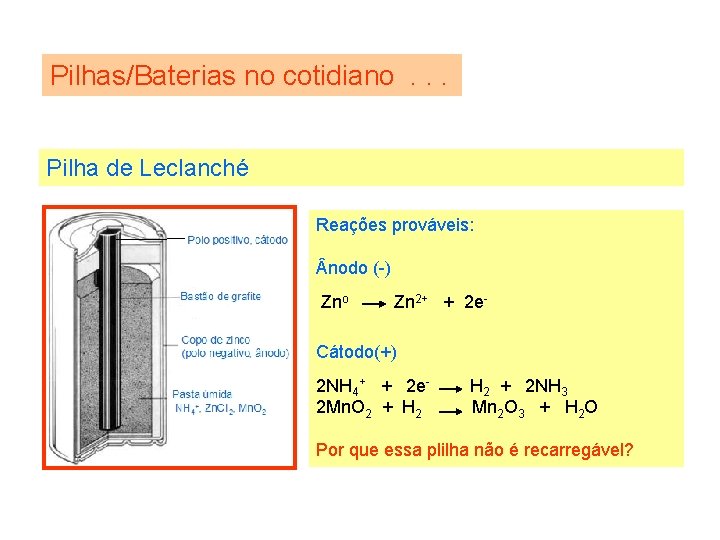
Pilhas/Baterias no cotidiano. . . Pilha de Leclanché Reações prováveis: nodo (-) Zno Zn 2+ + 2 e- Cátodo(+) 2 NH 4+ + 2 e 2 Mn. O 2 + H 2 + 2 NH 3 Mn 2 O 3 + H 2 O Por que essa plilha não é recarregável?

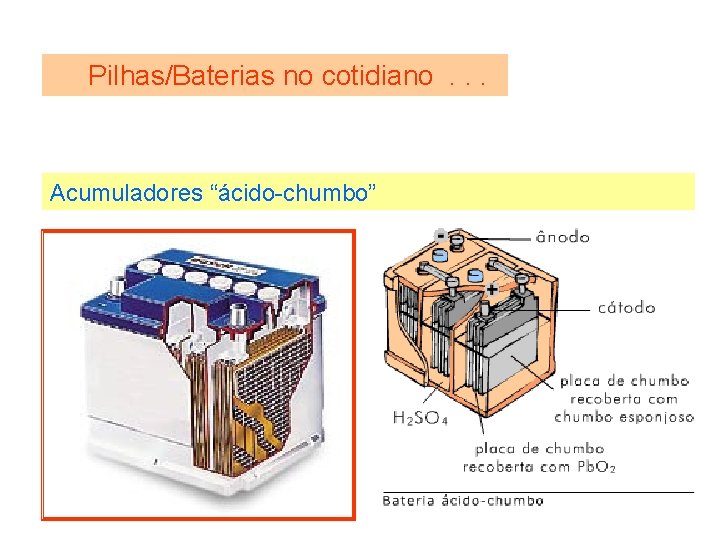
Pilhas/Baterias no cotidiano. . . Acumuladores “ácido-chumbo”

Pilhas/Baterias no cotidiano. . . Acumuladores “ácido-chumbo” Durante a descarga: Durante a carga: nodo (-) Cátodo (-) Pbo + SO 42 - Pb. SO 4 + 2 e- Cátodo (+) Pb. O 2 + SO 42 - + 2 e- Pb. SO 4 + 2 e- Pbo + SO 42 - Anodo (+) Pb. SO 4 Pb. O 2 + SO 42 - + 2 e-

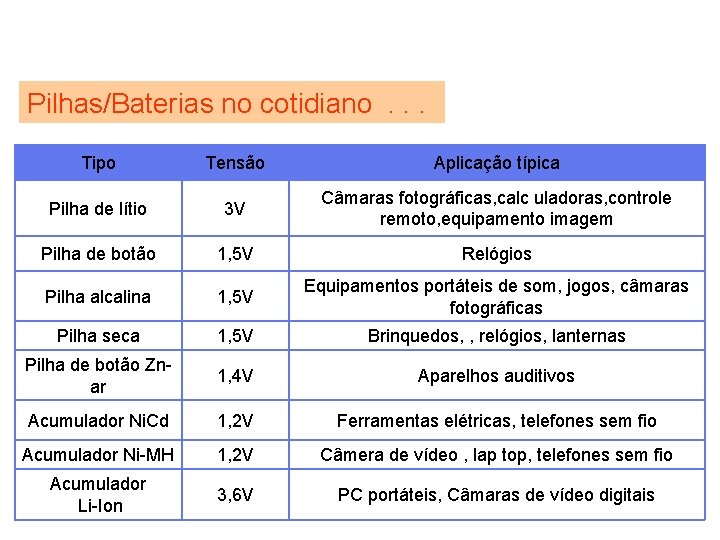
Pilhas/Baterias no cotidiano. . . Tipo Tensão Aplicação típica Pilha de lítio 3 V Câmaras fotográficas, calc uladoras, controle remoto, equipamento imagem Pilha de botão 1, 5 V Relógios Pilha alcalina 1, 5 V Equipamentos portáteis de som, jogos, câmaras fotográficas Pilha seca 1, 5 V Brinquedos, , relógios, lanternas Pilha de botão Znar 1, 4 V Aparelhos auditivos Acumulador Ni. Cd 1, 2 V Ferramentas elétricas, telefones sem fio Acumulador Ni-MH 1, 2 V Câmera de vídeo , lap top, telefones sem fio Acumulador Li-Ion 3, 6 V PC portáteis, Câmaras de vídeo digitais

Descarte de pilhas e baterias. . . De acordo com o CONAMA, Lei 257, publicada em 22 de julho de 1999, as pilhas e baterias devem conter o símbolo indicativo de descarte.

Descarte de pilhas e baterias. . . Podem ser descartadas em lixo doméstico; pilhas secas, alcalinas, Ni-H e de lítio. As demais, por conterem, por exemplo, Pb, Hg e Cd não podem ter descarte simples, devendo ser devolvidas ao fabricante.

Fim da primeira parte. Em seguida, eletrólise. Eletroquímica I Prof. Luiz Antônio Tomaz Turmas 101/ 201 e 102/ 202